经椎板间入路全脊柱内镜技术治疗腰椎间盘突出症的效果
方海名 张 明 桑裴铭 陈斌辉 顾仕荣 卢良杰
经椎板间入路全脊柱内镜技术治疗腰椎间盘突出症是近年来发展起来的一项新技术。Ruetten等[1]于2006年首次报道采用经皮内镜椎板间入路腰椎间盘切除术(percutaneous endoscopic interlaminar discectomy,PEID)摘除突出的椎间盘组织。PEID手术入路的解剖为脊柱外科医师所熟悉,且具有术中透视少,不受高髂嵴、椎间孔容积、背根神经节和出行神经根限制等优点[2],故经椎板间入路全脊柱内镜技术在近些年发展十分迅速。
1 对象与方法
1.1 研究对象 选取2015年6月—2016年7月间在宁波大学医学院附属李惠利医院行经椎板间入路全脊柱内镜技术治疗的患者84例,男44例、女40例,年龄22~81岁,平均年龄为(35.8±17.8)岁。所有患者术前均有不同程度的腰痛伴下肢疼痛,行腰椎正侧位、腰椎过伸过屈位X线检查和CT、MRI检查,诊断为腰椎间盘突出症,其中L4至L5节段突出3例、L5至S1节段突出81例。纳入标准:反复腰腿痛经保守治疗3个月以上无明显好转;MRI检查结果与患者症状、体征相符合;中央型或旁中央型腰椎间盘突出;X线检查见L4至L5或L5至S1椎板间隙>1 cm;腰椎动力位片显示,无明显腰椎不稳、单节段病变。排除标准:腰椎管狭窄;腰椎滑脱,或不稳定;腰椎间盘椎间孔型,或极外侧型突出;游离、脱垂、钙化型腰椎间盘突出;有马尾神经损伤症状;凝血功能障碍;无法耐受手术;多节段病变。
1.2 手术方法 所有患者均行全身麻醉,取俯卧位。经C臂机透视确定病变椎板间隙,于病变节段棘突旁开5 mm处作一长约7 mm的纵形实线作为体表标记。常规消毒、铺巾,切开皮肤和浅深筋膜,置入铅笔头状扩张管至黄韧带表面,沿扩张管旋入工作管道。经C臂机透视再次确定病变节段,置入脊柱内镜,在镜下用打孔钳切除部分黄韧带,探查神经根、硬膜囊和椎间隙位置,进入椎管后咬除下关节突内侧缘骨质,显露移行神经根外侧缘,行椎间盘摘除,不强行推挤神经根和硬膜囊,以减少对神经根的刺激和损伤。椎间盘摘除步骤:见神经根腋下突出的髓核组织和受压的神经根,松解突出或脱出的髓核组织,用髓核钳将其取出,应用射频电极消融絮状髓核,取出部分髓核后,旋转倾斜工作管道至神经根肩部,旋转手法应轻柔,将稍松弛的神经根推向内侧,寻找残余的髓核组织,从神经根肩上摘除残余的髓核组织。神经根肩上减压与神经根腋下减压形成“会师”, 探查并摘除神经根腋下可能残余的髓核组织。严密止血,探查神经根和硬膜囊无明显受压后取出套管,缝合切口。
1.3 术后处理 术后2 h内需绝对卧床,给予甲钴胺、甲泼尼龙、甘露醇等对症治疗以减少神经手术后的反应。术后2 h后患者可开始在腰围保护下下床活动,并嘱其术后3个月内避免重体力劳动,减少弯腰、持重物和久坐等活动。
1.4 临床疗效评估 分别于术前、术后1周、术后3和10个月采用疼痛VAS评分评估患者腰腿痛程度,采用Oswestry功能障碍指数(ODI)评估腰椎功能[3-4]。
1.5 术后并发症情况 记录麻醉苏醒过程中患者是否出现烦躁不安,记录随访期间患者有无硬脊膜和神经根损伤、下肢肌力下降、切口感染、下肢麻木等并发症发生。

2 结 果
所有患者手术均顺利完成,手术时间38~76 min,平均手术时间为(55.1±10.3) min。术前、术后1周、术后3个月、术后10个月的疼痛VAS评分分别为(3.7±1.6)、(1.7±1.0)、(0.4±0.1)、(0.4±0.1)分,腰椎ODI分别为28.1±9.2、14.2±8.2、4.0±1.1、2.8±0.3, 术后1周、术后3和10个月的疼痛VAS评分和ODI均显著低于术前(P值均<0.01), 术后3和10个月的疼痛VAS评分和ODI均显著低于术后1周(P值均<0.01), 术后3、10个月间疼痛VAS评分和ODI的差异均无统计学意义(P值均>0.05)。典型病例见图1。
2例患者在麻醉苏醒过程中出现烦躁不安、胡言乱语,经镇静等对症处理后缓解。术后患者均无马尾神经损伤症状(若有马尾损伤症状术后即刻即可发现)。随访期间无患者发生硬脊膜和神经根损伤、下肢肌力下降、切口感染;下肢麻木13例,给予营养神经等对症治疗,术后10个月随访时下肢麻木消失9例,好转2例,无明显缓解2例。术后无1例患者复发。
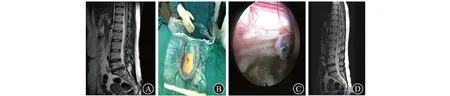
A 术前MRI检查示,L5至S1椎间盘向右后侧突出 B 术中照片,已置入工作套管 C 内镜下见已摘除突出的腰椎间盘组织,神经根无明显受压 D 术后10个月MRI检查示,L5至S1椎间盘无明显突出图1 患者,女,35岁,腰痛伴右下肢疼痛4个月
3 讨 论
L5椎板在L5至S1椎间隙的悬垂与其他腰椎椎间隙相比,产生了L5至S1水平较大的椎板间窗,为经椎板间入路全脊柱内镜技术提供了天然空间。因此,经椎板间入路全脊柱内镜技术主要应用于L5至S1节段,也可应用于椎板间窗较宽的腰L4至L5节段。有研究[5]明确了腰神经根起点与相应椎间隙的解剖位置关系,发现在75%的标本中S1神经根的起点位于L5至S1椎间隙上方,25%位于椎间隙水平,未发现有低于椎间隙水平发出的神经根。另有研究[6]发现,S1神经根从硬膜囊发出的起始角度平均为17.9°±5.8°。S1神经根的起始角度(从L5至S1节段发出)与其他节段发出神经根的角度相比较小,其特殊性决定了L5至S1椎间盘突出以腋下型最为常见。经椎板间入路全脊柱内镜技术处理L5至S1腋下型椎间盘突出时,易损伤神经根和硬膜囊。因此,采用经椎板间入路全脊柱内镜技术治疗腋下型腰椎间盘突出中,建议工作套管经过黄韧带破口进入椎管内时,不应立即、直接进入腋下部位,而应置于黄韧带与神经根、硬脊膜之间的硬膜外间隙,在脊柱内镜下观察、分辨清楚神经根、硬脊膜、突出髓核三者之间的关系,再摘除髓核致压物;如果突出的髓核组织较大,强行摘除可能会损伤神经根,可先分离髓核组织,并用打孔钳将髓核组织分块摘除、减压,以减少对神经根和硬膜囊的损伤。
随着脊柱微创理念的不断深入,脊柱手术器械的不断发展,经椎板间入路全脊柱内镜技术迅速发展,其具有切口小、术中出血少、术后恢复快的优点,可最大程度地保护椎旁肌、椎板、关节突关节、黄韧带,减少医源性损伤,维持脊柱正常序列。在脊柱内镜下摘除突出的椎间盘组织、减压神经根,可有效改善患者腰腿痛等临床症状,且操作安全、疗效确切。本研究结果显示,患者术后1周、术后3和10个月的疼痛VAS评分和ODI均显著低于术前,术后3和10个月的疼痛VAS评分和ODI均显著低于术后1周,术后3、10个月间疼痛VAS评分和ODI的差异均无统计学意义;表明经椎板间入路全脊柱内镜技术治疗后,患者的腰腿痛症状和活动功能均较术前显著改善,术后3、10个月时趋于正常。
李振宙等[7]对72例L5至S1非包含型腰椎间盘突出症患者行PEID,术后随访12个月,MacNab评分优良率为97%,神经根功能明显恢复,无神经损伤、感染等手术并发症发生,术后复发率为1.4%。
PEID对黄韧带和硬膜外脂肪的保护,减少了术后椎管内瘢痕形成,以及由其引起的神经粘连症状的发生,该结果在翻修手术中得以证实[8]。由于可以不切除椎板、关节突关节,PEID可降低术后腰椎不稳定的发生率[9]。
经椎板间入路全脊柱内镜技术治疗腰椎间盘突出症时,可取得非常好的临床疗效,但亦有相应的并发症发生,并发症的发生与术者的操作熟练程度、技术水平密切相关。常见的并发症如下[10-13]。① 神经根感觉异常:表现为神经根所支配的区域痛觉过敏和感觉麻木,通常为一过性的。由于S1神经根在椎管内走行的距离较长,在进行经椎板间入路全脊柱内镜操作时,易牵拉、推挤、损伤S1神经节,特别对于关节突内聚的患者。本研究中,有13例患者术后发生下肢麻木,均为在该技术开展的早期,由于手术医师缺乏脊柱内镜操作经验,有时会强行推挤、牵拉、刺激神经根,从而导致下肢麻木发生,经对症治疗后可缓解。② 硬脊膜破裂:因硬脊膜粘连紧密,强行剥离、粗暴操作均可造成硬脊膜破裂。术中应在脊柱内镜下仔细分辨组织结构,轻柔操作,切忌超出内镜范围盲目操作。③ 椎间隙感染、切口感染、不愈合:术中无菌操作规范、大量0.9%氯化钠溶液持续冲洗术野均可降低感染发生率;在冲洗过程中应注意0.9%氯化钠溶液引流,防止浸湿手术铺巾。④ 神经根损伤:与术中粗暴操作、镜下组织分辨不清、误伤,以及摘除巨大的髓核组织时挤伤等有关,故应注意术中操作。⑤ 根袖损伤:常见于腋下型腰椎间盘突出,在置入或移动工作套管时,如操作位置离神经根与硬膜囊发出点较近则易造成根袖损伤。⑥ 减压不充分、髓核残留:与术者的操作熟练程度、MRI检查时突出物大小的评估有关。⑦ 术后复发:是指腰椎间盘突出术后症状缓解至少6个月,其后出现同一节段同侧或对侧椎间盘再次突出。术后复发与术者对椎间盘破口的处理、患者术后康复锻炼和生活习惯有关。本研究中无1例患者术后复发,也可能与病例数不多有关。⑧全身麻醉苏醒过程中出现烦躁不安:本研究中有2例患者在麻醉苏醒过程中出现烦躁不安,可能与术中0.9%氯化钠溶液压力过高,椎管内高压、颅高压等有关,经镇静等对症处理后缓解。
综上所述,经椎板间入路全脊柱内镜技术安全、有效,其治疗腰椎间盘突出症的疗效佳,但仍需要继续随访,观察其长期疗效。

