确定有机混合物组成的方法
穆玉鹏
(山东省博兴县第一中学 256500)
一、根据混合物的平均式量确定构成混合物中的物质的分子式
例1相同状况下9 L甲烷与6 L某烯烃混合, 所得混合气体的密度等于相同条件下氧气的密度, 计算该烯烃的分子式.


Mr(CH4)=16
烯烃Mr=14n
(CnH2n)

解得n=4
烯烃的分子式为C4H8.

A.甲烷和乙烯 B.乙烷和乙烯
C.乙烷和丙烯 D.甲烷和丁烯

因为m(混合气)=m(H2)

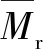
A.选项Mr(甲烷)=16<32Mr(乙烯)=28<32
故不为此题答案
B.选项Mr(乙烷)=30<32Mr(乙烯)=28<32
故不为此题答案
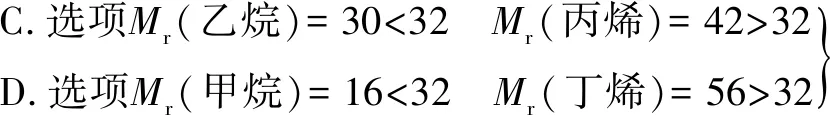

故C选项为本题正确答案.
二、根据混合物平均分子组成确定混合物中的物质分子式
例3 常温下一种烷烃A和一种单烯烃B组成的混合气,A或B分子最多只含4个碳原子, 且B分子的碳原子比A分子的多.
(1)将1 L该混合气体充分燃烧, 在同温同压下得到2.5 L二氧化碳, 试推断原混和气体中A和B所有可能的组合及其体积比, 并将结果填入下表.

组合编号A的分子式B的分子式A和B的体积比(VA∶VB)
(2)120℃时取1 L该混合气跟9 L氧气混合, 充分燃烧后, 当恢复到120℃和燃烧前的压强时, 体积增大6.25%,试通过计算确定A和B的分子式.
解(1)设混合气体平均分子组成为CxHy,则
依据题意CxHy~xCO2
1 LxL
1 L 2.5 L
x=2.5

A(烷烃)B(单烯烃)
满足B分子的碳原子大于A分子的碳原子数应为四种组合可填表

组合编号A的分子式B的分子式A和B的体积比(VA∶VB)(1)CH4C3H61∶3 (2.5130.51.5=13)(2)CH4C4H81∶1 (2.5141.51.5=11)(3)C2H6C3H61∶1 (2.5230.50.5=11)(4)C2H6C4H83∶1 (2.5241.50.5=31)

ΔV=(1+9)×6.25%=0.625(L)


ΔV2=0.5(L)(增加)

ΔV3=0.5(L)(增加)

ΔV4=1(L)(增加)
第一组合:
不是此题答案.
第二组合:
不为此题答案.
第三组合:
不是此题答案.
第四组合:
为此题答案.
故A分子式C2H6B分子式C4H8.
解Ⅱ

1 L
1 L (1 + 9)×6.25%(L)
故化学式为C2.5H6.5只有两种组合CH4
C4H8或C2H6
C4H8

分析CH4

C2H6

故A分子式为C2H6B分子式C4H8
三、通过讨论法解题确定混合物的组成
例4 常压120℃将1 L CO和某烯烃组成的混合气体与11L过量的氧气混合, 经点燃充分反应, 再恢复到原状态时, 测得气体的总体积为12L, 试确定烯烃的分子式及其所占的体积百分含量.
解此题如按一般设未知数列方程法求解显然是不可取解题方法(因为已知条件不充足), 所以应对题目做认真剖析找到解题突破口.
依据题意, 反应前气体总体积V前=1L+11L=12L, 反应后气体总体积V后=12L, 因此反应前后气体体积不变.


利用差量法解题, 设烯烃气体体积为x,则


x
x(0.5n-1)

2 L 1 L 2 L 2+1-2 L=1 L

由于反应前后体积不变 故ΔV减少=ΔV增加

讨论:烯烃为气态,则2≤n≤4.
故n=2x=1(不合理, 烯烃气体体积为1L, CO气体体积为0, 此种情况不会形成反应前后体积不变)

故若烯烃为C3H6时, 所占体积为50%.


