WHO 植物药专论解析
张晓群, 熊 晏, 黄倩倩, 陈 杨, 邹文俊, 瞿礼萍
(成都中医药大学药学院,四川 成都610041)
在崇尚绿色、回归自然的世界潮流下,随着化学药品研制成本高、医药费用贵、不良反应不断出现等问题,人们呼唤回归自然,希望使用天然药物治疗和保健,植物药在全球范围内日益受到关注和重视[1-2]。多个国家和地区在制定植物药管理法规的同时,也建立了相应的标准或专论以确保植物药的质量与安全有效性[3]。 《美国药典》、 《欧洲药典》 等收载的药典专论对植物药质量控制方面做出了基本要求;欧盟草药药品委员会(HMPC)、欧洲植物药疗法科学合作组织(ESCOP) 等亦针对植物药安全性、临床应用或有效性方面制定了相应专论[4-7]。而WHO 植物药专论则是WHO 应其成员国要求,科学评价并制定的涵盖植物药安全性、有效性(或临床应用)、质量控制这三大方面相关内容的专论。该专论的制定发布有效促进了包括中国、美国、欧盟、日本、印度等196 个成员国之间植物药技术领域的信息交流,其重要性得到了WHO 成员国的广泛认可,欧盟、加拿大等将WHO 植物药专论作为植物药质量评价、临床应用、安全性等方面的权威参考,巴西、马来西亚、墨西哥、越南、缅甸等多个国家更是直接参考WHO 植物药专论制定了本国专论[8]。
WHO 植物药专论自第一版发布至今已有19 年,但国内学者对此关注甚少,且尚未见相关报道。本研究拟通过系统解析WHO 植物药专论的背景与目的、制定流程、基本内容,并分析其特点,以期为我国编制相应“中药专论” 提供参考,助推中药国际化发展。
1 制定背景与目的
从20 世纪80 年代起,医学界开始认识到化学药品的局限性和不良反应,植物药在全球范围逐渐受到关注和重视,但当时各国一直缺乏植物药立法管理与相关技术规范。1986 年在东京召开的第四次国际药品监管当局会议(ICDRA) 中,各成员国建议WHO 制定植物药目录,为各国普遍使用的植物药制定相应国际规范。在此背景下,WHO 于1997 年率先发布了“草药评估指南”,为各成员国监管部门、科研机构和制药企业提供评价植物药质量、安全性和有效性(或临床应用) 的重要依据。此后于1999 年首次完成对28 个植物药的评价,制定发布了第一卷植物药专论;后续又相继于2003 年、2007 年、2009 年发布了第二至四卷,分别制定了30、31、28 个植物药专论。随后,2010 年WHO 还针对1991 年前苏联解体后形成的新独立国家(NIS) 常用的30 种植物药制定发布了NIS 植物药专论,其中,有17 个品种为前四卷已评价过的植物药。因而,目前WHO 合计完成了130 个植物药专论的制定。WHO 植物药专论制定的历史发展背景参见图1。需要特别说明的是,WHO 制定植物药专论的目的主要是促进各成员国之间植物药技术领域的信息交流,为监管部门、医生、药剂师、制药企业等提供植物药质量、安全性和有效性(或临床应用) 的重要科学依据和参考,但它不是药典专论,并不具有法律效力和强制性。
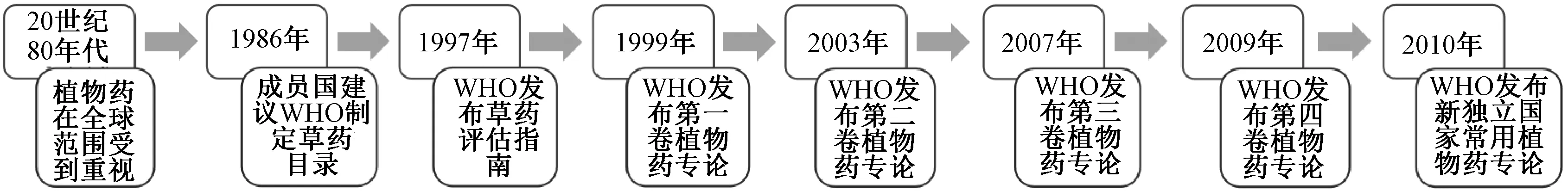
图1 WHO 制定植物药专论的历史发展背景
2 制定过程
WHO 植物药专论的制定涉及植物药遴选、专论评价、草拟制定及发布等基本流程[9],其核心是对植物药相关资料进行全面收集和科学评价,并实施内外部审评的过程。WHO 首先内部成立传统医学专家咨询小组,并在全球范围内遴选广泛使用的植物药品种。入选的植物药品种有2 个必要条件,一是至少在2 个WHO 成员国或地区中普遍使用,二是有充足的资料和数据用于评价[10]。植物药品种遴选完成后,WHO 传统医学专家咨询小组进一步系统收集相关资料或科学数据,如临床研究、系统评价、综述、各国家或地区官方药典及其他参考书籍和资料。在充分收集上述资料的基础上,由WHO 传统医学合作中心进行内部评价和讨论,之后根据讨论结果起草专论的草拟稿。在此之后,将面向传统医学专家咨询小组、国际药典与药物制剂专家咨询小组、药物评估与国家药物政策专家咨询小组等WHO下设的专家团体,以及WHO 各成员国药品监管部门的相关专家广泛征集科学意见。从目前发布的4 卷植物药专论来看,第一卷专论草拟稿征集了来自40 余个国家和地区的专家意见,第二卷专论增至超过50 个国家和地区,第三和第四卷参与专家分别来自65、81 个国家或地区,总人数超过100 人,到NIS 常用植物药专论更是有99 个国家的250 多个专家参与了草拟稿的意见征集。植物药草拟稿完成意见征集后,WHO 将再次召集专家和药品监管部门相关人员对纳入的草拟稿作进一步专家咨询和讨论,最后根据讨论结果决定是否发布专论。WHO 植物药专论的主要制定流程,见图2。
3 基本内容
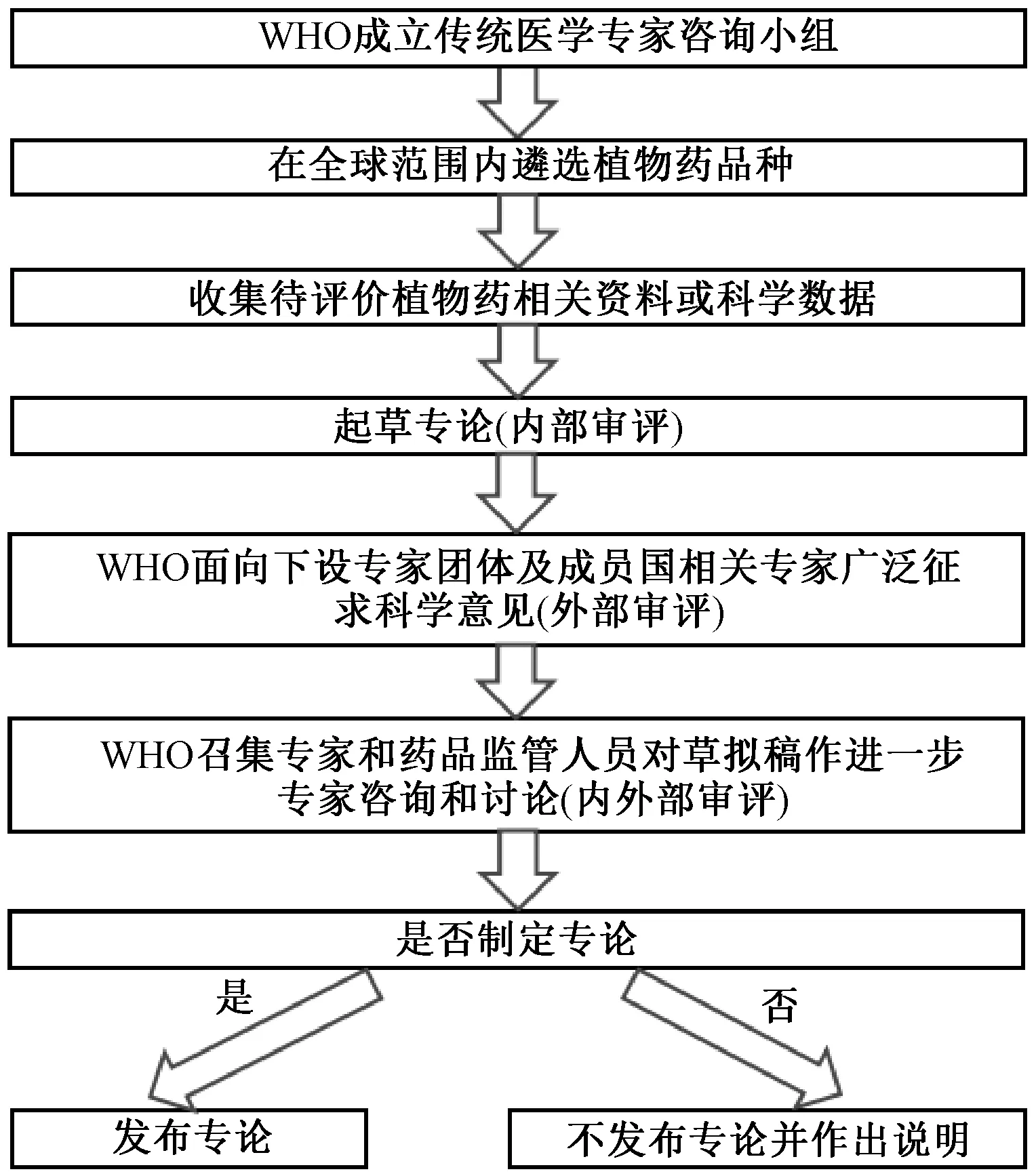
图2 WHO 植物药专论制定流程
WHO 植物药专论基本内容涉及药学、药理、毒理及临床应用等各个方面,具体项目按照编写顺序包括植物药的基源、异名、部分俗名、地理分布、植物形态、药材特征(包含药用部位、外观、感官特性、组织显微特征和粉末显微特征)、常规鉴别(理化性质鉴别、薄层色谱鉴别等)、纯度检验(包括微生物学、有机杂质、总灰分、酸不溶性灰分、水溶性浸出物、醇溶性浸出物和干燥失重)、主要化学成分、药理学(包含实验药理学、临床药理学)、临床应用(临床研究数据支持的用途、药典或国家处方集等记载的用途、传统医学中记载的用途)、毒理学、农药残留、重金属、放射性物质残留、不良反应、禁忌症、警示、注意事项(如致癌、致畸、致突变、生殖损害、药物相互作用、针对哺乳期母亲及儿童的说明等)、剂型、剂量和参考文献。可以看出WHO 植物药专论中记载的植物药相关内容详实,涉及了植物药质量、有效性(或临床应用) 和安全性这三大药品基本属性的详尽信息和相关数据。
自1999 年第一卷植物药专论面世,WHO 共计发布5卷专论,涉及了130 个全球范围内常用的植物药品种。经进一步比较发现,其科、属、种及药用部位均与2015 年版《中国药典》 所收载中药完全相同的有41 种,见表1,包括了黄芪、鸦胆子、柴胡、肉桂、黄连、麻黄、人参、甘草、大黄、桔梗、穿心莲、当归、黄芩、苦杏仁、厚朴等常用中药。为便于读者理解WHO 专论基本内容,以当归为例,比较WHO 植物药专论和《中国药典》 收载的具体内容,在质量控制方面,二者均收载了基源、性状、鉴别、检查(包括水分、灰分、酸不溶性灰分等) 及含量测定等项,除此之外,WHO 植物药专论还收载了《中国药典》 未有涉及的农药残留、重金属、放射性物质残留等内容。在有效性(或临床应用) 与安全性方面, 《中国药典》 主要记载为当归的性味与归经、功能与主治等中医理论相关信息,其配套书籍《中国药典临床用药须知》 补充收录了当归的效用分析、配伍应用、鉴别应用、方剂举隅、成药例证、本草摘要、药理毒理等内容。而WHO 植物药专论是以评价临床研究文献、各国专论与药典及民间医学资料等为基础,记载当归在治疗月经不调、闭经和痛经、风湿性关节炎、腹痛及手术后疼痛、便秘及贫血等方面的临床用途。同时,WHO 植物药专论亦收录了当归实验药理学、临床药理学、毒理学、不良反应、禁忌症、警示等内容。相较于《中国药典》,WHO 植物药专论记载当归的内容更为全面详实,对临床的指导意义更大。
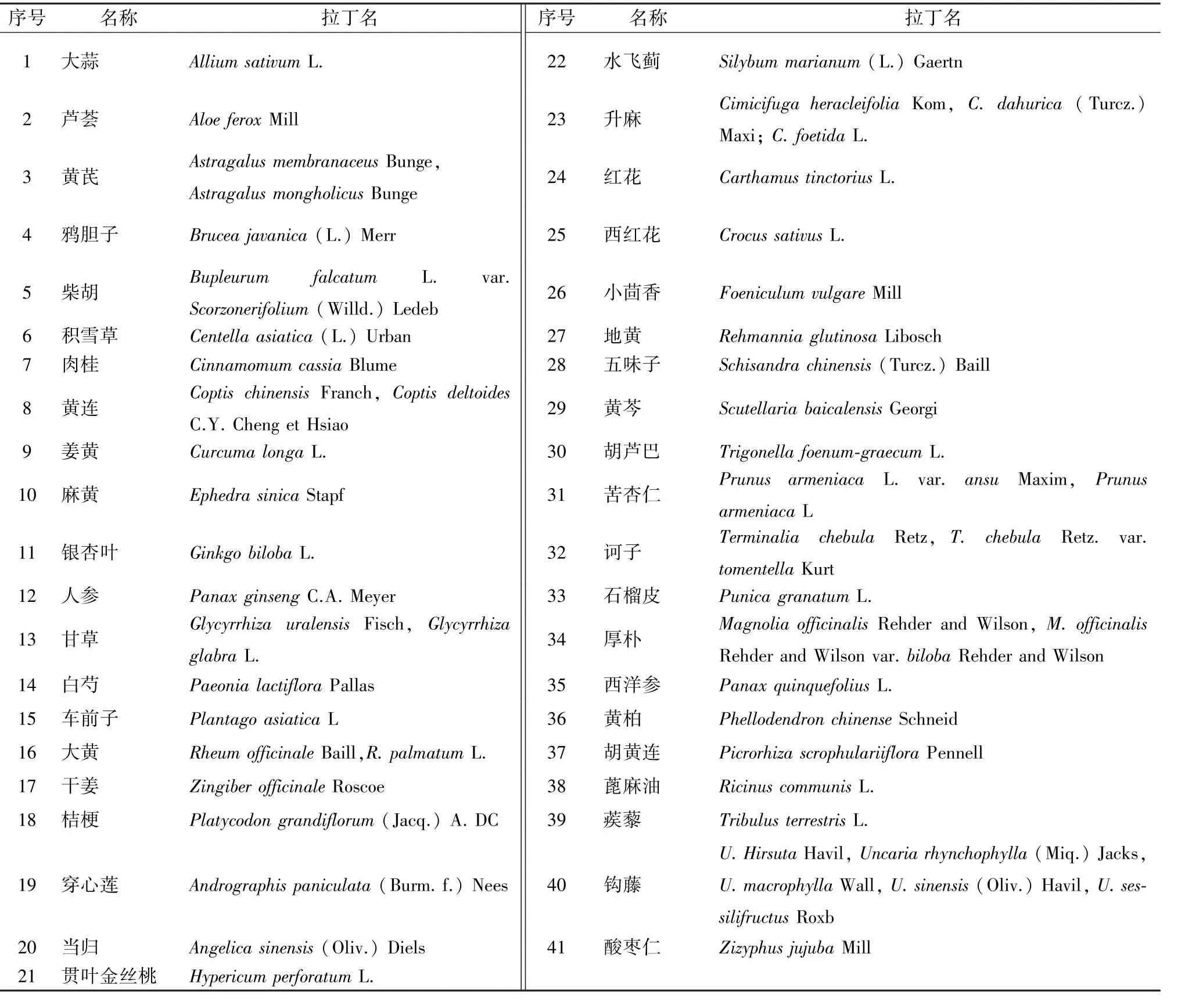
表1 WHO 植物药专论与2015 版《中国药典》 共同收载的中药品种
4 特点分析
4.1 评价制定过程科学严谨 WHO 植物药专论的整个制定过程中,从资料收集、评价到草拟稿和正式专论公开发布,都是科学规范和相对公开透明的。首先,WHO 在全球范围内遴选植物药品种并全面收集相关科学资料和数据,为评价植物药过程奠定了良好的基础。其次,在评价制定植物药专论的过程中,最初由WHO 专家进行内部评价,在此之后还将广泛征集WHO 其他多个相关专家组和各成员国药监部门专家意见进行外部评价,最后WHO 联合各国专家进行内外部研究讨论并公开评价结果。整个WHO植物药专论制定过程中有效结合了内部评价、外部评价及内外部评价相结合的方式。同时,随着第一卷植物药专论的发布,其受关注程度和国际影响力逐渐凸显,其后每卷专论的制定过程中,参与专家人数及药监部门相关人员的数量都有所增加。1999 年发布的第一卷专论制定过程中,有来自40 个国家的100 位专家参与,而到2010 年发布的NIS 常用植物药专论,参与的专家已增至来自99 个国家的256 名。参与评价植物药专论的专家不仅涉及WHO 下设传统医学咨询小组和其他相关专家组,还包括了WHO 各成员国药品监管部门的多个专家。整个参与制定专论的专家人数充足,涉及专业领域广泛,有效保证了专论制定过程的科学性和严谨性。
4.2 信息与数据 目前,全球范围内已制定多种植物药或中药的相应标准或专论,如以《美国药典》 《英国药典》《日本药局方》 《印度阿育吠陀药典》 《越南药典》 等国家药典为代表的药典专论主要收载植物药质量控制的相关要求,而欧盟草药专论、德国植物药专论等则主要收载有关植物药安全性、有效性 (或临床应用) 相关内容[11-13]。《中国药典》 在对中药材及饮片质量相关内容进行要求和规定的同时,虽然也涉及中药性味与归经、功能与主治、用法与用量、注意事项、规格及贮藏等信息,但内容有限。此外,为了进一步规范临床用药,国家药典委员会同时编撰了《中国药典》 的配套书籍《中国药典临床用药须知》,对中药效用分析、配伍应用、鉴别应用、方剂举隅、成药例证、本草摘要、药理毒理等信息进行了补充,对指导临床合理、安全、有效用药发挥了一定作用。但仍存在不足和局限性,如其虽然涉及到中药的安全性相关内容,但主要为毒理学研究综述,缺乏对临床不良反应的分析,临床使用注意事项亦过于简单。而WHO 植物药专论除了详细的质量控制相关内容外,还系统评价了各类文献与科学数据,详细记载了药物临床应用、实验药理学、临床药理学等内容,并将相关安全性内容单列为不良反应、临床禁忌症、警告、药物相互作用等项,形成了包含质量、安全性与有效性(或临床应用) 三大方面的全面的内容体系,对临床合理用药具有重要的指导价值。
4.3 分类评价 WHO 评价植物药临床应用的支撑证据包括3 个类别或级别[14],一是临床研究数据,如随机对照双盲试验、队列研究等;二是官方药典或专论,如《中国药典》 《英国草药典》 《印度阿育吠陀药典》 等;三是传统应用相关证据,如非官方药典或其他文献记载等。依据以上证据类别的不同,WHO 将植物药的临床应用分为“临床数据支持的用途” “药典或国家处方集等记载的用途” “传统医学中记载的用途” 三类。以姜黄为例,WHO 植物药专论中其临床应用项下涉及胃肠道疾病、疼痛、皮肤病、妇科疾病等多种疾病领域[15]。其中,胃肠道疾病中的胃酸分泌过多、胃肠胀气、消化不良等适应症,是基于对德国委员会专论、随机双盲对照临床研究等证据的评价;胃肠道疾病中的消化性溃疡和腹泻,即是基于对《中国药典》、消化性溃疡研究报告等资料的评价;其余临床应用,如皮肤病、痛经、闭经、癫痫、类风湿性关节炎引起的炎症反应及疼痛等均是基于《中国药典》 《非洲药用植物手册》 《越南药用植物》 《中药药理学与应用》 等资料的评价。特别说明的是,对于传统医学记载的用途中收载的癌症、艾滋病、肝炎等一些严重疾病,WHO 认为其属于现代医学范畴的术语,规定必须在具备药理学证据或充分的民族药理学研究报告的情况下才能收载。同时,也基于这类临床应用缺乏临床试验数据支撑,每卷WHO 植物药专论亦明确指出植物药的传统医学中记载的用途因缺乏科学数据,其临床应用过程中应当根据治疗方案慎重使用。总体而言,WHO 依据评价资料支撑证据的不同,分类评价和收载植物药的临床应用,其分类依据科学,在严格评价科学数据的同时,也认可传统应用证据。考虑包括中药在内大多传统药物都缺乏现代流行病学条件下的临床研究数据,因此WHO 植物药专论对此类药物的评价方法值得借鉴。
5 结论
第一版《中国药典》 及其配套书籍《中国药典临床用药须知》 分别出版于1953 年与1990 年,目前已更新至2015 版,为中药质量保证及临床安全用药提供了权威性规范和指导,但仍存在内容和资料评价不够全面等不足。同时,我国还出版了多个大型中药学工具书,如1975 年9 月出版的《全国中草药汇编》 (2014 年更新至第三版)、1999年10 月出版的《中华本草》、1977 年7 月出版的《中药大辞典》 (2006 年更新至第二版) 等,对中药鉴别与临床合理用药等亦具有重要的指导意义。但此类专著是作为一般性工具书,主要供我国医药研究者及工作者参考使用。总体而言,目前我国尚缺乏内容全面、经规范化评估程序编写的与国际接轨的中药专论。
WHO 植物药专论不仅为药品监管部门、医生、药剂师、制药企业提供了植物药质量、安全性、有效性或临床应用等多个方面的重要科学依据和参考,而且为各成员国制定本国专论提供了模板和基础,欧盟及包括加拿大在内超过13 个国家将其用作植物药技术领域的权威参考,巴西、墨西哥等超过46 个国家参考专论或直接以其为基础制定了本国植物药专论,促进了各成员国在植物药技术领域的信息交流,有利于植物药临床的合理使用。本研究系统分析后发现,WHO 植物药专论制定过程科学严谨,涵盖植物药质量、安全性与有效性(或临床应用) 三方面,内容全面、详实。尤其对于植物药临床应用的评价和记载,不仅依据科学研究文献与各国药典专论等对植物药的临床应用进行评价,分别收载为临床数据支持的用途与官方药典或专论记载的用途,也认可植物药的人用证据或民间医学资料,将其归为传统医学记载的用途。我国中药具有几千年的使用历史,但往往因缺乏现代流行病学条件下的临床数据支持而使得发展受阻。在当前《中华人民共和国中医药法》 提出坚持继承与创新结合的中医药发展方针背景下,WHO 分类评价和收载植物药临床用途的方式十分符合包括中药在内的传统药物的特点,对于中药的传承、创新发展思路具有重要参考价值。因此,无论从维护和提升我国在全球植物药领域重要地位角度出发,还是为规范我国中药在安全性、有效性和质量控制方面的技术协调、促进中药的传承与创新,建议我国政府相关部门或研究机构在考虑中药自身特殊性的基础上,借鉴WHO 植物药专论的评价与制定模式对我国临床常用的中药品种进行系统科学评价,尽早建立中国的“中药专论”,不仅有利于更好指导中药在全球范围内更加安全有效用药,也将有力推动和促进中药国际化发展。

