铅锌矿物冶金还原过程相态演变与特性述评
罗立群,郑波涛,魏晨曦
(1.武汉理工大学资源与环境工程学院,湖北 武汉 430070;2.矿物资源加工与环境湖北省重点实验室,湖北 武汉 430070)
铅锌是重要的有色金属,金属铅及其化合物可应用于铅酸蓄电池、汽油添加剂、电缆、化工设备、各种合金等[1];金属锌及其化合物在高性能合金、电池材料、机密仪器及微电子工业等领域有着广泛应用[2]。我国已成为世界上最大的铅锌生产和消费大国,其铅锌冶炼产量也迅速增长[3]。铅锌在炼铁过程中为有害杂质,而我国的铁矿石因地域产出或资源综合回收缘故,很多不同程度地含有铅锌杂质。赋存于铁矿中的铅锌影响铁精矿的品级,严重影响高炉寿命与炼铁效益[4-5]。铅高密度、低熔点、易挥发并有毒,易形成含铅沉淀,对高炉冶炼产生不利影响[6];锌因其密度小、化学性质活泼等特性在高炉内外形成双重循环,导致锌在炉料、炉衬及附着物中大量沉积,加剧高炉内外锌负荷[7]。
铁矿中铅-锌-铁嵌布关系复杂、颗粒微细,高温时矿相多变难以去除,因此,通过分析炼铁过程中铅锌杂质的产出与赋存状态,阐述铅锌矿物在冶金还原过程的工艺,归纳铅锌矿物在冶金还原过程中的相态演变,分析铅锌矿物在炼铁过程中的转化特征,有利于掌握铅锌高温还原过程的变化特性和控制含铁原料中的铅锌技术,为控制含铁原料铅锌杂质提供理论支撑,并推动铅锌综合利用的水平。
1 铅锌的产出与赋存状态
有色冶炼过程中的铅锌主要来源于方铅矿(PbS)、闪锌矿(ZnS)等铅锌硫化矿,部分为氧化矿,如:白铅矿(PbCO3)、红锌矿(ZnO)、菱锌矿(ZnCO3)等[8-9]。其资源显著特点是铅锌共生,一般为方铅矿与闪锌矿依附共存。炼铁过程中铅锌的来源有:自然铅锌矿物、含铅锌铁矿石、烧结矿和球团矿中的铅锌以及含锌(铅)粉尘等[6-15],炼铁过程中典型铅锌杂质的产出和赋存状态见表1。
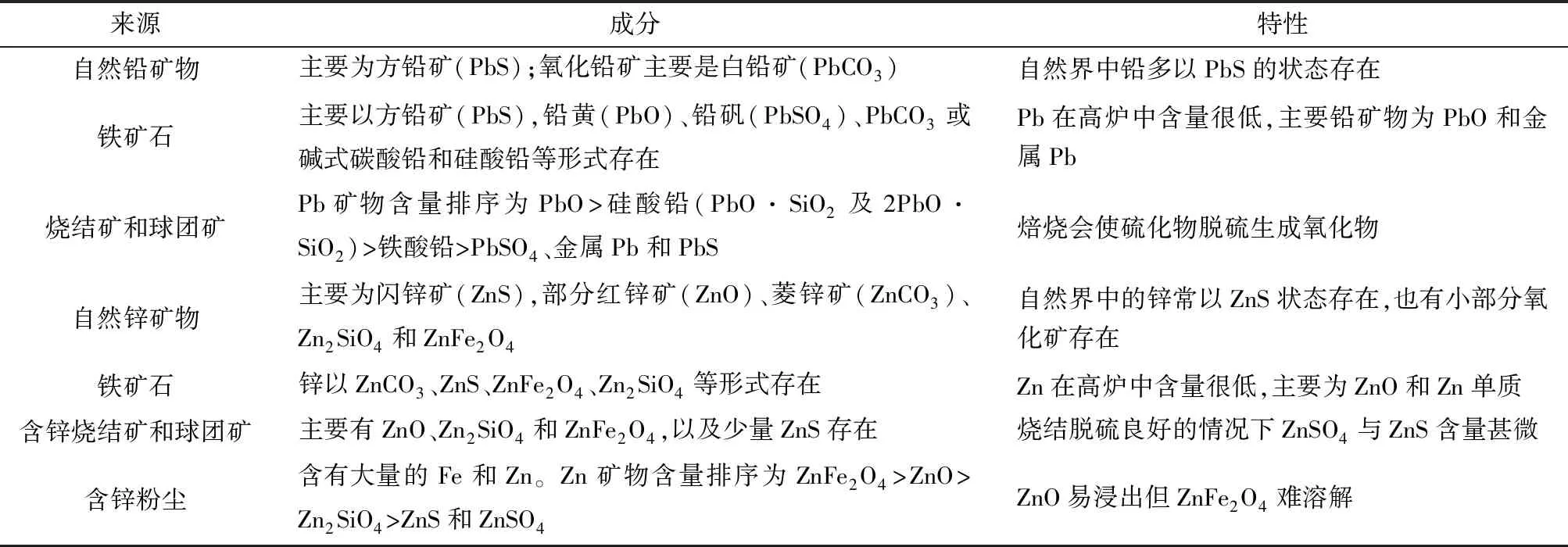
表1 铅锌的产出与赋存状态Table 1 Output and occurrence status of lead and zinc elements
1.1 铅产出
铅来源于自然铅矿物、含铅铁矿石以及含铅烧结矿和球团矿中。自然铅矿物通常以方铅矿(PbS)、铅矾(PbSO4)等硫化矿状态存在,也有小部分呈氧化矿存在,主要是白铅矿(PbCO3)[8]。
铁矿石中铅多以方铅矿(PbS),铅黄(PbO)、铅矾(PbSO4)、PbCO3或碱式碳酸铅和硅酸铅(PbO·SiO2及2PbO·SiO2)形式存在,且以氧化物为多[6];以碳酸盐、硫酸盐或硅酸盐形式存在的含铅矿物,入炉后很快分解成PbO或金属Pb[8],Pb在高炉中含量一般在0.2%~1%[10]。
烧结矿和球团矿中铅矿物主要有PbO、硅酸铅、PbO·Fe2O3、以及少量PbSO4、金属Pb和PbS[10]。焙烧会使铅精矿中的硫化物脱硫生成氧化物,且熔剂中的造渣组分(SiO2、CaO、Fe2O3)也会与PbO、PbS、PbSO4反应生成铅的铁酸盐和硅酸盐[5]。
1.2 锌产出
锌的产出可分为4类:自然锌矿物、含锌铁矿石、含锌烧结矿和球团矿以及含锌粉尘。自然锌矿物常以闪锌矿(ZnS)等硫化物状态存在,小部分以氧化矿形式存在,主要为红锌矿(ZnO)、菱锌矿(ZnCO3)、硅锌矿(Zn2SiO4)、ZnFe2O4和异极矿[Zn4(Si2O7)(OH)2·H2O]等[9,11]。铁矿石中锌含量一般低于1%,除极少量闪锌矿(ZnS)等含锌硫化矿物,以锌铁氧体、碳酸盐或硅酸盐形式存在的含锌氧化矿物入炉后高温下能很快还原分解成ZnO,甚至Zn单质[12]。烧结矿和球团矿中Zn多以ZnFe2O4、Zn2SiO4和ZnO状态存在,在烧结脱硫良好的情况下ZnSO4与ZnS在烧结块中含量甚微[13,16]。高炉含锌粉尘含有大量的Fe和Zn,其中锌主要以易浸出的ZnO、难溶解的ZnFe2O4、低熔点的Zn2SiO4及少量ZnS和ZnSO4的状态存在,且ZnFe2O4含量较高,一部分粉尘还含有C、Pb、K、Na、Ga和Ag等其他元素[17]。
含铁原料中与Zn共存的铁主要以Fe3O4、Fe2O3、FeO和ZnFe2O4的形式存在[18]。难以利用的尖晶石类物质ZnFe2O4,其氧离子呈紧密堆积状态,晶格具有较大的稳定性,一般酸浸难于溶出,难以实现铁锌分离[19]。采用还原焙烧方法,经磁选、酸浸或碱浸过程[20-22],分离回收锌和铁是可行的[23]。
2 铅锌冶金还原工艺与特征
2.1 铅锌冶金还原工艺现状
铅锌矿物冶金还原工艺的原理有:①通过氧化焙烧将铅锌硫化物转化为氧化物,而后利用碳质还原剂将PbO、ZnO分别转化为Pb液和Zn蒸汽;②高温还原条件下,使ZnO和ZnFe2O4被还原气化成Zn蒸汽;③利用PbS易与PbO和PbSO4发生交互反应直接生产金属铅。据此,可将铅锌冶金还原工艺分为火法炼铅、火法炼锌和含锌粉尘火法回收3种,铅锌冶金还原工艺技术特征见表2。
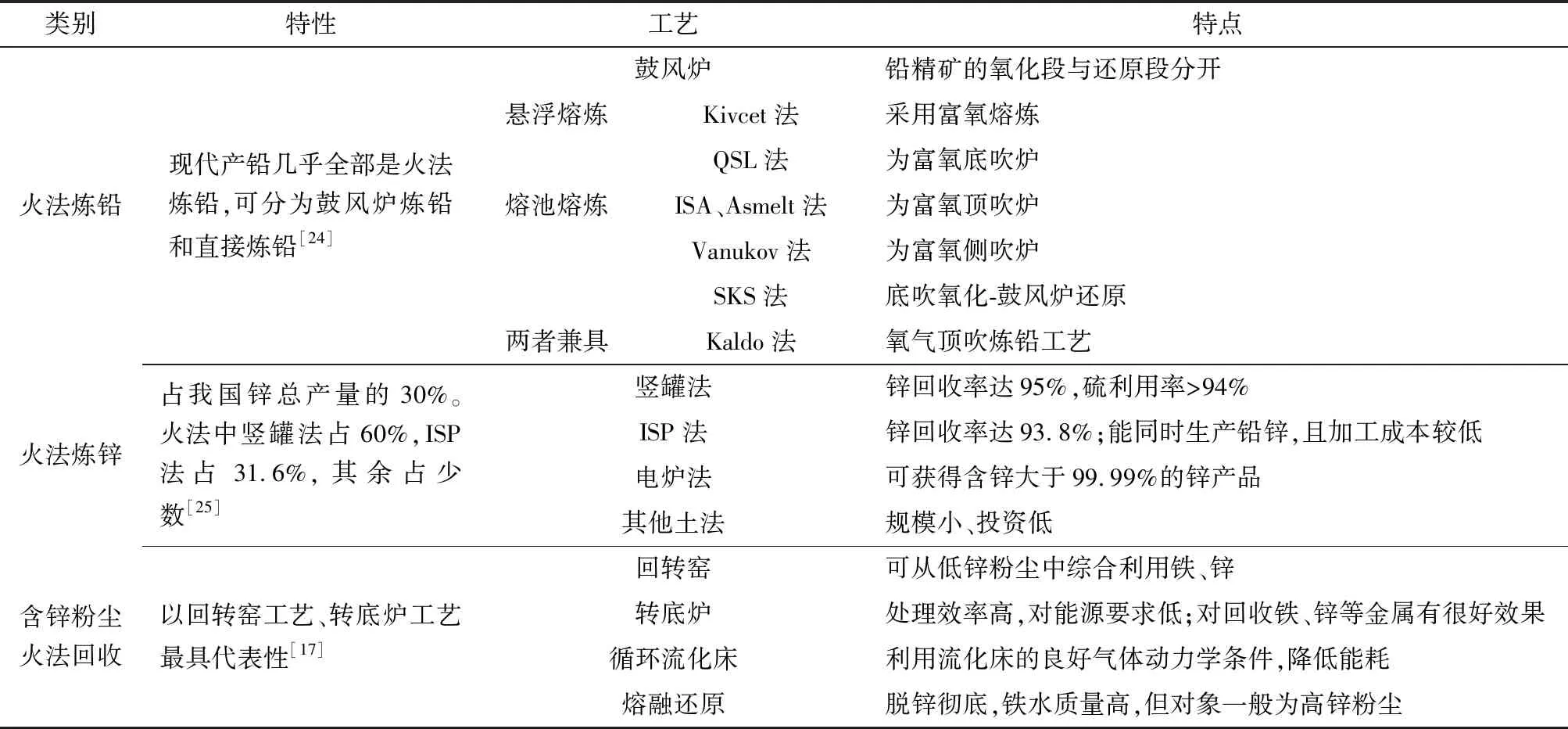
表2 铅锌冶金还原工艺技术特征Table 2 Technical characteristics of lead-zinc metallurgical reduction process
2.1.1 火法炼铅
鼓风炉还原熔炼仍是火法炼铅主流,目前世界上矿产铅中80%仍采用烧结-鼓风炉熔炼流程。其原理是在烧结焙烧阶段将精矿中PbS和其他金属硫化物氧化,而后利用焦炭作发热剂和还原剂将PbO还原成Pb液[24]。Pb液气化成Pb蒸汽经挥发、分离,然后氧化、富集从而回收铅。其缺点是S利用率低、铅蒸汽和含铅粉尘污染环境、消耗大量热能等。
通过对Pb—S—O系化学势图的研究,直接炼铅技术有了长足发展。直接炼铅法是PbS精矿不经烧结焙烧而直接熔炼生产金属Pb的冶炼方法。其特点有[26]:①充分利用PbS精矿的化学活性和氧化热;②采用富氧鼓风使化学反应和熔化过程很快进行;③将氧化和还原过程在一个单独的炉内分阶段进行,或在两个炉内分开连续进行。直接炼铅法并未解决炼铅过程中固有的问题,如制酸尾气和含铅逸出物的污染;且由于铅及其各种化合物的挥发性很强的特点,例如PbS在600 ℃时已开始挥发,PbO在空气中800 ℃时便显著挥发,故没有得到迅速应用。
2.1.2 火法炼锌
火法炼锌是将锌精矿进行氧化焙烧使ZnS变为ZnO,再通过碳质还原剂将ZnO还原,利用锌的低沸点(907 ℃),高温下获得锌蒸汽,冷凝收集后精馏获得金属锌锭[27]。其主要缺点是劳动生产率低,烧结过程的SO2及粉尘污染严重,故逐渐被湿法炼锌所取代。
2.1.3 含锌粉尘火法回收
含锌粉尘火法回收按还原方式不同可分为直接还原法和熔融还原法[17]。直接还原法基本原理是将ZnO和ZnFe2O4在高温还原条件下呈金属蒸气排出,使锌与渣固相分离[28]。熔融还原法指在熔融状态下将粉尘中的ZnO或ZnFe2O4进行还原、分离、氧化富集。利用回转窑的工艺有川崎法、waelz法、SL/RN法、SDR法等,目前waelz法应用最广泛。
2.2 含铅矿物还原
PbS为火法炼铅的主要原料,其还原非常复杂,它既能被金属Cu、Zn蒸汽、金属Fe和Na2CO3还原生成Pb液,也能与Pb的氧化物发生交互反应生成Pb液。
在700~900 ℃温度范围内,金属Cu和PbS发生置换生成Pb液和Cu2S。在1 000 ℃左右,易挥发的PbS被ZnO还原生成的锌蒸气置换[29]。PbS在1 200~1 400 K温度下进行烧结焙烧,可生成金属铅和SO2烟气,还可被炉气中的O2氧化生成PbO。在1 250 ℃时,Fe也可置换PbS中的Pb。PbS还可被Na2CO3还原成Pb蒸汽,热力学计算表明其自发发生的最低温度为1 429 ℃[1]。在1 050~1 100 ℃温度范围内,PbS易与Pb的氧化物发生交互反应,即将PbS部分氧化为PbO和PbSO4,与PbS相互反应,这一特性广泛应用于直接炼铅中[30],基本反应见式(1)和式(2)。
PbS(s)+2PbO(s)=3Pb(l)+SO2(g)
(1)
PbS(s)+PbSO4(s)=2Pb(l)+2SO2(g)
(2)
Pb的碳酸盐热分解是伴随着数种中间产物的连续分解生成PbO的过程。PbSO4开始分解为PbO的温度为750 ℃,而激烈分解的温度为950 ℃[23]。PbSO4能被C或CO还原生成金属铅,PbO和PbS。700~800 ℃时硅酸铅(PbO·SiO2及2PbO·SiO2)就开始融化分解出PbO和SiO2,游离出来的PbO再被还原成金属Pb[31]。1 000℃以下PbO·Fe2O3就可融化分解出PbO。金属Fe可将PbO还原出Pb液[32],天然存在的PbO以及含铅矿物氧化、还原、分解生成的PbO,碳热或CO还原是火法炼铅和高炉炼铁中铅循环的主要反应,见式(3)和式(4)。
PbO(s)+C(s)=2Pb(l)+CO(g)
(3)
PbO(s)+CO(g)=Pb(l)+CO2(g)
(4)
添加氯化剂如CaCl2进行氯化还原焙烧使PbO在高温氯化条件下转化为低沸点和挥发性较强的铅氯化物,即形成PbCl2蒸汽而回收[33]。含铅矿物还原过程中铅的迁移富集变化如图1所示。

图1 含铅矿物还原的迁移富集变化Fig.1 Migration and enrichment changes in reduction of lead-bearing minerals
2.3 含锌矿物还原

ZnFe2O4(s)+C(s)=
ZnO(s)+2FeO(s)+CO(g)
(5)
3ZnFe2O4(s)+C(s)=
3ZnO(s)+2Fe3O4(s)+CO(g)
(6)
3ZnFe2O4(s)+CO(g)=
3ZnO(s)+2Fe3O4(s)+CO2(g)
(7)
ZnFe2O4(s)+CO(g)=
ZnO(s)+2FeO(s)+CO2(g)
(8)
ZnFe2O4被CO还原成Fe3O4和ZnO在400 ℃就可发生,此时发生了反应见式(7)。ZnFe2O4在650 ℃分解为Fe3O4和ZnO,此时发生了反应见式(6)和式(7)。随着温度升高,ZnFe2O4颗粒表面ZnO逐渐增多,当温度大于850 ℃,此时发生了反应见式(5)和式(8),FeO产生且FeO部分还原成单质铁析出。当温度达到950 ℃时,ZnFe2O4可完全还原为单质铁。
热力学计算表明ZnSO4分解为ZnO和SO2的温度为1 194.2 K,ZnSO4还可被C或CO还原成ZnS。当温度为700~950 ℃,Zn2SiO4分解过程有两个反应步骤:Zn2SiO4分解为ZnO、SiO2;ZnO还原成Zn蒸汽[23]。ZnCO3低温下受热就可完全分解生成ZnO[37]。碱式碳酸锌[2ZnCO3·3Zn(OH)2]在大气中的热分解是一步完成的,且符合随机核化机理。在220~260 ℃间,热分解会产生ZnO、气态CO2和H2O[38]。
ZnO的还原剂有C、CO、CH4、H2、Fe等,其主要还原剂还是C和CO[13,32]。天然存在的ZnO以及含锌矿物氧化、还原、分解生成的ZnO,经碳热或CO还原是火法炼锌、含锌粉尘综合利用和高炉炼铁中锌循环的主要反应,见式(9)和式(10)。
ZnO(s)+CO(g)=Zn(g)+CO2(g)
(9)
ZnO(s)+C(s)=Zn(g)+CO(g)
(10)
与PbO的氯化还原焙烧类似,将ZnO转化为低沸点和挥发性较强的锌氯化物,即高温氯化形成ZnCl2蒸汽而回收[39]。含锌矿物还原过程中锌的迁移富集变化如图2所示。

图2 含锌矿物还原的迁移富集变化Fig.2 Migration and enrichment changes of reduction of zinc-bearing minerals
3 炼铁过程中铅锌的还原
炼铁过程中铅锌相态复杂,铅多以氧化物(PbO)、硅酸盐(PbO·SiO2及2PbO·SiO2)、碳酸盐[PbCO3或2PbCO3·Pb(OH)2]和硫酸盐(PbSO4)的形式而锌常以氧化物(ZnO)、ZnFe2O4、硅酸盐和碳酸盐的形式存在于高炉炼铁过程中。
3.1 炼铁过程中铅的还原
PbO碳热还原的理论反应起始温度为555 K[40],PbO在CO气氛中极易反应生成金属铅,其还原反应在377~457 K时可开始,在573~673 K时剧烈进行[5]。PbO还原是放热反应,升高温度不利于PbO的还原且其所需的CO浓度越大[29]。硅酸铅(PbO·SiO2及2PbO·SiO2)在冶金还原过程中可热分解生成PbO和SiO2。金属Fe也能将PbO还原成铅液。
PbCO3在空气中的热分解是PbCO3·2PbO(200~300 ℃)→红色α-PbO(300~370 ℃)→Pb3O4(400~450 ℃)→黄色β-PbO(500 ℃以上)的转变[41]。而陶冬平[42]认为PbCO3在空气中的热分解中间产物只有两种,254 ℃生成PbCO3·PbO,270 ℃生成PbCO3·2PbO且中间产物Pb3O4不会生成。
PbCO3的真空热分解是PbCO3·2PbO→PbCO3·2PbO的中间产物,再完全变为α-PbO(分解温度从310 ℃升至490 ℃)→α-PbO转变为β-PbO直至完全(580 ℃)的连续物相转变[43]。而碱式碳酸铅的热分解可分为[44]:①2PbCO3·Pb(OH)2在218~266 ℃内分解为2PbCO3·PbO;②在266~370 ℃内分解为PbCO3·2PbO和PbCO3·PbO;③在370~421 ℃内生成PbO。
PbSO4能热分解生成PbO,其分解是吸热反应,随着温度升高,硫酸盐将变得越来越不稳定,有利于铅的硫酸盐向着生成PbO的方向逐级分解,最后生成稳定的PbO。且PbSO4能被C或CO还原分别生成金属铅,PbO和PbS。常压条件下C直接还原PbSO4生成金属铅、PbO和PbS的理论临界温度分别为737 K、829 K和532 K[45]。PbO、PbO·SiO2、PbCO3或2PbCO3·Pb(OH)2、PbSO4的还原见式(11)和式(12)。
PbCO3[2PbCO3·Pb(OH)2](s)→PbO(s)
(11)
PbO(PbO·SiO2,2PbO·SiO2,PbSO4)(s)+
C(CO)(g)/Fe(s)→Pb(l)+CO(CO2)(g)+
(PbS,SiO2)(s)
(12)
3.2 炼铁过程中锌的还原
ZnO的还原必须在强还原气氛和高还原温度(950 ℃以上)下进行。热力学计算ZnO被C还原的起始温度为1 218 K,ZnO被CO还原的起始温度为1 601 K,故C还原ZnO的反应优于CO还原[46]。由于ZnO的还原是吸热反应,升高温度有利于ZnO的还原,且提高温度和CO分压有利于锌挥发分数的提高[47]。因C可以降低ZnO的挥发温度,可通过调整还原剂C含量配比来控制整个体系的反应气氛[48]。
ZnFe2O4的冶金还原根据还原剂的不同有碳热还原和CO还原之分。ZnFe2O4碳热还原反应模型分为五个历程[49]:①0~450 s:布多尔反应开始发生,ZnFe2O4分解为ZnO及Fe2O3,且Fe2O3开始被还原生成Fe3O4;②450~900 s:Fe3O4还原生成FeO+Fe;③900~1 800 s,铁氧化合物不断还原,ZnO也被还原生成Zn蒸气;④1 800~2 700 s,ZnO完全还原挥发,铁氧化合物基本还原生成Fe和少量FeO;⑤2 700~6 300 s,FeO继续被还原,但最终产物仍包含FeO和Fe两种物相。
典型的CO还原ZnFe2O4的步骤为[25]:ZnFe2O4还原为ZnO和Fe3O4;Fe3O4失氧转变为方铁矿(Fe1-xO),1-x的值在0.83~0.95之间;Fe1-xO与ZnO固溶生成铁锌固溶体(Fe0.85-xZnxO);Fe0.85-xZnxO失氧分解生成FeO和ZnO;FeO和ZnO被还原生成单质Fe和Zn蒸汽。即:ZnFe2O4的CO还原是由ZnFe2O4→ZnO+Fe3O4→FeO+ZnO→Fe+ZnO→Fe+Zn的连续物相转变[15]。
Zn2SiO4在冶金还原过程中会热分解生成ZnO和SiO2而ZnO会被还原生成Zn蒸汽。ZnCO3和碱式碳酸锌[2ZnCO3·3Zn(OH)2]低温下热分解就可完全生成ZnO[37]。ZnO、ZnFe2O4、Zn2SiO4、ZnCO3和碱式碳酸锌[2ZnCO3·3Zn(OH)2]的还原见式(13)和式(14)。
ZnCO3[2ZnCO3·3Zn(OH)2]→ZnO(s)
(13)
ZnO(ZnFe2O4,Zn2SiO4)(s)+C(CO)(g)/Fe(s)=
Zn(g)+CO(CO2)(g)+(2FeO,SiO2)(s)
(14)
不同铅锌物料在高炉内的迁移富集变化可归纳如图3所示。
典型铅锌矿物在高炉内的规律为:①当含铅锌物料从炉口入高炉时,由于上部温度较低,不会发生铅锌的还原反应,带入的水和化学结晶水开始被蒸发;②随着炉料的下降,温度达到400~700 ℃时,发生C/CO对ZnFe2O4的还原分解,生成ZnO,此时铅锌的碳酸盐已分解完成;PbSO4开始被还原,PbO开始被C/CO还原成Pb液;③炉料继续下降达到700~900 ℃时,上述的所有反应在此区域将更为强烈地进行。PbSiO3和Zn2SiO4在此温区熔化分解游离出PbO、ZnO和SiO2,PbSO4和ZnSO4开始分解;④当温度达到900~1 300 ℃时,上述各反应均可在此区完成,ZnO被C/CO还原成Zn蒸汽也在此温区发生。PbS、PbO及PbSO4开始相互反应而形成Pb液及SO2。
4 控制含铁原料中铅锌的前沿技术
4.1 选择性还原ZnFe2O4
我国每年会产生数亿吨含锌粉尘[17],ZnFe2O4中的锌一般占原料总锌的15%左右,有时可达到50%[35]。因此对ZnFe2O4的综合利用是控制含铁原料中锌铁含量的关键,碳质还原剂还原ZnFe2O4是可行的,因其还原气氛过强使ZnFe2O4易过还原成金属铁和锌蒸汽,虽实现了锌铁分离,经济效益难以令人满意。为达到锌铁分离的目的,只需还原成Fe3O4和ZnO便可用磁选或浸出方式分离锌与铁,大幅提高经济效益。故选择性还原焙烧ZnFe2O4被越来越多的学者关注。
HSC和Factsage软件计算表明CO能将ZnFe2O4选择性还原为ZnO和Fe3O4,具有较大的自发性且提高温度可以促进反应的发生。当还原温度分别为600 ℃、700 ℃、800 ℃和900 ℃时,获得Fe3O4优势区域的CO/CO+CO2分压比范围分别为4.4%~44.5%、3.1%~38.5%、2.3%~34.1%及1.7%~30.7%。因此,ZnFe2O4选择性还原焙烧的CO/CO+CO2范围应控制在30%以下[50]。
由于ZnFe2O4的选择性还原可在600 ℃的中温和弱还原气氛下进行,故已在湿法炼锌的氧化焙烧与低酸浸出之间增加还原焙烧工序[51],充分利用氧化焙烧(900 ℃以上)的余热进行还原焙烧,将ZnFe2O4选择性的分解为ZnO和Fe3O4,同时伴生贵金属(如Ag、Ga、Pb、Mn)也被还原富集在磁选尾矿中,方便进一步回收[52]。
4.2 真空还原
为综合利用铅锌矿物,真空还原被应用控制的铅锌含量,可大幅降低ZnO和PbO还原温度,研究结果见表3[40,53]。比如:C还原反应的气压由105Pa降至102Pa时,ZnO还原反应的温度可由1 221 K降到752 K。可见与其他火法方法相比真空碳热还原处理氧化铅锌矿物具有优越性,有利于Pb和Zn的提取,但产业工艺过程和成本值得研究。

图3 高炉内铅锌物料的还原过程Fig.3 Reduction process of lead and zinc materials in blast furnace
表3 ZnO和PbO还原反应的临界温度T0与系统压强的关系Table 3 The relationship between critical temperature T0 with system pressure for reduction of ZnO and PbO
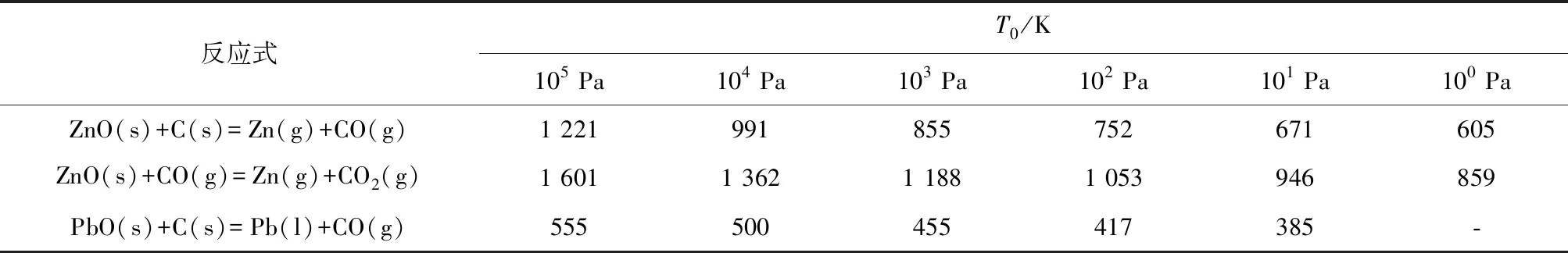
反应式T0/K105 Pa104 Pa103 Pa102 Pa101 Pa100 PaZnO(s)+C(s)=Zn(g)+CO(g)1 221991855752671605ZnO(s)+CO(g)=Zn(g)+CO2(g)1 6011 3621 1881 053946859PbO(s)+C(s)=Pb(l)+CO(g)555500455417385-
4.3 硅热还原
硅热还原工艺用于ZnO的还原在1 100~1 500 K内具有热力学上的可行性,加入CaO与SiO2造渣,抑制2ZnO·SiO2的生成,保证ZnO完全被还原成金属锌。因此Si可以作为还原剂,将ZnO还原为金属Zn[54]。
硅热还原工艺也可与真空还原工艺结合起来,真空还原可显著降低硅热还原ZnO的吉布斯自由能,随着体系压强的降低,有利于还原反应的进行。
5 结 语
铅锌元素的存在形式和铅锌矿物的产出多种多样,明确铅锌在还原过程中的相态特征和演变规律,对控制高炉炼铁和含铁物料的铅锌分离意义重大。铁矿中铅锌和含铅锌的铁物料利用须结合铅锌矿物类型和铁精矿品级确定工艺类别,合理控制焦炭用量或CO/CO+CO2分压比,精选适宜的温度范围,实现铁冶金和铅锌的高效资源化利用,拓展铅锌冶金还原的技术应用,促进节能减排。尽管铅锌的火法还原技术有多种选择且较为成熟,铅锌作为重要的有价金属,将含铁原料中铅锌的高效资源化利用已成为回收铁资源和综合利用铅锌的重要方式,并将逐渐发展成为追求经济与环境的统一与平衡。

