TTC法测定山豆根种子生活力条件的优化
(1.贵州中医药大学药学院,贵阳 550025;2.紫云自治县长萌农业科技开发有限责任公司,贵州 安顺 561000)
山豆根原植物为豆科植物越南槐(Sophoratonkinensis)[1]。山豆根为临床常用药,属清热解毒药[2]。同时,山豆根又是多种药品的原材料[3]。由于近年来市场需求逐年增大,野生资源采挖严重,各地积极开展人工种植,且无论是自然繁殖还是人工繁殖手段,都主要依靠种子[3]。种子的生活力检测是预判种子是否具有繁殖价值的重要手段,本研究采用正交试验、单因素试验和Central Composite Design响应面试验对TTC法测定山豆根种子生活力的条件进行优化,以期为后续的研究和生产提供指导。
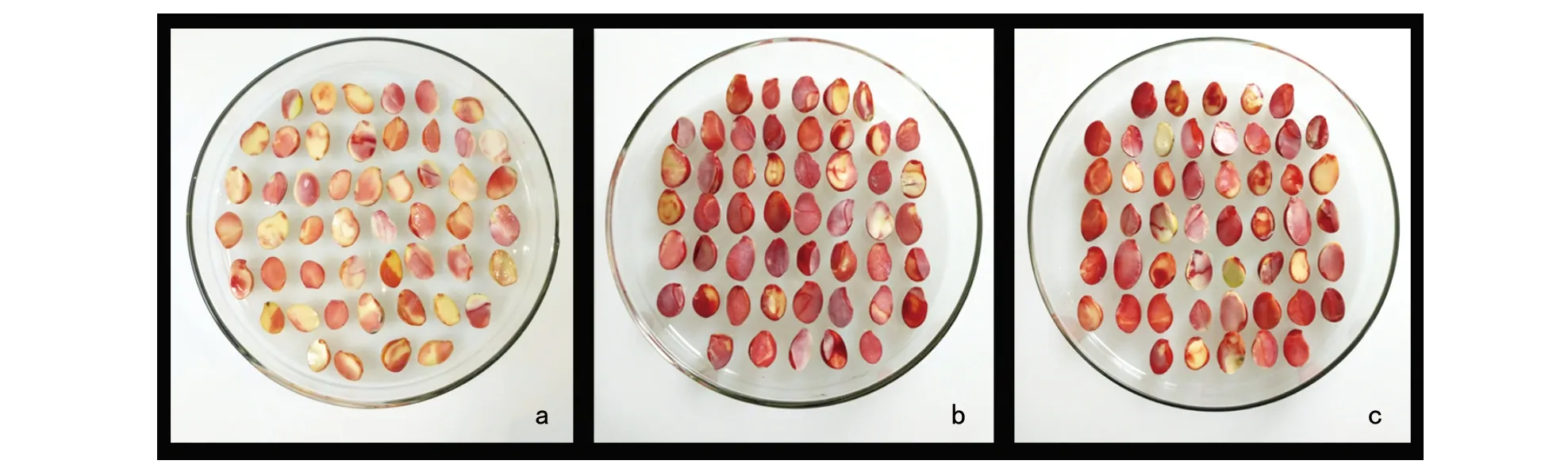
注:a为0.3%×30 ℃×2 h;b为0.3%×35 ℃×4 h;c为0.3%×40 ℃×3 h。图1 正交试验

注:d为0.5 %×35 ℃×3 h;e为0.5%×30 ℃×4 h;f为0.5%×40 ℃×2 h。图2 正交试验
1 材料与方法
1.1 材 料
山豆根种子于2018年9月30日采自安顺市紫云县猫营镇山豆根种繁基地,经贵州中医药大学药学院檀龙颜副教授鉴定为豆科植物越南槐(Sophoratonkinensis)的种子。室内阴干后,于4 ℃保存备用。测定试剂为氯化三苯基四氮唑(TTC)。
1.2 方 法
1.2.1种子处理
种子浸泡:将去除杂质,种皮无破损的山豆根种子置于烧杯中浸泡24 h后,剥掉种皮,从2片子叶中间切断,每50片子叶置于直径12 cm的培养皿中。
种子染色:每个培养皿分别加入不同浓度的TTC溶液,避光置于不同温度条件下染色,相应的对照培养皿中的种子置于沸水浴10 min后染色,每组3个重复。
1.2.2正交试验
选取TTC浓度(A)(0.3%、0.5%、0.7%)、染色温度(B)(30 ℃、35 ℃、40 ℃)、染色时间(C)(2 h、3 h、4 h)为指标,每组50片子叶,设计正交试验。
1.2.3单因素试验
染色温度试验:取50片山豆根子叶,TTC浓度设置为0.5%,时间设置为3 h,温度设置25 ℃、30 ℃、35 ℃、40 ℃和45 ℃等5个水平。
染色时间试验:取50片山豆根子叶,TTC浓度设置为0.5%,温度设置为40 ℃,时间设置1 h、2 h、3 h、4 h和5 h等5个水平。
TTC浓度试验:取50片山豆根子叶,温度设置为40 ℃,时间设置为4 h,TTC浓度设置为0.1%、0.3%、0.5%、0.7%和0.9%等5个水平。
1.2.4响应面试验
以TTC浓度(A)、染色温度(B)、染色时间(C)为变量,根据Central Composite Design设计原理,设计3因素5水平试验。每个处理50片子叶。以种子生活力为响应值(Y)进行响应面分析。
1.3 数据分析
种子生活力根据染色颜色的深浅和比率计算,利用SPSS 17.0软件和Design Expert 8.0.6软件进行数据分析,p<0.05表示差异显著,p<0.01表示差异极显著,每组试验重复3次。
2 结果与分析
2.1 正交试验结果
由图1、图2、图3和表1可知,各条件下山豆根种子生活力为42.3%(图1,a)、66.3%(图1,b)、53.0%(图1,c)、59.3%(图2,d)、75.3%(图2,e)、59.3%(图2,f)、83.3%(图3,g)、83.0%(图3,h)、81.7%(图3,i)。
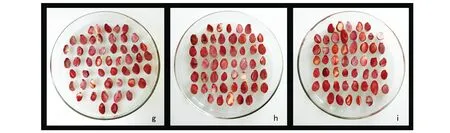
注:g为0.7%×40 ℃×4 h;h为0.7%×30 ℃×3 h;i为0.7%×35 ℃×2 h。图3 正交试验
从表1、图1和图3可以看出,组合0.7%(TTC浓度)×40 ℃(染色温度)×4 h(染色时间)的种子生活力最高,为83.3%(图3),组合0.3%(TTC浓度)×30 ℃(染色温度)×2 h(染色时间)的种子生活力最低,为42.3%(图1)。方差分析显示各因素间差异不显著(表2)。

表1 山豆根种子生活力测定正交试验结果

表2 山豆根种子生活力测定正交试验方差分析结果
2.2 单因素试验结果
从表3中可以看出,山豆根种子在染色温度25~40 ℃之间,颜色由浅粉色到粉色、深粉色和红色,生活力逐渐增大。尽管在45 ℃时颜色为深红色,但显示生活力降低,因而40 ℃为山豆根种子生活力TTC测定法的最佳温度。

表3 山豆根种子生活力与染色温度的关系
山豆根种子在染色时间1~4 h之间,颜色由浅黄色到浅粉色、深粉色和红色,生活力逐渐增大。染色5 h的种子颜色为深红色,但显示生活力降低较大,因而4 h为山豆根种子生活力TTC测定法的最佳染色时间(表4)。
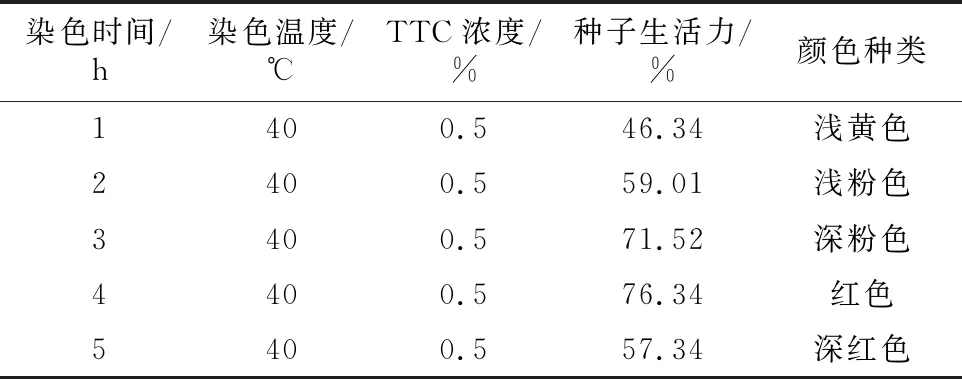
表4 山豆根种子生活力与染色时间的关系
山豆根种子在TTC浓度0.1%~0.7%之间,颜色由浅粉色到深粉色、红色和深红色,生活力逐渐增大。TTC浓度0.9%的种子颜色为暗红色,此时生活力较TTC浓度0.5%时低,因而0.7%为山豆根种子生活力TTC测定法的最佳TTC浓度(表5)。
基于以上结果,在单因素试验条件下,山豆根种子生活力TTC测定法的最佳条件为TTC浓度(0.7%)×染色温度(40 ℃)×染色时间(4 h),该结果与正交试验结果一致。

图4 TTC浓度(A)和染色时间(C)的相互作用对山豆根种子生活力的影响

图5 染色温度(B)和染色时间(C)的相互作用对山豆根种子生活力的影响

表5 山豆根种子生活力与TTC浓度的关系
2.3 响应面优化
2.3.1模型的建立与分析

模型系数的显著性检验表明,A、B、C各因素对山豆根种子生活力测定影响差异极显著,且各因素的影响顺序为染色时间>染色温度>TTC浓度。
2.3.2响应面分析
由图4可以看出,染色时间与TTC浓度的交互作用对响应值影响最大,响应面的倾斜度最高,其次是染色温度与染色时间(图5),最后是染色温度与TTC浓度(图6)。通过响应面法优化,山豆根种子生活力TTC法测定的最佳条件为TTC浓度(0.7%)×染色温度(40 ℃)×染色时间(4 h),此条件下,理论种子生活力为87.55%。在此条件下,进行验证,重复3次,实测生活力为83.88%、84.67%和84.53%,平均生活力为84.36%。试验生活力测定值与理论预测值的误差为3.64%(<5%),因此,应用Central Composite Design响应面设计优化山豆根种子TTC法测定条件是可行的。
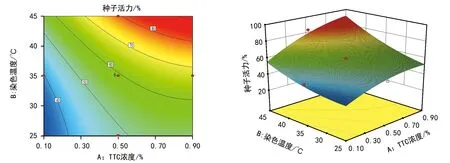
图6 TTC浓度(A)和染色温度(B)的相互作用对山豆根种子生活力的影响

表6 山豆根种子生活力测定响应面试验结果
3 结论与讨论
染色时间、染色温度和TTC浓度为TTC法测定种子生活力的主要因素,以往的研究也应用该法检测药用植物种子的生活力[4-5],但对于不同药用植物种子,3种因素对于生活力检测的影响也不同。
由于实际研究中,正交试验设计和单因素试验设计各有不足,特别是在检测因素水平较多时,本研究利用响应面法优化试验设计能在一定程度上对正交试验设计和单因素试验设计进行补充,从而使检测准确的同时,步骤更加简便,以达到省时省力的目的。
本研究发现,响应面法测定山豆根种子活力的最佳条件为0.7%(TTC浓度)×40 ℃(染色温度)×4 h(染色时间),与正交试验和单因素试验的结果一致。在羊耳菊(Inulacappa)种子[4]和头花蓼(Polygonumcapitatum)种子[5]生活力检测中,也得到相似的结论,实验表明利用响应面法优化TTC法测定山豆根种子生活力是可行的。

表7 山豆根种子生活力测定响应面试验方差分析
注:“**”表示差异极显著(p<0.01),“*”表示差异显著(p<0.05)。

