彩色多普勒超声对血液透析患者动静脉内瘘结构功能评估及并发症诊断价值
柯媛,唐敏
(池州市人民医院超声医学科,安徽 池州 247000)
血液透析(hemodialysis,HD)是目前治疗终末期肾病患者的有效手段,而良好的血管通路是HD治疗成功的基础和关键[1]。目前HD治疗时构建血管通路的方法较多,比如长期中心静脉导管置管、人工移植血管和动静脉吻合内瘘(autologous arteriovenous fistulae,AVF)等,其中AVF是一种将上臂或前臂动静脉直接进行吻合的外科操作方法,通过动静脉吻合达到HD所需的血流量,由于操作方便、并发症少和安全性高,已成为HD构建血管通路的首选[2]。AVF是否通畅直接影响到HD的顺利进行和并发症风险,因此早期积极评估AVF结构功能,比如观察AVF血流方向、速度和管腔内血流充盈情况等尤其重要[3]。彩色多普勒超声技术在HD相关领域的应用日益成熟,受到临床的高度重视。本研究旨在探讨彩色多普勒超声对HD患者AVF结构功能评估及并发症诊断的应用价值,现报告如下。
1 资料和方法
1.1 一般资料
研究对象为2017年6月至2019年3月在池州市人民医院接受血液透析(hemodialysis,HD)患者80例,其中男性52例,女性28例;年龄23~75岁,平均(53.27±11.25)岁;疾病类型包括糖尿病肾病28例,高血压肾病23例,慢性肾小球疾病18例,多囊肾7例,其他4例;吻合方式包括桡动脉-头静脉端端吻合71例,桡动脉-头静脉端侧吻合9例。本研究经医院伦理委员会批准。
纳入标准:(1)终末期肾病患者,年龄≥20岁;(2)采用AVF,即前臂桡动脉-头静脉内瘘接受HD治疗,且AVF使用次数>6次;(3)患者及家属知晓本研究目的,并签署知情同意书。排除标准:(1)静脉走行直、头静脉和桡动脉内径≤2 mm。左室射血分数<50%;(2)合并心、肝、肺等器质性病变或其他恶性肿瘤,合并严重感染、凝血功能障碍、急性脑血管意外、精神意识障碍疾病等;(3)血管条件较差,不能建立理想的血管通路,行人工血管移植建立动静脉瘘者;(4)中转腹膜透析、肾脏替代或死亡者。
1.2 方法
检查仪器为PHILIPS HD15彩色多普勒超声仪,探头频率5~17 MHz,由本院具有≥5年超声科工作经验的医师进行检查。嘱咐患者取仰卧位,造瘘上肢充分暴露,平放外展与躯干夹角约60°。先用二维超声仔细观察内瘘供应动脉(桡动脉与其发出动脉)、引流静脉(头静脉与其回流静脉)和吻合口位置,明确三者的解剖关系。然后采用彩色多普勒观察相关血管和血流通畅情况,如血管深度、位置、走行和管腔形态等是否正常,测量供应动脉、引流静脉和吻合口的血管内径和收缩期峰值流速(peak systolic velocity,PSV),内瘘血流量测定选择在上臂肱动脉处。观察血管壁是否增厚及其光滑程度,观察管腔内有无斑块或血栓等异常回声,以及是否引起管腔狭窄或闭塞等情况,彩色多普勒血流成像观察血管通路是否通畅,血流是否连续和有无缺损,并检测桡动脉、头静脉、吻合口和病变位置的血流速度,观察相应血管有无异常血流频谱波形等。操作人员检测时注意探头和皮肤表面保持垂直,以免浅表血管受压影响测量结果,每个部位测量3次取平均值记录。
1.3 观察指标
AVF成熟程度是反映其结构功能的常用指标,因此分别于术前和术后2周、4周、6周定期测量桡动脉管径(radial artery diameter,RAD)、肱动脉血流量和头静脉管径(cephalic vein diameter,CVD)的变化情况。AVF成熟判定标准:超声检查未发现明显并发症,CVD增宽且肱动脉血流量>500 mL/min,透析机泵控血流量达到200 mL/min。
根据AVF血流动力学、血管内径和超声图像情况判定AVF相关并发症。动脉端或吻合口狭窄:内径<2.0 mm,且狭窄处与其以上20 mm处桡动脉PSV比值>3;静脉端狭窄:静脉端内径<3.0 mm,且比相邻正常段内径下降50%,狭窄处与其以下20 mm处头静脉PSV比值>2;静脉瘤状扩张:正常瘘静脉管径≥4 mm,瘤样扩张最大径≥正常瘘静脉管径的3倍。
1.4 统计学分析
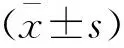
2 结果
2.1 手术前后AVF结构功能的定量评估比较
与术前测量AVF血流和血管内径结果比较,术后2周、4周、6周的RAD、肱动脉血流量和CVD有明显提高,不同时点两两比较差异均有统计学意义(P<0.01)。见表1。
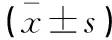
表1 彩色多普勒超声对HD患者AVF结构功能定量评估比较
*P<0.01,与术前测量值比较; #P<0.01,与术后2周比较;△P<0.01,与术后4周比较。
2.2 AVF血流通畅和并发症的评估
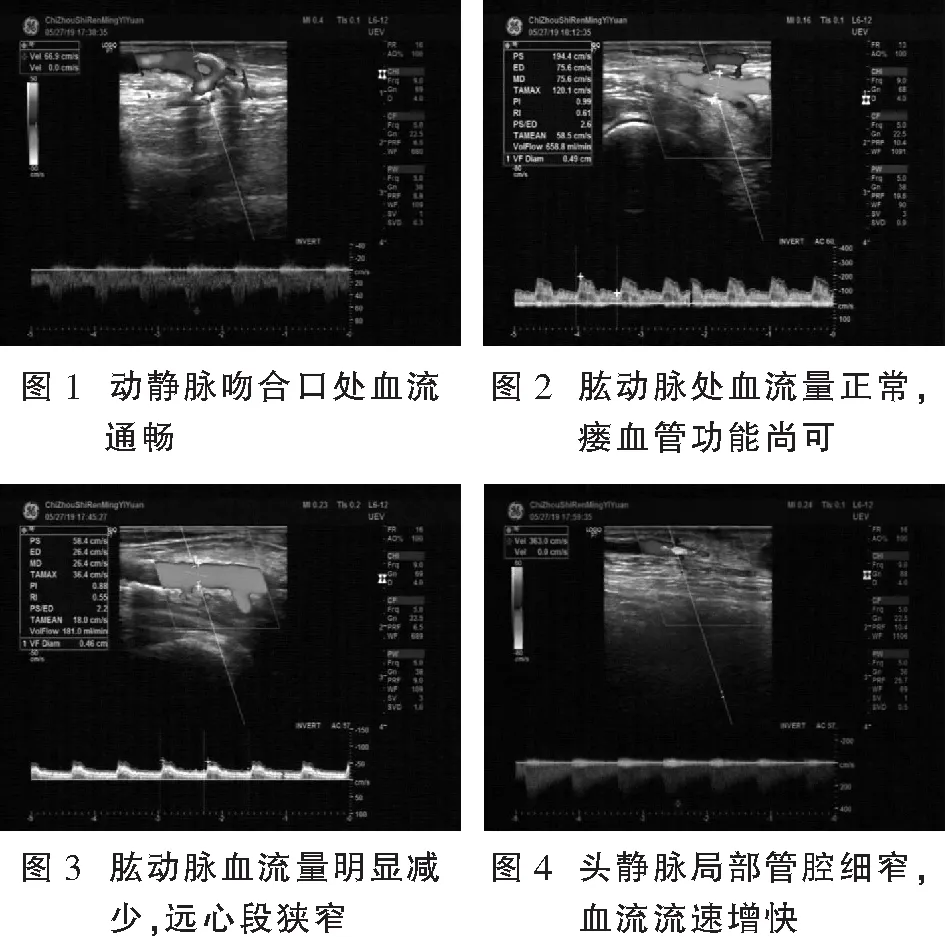
彩色多普勒超声检查显示:80例HD患者共有51例AVF血流通畅,占比63.75%(51/80),超声图像可见显示动静脉造瘘术后,动静脉吻合口处血流通畅,可见五彩镶嵌样的血流信号,频谱多普勒显示流速正常,引流静脉呈动脉化回心血流信号等(图1-图2)。29例HD患者出现AVF并发症,占36.25%(29/80),见表2。血栓形成13例,占比16.25%(13/80),超声图像比较直观,头静脉增粗和局部无血流。动静脉瘘狭窄11例,占比13.75%(11/80),超声可见动静脉血管内径后瘘口明显缩小,且探头适度加压管腔后无明显变形,狭窄段血管内血流充盈量较低,血流速度加快(图3-图4)。静脉瘤状扩张5例,占比6.25%(5/80),超声可见头静脉迂曲扩张,管径有明显增宽和管壁增厚,PSV测量值较邻近正常段有所降低。
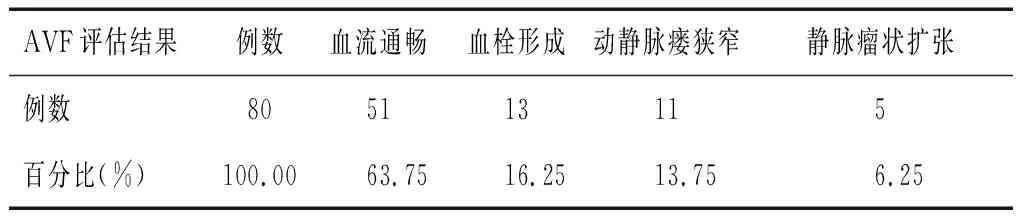
表2 80例HD患者AVF血流通畅和相关并发症情况
3 讨论
早在2001年美国国家肾脏基金会(NKF)制定的肾脏病预后质量指南(K/DOQI)就推荐终末期肾病患者采用自身动静脉构建血管通路行HD治疗,可长期重复使用,减少患者生理痛苦和经济负担。自体AVF构建是前壁血管重构的过程,本质上是一种非生理性的高顺应性操作,以构建满足HD治疗的血流动力学血管环境[4]。但终末期肾脏病患者受年龄增长、合并基础疾病、反复穿刺操作等因素影响,AVF术后早期易受血流量不足、血管通路闭塞等所致瘘成熟不良,或者AVF结构功能发生进行性变化,当透析流量下降或出现相关症状体征时,可能HD患者的AVF并发症已经十分严重甚至内瘘功能趋于失效,最终导致AVF失败[5-6]。因此AVF术后加强其结构功能评估和并发症诊断意义重大,应该成为HD患者的必要检查评估项目。
血管造影对评估AVF结构功能具有一定价值,但该方法为有创检测,存在一定安全风险,不宜频繁使用和临床推广[7]。彩色多普勒超声检查具有无创、精确、操作简单、可重复和费用低廉等优点,是AVF监测的重要手段。本研究采用彩色多普勒超声能较好评估HD患者AVF成熟进程,在内瘘建立初期,能清晰观察血管通路通畅程度以及明确血管管径和管壁厚度有无异常,借助血流成像还能定量评估AVF部位血流速度、管腔狭窄程度等信息[8-9]。本研究显示,AVF术后RAD、肱动脉血流量和CVDF均呈增高趋势,和术前或术后2周比较均有显著差异,和文献[10-11]报道相吻合,说明彩色多普勒超声能较好定量动态评估AVF成熟情况,而AVF成熟情况与其结构功能具有一致性,因此彩色多普勒超声对评估AVF结构功能变化具有积极作用。内瘘血流量是反映其功能的重要指标,本研究选择在上臂肱动脉出进行血流量测定,而非传统选择的供血桡动脉,原因是考虑到HD时内瘘血流量的供血机制,选择桡动脉测量可能会低估透析时的血流量。一般来说肱动脉血流量>500 mL/min时说明瘘功能较好,并发症风险较低。而对于超声测得肱动脉血流量<500 mL/min患者需重点加强检测和相关临床干预,减少并发症和内瘘失功的发生。
AVF术后并发症主要有血栓形成、动静脉瘘狭窄和静脉瘤状扩张等,其发生原因复杂多样,但一般和血流动力学改变、手术操作不当造成血管损伤和患者个体因素(高龄、合并症等)等有关,早期及时发现AVF并发症和内瘘失功的潜在因素,对指导临床采取相关措施、延长AVF的使用尤为重要[12]。本研究彩色多普勒超声检查显示,AVF血流通畅有51例,占63.75%,有29例出现AVF并发症,其中血栓13例、动静脉瘘狭窄11例和静脉瘤状扩张5例,借助内瘘血流信息、超声声像图等均能较好诊断。
血栓作为最常见的AVF并发症,超声不仅能直观显示管腔内血栓形态及其范围,满足诊断需要,而且能通过血栓的回升强度估测血栓的形成时间,若内瘘血栓发生在24 h内,可首选局部血管内注射尿激酶溶栓治疗[13]。动静脉瘘狭窄主要发生在引流静脉和内瘘口处,二维超声能较好显示狭窄部位的血管管腔变窄,彩色多普勒血流成像下狭窄部管腔内有五彩嵌顿的血流信号,狭窄远端血管内的血流信号明显减少,且易合并血栓形成。临床中明确动静脉狭窄部位后,可在超声指导下选择合适的穿刺部位处理,达到满足HD治疗的有效透析血流量。静脉瘤状扩张也是比较常见的AVF并发症,其发生原因一般和内瘘过早使用、同一部位反复静脉穿刺操作以及瘘口血流动力异常等有关[14-16]。静脉瘤状扩张超声检查可见局部管径有明显增宽、管壁增厚和PSV下降,超声诊断较为直观、简单。
综上所述,彩色多普勒超声能直观准确、定量评估AVF血流动力学、内瘘形态和管径变化等信息,对临床评估AVF结构功能、并发症诊断以及指导干预治疗具有重要价值。

