基于培养学生证据意识的高中化学教学探索
计从斌 余焕焕 林建芬


[摘 要]
通过“证据推理”核心素养培养学生思维逻辑的严密性,从标准热力学数据、键能、离解能等角度,阐述甲烷与氨气的热稳定性反常现象的原因,丰富和发展氢化物稳定性判断的方法。
[关键词]
高中化学;证据意识;稳定性
一、研究背景
《普通高中化学课程标准(征求意见稿)》指出,化学核心素养由“宏观辨识与微观辨析”“变化观念与平衡思想”“证据推理与模型认知”“科学探究与创新意识”“科学精神与社会责任”这五个要素构成。其中,“证据推理”核心素养要求学生具有证据意识,初步学会收集各种证据,能基于证据对物质组成、结构及其变化提出可能的假设,通过分析推理加以证实或证伪;能解释证据与结论之间的关系,确定形成科学结论所需要的证据和寻找证据的途径;建立观点、结论和证据之间的逻辑关系;知道可以通过分析、推理等方法,认识研究对象的本质特征、构成要素及其相互关系。
气态氢化物的稳定性大小比较是中学化学教学中常遇见的问题,也是培养学生基于证据意识研究物质结构与性质的能力的优质教学素材。很显然,这里所指的稳定性是指热稳定性,而非化合物的反应活性。笔者在教材分析与备课研究中,从现行三种高中化学教材(人教版、苏教版、鲁科版)引入氢化物稳定的叙述中就已充分体现出此概念的含义,相关文献也有进一步的描述。根据元素周期律,同一周期或同一主族的非金属元素,随着元素原子序数的增加,元素的非金属性逐渐增强,元素对应的气态氢化物的稳定性也逐渐增强。然而在第二周期中,氮元素非金属强于碳元素,对应的氢化物稳定性NH3应该强于CH4,但NH3和CH4的分解温度分别为1073 K、1273 K,這就说明CH4的稳定性强于NH3,此结果与元素周期律相悖。吴孙福等人从中心元素的电负性、实验事实、C-H和N-H的键能等角度,阐述了CH4与NH3稳定性强弱原因。
笔者通过查阅文献与教材分析的双重实证研究中,认为需要补注几种证据从而进行多方位解释,并得出通过三种方式引导学生基于证据意识对甲烷与氨气稳定性进行系统研究与学习,提高优质学生的思考维度,同时也为教师备课提供参考。这三种实证研究渠道分别为:分子型氢化物标准热力学数据、键能与离解能数据、元素的电负性与分子的极性。
二、分子型氢化物标准热力学数据
简单分子型氢化物完全热分解产物通常是单质,根据ΔH?=ΔH?f生成物-ΔH?f反应物=-ΔH?f反应物,该化合物的生成热即是热分解反应热的负值。由于ΔG? = ΔH?-TΔS?,单质的熵都很小,对反应影响较小,故可忽略ΔS项, 因此ΔG? = ΔH? = -ΔH?f反应物,故可用-ΔH?f反应物来判断氢化物热稳定性问题,化合物的生成热负值越大, 其热稳定性越高,表1列出了第二周期常见非金属元素的气态氢化物的标准热力学数据。
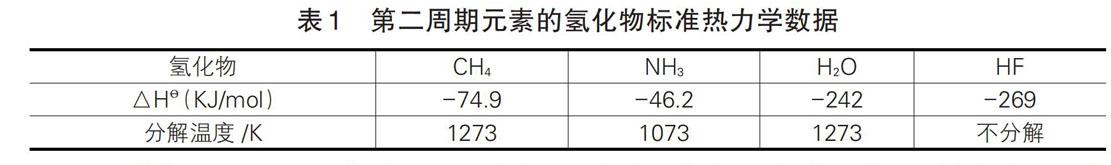
表1 第二周期元素的氢化物标准热力学数据
[氢化物 CH4 NH3 H2O HF △H? (KJ/mol) -74.9 -46.2 -242 -269 分解温度 /K 1273 1073 1273 不分解 ]
表1数据显示,同一周期非金属元素随原子序数的增大,其氢化物的反应热的大小与分解温度大小变化是一致的。因此用生成热判断分子型氢化物的热稳定性是可行的。
三、分子型氢化物键能与离解能
键能是从能量方面对共价键强弱进行量度的重要参数。同一分子中的不同键和不同分子中的同一种类型键的键强度都是不同的;一般而言,键能越大,键越强越稳定。对于ABn 型分子来说,分子中各键的键能是相同的, 且键能具有加和性,故分子的总键能是各个键的键能之和:E = ΣEAB,即EAB= E/n。
对于双原子分子(A2或AB型分子)来说键能和离解能在数值上相等,符号相反,但在ABn(n ≥ 2)型分子中情况就不一样了。键能和离解能是两个不同的概念,但它们有一定的关系,键能的数据一般从测定其离解能求得,如表2。
表2数据显示,从总键能和键能、离解能的数据均说明了CH4稳定性要强于NH3,利用总键能、键能和离解能判断分子型氢化物的热稳定性也是可行的,这与利用标准热力学数据判断方法得出的结论一致。
四、元素的电负性与分子的极性
关于分子型氢化物的稳定性有文献指出,非金属与氢的电负性差值越大,组成的氢化物分子的极性就越大,其热稳定性也越大;反之,这个差值越小则越不稳定。表3列出了第二周期常见非金属氢化物的电负性与分子偶极矩的数据,根据文献提出的规律,CH4的稳定性比NH3的要弱,但是从氢化物分解的温度来看,这是相互矛盾的。吴孙福等人解释CH4与NH3利用电负性与热稳定性的矛盾关系时,指出CH4是因为其分子结构高度对称,分子偶极矩为零,从而导致分子比较稳定,但表3的数据显示了分子的偶极矩越大热稳性越强的趋势。
因此,元素的电负性与分子的极性只能作为一般规律使用,不能解释氢化物热稳定性的本质。
五、教学建议
化学教学不只是传授化学知识、技能和方法;设计组织实验、开展科学探究活动也不只是让学生动手,学习诸如观察、推断和实验等各种探究技能和方法。要引导学生通过探究学习活动,经历科学发现和探究的基本过程,在活动中认识和理解科学的本质。
高中教师在课堂上要选择化学概念与原理作为内容载体,通过设置若干核心问题驱动学生“证据导向式”论证活动,学生在科学探究和数据分析的论证过程中,培养证据意识、提升逻辑推理和论证能力。
总之,在中学基础化学中,存在许多一般规律和特殊规律,教师在备课思考时应多角度不同层面去佐证,化学基本概念与原理中一般与特殊关系矛盾与统一关系,是否符合中学生认知范畴都是要考虑的。
[参 考 文 献]
[1]宋心琦.普通高中课程标准实验教科书?化学2(必修)[M].北京:人民教育出版社,2014.
[2]王祖浩.普通高中课程标准实验教科书?化学2(必修)[M].南京:江苏教育出版社,2008.
[3]王磊.普通高中课程标准实验教科书?化学2(必修)[M].济南:山东科学技术出版社,2008.
[4]张莉.是否可用化合物的生成热判断其热稳定性[J].安庆师范学院学报(自然科学版),1996(3).
[5]赵元力,周享春.常见元素的氢化物及其特性[J].长江大学学报(自然科学版),2004(1).
[6]吴孙富,张道林.CH4与NH3稳定性的比较[J].化学教育,2008(5).
(责任编辑:张华伟)

