超声引导下血管成形术治疗DSA相对禁忌下肢动脉硬化闭塞症
庄 勇,曾锦树,叶小剑*,戴贻权,郭平凡,蔡方刚
(1.福建医科大学附属第一医院超声影像科,2.血管外科,福建 福州 350005)
血管腔内治疗已逐渐成为治疗下肢动脉硬化闭塞症(arteriosclerosis obliterans, ASO)的主要方法。近年来,随着药物支架与长球囊等治疗手段的应用,PAD疗效显著提高,腔内治疗的适应证也不断拓展。对于慢性肾病或碘对比剂过敏患者,相比DSA引导下腔内治疗,超声引导下的腔内治疗无辐射,无需使用对比剂,具有独特优势,并逐渐进入临床[1]。本研究探讨超声引导下介入治疗DSA相对禁忌患者下肢ASO的临床价值。
1 资料与方法
1.1 一般资料 选取2012年3月—2016年9月我院PAD患者18例,其中男15例,女3例,中位年龄59.0岁;均有严重间歇性跛行和静息痛。18例中,3例碘对比剂过敏,15例慢性肾功能不全;高血压13例,糖尿病11例;16例单侧下肢ASO,2例双侧下肢ASO,共20支受累动脉。排除急性动脉栓塞或血栓形成、股动脉搏动明显减弱或消失、严重心功能不全者。
1.2 仪器与方法 采用Philips iU22彩色超声诊断仪,L9-3线阵探头,频率3~9 MHz,确定动脉狭窄或闭塞部位及范围(图1A),并做好体表标记。根据术前超声检查结果,对股浅动脉中下段病变选择同侧顺行穿刺,股浅动脉中上段病变选择对侧逆行穿刺翻山治疗[2]。术中采用Sonosite超声检查仪,L38e探头,频率5~10 MHz,在超声引导下以Seldinger法于患侧顺行穿刺股动脉成功后置入4F血管鞘,或于健侧逆行穿刺股动脉翻山成功后置入5F/6F血管鞘,术中于超声直视下将导管送至靶病灶近心端(图1B、1C),导丝穿过闭塞段或狭窄段达远心端真腔,依据邻近正常血管内径及病变长短选择相应直径及长度的球囊(球囊直径需与正常血管直径等大,长度以可超越病变两端至少1 mm为宜),行球囊扩张(图1D),观察管腔内血流充盈情况及狭窄扩张段近、远端血液流速。
球囊扩张后即刻进行超声评估:扩张后管腔狭窄率<30%且血流充盈良好提示扩张成功;扩张后管腔狭窄率≥30%~49%,病变处收缩期血流峰值流速(peak systolic velocity, PSV)150~200 cm/s,收缩期血流峰值流速比值(peak systolic velocity ratio, PSVR)达1.5∶1.0~2.0∶1.0为球囊扩张相对满意,可予观察,之后定期随访;如残余管腔狭窄率≥30%,PSV>200 cm/s,PSVR>2.0∶1.0,则加行超声引导下支架植入术(图1E),选择较邻近正常血管直径大1 mm左右的支架,植入后观察支架腔内血流充盈情况(图1F),同时测量支架近端及远端血流流速,实时评估治疗动脉管腔血流通畅情况。对所有患者于术后24 h、3个月、6个月、12个月和24个月进行随访,测量PSV,计算不同时间狭窄和闭塞的总复发率。
1.3 统计学分析 采用SPSS 22.0统计分析软件。计量资料以±s表示,术前和术后不同时间PSV比较采用单因素方差分析,两两比较采用LSD法。以P<0.05为差异有统计学意义。
2 结果
20支动脉中,15支完全闭塞, 5支重度狭窄(狭窄率70%~99%)。对19支动脉于超声引导下一次性穿刺成功,1支经股动脉顺行穿刺后导丝进入靶病灶内膜下而无法破膜到真腔,改行足背动脉切开逆行操作成功。超声引导下球囊扩张成形术成功率40.00%(8/20),支架植入术成功率100%(12/12)。
术前与术后各时间点病变处PSV总体差异有统计学意义(F=4.26,P=0.046),术后各时间点与术前比较差异均有统计学意义(P均<0.05),术后12个月和24个月与术后24 h比较差异有统计学意义(P均<0.05),余两两比较差异均无统计学意义(P均>0.05)。术后24 h复查患肢动脉彩色多普勒超声评估20支治疗动脉管腔均通畅,通畅率100%;术后3个月、6个月、12个月和24个月总复发率分别为5.00%(1/20)、10.00%(2/20)、20.00%(4/20)及50.00%(10/20),见表1。

表1 术前及术后PSV和血管狭窄、闭塞情况(n=20)
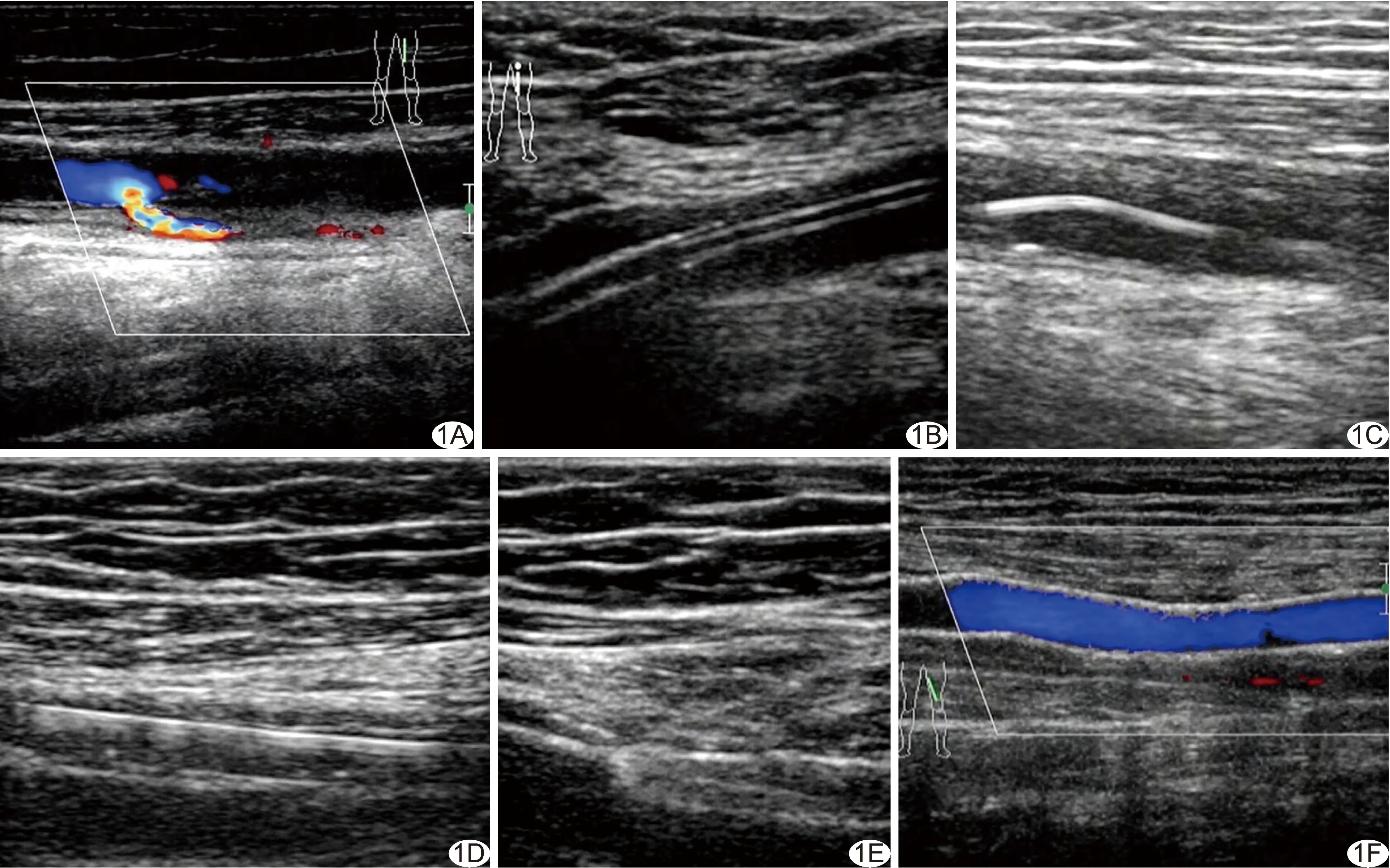
图1 患者男,59岁,左下肢ASO A.治疗前股浅动脉闭塞伴侧支形成; B.超声引导下将导管导入病灶近心端; C.导丝顺利通过闭塞段; D.扩张球囊,其内部可见导丝; E.超声引导下植入支架; F.支架植入后腔内血流通畅
3 讨论
近年来,随着生活水平的提高及人口老龄化,下肢ASO发病率逐步提高[3],高血压、高血脂、糖尿病及吸烟等为其重要危险因素。早期下肢ASO患者表现为间歇性跛行,远侧动脉搏动减弱或消失,后期可出现静息痛、皮温降低,严重时可出现皮肤破溃及坏疽,致残率极高[4]。常见治疗方法有保守治疗、手术治疗及介入治疗。保守治疗方案常为降压、调脂稳斑、抗血小板聚集等,仅可在一定程度上缓解症状,无法解除下肢动脉狭窄或闭塞[5]。开放手术治疗创伤大,对患者心、肺、肾等重要器官影响较大,尤其不适用于严重心脑血管疾病及糖尿病患者。腔内介入治疗具有微创、并发症较少、住院时间短、可重复操作治疗等优点,常为该病的首选治疗方式[6];但对于慢性肾功能不全及碘对比剂过敏者,DSA引导下腔内治疗受限。
相比DSA,彩色多普勒超声引导腔内治疗下肢ASO有以下优点[7]:①超声仪器相对便携,亦可使用简易床旁超声,场地需求相对较低;②患者及操作者可避免X线辐射;③避免碘对比剂引起的过敏性休克及对比剂肾病等不良反应;④超声引导下操作可动态观察导丝进入真腔情况,避免出现血管穿孔、导丝打结、误入假腔等情况发生;⑤可依据术前评估情况选择大小合适的球囊或支架,并实时观察球囊扩张或支架植入后血流动力学变化;⑥术中可观察腔内、血管壁及周围组织的情况,便于及时发现血栓、血肿等并采取措施;⑦费用相对较低。本组采用彩色多普勒超声,通过观察血管走行、监测血流动力学改变,不仅能很好地分辨血管腔、血管壁及周围组织,而且可清楚显示血管腔与导丝和球囊及支架,与既往研究[8]报道相一致。
超声引导下血管腔内治疗要点如下。①入路选择:选择合理的入路是保证手术安全与成功的关键,需依据病变部位采用不同入路;对股浅动脉近端病变可自对侧股动脉入路;对于股浅中段以远病变,可选择对侧股动脉入路或同侧股动脉入路;以顺行入路通过闭塞病变受阻时,可采用经膝下动脉穿刺的逆行入路技术以及顺行逆行相结合的双入路技术[9];自对侧入路时,应用翻山鞘可提供足够的支撑力,有助于顺利进行腔内治疗[10]。②超声引导导丝导管达靶病灶近心端:术中于超声直视下将导管送达靶病灶近心端是腔内治疗的首要条件。对侧入路应用翻山技术时,如肠气干扰严重,可借助X线透视进行翻山,达同侧后于超声引导下操作。③导丝通过闭塞段:超声实时观察导丝是否在真腔内,可直观引导导丝导管通过狭窄段。根据病变范围选择适宜球囊,先进行球囊扩张,之后评估血流,若管腔残余狭窄率>50%、PSVR>2则植入支架[11]。本组超声引导下球囊扩张成形术成功率40.00%,超声引导下支架植入术成功率100%。④腔内成形术后需观察腔内血流充盈情况及原狭窄段近端和远端流速。本组术后各时间点PSV均较术前下降(P均<0.05)。
超声引导下肢动脉腔内成形术目前仍有一定局限性[12]。①超声对于显示血管具有很高的敏感度,但在对侧入路应用翻山时,髂动脉区易受腹腔内肠气干扰而显示不清。②受超声混响伪像和硬斑后方声衰减影响,判断导丝是否在真腔内前行、尤其在通过长段闭塞段时较为困难,需使用高分辨率探头进行多切面、多角度扫查,以提高判断准确率。采用血管腔内超声有助于提高腔内治疗的成功率。Baker等[13]以血管腔内超声辅助腔内治疗髂股动脉慢性完全闭塞病变, 20例患者中,重度肢体缺血11例,18例治疗成功,无治疗相关并发症;术后6个月3例出现再狭窄,12个月通畅率62%,总复发率达38%,可能与患者依从性、生活习惯以及对基础疾病的控制情况等有关。本组术后12个月总复发率20.00%。③测定血流流速受超声入射角的影响,故在一定程度上存在操作者依赖性。
总之,超声引导下腔内治疗下肢ASO成功率高,具有术前定位准确、术中全程实时监测、可实时评估疗效等优点,对不宜行DSA引导下介入治疗的肾功能不全或对比剂过敏下肢ASO患者有重要临床应用价值。