国内外短缺药品监测预警体系对比分析*
刘青泽,韩 月,朱 虹,姜 雪,刘兰茹
(哈尔滨医科大学人文社会科学学院,黑龙江 哈尔滨 150000)
2018年9月,国务院《关于完善国家基本药物制度的意见》明确提出,要加强药品短缺预警应对措施。国家药品供应保障综合管理信息平台2018年1月至5月《短缺药品监测结果快报及附件》报告显示,全国公立医院短缺药品监测岗哨涉及短缺药品1 947个,而2017年为860个,可见各级机构对短缺药品监测越来越重视。药品短缺成因复杂,涉及产业链中研发、生产、流通、使用等环节[1]。建立完善的风险短缺预警监测体系,及时发现问题,并制订应对策略,是国内外解决药品短缺行之有效的做法[2]。本研究旨在通过了解国内外药品短缺预警监测体系的现状,总结短缺药品监测预警经验,为切实解决短缺药品供应,促进药品流通行业发展,以及完善国家短缺药品预警体系提供参考。
1 药品短缺的概念
由于供需情况、管理难度等因素差异,不同国家、地区对药品短缺的定义也不同。美国和加拿大从满足临床需求角度定义,欧盟从生产中断角度展开[3]。世界卫生组织(WHO)将药品短缺分为药品缺乏和药品缺货,前者是指药品供应方无法完全满足公共卫生和患者需求,后者是指面向患者的某类药品完全断货。我国对药品短缺没有统一规定,但一些地方性文件给出过相关概念,如《江苏省短缺药品供应保障方案》《北京市药品集中采购短缺药品目录调整制定办法》等,均从供需角度给予了相应定义[4]。
2 发达国家短缺药品监测预警体系比较[5]
美国:美国药物评价和研究中心(CDER)在美国食品药物管理局(FDA)网站上建立了药品短缺信息平台,采取以生产企业强制上报与其他相关者(医院、医师、患者等)自愿上报相结合的方式,并专门设置了药品短缺工作小组(DSS)。2012年7月签署的FDA安全和创新法案(FDASIA)中列出了对药品生产企业强制性的报告要求,要求生产企业至少在药品停产前6个月向FDA报告相关信息,包括预期持续停产时间等[6]。DSS收集来自生产企业、分销商及FDA的办事处等关于药品短缺的信息,结合市场调研数据对市场需求、库存信息、厂商分销情况等方面,并结合专家意见进行评估,对药品短缺或生产中断的真实性进行验证和判断。当确认药品短缺实际存在后,FDA会先判定短缺药品是否为医疗必需和来源是否单一,然后有针对性地采取鼓励生产和临时进口、加快注册审批、联系供应商等方式应对[7]。同时,FDA将药品短缺相关信息发布到其官方网站上并及时更新,主要列出医疗必需品的短缺,提供从生产企业处获得的信息,以及利益相关者在解决防治短缺方面的信息。FDA还通过美国卫生系统药师协会(ASHP)的药品短缺资源中心网站(www.ashp.org/shortages)发布药品短缺信息,方便利益相关者共享信息,沟通交流。
英国:英国卫生部(DH)设立商业药品团体(CSU)负责药品短缺信息的收集处理,并采用了“药品短缺联络人”制度,要求药品生产企业委派1名专业人员作为药品短缺联络人,由其对生产企业的药品短缺可能产生的影响进行评估,并决定是否向DH上报[8]。同时,DH也设置药品短缺联络人,负责汇总信息。信息上报采取药品生产企业停产提前报告制,要求生产企业必须在停产前12个月上报,上报的信息包括短缺药品的公司信息、产品信息、短缺原因、预计短缺时间等。这种由专人直接负责上报的制度,保证了所提交短缺信息的真实性。DH在收到上报信息后,汇集医药联合会、医疗机构、医师、患者等利益相关者的意见,对信息进行判断,以确认短缺情况。当确认信息的真实性后,根据短缺药品的关键性及短缺影响风险进行评估,在评估后及时将信息公开。采取加快药品审批程序、推动医保与供应商合作、确定供应困难的药品目录、加强短缺药品或替代药品的供应等方式进行处理。
加拿大:加拿大卫生部(HC)成立了药品短缺多方利益相关者指导委员会(MSSC),负责药品短缺处理的工作。MSSC开发了药品短缺通报和通报议定书,明确规定了对药品短缺的监测预警和处理的相关要求,并于2017年发布了《药品短缺和中止报告指南草案》,对“药物授权持有人”“药品中断”等概念进行了定义,并要求生产企业至少在药品停产前6个月通过药品短缺信息处理网站上报短缺和生产中止信息,包括企业信息、药品信息及药品短缺原因等。在信息上报方面,采用“分类定级”处理:第一层级,利益相关者发现供应链任一环节发生短缺并上报;第二层级,实际已发生,但不会产生重大影响;第三层级,对国家卫生保健系统产生巨大影响[9]。MSSC还开发了一个多利益相关方工具包,根据利益相关者(如生产企业、供应商、医师、药师等)对信息进行共享。HC在MSSC的协调下对于药品短缺的数量、时间等因素进行分析、判断,最后针对药品短缺原因,采取制订基本药物目录,扩大药品供应商,审查药品定价策略等方式进行处理。
美国、英国、加拿大均采用“收集-判断-处理”的流程(见图1),以相对完善的法律体系为支撑,设立专门的管理机构,采取有效的上报和判断方式,保证了信息的真实性,并注重利益相关者的信息共享与沟通,构建了较为完善的短缺药品监测预警体系,以便采取针对性的处理措施,保障药品的市场供应。
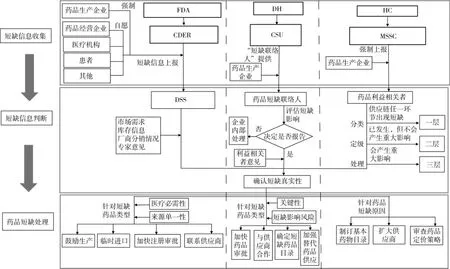
图1 国外药品短缺监测预警流程对比图
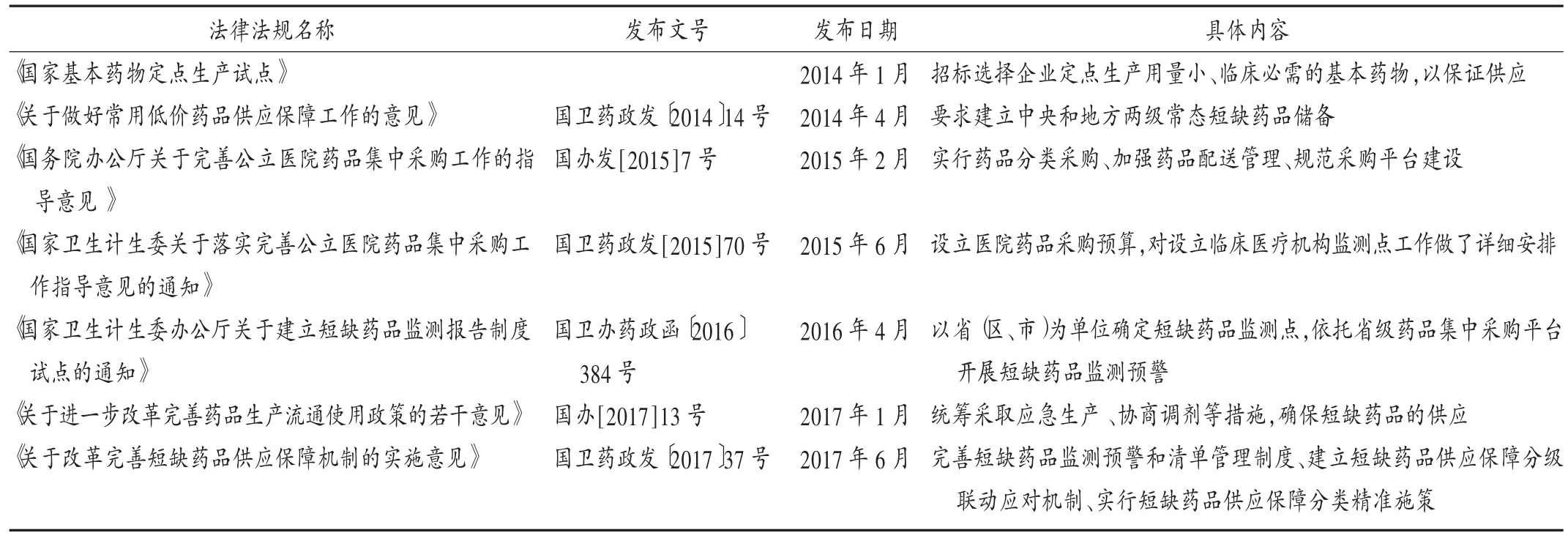
表1 我国短缺药品供应保障政策汇总
3 我国短缺药品监测预警实施现状分析
3.1 我国短缺药品监测预警实施现状分析
通过搜索国家卫健委、工信部、中国政府网,以及国家药品监督管理局官方网站的政策法规等,梳理近年来短缺药品供应保障政策,综合分析我国短缺药品监测预警的实施现状(见表1)。可见,相对于其他发达国家,我国应对药品短缺方面虽起步较晚,但也取得了可喜的成绩。如我国在短缺药品监测预警体系的构建方面逐渐完善并逐渐精细化。2014年以来,国家针对药品短缺建立了一系列政府干预措施,包括完善监测预警体系,优化药品研发生产流程,完善药品生产流通环节等[10]。对于药品短缺监测平台建设方面,我国于2015年至2016年陆续发布了一系列文件,对医疗及机构的短缺药品监测工作进行了针对性部署,要求各省市至少选择15家医疗机构作为国家级短缺药品监测哨点,由于药品短缺问题反映到临床需要时间,可能会导致上报信息存在滞后性。2017年6月,原国家卫计委等多部门联合发布了《关于改革完善短缺药品供应保障机制的实施意见》(以下简称“意见”),精准部署了药品供应保障工作,进一步明确了完善药品短缺供应保障机制和措施。由国家指导地方各级部门分析处理上报信息,并将监测平台建设工作的牵头部门归为原卫计委。但由于各省的平台管理职权划分不一致,可能导致监管分工不明确,且未要求公开监测点处理短缺问题的信息,可能导致生产、流通企业无法掌握药品短缺现状。
3.2 省级短缺药品监测预警实施现状分析
江苏:率先建立了省级短缺药品信息平台,在全省范围内建立短缺药品信息“每月零报告”制度,结合监测点直接报告和其他机构省、市、县三级逐级上报的方式,在短缺药品的上报系统中加入了实时动态预警和分析的功能来提高监测工作的精确度和效率[11]。由省医疗机构药品和医用耗材集中采购工作领导小组办公室对上报信息进行评价,并采取责任约谈、协商调拨等方式进行处理。
辽宁:出台了《辽宁省关于改革完善短缺药品供应保障机制的实施意见》,从药品生产企业、经营企业和医疗卫生机构层面开展三维监测,省、市、县分级联动应对,并采取省、市、县三级预警的方式,由各级行政部门对上报的信息层层核查、对比甄选,并上报预警。这是全国首次出台相关政策。该省还建立了药品短缺信息库,每季度向医疗机构和社会发布一次预警预报[12]。并采取协商调剂、临时采购、常态储备等措施处理药品短缺问题。
广东:依托省级第三方药品电子交易平台、深圳采购平台,整合国家短缺药品哨点检测。在收集药品短缺信息的基础上,将可能出现供应短缺的品种列为重点监控品种。同时,采取药品短缺清单制度对上报信息进行评价,并通过定点生产、完善药品储备推进委托议价及联合议价等方式应对药品短缺问题。
我国部分省份已建立省级药品信息平台,负责短缺药品监测预警,并采取了相应的“精准施策”,如江苏省上报系统的实施动态预警分析,辽宁省定期发布预警预报,广东省设立重点监控品种等。但由于各省的短缺药品信息监测平台实力差距悬殊,导致监测预警效果不均衡,而且大多数省份短缺信息获取主要依靠药品采购平台,获取渠道单一,药品采购信息不透明,缺乏相应的信息沟通机制[13]。
通过国内外药品短缺监测预警体系的对比分析(见表2)发现,我国在该领域起步较晚,政策实施时间较短,经验不足,在实施过程中存在一些问题。如在监测预警平台建设方面,各省的短缺药品监测预警平台依托省级药品集中采购平台,而监测预警平台工作的牵头部门归为原卫计委,可能导致职权责任划分不明确;在短缺信息收集方面,主要依靠医疗机构上报,导致信息上报存在一定的滞后性,且由于各医疗机构上报者对“药品短缺”的定义理解不同,对上报真实性的核查增加了信息处理部门识别的难度[14];在短缺信息公开方面,国家对于监测点的短缺问题向上级卫生部门汇报后信息公开无统一规定,仅有部分省份发布短缺清单,导致生产流通企业无法及时掌控药品短缺现状药品短缺现状并调整产能。

表2 国内外药品短缺监测预警体系对比分析
4 建议
4.1 细化各级部门具体职责
政府部门作为短缺药品监测预警实施的关键力量,在各项职责上仍有进一步细化的空间。各级部门应充分认识到实施短缺药品监测预警的重要性,加强部门间协作,明确并细化各级部门的职责,同时加大监管力度,推进药品短缺监测预警的实施。发挥政府的沟通协调作用,可以通过借鉴发达国家制订短缺药品管理指南,指南中应包括短缺药品定义、范围、成因、处理政策及解决方案等,从而引导各环节“对症下药”。
4.2 完善药品短缺信息采集平台建设
完善短缺药品预警监测体系的最有效形式就是建立短缺药品信息采集平台。我国对于药品短缺信息采集平台的建设还处在探索阶段,采集的信息主要来源于医疗机构监测点。首先,医疗机构应落实上报责任,提高上报的积极性,并保证上报信息的真实性和准确性;其次,可借鉴发达国家要求生产企业强制上报的要求,并在生产企业设置药品短缺联络人负责短缺信息的收集和上报。同时,采取定期对生产企业进行调查与约谈、建立上报奖励制度等方式,鼓励生产企业积极参与监测工作。也可通过在短缺信息采集平台中加入动态预警分析功能,强化省级机构短缺药品分析和处理责任,提高监测哨点的工作效率。
4.3 加强短缺药品信息沟通
国外应对药品短缺的监测预警制度中,共同点是加强了医院、医师、患者、药品生产企业等相关利益者对于药品短缺信息的沟通。基于利益相关者诉求,妥善建立合理的信息沟通机制,才能带来理想的监测预警实施效果[14]。可通过在官网上定期提供有关药品短缺的信息及有关预期短缺的预先通知,使相关者充分了解短缺药品的情况;实时动态监测,为药品短缺提供早期预警;及时公开短缺信息处理结果,根据药品短缺信息指导、协调生产企业积极应对。

