生长激素预处理在卵巢低反应患者体外受精治疗中的应用
葛小花,王建业,张雅梦,章志国,郑贤芳,周 平,曹云霞
卵巢低反应 (poor ovarian response, POR) 是卵巢对促性腺激素(gonadotropins,Gn) 刺激反应不良的病理状态,具体表现主要是促排卵周期Gn用量多、卵泡的发育少、血雌激素峰值低,导致取卵周期取消率高、获卵数少和临床妊娠率低。近年随着生育年龄的延迟,POR患者有明显增加趋势,且一直无有效的治疗方法。30多年前生长激素(growth hormone,GH)就被应用于辅助生殖领域,但因GH应用时,患者选择标准、卵巢刺激方案、GH治疗时间或优化剂量等方面没有共识,所以其改善体外受精结局的有效性一直存在争议[1-3]。该文回顾性分析136例POR患者,探讨GH预处理对POR患者体外受精(invitrofertilization,IVF)治疗结局的影响,以期发现GH更合理的用药方法。
1 材料与方法
1.1 病例资料回顾性分析2017年4月~2018年10月在安徽医科大学第一附属医院生殖中心就诊的136例POR患者,纳入标准基本参照2011年欧洲人类生殖和胚胎协会(European Society of Human Reproduction and Embryology,ESHRE)制定的POR博洛尼亚标准[4]:① 高龄(≥38岁)或存在卵巢反应不良的其他危险因素;② 前次IVF周期应用常规促排卵方案,最终表现符合POR的主要表现,其中获卵数≤3个;③ 卵巢储备下降抗苗勒氏管激素(anti miillerian hormone,AMH)<1.1 μg/L或窦卵泡计数(antral follicle count ,AFC)<5~7个或卵泡生成激素(follicle- stimulating hormone,FSH)>10 mU/ml](满足以上3条中的任意一条)。满足以上①②③标准任意2条。排除标准:① 男方原因引起的不孕患者;② 女方患有除卵子质量问题外严重影响妊娠结局的妇科疾病如:子宫内膜病变、引起宫腔形态变化的子宫肌瘤及子宫畸形、子宫腺肌症、卵巢手术史等;③ 女方合并内科疾病,包括代谢性、免疫系统疾病,如:糖尿病、甲状腺疾病、系统性红斑狼疮等;严重肝肾方面疾病,如:急性活动性肝炎、肝硬化、急行肾炎、慢性肾功能不全等。
研究分组间对照和自身对照。其中组间对照107例,应用GH预处理组(Gn启动前应用约4周的GH治疗,n=58)与非预处理组(Gn启动开始间断予以GH治疗,n=49),自身对照29例,移植或取卵失败后应用GH预处理(Gn启动前连续应用约4周的GH治疗);分别组间对照和自身对照比较Gn使用总量、使用天数、获卵数、胚胎数、优质胚胎数、种植率、生化妊娠率/生化妊娠数及临床妊娠率/临床妊娠数。
1.2 研究方法
1.2.1治疗方案 GH预处理:Gn启动前约4周开始用GH 2 U 皮下注射 1次/日,Gn启动日改为4 U皮下注射 1次/日直至人绒毛膜促性腺激素(human chorionic gonadotropin,HCG)日。GH非预处理:Gn启动日开始给予4 U皮下注射 1次/隔日直至HCG日。
所有患者均采用拮抗剂方案促排卵。Gn启动周期后通过阴道超声(transvaginal ultrasonography,TVS)监测子宫内膜厚度及窦卵泡直径,Gn具体用量根据卵巢反应调整。只有监测发现1个主导卵泡直径13 mm左右或血清雌二醇(estradiol,E2) >360 ng时才开始加用拮抗剂,且拮抗剂持续用至HCG日。当至少有2个优势卵泡直径≥ 8 mm时才停用Gn,给予扳机,扳机应用36 h左右在TVS引导下行穿刺取卵,术后给予黄体支持。再将培养至5 ~6 d的可利用囊胚全部冷冻,在取卵后第2次月经来潮开始人工周期准备内膜,待TVS监测宫内条件合适(内膜厚约9 mm左右、均匀、稳定且宫腔无积液)行解冻胚胎移植,移植胚胎1~2枚。移植后14 d测血HCG明确是否妊娠,30 d行B超检査妊娠囊数目和胎心管搏动情况明确是否临床妊娠。
1.2.2囊胚的分级标准 本研究中囊胚的分级标准是按照 Gardner囊胚分级法标准[5],对第5天(day 5,D5)胚胎或D6胚胎进行分级。Gardner囊胚分级标准首先根据囊胚的孵化程度和囊胚腔的大小,将囊胚发育分为6个时期:① 囊胚腔小于胚胎体积的一半;② 囊胚腔大于等于胚胎体积的一半;③ 完全扩张囊胚,囊胚腔完全占据了胚胎的总体积;④ 扩张囊胚,囊胚腔完全充满胚胎,胚胎总体积变大,透明带变薄;⑤ 正在孵出的囊胚,囊胚的一部分从透明带中逸出;⑥ 孵出的囊胚,囊胚从透明带中全部逸出。其中① ~②期为早期囊胚,③~⑥期的囊胚再根据囊胚内细胞团数目和滋养外胚层细胞数目分为A、B、C 3个等级。对内细胞团的评级标准如下:A:细胞多、致密;B:细胞数目偏少、松散分组;C:非常少的细胞。对滋养外胚层的评级标准如下:A:许多细胞形成黏附的上皮;B:少数细胞形成疏松的上皮;C:非常少的大细胞。将≥3BB的囊胚定义为优质囊胚。
1.2.3统计指标 ① 年龄、不孕年限、FSH、FSH/促黄体生成素(luteotropic hormone,LH)、身体质量指数(body mass index,BMI)、AFC;② Gn使用总量和使用天数、获卵数、胚胎数、优质胚胎数;③ 种植率、生化妊娠率/生化妊娠数、临床妊娠率/临床妊娠数。

2 结果
2.1 一般资料比较GH预处理组与非预处理组患者的年龄、不孕年限、FSH、FSH/LH、BMI和AFC的比较,差异无统计学意义(P>0.05)。见表1。
2.2 临床数据比较
2.2.1GH预处理组与非预处理组的比较 预处理组的Gn使用总量和使用天数明显少于非预处理组,且预处理组的胚胎数、优质胚胎数、种植率、生化妊娠率、临床妊娠率明显高于非预处理组,差异均有统计学意义(P<0.05),但获卵数无明显变化,差异无统计学意义(P>0.05)。见表2。
2.2.2GH预处理前后自身的比较 应用GH预处理后Gn的使用时间与总量少于预处理前,其获卵数、胚胎数、优质胚胎数、种植率、生化妊娠数、临床妊娠数均高于预处理前,差异均有统计学意义(P<0.05)。见表3。
3 讨论
本文通过对POR患者辅助生殖中应用GH治疗进行回顾性研究,发现不管是组间对照还是自身对照,GH预处理后Gn的使用总量和使用天数明显减少,其胚胎数、优质胚胎数、移植率、生化妊娠率/生化妊娠数、临床妊娠率/临床妊娠数明显升高,差异均有统计学意义(P<0.05);但组间对照中获卵数差异无统计学意义(P>0.05)。说明GH预处理在POR患者辅助生殖中能明显提高其优质胚胎数、生化妊娠率及临床妊娠率,且Gn用量少、时间短。而GH非预处理治疗仅能提高获卵数。
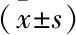
表1 GH预处理组与非预处理组患者的一般资料比较
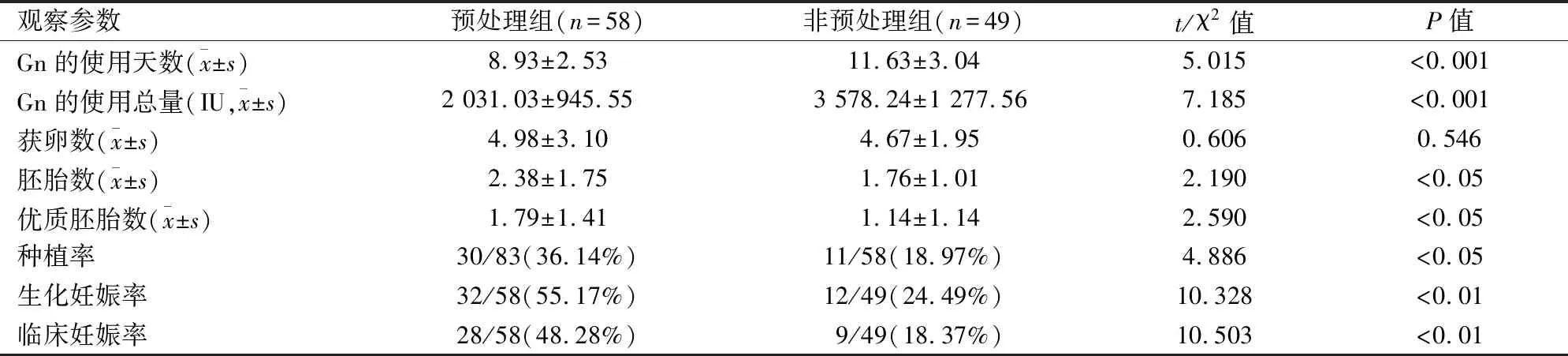
表2 GH预处理组与非预处理组患者的临床资料比较

表3 GH预处理前后自身的临床资料比较(n=29)
GH是由垂体前叶分泌的,调节脊椎动物生长发育的重要多肽类激素之一,包含191个氨基酸,在人体的细胞生长及新陈代谢上起重要作用。本研究结果与近年国内外多篇文献报道的一致。Choe et al[6]和吴洪波 等[7]研究表明GH的应用仅能提高获卵数,并不能改善妊娠结局,其中GH的应用方法分别为间断给药和Gn启动后给药。而Keane et al[8]和Cai et al[9]研究表明GH的应用可明显提高POR患者的IVF结局,其中Keane et al[8]指出GH 治疗时机为启动前4~6周、剂量为1~1.5 U/d、持续至HCG日,Cai et al[9]也指出GH的治疗时机为取卵前约6周,剂量为2 U/d,持续至HCG日。
但是本次研究也与有关文献[2-3]报道的不一致。Lattes et al[2]通过自身对照发现GH应用后获卵数和Gn量无差异,但临床妊娠率明显提高,用药方法为给予POR患者重复周期从Gn启动日开始予以GH 0.5 U/d,持续至HCG日。Dunne et al[3]研究显示GH应用并不能改善POR患者的优胚率和临床妊娠率,用药方法为微刺激方案前黄体期给予GH 10 U/d,持续14 d。通过对比显示,GH在POR患者体外受精中的作用取决于GH的应用时机、剂量和持续时间。
本研究表明GH在Gn启动前约4周小剂量的应用可明显改善POR患者的妊娠结局。原因可能是因为这个时机是小窦卵泡阶段,也是颗粒细胞发育及线粒体增殖的启动时机,这时应用GH有助于始基卵泡的募集与激活,能通过提高卵母细胞发育能力来提高胚胎的质量,而非仅仅的数量变化。然而,GH在生殖领域具体的作用机制目前为止仍不清楚。部分研究[10]认为,GH能改善POR患者的促排反应,与其增加卵泡液中胰岛素样生长因子- I (insulin- like growth factor- 1,IGF- I)的水平有关。Walters et al[11]研究表明IGF- I在调节体细胞和生殖细胞成熟和早期窦卵泡发育中起重要作用,且作用大小与IGF- I使用的剂量和阶段有关。这些与Serafim et al[12]的研究结果吻合。他们研究发现GH以剂量依赖性的方式维持卵泡形态,并与FSH联合刺激体外卵泡生长和E2的产生。这也与Dunne et al[3]的研究结果吻合,Dunne et al[3]在Gn启动前应用GH是觉得这样更有助于卵泡的募集,但结果没有达到预期的结果,可能是因为卵泡期缺少GH的维持。也有部分研究认为,GH通过促进卵泡液中GH受体的表达和线粒体的功能活力来提高着床前胚胎的发育潜能[13],也可通过提高卵泡液中GH的量来提高卵巢对Gn的敏感性,减少Gn量[14]。另少部分研究[15]显示GH对子宫内膜也有作用,GH不仅在诱导排卵和子宫内膜厚度的发育上起重要作用,而且可以提高子宫内膜的容受性。
综上所述,GH预处理能明显改善POR患者的IVF结局,既有临床实践结果支持,又有基础理论支持,为POR患者治疗提供一种新的思路。但因样本量小、回顾性分析中研究对象选择的偏倚以及GH在生殖领域具体作用机制仍不详,所以接下来需要大样本前瞻性研究来证实这一结果及探讨其具体作用机制。

