非衍生化溶剂体系制备再生纤维素膜及其性能研究
王澌洁 李怡 李丹 吴忠旋 蒲俊文
摘 要:以NaOH/尿素/硫脲、[Amim]Cl、[Amim]Cl/DMF和氯化胆碱/尿素低共熔溶剂4种溶剂作为纤维素浆粕的溶剂体系并制备再生纤维素膜。采用红外光谱、X射线衍射、热重分析、扫描电镜和万能材料试验机对再生纤维素及再生纤维素膜进行结构表征。结果表明,将纤维素溶解在不同溶剂体系中,再生纤维素晶型均由纤维素Ⅰ型转变为纤维素Ⅱ型,再生纤维素的结晶度、热稳定性及再生纤维素膜的力学性能均有不同程度的降低。从再生纤维素膜性能及成本核算方面考虑,[Amim]Cl /DMF溶剂体系制备再生纤维素膜效果最佳。
关键词:离子液体;低共熔溶剂;纤维素膜;性能
中图分类号:TS721;TQ352.7
文献标识码:A
DOI:10.11981/j.issn.1000-6842.2019.02.20
纤维素是植物光合作用的产物,是地球上最廉价、最丰富的生物质资源[1]。纤维素具有可再生、生物可降解等特点,其应用对减少环境污染和可持续发展方面具有重要意义。纤维素是葡萄糖通过β-14糖苷键连接的天然高分子化合物,分子间和分子内强烈的氢键作用使得纤维素不溶于大多数溶剂[2],这在很大程度上制约了纤维素的应用。
近年来,几种纤维素溶剂体系[3],如:N-甲基氧化吗啉 (NMMO)/H2O、LiCl/极性溶剂、胺基化合物/盐、多聚甲醛/二甲基亚砜(DMSO),除NMMO/H2O溶剂体系外,其他溶剂体系都存在溶解能力不强、不稳定、价格昂贵等问题,因而限制了其应用。NMMO/H2O溶剂体系溶解纤维素,虽然实现了纤维素纤维的绿色化工业生产,但NMMO高温易分解,使该体系在溶解纤维素过程中具有一定的危险性[4]。因此,开发合适的纤维素溶剂具有重要的意义。
Zhang等[5]研究发现,低温条件下,一定比例的NaOH/尿素或NaOH/硫脲体系对纤维素纤维具有很好的溶解作用,反应过程无衍生物的生成,制备方法简单、绿色无污染。查纯喜[6]研究发现,NaOH/尿素/硫脲体系(8∶8∶6.5, 质量比)较三组分的NaOH/尿素/水、NaOH/硫脲/水體系具有更好的溶解纤维素的能力,该体系在-10℃条件下能快速溶解平均聚合度为500的纤维素,并获得溶解度为6%的纤维素铸膜液。Swatloski等[7]报道,离子液体溶解纤维素后,利用离子液体溶解纤维素及碳水化合物已引起学术界和企业界的高度重视。但是能够溶解纤维素的离子液体大都存在熔点较高、黏度较大、价格昂贵、溶解时间长等缺点,导致再生纤维素严重降解,限制了离子液体在纤维素溶解转化方面的应用。许爱荣[8]提出,向不同咪唑类离子液体中添加极性非质子溶剂 (如DMSO)可以显著提高离子液体对纤维素的溶解能力。低共熔溶剂具有与离子液体相似的物化性质,且更加环保易得,是可以取代离子液体的新型绿色环保溶剂。低共熔溶剂是由一定化学计量比的季铵盐和氢键供体(HBD)组合成的两组分或多组分低共熔混合物[9]。由于季铵盐与氢键供体之间的相互作用使得低共熔溶剂的熔点大幅下降,显著低于各组分纯物质的熔点。刘会茹等[10]对不同配比的尿素/己内酰胺、尿素/乙酰胺和乙酰胺/己内酰胺3种低共熔溶剂进行研究;结果表明,固体有机物合成的低共熔溶剂可以直接溶解纤维素。因此,本课题对碱复合溶剂NaOH/尿素/硫脲、[Amim]Cl、[Amim]Cl/DMF及氯化胆碱/尿素低共熔溶剂4种溶剂体系溶解再生纤维素的工艺进行探讨,并对再生纤维素和再生纤维素膜的结构和性能进行分析比较。
1 实 验
1.1 实验材料
纤维素浆粕(预水解硫酸盐针叶木浆粕,聚合度为550,α-纤维素含量>95%,山东亚太森博浆纸有限公司),1-烯丙基-3-甲基咪唑氯盐(离子液体[Amim]Cl,上海爱纯生物科技有限公司),氯化胆碱、NaOH、尿素、硫脲、DMF由天津市恒兴化学试剂制造有限公司提供,均为分析纯。
1.2 实验仪器
傅里叶变换红外光谱仪(FT-IR,中国 Perkin Elmer Frontier);X射线衍射仪(XRD,XRD-6000,日本岛津);热重分析仪(TGA,DSCⅠ,瑞士Mettler Toledo);偏光显微镜(CX41,日本Olympus);扫描电子显微镜(SEM,JSM-7001F,日本JEOL);万能材料试验机(Z2.5,德国Zwick Roell)。
1.3 实验方法
1.3.1 溶剂体系的制备
称取一定质量的NaOH、尿素、硫脲,按照NaOH/尿素/硫脲(8∶8∶6.5,质量比)配制水溶液,充分溶解后在-15℃冰箱中冷冻备用。
将氯化胆碱与尿素按照1∶2的摩尔比,在100℃下磁力搅拌2 h,得到无色透明的低共熔溶剂。
配制[Amim]Cl/DMF(7∶3,质量比)的混合溶剂体系,备用。
1.3.2 纤维素在不同溶剂体系中溶解过程的形貌观察
取充分干燥的纤维素浆粕逐渐添加到预冷的NaOH/尿素/硫脲、90℃的[Amim]Cl、90℃的[Amim]Cl/DMF及90℃的氯化胆碱/尿素4种溶剂体系中并进行磁力搅拌,在偏光显微镜下观察纤维素的溶解情况,当观察视野范围内无纤维形态,即纤维素在各溶剂体系中溶解完成。
1.3.3 再生纤维素与再生纤维素膜的制备及其性能分析
(1)再生纤维素的制备
将粉碎后的纤维素浆粕在105℃条件下干燥24 h后备用。在90℃时,将1%(质量分数)的纤维素溶解于氯化胆碱/尿素体系中,静置脱泡后以水作为再生溶剂,制备再生纤维素。将4%(质量分数)的纤维素分别加入到预冷的NaOH /尿素/硫脲、90℃的[Amim]Cl及90℃的[Amim]Cl/DMF(7∶3,质量比)体系中溶解1 h,静置脱泡后以水作为再生溶剂,制备再生纤维素。
(2)再生纤维素膜的制备
将4%(质量分数)的纤维素分别加入到预冷的NaOH /尿素/硫脲、90℃的[Amim]Cl及90℃的[Amim]Cl/DMF(7∶3,质量比)体系中溶解1 h,静置脱泡后倾倒在干净玻璃板上,用刮刀迅速刮制出25 μm厚度的均匀薄膜。将玻璃板浸入蒸馏水中,洗脱溶剂后将膜取下,自然风干后得到再生纤维素膜。
利用FT-IR、XRD、TGA、SEM及万能材料试验机对再生纤维素及再生纤维素膜进行表征及分析。
2 结果与分析
2.1 纤维素溶解过程微观形态观察
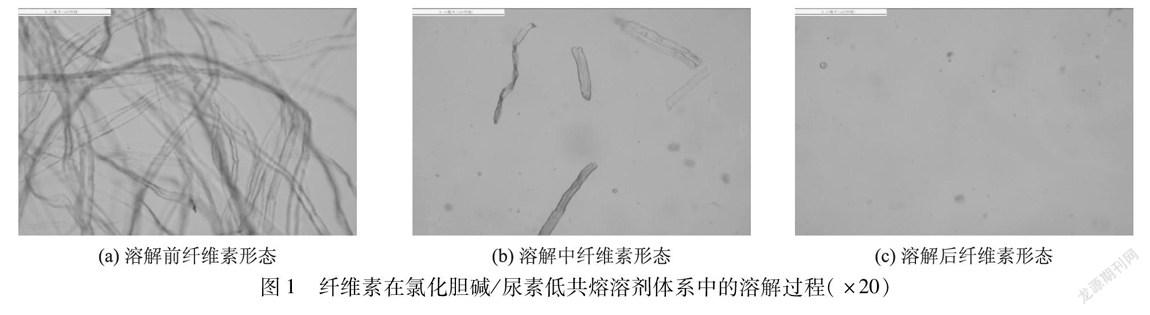
由于纤维素在不同溶剂体系中的溶剂具有相似的微观形态特点,现以氯化胆碱/尿素低共熔溶剂溶解纤维素为例探讨纤维素的溶解过程。在90℃条件下,纤维素溶解于氯化胆碱/尿素低共熔溶剂中,其溶解过程微观形态图如图1所示。由图1(a)可知,溶解前纤维素保有比较完整的纤维形态,由于氢键受体氯化胆碱与氢键供体尿素的相互作用,纤维素在氯化胆碱/尿素低共熔溶剂中逐渐溶解,纤维素出现大量的分丝帚化,并逐渐变短、变细。随着溶解过程的进行,大部分纤维素完全溶解,如图1(c)所示。由此可知,该体系具有溶解纤维素的能力,且适当地提高溶解温度,可加快纤维素的溶解以及提高纤维素的溶解度,这为低共熔溶剂溶解纤维素的应用提供了参考。通过对4种溶剂体系溶解纤维素过程的分析发现,氯化胆碱/尿素低共熔溶剂体系溶解纤维素的时间较长、纤维素溶解度相对较低,在制备再生纤维素膜方面有局限,因此还需寻找更合适的溶剂体系。
2.2 不同溶剂体系溶解再生纤维素的红外光谱图
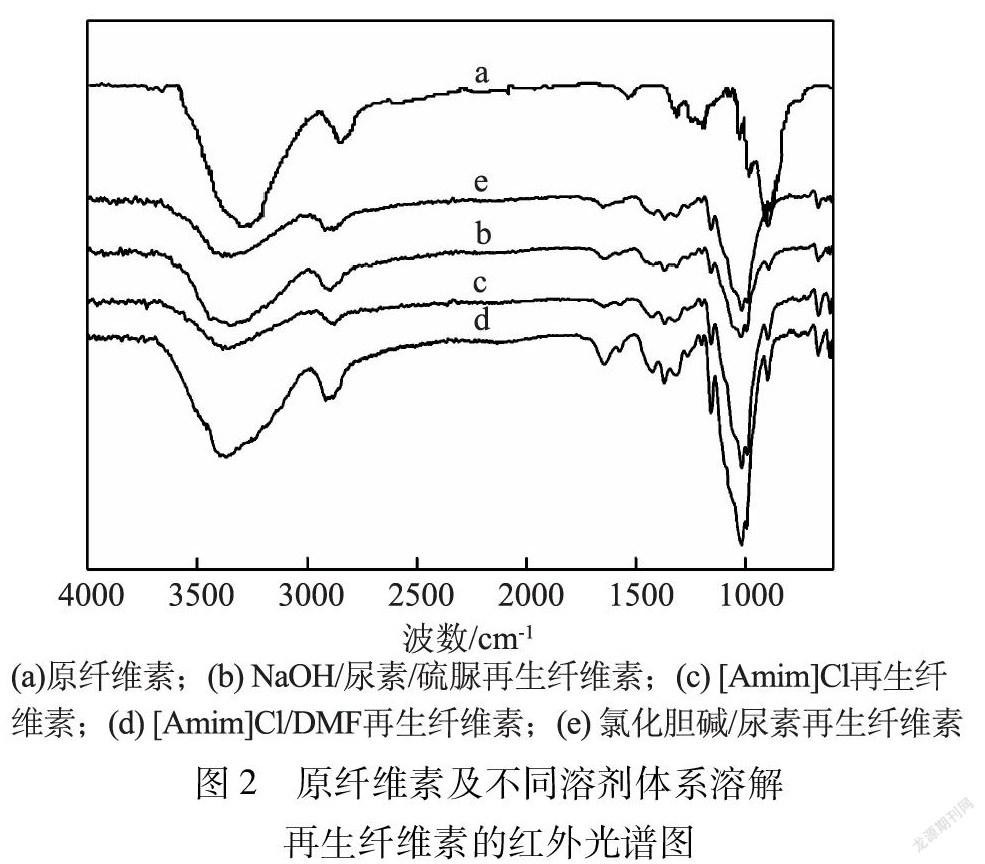
图2为原纤维素和不同溶剂体系溶解再生纤维素的红外光谱图。由图2可知,不同溶剂溶剂体系溶解制备再生纤维素的过程中,没有发生官能团的变化,可以推测不同溶剂体系溶解制备再生纤维素没有改变纤维素大分子的化学结构,即未发生衍生化反应。比较不同纤维素样品在3400 cm-1处的羟基伸缩振动峰可知,与原纤维素相比,不同溶剂体系溶解再生纤维素的羟基峰峰强都小于原纤维素的峰强,且都发生红移现象,这是由再生纤维素分子间和分子内氢键作用减弱引起的。并且不同溶剂体系溶解再生纤维素的紅外谱图中,1429 cm-1处的—CH2伸缩振动吸收峰减弱,并出现1422 cm-1处的—CH2剪切振动吸收峰,表明再生纤维素由纤维素Ⅰ型转变成纤维素Ⅱ型。
2.3 不同溶剂体系溶解再生纤维素XRD分析
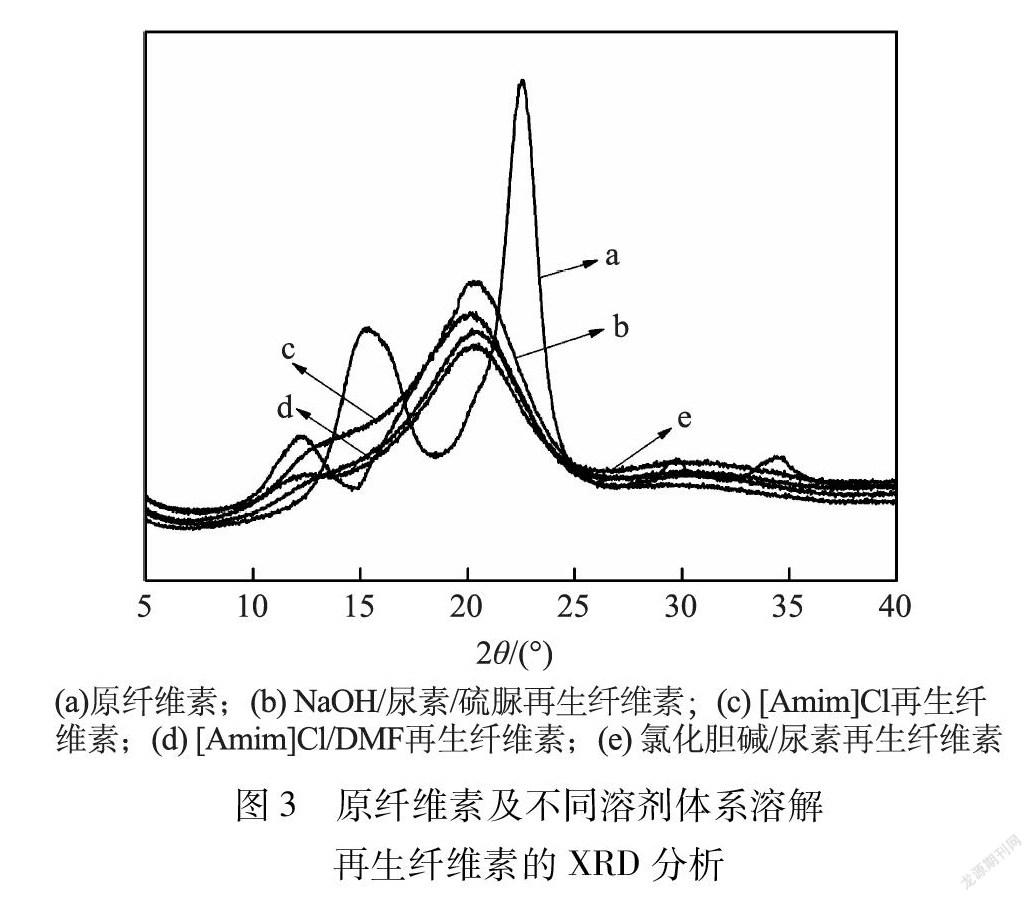
原纤维素及不同溶剂体系溶解的再生纤维素XRD分析结果如图3所示。由图3可知,原纤维素的主要衍射峰在2θ=15.3°、22.5°和34.4°处,是纤维素Ⅰ型的特征峰[11]。经不同溶剂体系溶解再生的纤维素衍射峰都在2θ=20°左右,为纤维素Ⅱ型的特征峰。由此可知,经过不同溶剂体系溶解再生的纤维素由Ⅰ型转变成Ⅱ型,再生纤维素仅发生晶态变化,反应没有其他副产物生成,这一结果与红外光谱图的分析结论一致。经计算,原纤维素的结晶度为60.7%,再生纤维素结晶度,由b到e分别为56.8%、46.4%、45.5%及54.6%,较原纤维素的结晶度均有所下降,说明再生纤维素的结晶区遭到破坏,部分结晶区转变为无定型区[12]。
2.4 不同溶剂体系溶解再生纤维素的热重分析
图4为原纤维素与不同溶剂体系溶解再生纤维素的热稳定性分析图。原纤维素和不同再生纤维素的热分解均分为3个阶段:初始裂解阶段、主要裂解阶段及焦热裂解阶段。由图4可知,在初始裂解阶段,由于各样品中残余水分的蒸发,原纤维素和不同再生纤维素在100℃附近均有轻微的质量损失。在主要裂解阶段,原纤维素比再生纤维素具有更好的热稳定性,热分解速率比各再生纤维素快,最大质量损失发生在360℃,持续到约400℃,此时固体剩余约为14%。原纤维素与不同溶剂体系溶解再生纤维素的热稳定性顺序为:原纤维素>[Amim]Cl再生纤维素>NaOH/尿素/硫脲再生纤维素>[Amim]Cl /DMF再生纤维素>氯化胆碱/尿素再生纤维素。NaOH/尿素/硫脲再生纤维素、[Amim]Cl再生纤维素、[Amim]Cl/DMF再生纤维素以及氯化胆碱/尿素再生纤维素分别在300℃、315℃、295℃和290℃开始出现明显热降解。这可能是因为纤维素经溶解再生后,聚合度下降,分子间的氢键数目减少使得分子间作用力减弱,所以导致热分解温度降低。
2.5 不同溶剂体系溶解再生纤维素膜的扫描电镜图
由于氯化胆碱/尿素体系溶解再生纤维素的溶解度较低,因此无法制备纤维素膜,现以其余3种溶剂体系制备再生纤维素膜。不同再生纤维素膜及原纤维素的扫描电镜图如图5所示。由图5可知,原纤维素的表面平整光滑,NaOH/尿素/硫脲体系溶解再生后的纤维素长度变短,膜表面凹凸不平,有空隙,说明纤维素在NaOH/尿素/硫脲体系中溶解得不是很好。[Amim]Cl和[Amim]Cl/DMF体系制备的再生纤维素膜表面平整、无空隙、具有致密的均相结构。由此可知,[Amim]Cl和[Amim]Cl/DMF体系溶解制备再生纤维素的效果最好,形成的再生纤维素膜形貌最佳。
2.6 不同溶剂体系溶解再生纤维素膜的力学性能
表1为不同溶剂溶解再生纤维素膜的力学性能。由表1可知,NaOH/尿素/硫脲体系溶解再生纤维素膜的力学强度最差,[Amim]Cl溶解再生纤维素膜的力学强度最好。[Amim]Cl/DMF溶解再生纤维素膜较[Amim]Cl溶解再生纤维素膜的力学强度下降,这可能是因为DMF的加入,破坏了纤维素分子链及结晶区,使再生纤维素的结晶度和再生纤维素膜的力学强度均有所下降。
3 结 论
对4种不同溶剂体系溶解再生纤维素膜的结构与性能进行比较,得出以下结论。
3.1 NaOH/尿素/硫脲、[Amim]Cl、[Amim]Cl/DMF和氯化胆碱/尿素低共熔溶剂体系均可直接溶解纤维素,不产生其他衍生物,且再生纤维素膜的形态发生明显变化,纤维素表面出现不同程度的破坏。
3.2 经不同溶剂体系溶解再生后的纤维素,其结构晶型均从纤维素Ⅰ型转变为纤维素Ⅱ型,再生纤维素的结晶度和热稳定性也均有所下降。经NaOH/尿素/硫脲体系溶解再生后的纤维素膜力学强度最差,[Amim]Cl再生纤维素膜力学强度最好,[Amim]Cl /DMF再生纤维素膜其次。
综上可知,NaOH/尿素/硫脲和氯化胆碱/尿素体系成本低廉,但是溶解条件苛刻、成膜性能不佳,难以实现工业化生产。[Amim]Cl/DMF溶剂体系制备的再生纤维素膜的性能较[Amim]Cl离子液体体系的略有下降,但从经济成本考虑,其溶解再生效果是最好的。基于DMF良好的助溶效果,有望得到高效低成本的复合离子液体溶剂,这对离子液体溶解制备再生纤维素及纤维素改性的应用方面具有重要的意义。
参 考 文 献
[1]Salmon S, Hudson S. Crystal Morphology, Biosynthesis, and Physical Assembly of Cellulose, Chitin, and Chitosan[J]. Journal of Macromolecular Science: Part C, 1997, 37(2): 199.
[2]Zhang Z, Wang R, Wang Y, et al. Study on the Development of Polymer Ionic Liquids[J]. Acta Polymerica Sinica, 2004(2): 63.
张振琳, 王荣民, 王云普, 等. 高分子离子液体的研究进展[J]. 高分子通报, 2004(2): 63.
[3]Ang L, Zhang L. Advance in Solvents of Cellulose[J]. Acta Polymerica Sinica, 2007, 7(10): 937.
[4]Heinze T, Schwikal K, Barthel S. Ionic Liquids as Reaction Medium in Cellulose Functionalization[J]. Macromolecular Bioscience, 2005, 5(6): 520.
[5]Zhang L, Dong R, Gao S. Dissolution and Regeneration of Cellulose in NaOH/Thiourea Aqueous Solution[J]. Journal of Polymer Science: Part B: Polymer Physics, 2002, 40(14): 1521.
[6]Zha C. Dissolution and Solution Properties of Cellulose in NaOH/Thio-urea/Urea Aqueous Solution[D]. Shanghai: Donghua University, 2007.
查純喜. 纤维素在氢氧化钠/硫脲/尿素水溶液中的溶解及溶液性质的研究[D]. 上海: 东华大学, 2007.
[7]Swatloski R P, Spear S K, Holbrey J D, et al. Dissolution of Cellulose with Ionic Liquids[J]. Journal of the American Chemical Society, 2002, 124(18): 4974.
[8]Xu A. The Dissolution and Selective Seperation for the Biomass Components with Anion-functionalized Ionic Liquids[D]. Lanzhou: Lanzhou University, 2010.
许爱荣. 阴离子功能化离子液体对生物质原料组分的溶解及选择性分离[D]. 兰州: 兰州大学, 2010.
[9]Zhang Q, De Oliveira Vigier K, Sébastien R, et al. Deep Eutectic Solvents: Syntheses, Properties and Applications[J]. Chemical Society Reviews, 2012, 41(21): 7108.
[10]Liu H, Zhou E, Zhang X, et al. Study of Deep Eutectic Solvents Prepared from Solid Organic Compounds and Their Application on Dissolution for Cellulose[J]. Materials Review, 2013, 27(20): 95.
刘会茹, 周二鹏, 张雪红, 等. 固体有机物合成的低温共熔溶剂的研究及其对纤维素的溶解[J]. 材料导报, 2013, 27(20): 95.
[11]French A D. Idealized Power Diffraction Patterns for Cellulose Polymorphs[J]. Cellulose, 2014, 21(2): 885.
[12]Guo Y, Wang X, Shu X, et al. Self-Assembly and Paclitaxel Loading Capacity of Cellulose-graft-poly(lactide) Nanomicelles[J]. Journal of Agricultural and Food Chemistry, 2012, 60(15): 3900.
Preparation of Cellulose Membrane in Non-derivative Solvents and Its Properties
WANG Sijie LI Yi LI Dan WU Zhongxuan PU Junwen*
(College of Materials Science & Technology, Beijing Forestry University, Beijing, 100083)
(*E-mail: jwpu@bjfu.edu.cn)
Abstract:Regenerated cellulose membranes were prepared in the presence of four types of solvent systems, namely NaOH/urea/thiourea, [Amim]Cl, [Amim]Cl/DMF and choline chloride/urea. Regenerated celluloses and regenerated cellulose membranes were analyzed by Fourier transform infrared spectroscopy (FT-IR), X-ray diffraction (XRD), thermogravimetry analysis (TGA), scanning electron microscope (SEM) and a universal tensile tester. It was found that the crystalline structure of regenerated celluloses transformed from cellulose I to cellulose II. Furthermore, the crystallinity, thermal stability and mechanical strength decreased. Considering the optimum properties of regenerated cellulose membranes and economic cost, the [Amim]Cl/DMF was the optimal solvent system for preparing the regenerated cellulose membranes.
Keywords:ionic liquid; deep eutectic solvent; cellulose membrane; performance

