个体化给药辅助决策系统JPKD和SmartDose在万古霉素个体化给药中的应用
林良沫 符祥俊 陈君 钟莉莉 吴琼诗 黄春新 王敏
摘 要 目的:評估个体化给药辅助决策系统JPKD和SmartDose在万古霉素个体化给药中的应用。方法:以2018年4月-2019年3月在海南省人民医院住院并静脉使用万古霉素的成人患者为研究对象进行回顾性研究。使用SmartDose预测万古霉素初始给药方案的稳态血药谷浓度,计算实测浓度与预测浓度之间的绝对权重偏差和相对预测误差。采用χ2检验或连续校正的χ2检验分析患者体质量指数(BMI)正常与否、急性肾损伤(AKI)发生与否分别对绝对权重偏差的影响。对于稳态血药谷浓度不达标的患者进行万古霉素给药方案调整,使用JPKD和SmartDose系统分别预测调整给药方案后的万古霉素稳态血药谷浓度,计算实测浓度与预测浓度之间的绝对权重偏差和相对预测误差,评估两者的预测能力并针对3例患者进行实例分析。结果:SmartDose预测初始给药方案的患者入组85例,其万古霉素稳态血药谷浓度预测值为(11.36±5.96) μg/mL(2.34~29.33 μg/mL),实测浓度为(11.44±6.57) μg/mL(3.10~29.50 μg/mL),绝对权重偏差为22.95%,相对预测误差为2.72%。BMI正常与否对绝对权重偏差有显著影响(χ2=4.75,P=0.029),AKI发生与否对绝对权重偏差无显著影响(χ2=0.236,P=0.627)。JPKD和SmartDose预测调整给药方案的患者入组22例,其万古霉素的稳态血药谷浓度预测值分别为(11.06±3.58)、(12.15±4.35) μg/mL,实测浓度为(12.57±4.50) μg/mL,绝对权重偏差分别为18.30%、18.68%,相对预测误差均值分别为-8.65%、-0.44%。两个系统预测值的绝对权重偏差均<30%。3例患者预测结果的绝对权重偏差也均<30%。结论:JPKD和SmartDose系统在临床应用中对万古霉素血药浓度具有良好的预测能力,可用于优化万古霉素个体化给药方案。
关键词 万古霉素;个体化给药辅助系统;JPKD;SmartDose;血药浓度;预测
ABSTRACT OBJECTIVE: To evaluate the application of individualization dosage auxiliary system JPKD and SmartDose in individualization administration of vancomycin. METHODS: A retrospective study was conducted among adult inpatients in Hainan Provincial People’s Hospital from Apr. 2018 to Mar. 2019 with intravenous use of vancomycin. SmartDose was used to predict the steady blood trough concentration of vancomycin in the initial dosage regimen, and the absolute weight deviation and relative prediction error between the measured concentration and the predicted concentration were calculated. The effects of body mass index (BMI) and acute kidney injury (AKI) on absolute weight deviation were analyzed by χ2 test or continuously corrected χ2 test. Vancomycin drug delivery scheme was adjusted for patients with ungualified steady blood drug trough concentration. JPKD and SmartDose system were used to predict the blood concentration of vancomycin after adjusting the dosage regimen. The absolute weight deviation and relative prediction error between the measured concentration and the predicted concentration were calculated. The prediction ability of the two systems was evaluated and 3 examples was analyzed. RESULTS: Predicted steady blood trough blood concentration of 85 included patients in SmartDose predicted initial dosage regimen were (11.36±5.96) μg/mL (2.34-29.33 μg/mL); the measured concentration was (11.44±6.57) μg/mL (3.10-29.50 μg/mL); absolute weight deviation was 22.95%, and the relative prediction error was 2.72%. Whether BMI was normal or not had significant effects on the absolute weight deviation (χ2=4.75, P=0.029), and whether AKI occurred or not had no significant effects on the absolute weight deviation (χ2=0.236, P=0.627). JPKD and SmartDose predicted that predicted steady blood trough concentrations of vancomycin in 22 included patients were (11.06±3.58) and (12.15±4.35) μg/mL, and the measured concentration was (12.57±4.50) μg/mL; absolute weight deviations were 18.30% and 18.68%; relative prediction errors were -8.65% and -0.44%, respectively. The absolute weight deviations of the predicted values of the two systems were less than 30%. The absolute weight deviations of prediction results were also less than 30% in 3 patients. CONCLUSIONS: JPKD and SmartDose system have good predictive ability for blood concentration of vancomycin in clinical application, and can be used to optimize the individualized administration of vancomycin.
KEYWORDS Vancomycin; Individualization dosage auxiliary system; JPKD; SmartDose; Blood concentration; Prediction
万古霉素是治疗耐甲氧西林金黄色葡萄球菌(Methicillin-resistant staphylococcus aureus,MRSA)感染的一线药物,其治疗窗窄,具有明显的个体差异,目前已有多部指南和专家共识用于指导万古霉素的临床应用,并且一致推荐进行治疗药物监测(Therapeutic drug monitoring,TDM)[1-5]。中国药理学会治疗药物监测研究专业委员会于2015年发布了我国首个治疗药物监测指南,通过对万古霉素TDM的必要性进行系统评价和Meta分析,明确表明万古霉素TDM可以显著提高治疗有效率和降低肾毒性[6]。指南建议非重症患者稳态血药谷浓度维持在10~15 μg/mL,重症患者维持在10~20 μg/mL,推荐选择符合各自医院患者的群体药动学(Poulation pharmacokinetics,PPK)模型和方法,提出基于模型给药有利于提高患者血药浓度达标率和细菌清除率[5]。已有多项研究表明,使用PPK模型有助于更加精准和个体化的给药方案设计[7-11]。
为了方便临床应用,一些操作简便、自动化程度高的用药辅助软件被开发出来,如台湾高雄医科大学开发的Java PK® for Desktop(JPKD)可用于多种药物的给药方案设计并可用于运行新的药动学模型,主界面包括“Input”“Output”和“Estimate”三个部分。近年来上海复旦大学附属华山医院牵头收集中国人群万古霉素PPK特征参数,结合R语言rjags包的最大后验贝叶斯反馈法开发出了个体化给药决策辅助系统SmartDose,可针对普通成人以及新生儿、老年人、神经外科患者等特殊人群制订个体化的给药方案,包括制订初始方案、根据监测结果调整方案和自定义方案三大功能模块[12]。上述两款软件均采用了基于贝叶斯和PPK的方法进行剂量调整的计算。我院于2014年开展万古霉素TDM工作,逐步将JPKD和SmartDose应用于临床,现将上述两种个体化给药辅助系统的临床应用情况进行分析,探讨二者在万古霉素个体化给药中的应用效果。
1 资料来源与方法
1.1 病例资料
以2018年4月-2019年3月在海南省人民医院住院并静脉使用万古霉素的成人患者为研究对象进行回顾性研究。纳入标准:(1)住院期间静脉使用万古霉素并至少监测1次血药浓度;(2)年龄≥18岁;(3)万古霉素血药浓度达到稳态;(4)采血方法、时间等均正确。排除标准:(1)年龄<18岁;(2)进行血液滤过、血液透析和腹膜透析;(3)万古霉素血药浓度未达到稳态;(4)采血方法或时间不正确。收集记录入组患者的身高、体质量、血肌酐、万古霉素给药剂量、万古霉素血药浓度等信息,采用美国慢性肾脏病流行病合作工作组开发的CKD-EPI公式计算肌酐清除率(CCR)[13],采用体质量(kg)与身高(m)平方的比值计算体质量指数(BMI)。
1.2 血药浓度监测方法
使用西门子Viva-E全自动药物浓度分析仪,采用均相酶放大免疫法测定万古霉素血药浓度,检测试剂盒为西门子公司万古霉素检测试剂盒(Emit®2000 Vancomycin Assay),定标试剂为西门子公司万古霉素定标液(Emit®2000 Vancomycin Calibrators),质控品为伯乐生物制剂公司血清质控品(Liquichek therapoutic drug monitoring control)。严格遵守试验操作规范和试剂使用说明绘制标准曲线和进行检测方法的质量控制,定量范围为2.0~50.0 μg/mL。
初始给药方案的稳态血药谷浓度监测时间为万古霉素血药浓度达到稳态后(肾功能正常者给药48 h后,肾功能不全者给药72 h后)的下次给药前0.5 h,采集2 mL静脉血,3 500 r/min离心5 min后,取上清液进行测定。如调整给药方案,则在至少给药3次后的下次给药前0.5 h方可采血复查[14]。
1.3 JPKD使用步骤
下载并安装JPKD软件,选择万古霉素,计算方法选择最大后验贝叶斯反馈法,在“Input”栏里选择患者性别,依次输入年龄(岁)、体质量(kg)、血肌酐(mg/dL)、单次给药剂量(mg)、给药间隔(h)、输注时间(h)、输注结束至取样的时间(h)以及患者已知的血药浓度(cs,μg/mL),点击中间的箭头即可在“Output”栏生成该患者的清除率(CL)和表观分布容积(Vd),在“Estimate”栏输入计划调整的给药剂量、给药间隔和输注时间,即可预测调整给药方案后万古霉素稳态血药谷浓度。
1.4 SmartDose使用步驟
登录SmartDose应用网站(网址为http://139.196.91. 207:280801/#/tdm/account/login),输入账号和密码进入个体化给药界面,监测药物选择万古霉素,人群依据患者科室选择“普通成人和老年患者”或者“神经外科患者”。该系统可用于预测患者初始给药方案的稳态血药谷浓度。选定患者人群后,在“初始方案”栏中输入患者年龄、体质量、血肌酐和性别即可估算该患者的CL和Vd,在“自定义方案”模块中选定给药间隔,输入初始给药剂量和输注时间,多次点击“添加”按钮即可生成该患者预测的血药浓度曲线图。将鼠标在曲线上移动可以显示相应时间点预测的血药浓度值,以给药48 h后下次给药前0.5 h显示的数值为初始给药方案预测的稳态血药谷浓度。对于初始给药方案的稳态血药谷浓度不达标的患者,在“调整方案”里可以输入调整的给药数据,录入完成后点击“确定”按钮可生成该患者新的CL和Vd。在“自定义方案”模块输入患者已知的浓度结果,设定目标浓度范围(普通患者10~15 μg/mL,重症患者10~20 μg/mL)和给药间隔,然后添加具体的给药时间、给药剂量和输注时间,随着模拟给药次数的增多,在系统右侧随即形成相应的血药浓度变化曲线,以给药至少3次后、下次给药前0.5 h的数值为调整方案后稳态血药谷浓度的预测值。
1.5 数据分析方法
按公式计算绝对权重偏差和相对预测误差,绝对权重偏差用于评价预测的精密度,相对预测误差用于评价预测的准确度。绝对权重偏差(%)=(│预测浓度-实测浓度│/实测浓度)×100%,相对预测误差(%)=[(预测浓度-实测浓度)/实测浓度]×100%。采用SPSS 19.0软件进行数据统计分析,描述性结果以x±s、中位数、极小值和极大值表示,组间差异采用χ2检验或者连续校正的χ2检验,考察BMI正常与否和急性肾损伤(AKI)发生与否对绝对权重偏差的影响,P<0.05表示有相关性。
2 结果
2.1 初始给药方案
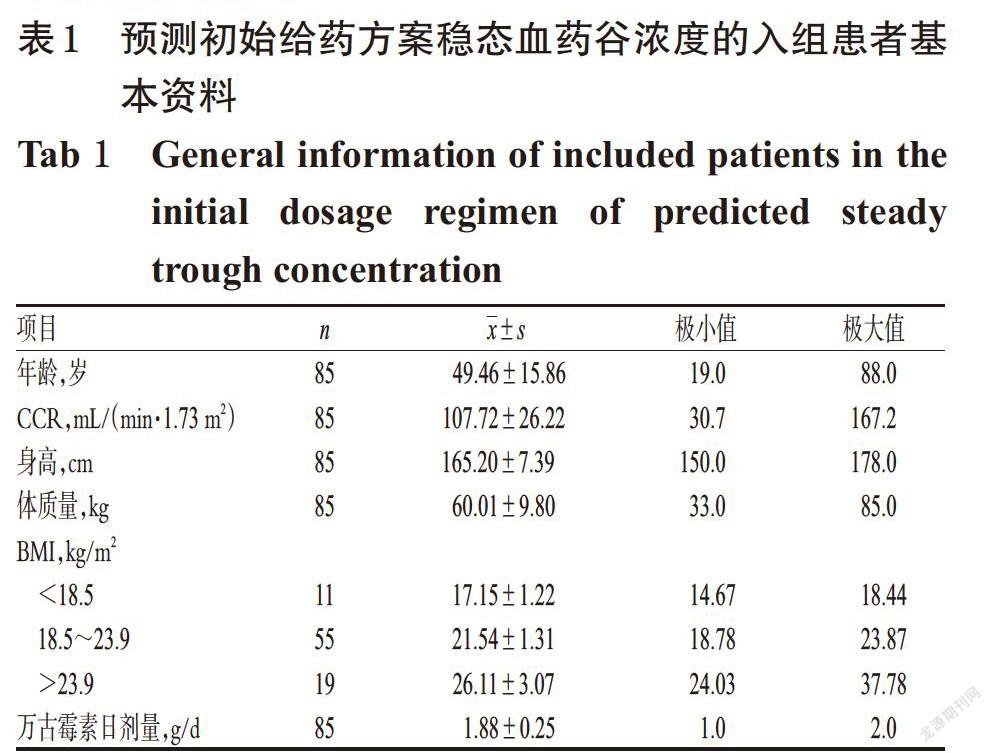
2.1.1 入组患者基本资料 入组预测首次血药浓度研究的患者共85例,其中男性62例,女性23例;平均年龄(49.46±15.86)岁,中位年龄50岁;万古霉素初始给药方案为1g,q12 h的55例;0.5 g,q6 h的13例;0.5 g,q8 h的14例;0.5 g,q12 h的3例。中国肥胖问题工作组建议我国成年人BMI 正常范围为18.5~23.9 kg/m2[15],因此本文按BMI<18.5、18.5~23.9、>23.9 kg/m2分为3组,入组患者分别为11、55、19例。入组患者的送检科室分别为血液内科31例、神经外科17例、重症医学科13例、急诊科5例、烧伤和皮肤修复科5例、呼吸内科5例、其他科室9例。预测初始给药方案稳态血药谷浓度的入组患者基本资料详见表1。
2.1.2 SmartDose预测结果 SmartDose估算85例患者万古霉素的CL和Vd均值分别为(5.18±2.35) L/h和(52.79±20.77) L,预测稳态血药谷浓度为(11.36±5.96) μg/mL(2.34~29.33 μg/mL),实测浓度为(11.44±6.57) μg/mL(3.10~29.50 μg/mL),计算绝对权重偏差为22.95%,相对预测误差为2.72%。参考何娟[16]的研究,以绝对权重偏差<30%作为软件对血药浓度预测能力较好的指标,本研究结果表明,SmartDose对初始给药方案的稳态血药谷具有较好的预测能力;同时相对预测误差的数值也较小,表明准确度较高。
2.1.3 BMI正常与否与绝对权重偏差间的相关性 BMI 正常范围为18.5~23.9 kg/m2。85例患者中,BMI正常者有55例,BMI均值为(21.54±1.31) kg/m2;BMI非正常者有30例,其中BMI<18.5 kg/m2的11例[(17.15±1.22) kg/m2],BMI>23.9 kg/m2的19例[(26.11±3.07) kg/m2]。绝对权重偏差≥30%的患者中有51.85%的BMI不在正常范围内,而绝对权重偏差<30%的患者中只有27.59%的BMI不在正常范围内。χ2检验结果显示,BMI正常与否和绝对权重偏差具有相关性,χ2=4.750,P=0.029<0.05。BMI正常与否与绝对权重偏差间的相关性考察结果见表2。
2.1.4 AKI发生与否与绝对权重偏差的相关性 血肌酐是反映患者肾功能的指标,在入组患者中共观察到9例患者在监测万古霉素血药浓度期间(前后3 d内)发生AKI,即48 h内血肌酐上升≥26.5 μmol/L[17]。选择连续校正的χ2检验结果显示,监测血药浓度时AKI发生与否与绝对权重偏差间无显著相关性,χ2=0.236,P=0.627>0.05。AKI发生与否与绝对权重偏差间的相关性考察结果见表3。
2.2 调整给药方案
2.2.1 入组患者基本资料 入组预测调整给药方案后稳态血药谷浓度研究的患者共22例,其中男性11例、女性11例;万古霉素初始给药方案为1 g,q12 h的15例;0.5 g,q6 h的3例;0.5 g,q8 h的2例;0.5 g,q12 h的2例;需增加剂量的11例,减少剂量的5例,仅调整频次的6例。预测调整给药方案后稳态血药谷浓度的入组患者基本资料见表4。
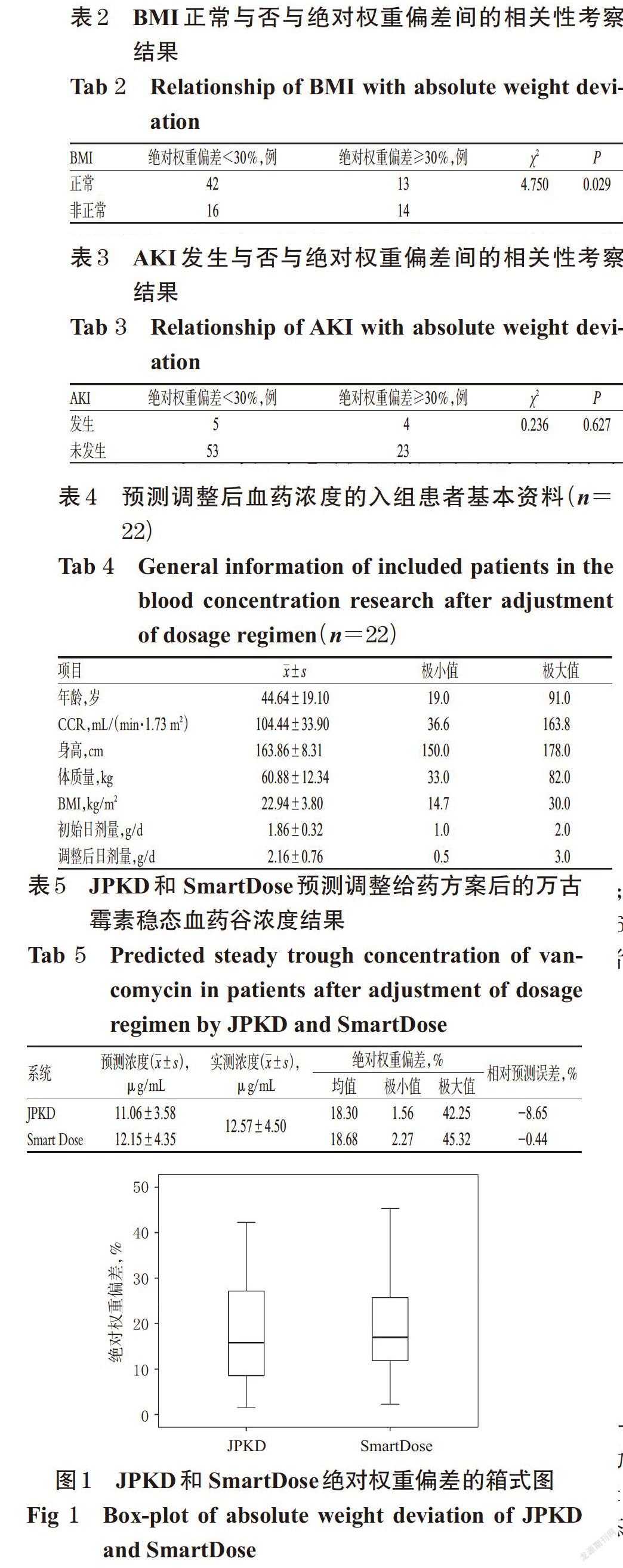
2.2.2 JPKD和 SmartDose预测结果 JPKD和 SmartDose估算22例调整给药方案后患者的CL分别为(6.22±2.77)、(5.60±2.81) L/h,Vd分别为(60.38±14.07)、(50.16±21.69) L,预测调整给药方案后的稳态血药谷浓度分别为(11.06±3.58)、(12.15±4.35) μg/mL,实测浓度均值为(12.57±4.50) μg/mL,可见两种方法的预测浓度与实测浓度均接近,且绝对权重偏差均<20%,提示两种方法均具有良好地预测调整后血药浓度的能力。SmartDose的相对预测误差小于JPKD,绝对权重偏差的箱式图可见SmartDose的绝对权重偏差数据离散分布较JPKD更集中,初步推测SmartDose比JPKD预测值更准确,但由于本研究样本量太少,结论需进一步验证。JPKD和 SmartDose预测调整给药方案后的稳态血药谷浓度结果见表5,JPKD和 SmartDose绝对权重偏差的箱式图见图1。
22例患者中,BMI正常者11例,BMI不正常者11例,在绝对权重偏差>30%的患者中有2例为BMI正常者,3例为BMI非正常者。同样按BMI正常与否分组进行连续校正的χ2检验,未观察到明显差异,可能与病例数过少有关。22例患者中有4例在监测血药浓度期间发生AKI,由于病例数太少,不另进行分析。
2.3 个体化给药辅助系统临床应用案例分析
2.3.1 案例1:干細胞移植术后患者万古霉素给药方案的调整
患者男性,30岁,体质量54 kg,确诊慢性粒细胞白血病6年余,2018年3月病程进入加速期,于2018年4月5日行造血干细胞移植术。移植后第9天患者发热,稍觉畏寒,便后肛周疼痛,考虑肛周软组织感染,另患者长期留置中心静脉导管,不排除导管相关性感染,因此在原广谱抗细菌和真菌的基础上加用万古霉素1 g,q12 h。4月11日辅助检查:白细胞计数0.05×109 L-1↓(↓表示低于正常范围)、中性粒细胞计数0↓(白血病患者移植前进行清髓性预处理,是会导致粒细胞减至0,供者干细胞植入后才会逐渐回升)、血红蛋白57 g/L↓、血小板计数12×109 L-1↓、血肌酐109.0 μmol/L、降钙素原0.76 ng/mL、C反应蛋白20.45 mg/L。万古霉素使用48 h后监测血药浓度为26.1 μg/mL,且血肌酐由4月14日的101.0 μmol/L升至4月16日的143.0 μmol/L,考虑为万古霉素浓度偏高易发生AKI。药师建议调整给药方案为0.5 g,q8 h,采用JPKD预测调整后的稳态血药谷浓度为21.09 μg/mL,采用SmartDose预测调整后的稳态血药谷浓度为21.12 μg/mL。调整方案3 d后复查血药浓度降至18.6 μg/mL,4月20日血肌酐降至83.0 μmol/L。计算JPKD和SmartDose两种方法预测浓度与实测浓度的绝对权重偏差分别为13.39%和13.55%,表明两种方法均有较好的预测能力。
2.3.2 案例2:重症医学科患者万古霉素给药方案的调整
患者男性,24岁,体质量70 kg。2018年12月24日因车祸致全身多处外伤入院,给予急诊手术后转入重症医学科进行监护和治疗。患者多处开放性损伤、皮肤软组织挫裂伤,体温升高,降钙素原3.13 ng/mL↑(↑表示高于正常范围),C反应蛋白158.74 mg/L↑,考虑为阴性菌和阳性菌混合感染,给予哌拉西林钠舒巴坦钠和万古霉素治疗。12月24日辅助检查:白细胞计数14.69×109 L-1↑、中性粒细胞计数9.14×109 L-1↑、血肌酐103.0 μmol/L、丙氨酸转氨酶78.8 U/L↑、天冬氨酸转氨酶183.7 U/L↑、白蛋白24.9 g/L↓。考虑到患者入院时存在应激性肾损伤,万古霉素初始劑量为0.5 g,q8 h。12月26日患者血肌酐降至85.8 μmol/L,采用SmartDose预测患者稳态血药谷浓度为5.49 μg/mL,当天实测浓度为6.8 μg/mL,绝对权重偏差为19.26%。药师认为6.8 μg/mL浓度偏低,建议调整给药方案为0.5 g,q6 h,每剂维持2 h,采用JPKD预测调整后稳态血药谷浓度为9.73 μg/mL,采用SmartDose预测调整后稳态血药谷浓度为9.83 μg/mL。医师采纳新的给药方案,12月29日复查万古霉素血药浓度升至10.50 μg/mL,计算JPKD和SmartDose两种方法调整后的预测浓度与实测浓度的绝对权重偏差分别为7.33%和6.38%,表明两种方法对调整给药方案后稳态血药谷浓度均具有较好的预测能力。
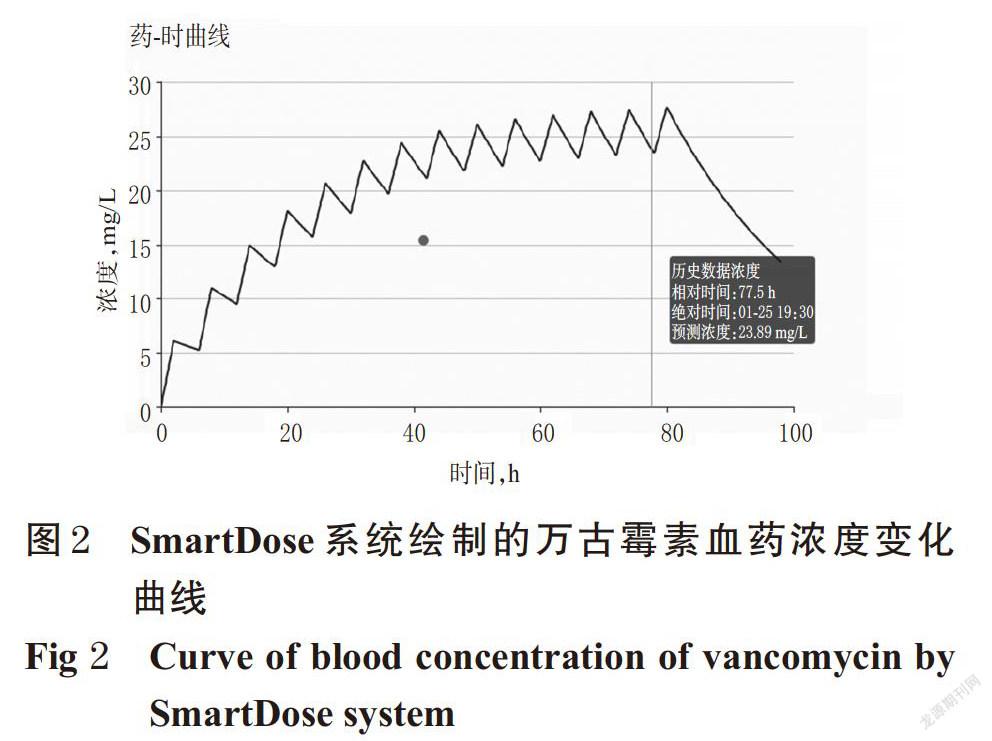
2.3.3 案例3:SmartDose绘制老年患者万古霉素血药浓度变化曲线
患者男性,88岁,体质量65 kg,因反复头痛4 d于2019年1月16日入院,入院6 d后患者血培养出金黄色葡萄球菌(MRSA,万古霉素最低抑菌浓度≤2 μg/mL),伴有畏寒高热,给予万古霉素0.5 g,q6 h治疗。1月22日辅助检查:白细胞计数13.6×109 L-1↑、中性粒细胞计数12.06×109 L-1、血肌酐87.0 μmol/L、丙氨酸转氨酶52.5 U/L、白蛋白20.8 g/L↓、C反应蛋白235.57 mg/L↑。患者1月22日晚22时给予首剂万古霉素,于1月24日早上监测血药浓度为15.4 μg/mL。药师认为该患者高龄,虽然CCR 68.2 mL/(min·1.73 m2)在正常范围内,但最好应当按照轻度肾功能不全患者给药,参照中国万古霉素治疗药物监测指南,肾功能不全的成人患者推荐给药72 h后监测稳态血药谷浓度。在SmartDose的“调整方案”模块中录入该患者前4 d的用药数据,生成万古霉素的血药浓度变化曲线,曲线结果显示,第4剂或者第5剂给药前预测的血药浓度尚未达稳态,给药结果偏低;而77.5 h的血药浓度23.89 μg/mL,与1月29日复查的实测浓度22.20 μg/mL非常接近,绝对权重偏差为7.6%,表明SmartDose具有较好的预测能力。此病例还提示,对于老年患者可能需要给药更长的时间,药物浓度才能达到稳态,尽管给药频次密集但仍然建议在给药72 h后监测稳态血药谷浓度。SmartDose绘制的万古霉素血药浓度变化曲线见图2。
3 讨论
3.1 JPKD和 SmartDose的应用体会
在使用过程中发现,JPKD和SmartDose都具有良好的对万古霉素血药浓度的预测能力,在没有条件进行TDM的情况下可以借助上述个体化给药辅助系统优化临床给药方案,实现个体化用药。JPKD是单机版,操作简便,具有自定义功能,可以在软件中建立新的模型公式,已有将其应用于临床并取得良好效果的报道[18]。SmartDose是网页版,操作界面美观且具有预测首次浓度的功能,可以形成剂量-浓度直方图和绘制血药浓度变化曲线并导出报告单,结果更直观、更有说服力。
3.2 预测浓度的影响因素
建立PPK模型的时候要求对采血时间和用药时间进行准确记录,但是在临床实际中护士执行医嘱的时间很难完全遵照q12 h或者q8 h,在采集血样时有时候也难以在给药前0.5 h采样,以上时间偏差可能会对预测结果造成一定影响。
万古霉素主要以原形经肾消除,当监测期间患者肾功能发生变化而使用软件预测时只采用一个肌酐数据可能也会影响预测结果的准确性。本研究中监测血药浓度期间患者是否发生AKI与预测浓度的绝对权重偏差之间未发现有相关性,可能与病例数过少有关,有待进一步研究。
近年来研究发现肥胖可导致万古霉素药动学发生改变,半衰期缩短、清除率升高[19-21],但仅参考体质量的数值难以反映患者的肥胖水平,BMI可能会是更好的参考指标。本研究结果显示,BMI正常与否与绝对权重偏差具有相关性。除了肥胖,患者的机体功能也同样影响药物代谢,重症患者机体功能差、合并疾病多、有创操作多、脏器功能受损、存在呼吸机支持和血液净化治疗等情况,使得药物在吸收、分布、代谢、排泄等方面发生较大变化[22]。中性粒细胞缺乏作为一种特殊的机体功能状态也可能影响万古霉素的代谢[23],对于中性粒细胞缺乏人群的药动学研究较少,同样需要进一步研究。申庆荣等[24]研究还发现,肝功能和外周水肿也可能影响万古霉素的血药浓度。可见影响万古霉素药动学的因素众多,不同的人群具有其特殊性,可能是造成预测偏差的重要因素之一。JPKD没有人群选择,而SmartDose分为“普通成人和老年患者”和“神经外科患者”两种人群,在使用过程可以进行选择。
本研究样本数较少,研究时间较短,存在较多不足之处。但通过TDM的临床实践证明,个体化给药辅助系统是群体药动学应用于临床的良好工具,可以发挥优化临床给药方案的作用,有利于提高治疗效果、减少药品不良反应,促进个体化治疗。
参考文献
[ 1 ] 陈春辉,李光辉.美国感染病学会治疗成人及儿童甲氧西林耐药金黄色葡萄球菌感染临床实践指南[J].中国感染与化疗杂志,2011,11(6):428-435.
[ 2 ] MATSUMOTO K,TAKESUE Y,OHMAGARI N,et al. Practice guidelines for therapeutic drug monitoring of vancomycin:a consensus review of the Japanese society of chemotherapy and the Japanese society of therapeutic drug monitoring[J]. JIC,2013,19(3):365-380.
[ 3 ] 萬古霉素临床应用剂量专家组.万古霉素临床应用中国专家共识:2011版[J].中国新药与临床杂志,2011,30(8):561-562.
[ 4 ] 万古霉素临床应用剂量专家组.万古霉素临床应用剂量中国专家共识[J].中华传染病杂志,2012,30(11):641- 645.
[ 5 ] YE ZK,CHEN YL,CHEN K,et al. Therapeutic drug monitoring of vancomycin:a guideline of the division of therapeutic drug monitoring,Chinese pharmacological society[J]. J Antimicrob Chemother,2016,71(11):3020-3025.
[ 6 ] YE ZK,TANG HL,ZHAI SD. Benefits of therapeutic drug monitoring of vancomycin:a systematic review and meta-analysis[J]. PLoS One,2013,8(10):e77169.
[ 7 ] 陈冰,杨婉花.群体药物动力学在万古霉素治疗监测的应用[J].中国临床药理学杂志,2011,27(9):712-716.
[ 8 ] 史欣.当前形势下群体药代动力学在万古霉素治疗药物监测的应用漫谈[J].中国医药指南,2014,12(30):337-378.
[ 9 ] 何笑荣,刘志鹤,季双敏,等.中国患者人群中万古霉素的群体药代动力学研究及药效预测[J].药学学报,2014,49(11):1528-1535.
[10] 蒙龙,方芸. NONMEM法建立成年人的万古霉素群体药代动力学模型[R].第四届全国治疗药物监测学术年会.北京:中国药理学会治疗药物监测研究专业委员会,2014.
[11] 宋林,田晓江,田维金,等.万古霉素在新生儿和小婴儿患者中的群体药动学研究[J].中国新药与临床杂志,2017,36(4):215-220.
[12] 高玉成,焦正,黄虹,等.万古霉素个体化给药决策支持系统的研制[J].药学学报,2018,53(1):104-110.
[13] 王寅,王蓓莉.肾小球滤过率计算公式的发展和比较[J].检验医学,2015,30(7):668-672.
[14] 何志超,伍俊妍,邱凯锋.万古霉素个体化给药临床药师指引[J].今日药学,2015,25(2):78-82.
[15] 何耀.我国超重/肥胖流行趋势及其对公共卫生的挑战[J].中华流行病学杂志,2014,35(4):345-348.
[16] 何娟,杨婉花.基于群体药动学的万古霉素个体化给药模式的建立和临床应用[J].中国临床药学杂志,2015,24(1):27-31.
[17] KHWAJA A. KDIGO clinical practice guidelines for acute kidney injury[J]. Nephron Clinical Practice,2012,120(4):179-184.
[18] 赖珺,李欣晴,吴丽丽,等.万古霉素个体化给药流程的建立及案例分析[J].中国医院药学杂志,2018,38(15):1656-1660.
[19] GRACE E. Altered vancomycin pharmacokinetics in obese and morbidly obese patients:what we have learned over the past 30 years[J]. Antimicrob Chemother,2012.DOI:10.1093/jac/dks066.
[20] ALVAREZ R,LÓPEZ CORTÉS LE,MOLINA J,et al. Vancomycin:optimizing its clinical use[J]. AAC,2016.DOI:10.1128/AAC.03147-14.
[21] 凌静,蒋艳,邹素兰,等.基于群体药代动力学研究胱抑素C对万古霉素药动学参数的影响[J].中国药房,2018,29(20):2821-2827.
[22] 董芊汝,赵夕岚,翟所迪.重症监护病房患者万古霉素治疗药物监测的系统评价[J].中国临床药理学杂志,2015,31(13):1358-1360.
[23] 李萍,陈恳,刘维,等.中性粒细胞缺乏患者的万古霉素临床抗感染治疗分析[J].临床药物治疗杂志,2017,15(3):1-3.
[24] 申庆荣,李刚,卢秋玉,等.万古霉素血药浓度的影响因素分析[J].中国抗生素杂志,2017,42(5):429-431.
(收稿日期:2019-06-05 修回日期:2019-08-07)
(编辑:邹丽娟)

