注射用血塞通治疗脑梗死恢复期瘀血阻滞证的随机对照研究
李楠楠 孟繁兴 高芳 高燕洁 李迎春 陈志刚
摘要 目的:評价注射用血塞通(冻干)治疗脑梗死恢复期瘀血阻滞证的有效性和安全性。方法:采用区组随机、盲法、阳性药/安慰剂平行对照、多中心临床研究的方法,选取2012年10月至2014年1月北京中医药大学东方医院收治的脑梗死恢复期患者282例,随机分为观察组(高剂量)105例、阳性药对照组35例、低剂量组71例及安慰剂组71例。疗程均为15 d。观察各组患者治疗前后美国国立卫生研究所卒中量表(NIHSS)评分、改良Rankin量表(mRS)评分、Barthel指数、中医证候积分、各项生命体征及相关实验室检查的变化,并观察不良反应。结果:观察组在改善NIHSS评分、mRS评分、Barthel指数及中医证候方面疗效皆优于阳性药物组、低剂量组、安慰剂组,差异有统计学意义( P <0.05);观察组与其他各组比较,能明显改善中医单项症状中下肢不遂、口舌歪斜、舌强言謇或不语、偏身麻木、头痛、头晕、唇色紫暗( P <0.05)。各组不良反应发生率差异无统计学意义( P >0.05)。结论:注射用血塞通(冻干)用于脑梗死恢复期疗效好,安全性较高。
关键词 注射用血塞通;脑梗死;恢复期;随机对照研究;瘀血阻滞证;卒中量表;盲法
A Randomized Controlled Trial of Xuesaitong for Injection in the Treatment of Stagnation of Blood Stasis Syndrome during Cerebral Infarction
Li Nannan,Meng Fanxing,Gao Fang,Gao Yanjie,Li Yingchun,Chen Zhigang
(Department of Encephalopathy,Dongfangl Hospital,Beijing University of Chinese Medicine,Beijing 100078,China)
Abstract Objective: To evaluate the efficacy and safety of freeze-dried Xuesaitong injection in the treatment of cerebral infarction with blood stasis syndrome at the recovery stage. Methods: A total of 282 subjects who were selected from October 2012 to January 2014 in Dongfang Hospital affiliated to Beijing University of Chinese Medicine were randomly divided into experimental (high-dose) group,positive drug group,low-dose group and placebo group with a course of treatment of 15 days.Changes in National Institutes of Health Stroke Scale (NIHSS) score,modified Rankin Scale (mRS) score,Barthel index,the efficacy score of traditional Chinese medicine (TCM) syndromes,vital signs,and related laboratory examination of each group were observed.Moreover,adverse reactions were observed. Results: Compared with the positive drug group,low-dose group and placebo group,the efficacy score of NIHSS,mRS,Barthel,and the TCM syndromes in the experimental group improved ( P <0.05).The experimental group had an advantage of TCM syndromes include paralysis of lower limb,skew of tongue and mouth,stiff tongue,dysphasia and aphasia,hemianesthesia,headache,dizziness,oral dark purple ( P <0.05).The incidence of adverse reactions showed no statistical differences among each group. Conclusion: Application of freeze-dried Xuesaitong injection in the treatment of cerebral infarction with blood stasis syndrome at the recovery stage presents certain efficacy and high safety.
Key Words Freeze-dried Xuesaitong injection; Cerebral infarction; Recovery stage; Randomized controlled trial
中图分类号:R743.33 文献标识码:A doi: 10.3969/j.issn.1673-7202.2019.02.028
脑梗死是一种严重威胁中老年人健康的疾病。我国脑卒中的发病率为120~180/10万人口,每年新发病例超过150万,其中60% ~80%的病例为脑梗死患者[1-3]。同时,脑梗死是成人致残的重要病因,严重影响患者的生命质量,给家庭和社会带来沉重的负担。目前脑梗死治疗以急性期及一、二级预防治疗为主,众多诊治指南很少涉及脑梗死恢复期及后遗症期的治疗。但是不可否认,脑梗死恢复期的治疗对于脑梗死患者生命质量的改善及远期预后有较大影响。本研究应用中药制剂注射用血塞通治疗脑梗死恢复期瘀血阻滞证,取得了良好的效果。现报道如下。
1 资料与方法
1.1 一般资料 选取2012年10月至2014年1月,包括北京中医药大学东方医院在内10家分中心的脑梗死恢复期(中医中风-中经络、瘀血阻滞证)患者282例,采用区组随机法随机分为观察组105例、阳性药对照组35例、低剂量组71例及安慰剂组71例。观察组中男49例,女56例;年龄38~76岁,平均年龄(60.51±8.89)岁;病程14~90 d,平均病程(43.21±22.36)d。阳性药对照组中男18例,女17例;年龄44~75岁,平均年龄(59.16±9.31)岁;病程15~86 d,平均病程(46.06±23.12)天。低剂量组中男33例,女38例;年龄35~76岁,平均年龄(59.32±9.42)岁;病程14~86 d,平均病程(45.55±24.06)d。安慰剂组中男34例,女37例,年龄38~76岁,平均年龄(59.32±9.42)岁; 病程15~90 d,平均病程(45.55±24.06)d。4组患者一般资料比较,差异无统计学意义( P >0.05),具有可比性。
1.2 诊断标准 西医诊断标准参照国际公认对缺血性脑血管病的病因学TOAST亚型分类标准拟定,入选患者均符合西医大动脉粥样硬化性脑梗死的诊断标准(属于前循环障碍)。中医诊断标准参照《中风病诊断疗效评定标准》(试行)[4]及《中药新药临床研究指导原则》(2002年版)[5]拟定。本研究已获得各中心伦理委员会批准(伦理审批号2012081504-2)。
1.3 纳入标准 符合西医大动脉粥样硬化性脑梗死的诊断标准;符合中医中风病-中经络、瘀血阻络证诊断;2周≤病程≤3个月;神经功能缺损(NIHSS)评分>7分且<21分;签署知情同意书者。
1.4 排除标准 1)经诊断为短暂性脑缺血发作、脑出血、脑栓塞、腔隙性梗死、蛛网膜下腔出血及心源性脑梗死等患者;2)由其他心脏病合并房颤引起的脑栓塞者;3)有慢性肝、肾功能障碍者;4)服用治疗脑梗死中西药物或停用治疗药品不足5个半衰期(中药1周以上);5)妊娠或哺乳期妇女;6)对三七、乙醇过敏或易过敏体质者;7)合并有严重心、肺、肝、肾疾病者。
1.5 脱落与剔除标准 患者病历资料缺失或不配合研究。
1.6 治療方法 所有患者均给予基础用药,即阿司匹林肠溶片,口服,1片/次,1次/d。在基础用药的同时,观察组(高剂量组)给予注射用血塞通(冻干)400 mg(昆药集团股份有限公司,国药准字:Z20026438)静脉点注,1次/d;阳性药对照组给予灯盏细辛注射液(云南生物谷药业股份有限公司,国药准字:Z53021620)40 mL,静脉点注,1次/d;低剂量组给予注射用血塞通(冻干)200 mg(昆药集团股份有限公司,国药准字:Z20026438),静脉点注,1次/d;安慰剂组给予0.9%氯化钠注射液250 mL,静脉点注,1次/d。各组给药周期均为15 d。
1.7 观察指标
1.7.1 疗效性指标 包括美国国立卫生研究所卒中量表(NIHSS)、改良Rankin量表(病残程度)、中医证候疗效、ADL量表(Barthel指数),其中以卒中量表(NIHSS)、改良Rankin量表(病残程度)及中医证候疗效为主要评价指标。
1.7.2 安全性指标 观察包括试验中出现的不良事件、血常规+网织红细胞计数、尿常规、便常规+潜血、心电图和肝功能(ALT、AST、TBIL、γ-GT、ALP)、肾功能(BUN、Cr)、凝血四项等,其中以不良反应发生率为主要安全性评价指标。
1.7.3 具体观察时点 人口学资料、诊断性指标及实验室指标在基线点诊查,其中部分指标在试验终点复查;中医证候和一般体检项目每次就诊时诊查;试验中出现的不良事件在用药后随时观察。
1.8 疗效判定标准 1)NIHSS评分疗效评价:根据美国国立卫生研究所卒中量表(NIHSS)评价标准[6-7]:基本痊愈:评分减少≥90%;显著进步:评分减少>45%<90%;进步:评分减少≥18%≤45%;无变化:评分减少或增加<18%;恶化:评分增加>18%。2)中医证候疗效评定[8]:临床痊愈:临床症状体征消失或基本消失,证候积分减少≥95%;显效:临床症状、体征明显改善,证候积分减少≥70%,<95%;有效:临床症状体征均有好转,证候积分减少≥30%,<70%;无效:临床症状体征均无明显改善或加重。
1.9 统计学方法 采用SPSS 20.0统计软件进行数据分析。计量资料用均数±标准差 ( ±s) 表示,采用 t 检验或Wilcoxon秩和检验;计数资料用率(%)表示,采用χ2检验或CMH检验。以 P <0.05为差异有统计学意义。
2 结果
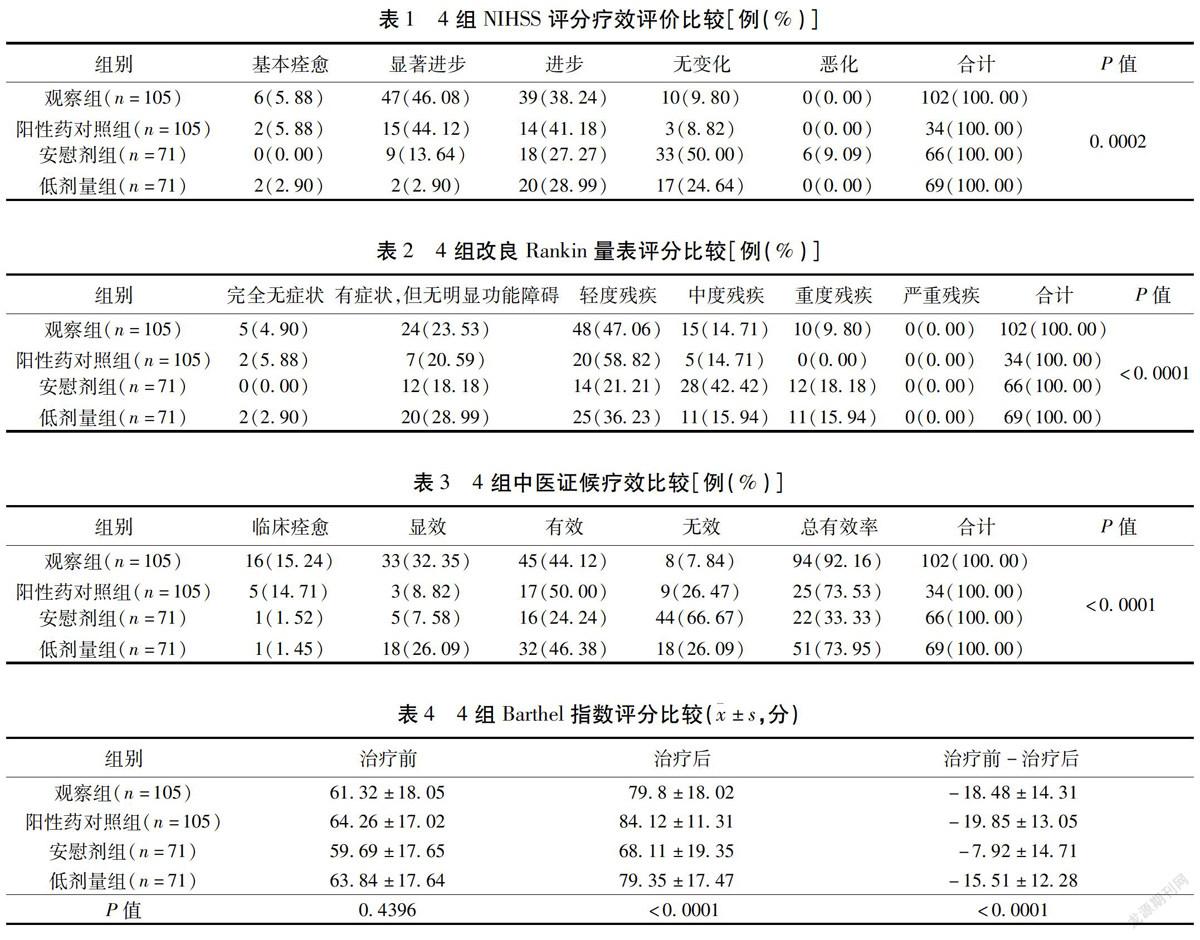
2.1 4组NIHSS评分疗效比较 用药后4组间比较,差异均有统计学意义( P <0.05)。两两比较:观察组、阳性药对照组、低剂量组与安慰剂组比较,差异均有统计学意义( P <0.0083),观察组与阳性药对照组、低剂量组比较,差异均无统计学意义( P >0.05)。见表1。
2.2 4组改良Rankin量表评分比较 用药后,4组改良Rankin量表评分比较,差异有统计学意义( P <0.05)。观察组、阳性药对照组、低剂量组分别与安慰剂组比较,差异均有统计学意义( P <0.0083);观察组与阳性药对照组、低剂量组比较,差异均无统计学意义( P >0.05)。见表2。
2.3 4组中医证候疗效比较 用药后,4组中医证候疗效比较,差异有统计学意义( P <0.05)。两两比较:观察组与其他3组比较,差异均有统计学意义( P <0.0083);阳性药组、低剂量组与安慰剂组比较,差异有统计学意义( P <0.0083);阳性药组与低剂量组比较,差异无统计学意义( P >0.05)。见表3。
2.4 4组单项中医症状疗效比较 用药后,4组间比较单项中医症状,差异均有统计学意义( P <0.05)。观察组主症下肢不遂、口舌歪斜、舌强言謇或不语、偏身麻木和次症头痛、头晕、唇色紫暗,与安慰剂比较,差异均有统计学意义( P <0.0083);主症口舌歪斜、舌强言謇或不语、偏身麻木和次症头晕、唇色紫暗,与阳性药对照组和低剂量组比较,差异均有统计学意义( P <;0.0083)。阳性药组主症下肢不遂、舌强言謇或不语、偏身麻木和次症唇色紫暗,与安慰剂组比较,差异均有统计学意义( P <0.0083)。低剂量组主症下肢不遂、口舌歪斜、舌强言謇或不语、偏身麻木和次症头晕、唇色紫暗,与安慰剂组比较,差异均有统计学意义( P <0.0083)。
2.5 4组Barthel指数评分比较 用药后,4组Barthel指数、Barthel指数改善及变化率比较,差异均有统计学意义( P <0.05)。观察组、阳性药对照组、低剂量组Barthel指数及Barthel指数改善与安慰剂组比较,差异均有统计学意义( P <0.0083),观察组、阳性药对照组及低剂量组之间比较,差异均无统计学意义( P >0.0083)。Barthel指数变化率仅观察组、阳性药对照组与安慰剂组比较,差异有统计学意义( P <0.0083)。见表4。
2.6 安全性评价 本次临床试验共发生不良事件9例(3.18%),其中观察组2例均为用药后尿白细胞异常,低剂量组2例,分别为手指割伤和肝功轻度异常,阳性药对照组患者1例发生肝功能异常,安慰剂组4例,分别为网织红细胞异常,白细胞计数异 常,尿白细胞异常,红细胞计数异常、血红蛋白异常和凝血酶原时间异常。患者不良反应发生均与用药无关,且无需特殊干预可自行恢复。4组不良事件发生率比较,差异无统计学意义( P >0.05)。
3 讨论
脑梗死是中老年人常见病、多发病,具有发病率高、致残率高、复发率高的特点,严重降低患者的生命质量[9-12]。脑梗死恢复期是指脑梗死后2周至6个月,这一时期患者脑梗死病情一般趋于稳定,多数脑梗死患者的临床症状尚未完全消失,在恢复期积极治疗和康复对于改善患者生命质量、减少后遗症的发生具有积极意义。但目前对于脑梗死的治疗主要针对急性期及一二级预防,对于脑梗死恢复期及后遗症期的关注较少,国际国内都没有成熟的方案和指南。中医药在脑梗死恢复期的应用较为广泛且效果显著,具有较好的临床研究价值。
注射用血塞通(冻干)主要成分是三七总皂苷,三七总皂苷是中药三七的主要生理活性成分。三七为五加科人参属植物的干燥根,性甘,微苦,温,具有活血化瘀、消肿止痛、滋补强壮的功效,故注射用血塞通(冻干)的功能主治为活血祛瘀、通脉活络。现代药理研究[13-15]表明,三七总皂苷通过抑制血小板活性、促进纤维蛋白原活性及清除氧自由基等机制发挥抗动脉粥样硬化的作用。研究结果[16-18]表明,三七总皂苷能够通过降低血栓的湿重达到抑制血栓的作用。有研究[19]发现,三七总皂苷可抑制血小板聚集、舒张脑血管、改善红细胞变形能力、改善缺血区的微循环等。以上药理研究均表明,三七總皂苷对于脑梗死后神经功能损伤、缺血区微循环障碍等均具有改善作用,可见注射用血塞通改善脑梗死恢复期患者症状证据充分。
本研究采用多中心、随机、双盲、阳性药平行对照临床研究,以行业公认中西医量表作为疗效评价标准,以临床广泛应用的灯盏细辛注射液作为阳性对照药,研究结果表明,注射用血塞通(冻干)改善脑梗死(恢复期)(瘀血阻滞证)患者中医临床证候疗效确切,高剂量注射用血塞通组能有效改善患者的中医证候,疗效优于阳性对照灯盏细辛注射液及安慰剂,提高了患者的生命质量;低剂量组与阳性对照灯盏细辛注射液改善患者中医证候疗效相当,但疗效优于安慰剂。NIHSS评分、Barthel指数及改良Rankin评分方面,注射用血塞通组较其他各组均差异无统计学意义,但是分值的改变较其他组具有优势。临床安全性评价方面,临床不良反应为轻度不良反应,无严重的不良事件发生。因此,在脑梗死恢复期瘀血阻滞证的临床治疗中,注射用血塞通(冻干)安全有效。
参考文献
[1] 孟亮亮,徐大伟,张敬,等.脑梗死后运动功能恢复机制的弥散磁共振成像研究进展[J].中华生物医学工程杂志,2015,l(12):91-94.
[2]金瑛,田勇,叶丹,等.护理干预对颅脑外伤保守治疗期间合并大面积脑梗死患者并发症及预后的影响[J].中华现代护理杂志,2014,20(17):2068-2070.
[3]顾志娥.应用临床护理路径对急性脑梗死静脉溶栓治疗的探讨[J].实用临床医药杂志,2014,18(20):25-27.
[4]国家中医药管理局脑病急症协作组.中风病诊断与疗效评定标准(试行)[J].北京中医药大学学报,1996,19(1):55-56.
[5]国家食品药品监督管理局.中药新药临床研究指导原则(试行)[S].北京:中国医药科技出版社,2002.
[6]李勇君,杨媛.脑梗塞超早期静脉溶栓治疗的护理体会[J].医药前沿,2014,21(7):255-256.
[7]易伟,罗娟.脑梗塞超早期静脉溶栓治疗的临床护理观察[J].中国保健营养(上旬刊),2014,24(5):2745-2746.
[8]肖桂荣,王赵伟,朱仁洋,等.丁苯酞注射液联合依达拉奉治疗急性脑梗死的疗效观察[J].中国神经免疫学和神经病学杂志,2016,23(1):51-54.
[9]黄华栋,施伟红,李冬辉,等.丁苯酞胶囊联合刺五加治疗急性脑梗死的临床研究[J].中国临床药理学杂志,2016,32(24):2218-2221.
[10] 孙秀芳,马丽,赫文清,等.脑梗死后遗症患者临床综合护理观察[J].中西医结合心血管病(连续型电子期刊),2014,9(13)167-168.
[11]曹祝华,邝艳云,黄伟珠,等.临床护理途径在初次脑梗死患者中的疗效对比分析[J].医学理论与实践,2015,8(13):1100-1102.
[12]方鹏飞,常丽霞,宋渊,等.三七总皂苷临床应用研究进展[J].中医药学报,2016,44(3):120-123.
[13]LIU J J,WANG Y T,QIU L,et al.Saponins of Panax notoginsengchemistry,cellular targets and therapeutic opportunities incardiovascular diseases[J].Expert Opin Investig Drugs,2014,23(4):523-523.
[14]臧妍妍,李衛红,郭晓谨,等.三七总皂苷对拟缺血损伤脑微血管内皮细胞转化生长因子-β、血管内皮生长因子表达的影响[J].云南中医学院学报,2016,39(2):1-4.
[15]程丽波.血塞通软胶囊治疗脑梗塞临床疗效观察[J].药学与临床,2014,8(6):147.
[17]段寅慧,吴敏.三七总皂苷药理研究及临床应用进展[J].中医药信息,2014,31(2):108-110.
[18]王东华,马斌,孙春燕,等.注射用血塞通(冻干)治疗脑梗死恢复期(瘀血阻滞证)的多中心临床研究[J].现代药物与临床,2017,21(10):1864-1871.
[19]程丽波.血塞通软胶囊治疗脑梗塞临床疗效观察[J].药学与临床,2014,8(6):147.

