青风藤碱血药浓度测定及其在家兔体内的药动学研究
朱丽媛 彭朝蕊 赵远翠 刘云宽 马云淑






中圖分类号 R969.1;R284.1 文献标志码 A 文章编号 1001-0408(2019)20-2767-05
DOI 10.6039/j.issn.1001-0408.2019.20.07
摘 要 目的:建立检测家兔血浆中青风藤碱浓度的方法,并进行药动学研究。方法:将家兔按性别分组,每组6只。所有家兔均于耳缘静脉单次注射青风藤碱药液(5 mg/kg),分别于给药前及给药后5、10、15、30、45、60、90、120、180、240 min时于其耳缘静脉取血1 mL,分离血浆,用乙酸乙酯萃取后,以青藤碱为内标,采用高效液相色谱法(HPLC)测定。色谱柱为Agilent Zorbax Extend-C18,流动相为甲醇-2 mmol/L磷酸氢二钠水溶液(含0.016%三乙胺,pH为9.8)(45 ∶ 55,V/V),流速为1 mL/min,检测波长为262 nm,柱温为30 ℃,进样量为20 μL。采用DAS 3.0软件计算药动学参数,采用t检验考察两组的差异。结果:青风藤碱检测血药浓度的线性范围为0.1~5.0 mg/L,定量下限为0.1 mg/L,最低检测限为0.08 mg/L;日内、日间RSD均小于10%,准确度为(99.80±8.21)%~(103.61±8.55)%,提取方法不影响待测物的定量分析。家兔静脉单次注射青风藤碱的平均药-时曲线符合二室模型,所有家兔的分布半衰期为(10.99±2.52)min,消除半衰期为(147.08±32.41)min,AUC0-t为(190.82±30.82)mg·min/L,AUC0-∞为(289.82±73.27)mg·min/L;雌、雄家兔主要药动学参数组间比较,差异均无统计学意义(P>0.05)。结论:本研究建立的HPLC法操作简便、专属性强、灵敏度高,可用于青风藤碱血药浓度的测定及药动学的研究。该化合物在家兔体内的药动学过程符合二室模型,药动学参数无性别差异,且分布迅速、消除较快。
关键词 青风藤碱;药动学;家兔;血药浓度;高效液相色谱法
ABSTRACT OBJECTIVE: To establish a method for concentration determination of sinoacutine in rabbit plasma, and to conduct its pharmacokinetic study. METHODS: The rabbits were grouped according to gender, 6 rabbits in each group. Rabbits were injected with sinoacutine solution (5 mg/kg) via ear vein. Each blood sample 1 mL was collected before medication and 5, 10, 15, 30, 45, 60, 90, 120, 180, 240 min after medcation. After the plasma isolated and extracted with ethyl acetate, HPLC method was adopted by using sinomenine as internal standard. The determination was performed on Agilent Zorbax Extend-C18 column with mobile phase consisted of methanol-2 mmol/L disodium hydrogen phosphate aqueous solution (containing 0.016% triethylamine, pH 9.8) (45 ∶ 55, V/V) at the flow rate of 1 mL/min. The detection wavelength was set at 262 nm, and column temperature was 30 ℃. The sample size was 20 μL. The pharmacokinetic parameters were calculated by using DAS 3.0 software. The difference of 2 groups were investigated by t-test. RESULTS: The linear range of sinoacutine were 0.1-5.0 mg/L; the limit of quantitation was 0.1 mg/L, and the lowest detection limit was 0.08 mg/L. RSDs of intra-day and inter-day were both less than 10%; the accuracy ranged from (99.80±8.21)%-(103.61±8.55)%. The extraction method did not affect the quantitative analysis of the substance to be measured. The average plasma-time curve of sinomenine with single intravenous injection in rabbits was in line with the two-compartment model. The distribution half-life of all rabbits was (10.99±2.52) min, and the elimination half-life was (147.08±32.41) min. AUC0-t was (190.82±30.82)mg·min/L, and AUC0-∞ was (289.82±73.27) mg·min/L. There was no statistical significance in pharmacokinetic parameters between female and male rabbits (P>0.05). CONCLUSIONS: Established HPLC method is simple, specific and sensitive, and can be used for plasma content determination of sinoacutine. Pharmacokinetic study shows that the pharmacokinetic process of the compound is in line with two-compartment model in rabbits. The pharmacokinetic parameters of the compound have no sex difference, and the compound is distributed rapidly and eliminated fast.
KEYWORDS Sinoacutine; Pharmacokinetics; Rabbit; Plasma concentration; HPLC
青风藤碱(Sinoacutine,结构式见图1A)為异喹啉类生物碱,是从防己科千金藤属云南地不容(Stephania yunnanensis Lo)等多种植物中提取分离而得[1]。研究发现,青风藤碱具有镇静、镇痛、抗炎、抗心律失常等活性,例如青风藤碱能明显提高小鼠热板痛阈和足趾电刺激痛阈,减少醋酸所致的小鼠扭体次数;与戊巴比妥钠联用后,可增强后者的镇静催眠作用[2];此外,青风藤碱还具有抗Ⅱ型胶原蛋白致大鼠类风湿性关节炎的作用,并可明显降低氯仿致小鼠室颤的发生率[3-4]。本课题组前期研究发现,青风藤碱能明显缩短氯化钡致心律失常模型大鼠恢复窦性心律所需的时间。青风藤碱的结构与青藤碱(Sinomenine,结构式见图1B)极其相似,后者具有抗炎、免疫调节、抗肿瘤、保护受损器官及镇痛等广泛的药理活性[5-7]。目前已有多种青藤碱制剂上市,如正清风痛宁片/缓释片、盐酸青藤碱注射液等,被广泛应用于类风湿性关节炎、心率失常等症的临床治疗,效果较好[8]。本课题组前期研究发现,在同等剂量下,青风藤碱对诱导型一氧化氮合酶(iNOS)表达和c-Jun氨基末端激酶(JNK)磷酸化水平的抑制作用均强于青藤碱,极具开发价值;此外,有关青藤碱及其制剂的药动学研究报道较多[9-12],而青风藤碱药动学的相关研究则较少。鉴于此,本研究通过建立检测家兔血浆样品中青风藤碱质量浓度的高效液相色谱法(HPLC),对该化合物的体内药动学行为进行初步探讨,旨在了解其体内代谢特征,为青风藤碱后续制剂的开发及临床应用提供实验依据。
1 材料
1.1 仪器
1260型HPLC仪(美国Agilent公司);HSC-12A型氮吹仪(天津市恒奥科技发展有限公司);TGL-16G型高速台式离心机(上海安亭科学仪器厂);XK96-A型快速混匀器(姜堰市新康医疗器械有限公司);BT25S型分析天平[赛多利斯科学仪器(北京)有限公司];SK3300型超声机(上海科导超声仪器有限公司);BE-1100型四维旋转混合仪(海门市其林贝尔仪器制造有限公司)。
1.2 药品与试剂
青风藤碱原料药(纯度:98%)、青风藤碱对照品(纯度:98%)均为本实验室自制;青藤碱对照品(内标,中国食品药品检定研究院,批号:110774- 201808,纯度:供鉴别和含量测定用);甲醇为色谱纯,乙酸乙酯、乙胺等其余试剂均为分析纯,水为纯化水。
1.3 动物
SPF级健康家兔12只,雌雄各半,10~12周龄,体质量2.0~2.5 kg,购自昆明楚商科技有限公司,动物生产许可证号:SCXK(滇)K2018-0001。
2 方法与结果
2.1 色谱条件
色谱柱:Agilent Zorbax Extend-C18(250 mm×4.6 mm,5 μm);流动相:甲醇-2 mmol/L磷酸氢二钠水溶液(含0.016%三乙胺,pH为9.8)(45 ∶ 55,V/V);流速:1 mL/min;检测波长:262 nm;柱温:30 ℃;进样量:20 μL。
2.2 溶液的配制
2.2.1 青风藤碱标准溶液 精密称取青风藤碱对照品10 mg于10 mL量瓶中,用甲醇溶解并定容,制成质量浓度为1.0 mg/mL的对照品贮备液。取上述对照品贮备液适量,用甲醇进一步稀释,制成质量浓度分别为1.0、5.0、10.0、15.0、25.0、40.0、50.0 mg/L的青风藤碱系列标准溶液,于-20 ℃下密封保存,备用。
2.2.2 内标溶液 精密称取青藤碱对照品10 mg于10 mL量瓶中,用甲醇溶解并定容,制成质量浓度为1.0 mg/mL的内标贮备液。取上述内标贮备液适量,用甲醇进一步稀释,制成质量浓度为100.0 mg/L的内标溶液,于-20 ℃下密封保存,备用。
2.2.3 青风藤碱药液 精密称取青风藤碱原料药250 mg于50 mL量瓶中,加入10%柠檬酸溶液1 mL,超声(功率:400 W,频率:40 kHz)溶解,加生理盐水定容,制成质量浓度为5 mg/mL的青风藤碱药液(现配现用)。
2.3 血浆样品的处理
精密吸取血浆样品0.5 mL,加入100.0 mg/L内标溶液20 μL,涡旋3 min,加入乙酸乙酯3 mL,涡旋3 min,使用四维旋转混合仪萃取20 min后,以6 000 r/min离心10 min;精密吸取上清液2.4 mL,于50 ℃水浴中以氮气流吹干;残渣加入甲醇150 μL复溶,涡旋3 min后,以4 000 r/min离心10 min,取上清液,经0.22 μm微孔滤膜滤过,取续滤液20 μL,进样分析。
2.4 方法学考察
2.4.1 专属性 取空白血浆、空白血浆+内标(100.0 mg/L)+青风藤碱(50.0 mg/L)、雌性家兔给药后5 min的血浆样品各适量,按“2.3”项下方法处理(其中,空白血浆不加内标溶液)后,再按“2.1”项下色谱条件进样测定,记录色谱图。结果,各待测物的理论板数均大于4 000;内标与青风藤碱的保留时间分别约为20.8、24.3 min,呈基线分离,分离度大于1.5,且血浆内源性物质无干扰,详见图2。
2.4.2 线性关系、定量下限及最低检测限考察 精密量取家兔空白血浆450 μL,分别加入“2.2.1”项下青风藤碱系列标准溶液各50 μL,得质量浓度分别为0.1、0.5、1.0、1.5、2.5、4.0、5.0 mg/L的青风藤碱系列血浆样品,按“2.3”项下方法处理后,再按“2.1”项下色谱条件进样分析,记录色谱图。以待测物质量浓度(x,mg/L)为横坐标、待测物与内标的峰面积比值(y)为纵坐标进行线性回归,得回归方程为y=0.504 5x-0.072 9(r=0.999 5)。结果,青风藤碱检测血药浓度的线性范围为0.1~5.0 mg/L,定量下限为0.1 mg/L(信噪比为10 ∶ 1);以信噪比3 ∶ 1测得最低检测限为0.08 mg/L。
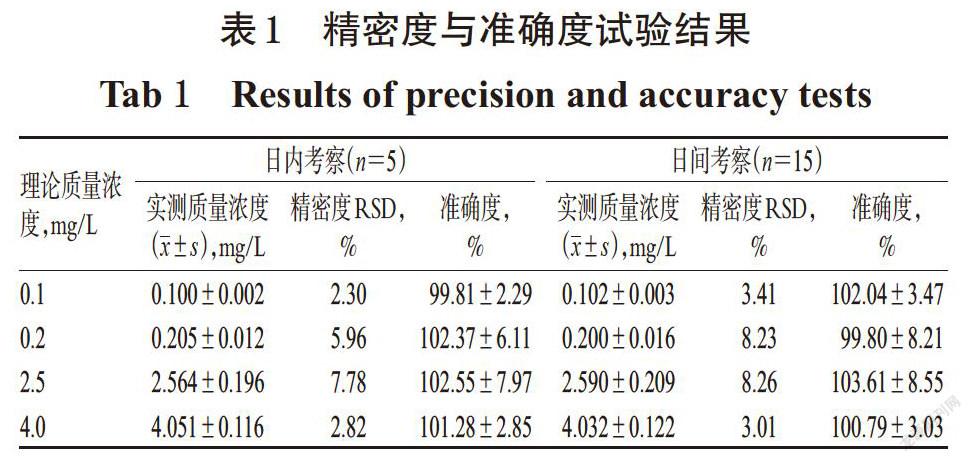
2.4.3 精密度与准确度试验 分别按“2.4.2”项下方法配制定量下限质量浓度(0.1 mg/L)血浆样品以及低、中、高质量浓度(0.2、2.5、4.0 mg/L,下同)的质控样品各5份,按“2.3”项下方法处理后,再按“2.1”项下色谱条件进样分析,考察日内精密度;连续测定3 d,考察日间精密度。同时,以实测质量浓度与理论质量浓度进行比较,考察准确度,结果见表1。
2.4.4 提取回收率试验 按“2.4.2”项下方法配制低、中、高质量浓度的质控样品各5份,按“2.3”项下方法处理后,再按“2.1”项下色谱条件进样分析,记录青风藤碱与内标的峰面积比值(R1);精密量取空白血浆适量,共5份,按“2.3”项下“精密吸取血浆样品0.5 mL……精密吸取上清液2.4 mL”方法处理后,加入相应质量浓度的青风藤碱标准溶液50 μL,使最终质量浓度与上述质控样品对应,以氮气流吹干,残渣用甲醇150 μL复溶,涡旋3 min后,以4 000 r/min离心10 min,取上清液滤过后,进样分析,记录青风藤碱与内标的峰面积比值(R2)。提取回收率=(R1/R2)×100%,结果见表2。
2.4.5 稳定性试验 按“2.4.2”项下方法配制低、中、高质量浓度的质控样品各5份,分别于室温放置24 h、反复冻融(-20 ℃~室温)3次、-80 ℃放置2周后,按“2.3”项下方法处理,再按“2.1”项下色谱条件进样分析,记录峰面积,以实测质量浓度与理论质量浓度的比值(即回收率)考察上述样品的稳定性,结果见表3。
2.5 药动学实验
将家兔按性别分组,每组6只。禁食、不禁水12 h后,于家兔耳缘静脉单次注射“2.2.3”项下青风藤碱药液5 mg/kg[参照本课题组前期所得小鼠静脉注射的半数致死剂量(54.319 mg/kg)并按体表面积折算法换算而得]。分别于给药前及给药后5、10、15、30、45、60、90、120、180、240 min时于家兔耳缘静脉取血1 mL,置于含肝素钠的抗凝管中,以10 000 r/min离心10 min后,分离上层血浆,按“2.3”项下方法处理后,再按“2.1”项下色谱条件进样分析,记录色谱图。采用内标法,按随行标准曲线计算家兔血浆中青风藤碱的血药浓度,并采用DAS 3.0软件绘制平均药-时曲线,并对上述平均药-时曲线数据进行分析,拟合房室模型,同时计算相关药动学参数;采用SPSS 20.0軟件对数据进行统计分析,数据以x±s表示,组间比较采用t检验,P<0.05为差异有统计学意义,结果见图3、表4。
由图3、表4可知,家兔静脉注射青风藤碱后的药-时曲线符合二室模型,不同性别家兔药动学参数比较,差异均无统计学意义(P>0.05)。所有家兔测得数据经处理,t1/2α为(10.99±2.52)min,t1/2β为(147.08±32.41)min,表明青风藤碱在家兔体内分布迅速、消除较快(t1/2β<3 h)。
3 讨论
3.1 内标化合物的选择
本研究采用内标法检测了家兔血浆中青风藤碱的质量浓度。在前期内标化合物的筛选中,笔者以色谱峰峰形及提取回收率为指标,对克班宁、异克利定、荷叶碱、光千金藤定碱、青藤碱等5种异喹啉类生物碱进行了考察。结果显示,上述化合物的提取回收率为67%~85%,RSD均小于15%,其中以青藤碱的提取回收率最为稳定且相对较高;此外,青藤碱与青风藤碱的保留时间虽较为接近,但峰形和分离度均较好,有利于缩短检测所需时间,故最终选择青藤碱作为内标。
3.2 色谱条件的优化及血浆样品处理方法的筛选
本研究在2015年版《中国药典》(一部)青风藤中青藤碱含量测定方法[13]的基础上对色谱条件进行了优化。结果发现,青风藤碱和青藤碱对流动相的比例和pH值非常敏感,最终本研究将色谱条件确定为甲醇-2 mmol/L磷酸氢二钠水溶液(含0.016%三乙胺,pH为9.8)(45 ∶ 55,V/V)。在血浆样品处理方法的筛选过程中,笔者分别尝试了蛋白直接沉淀法和液-液萃取法,先后以甲醇、乙腈以及异丙醇、乙醚、氯仿、乙酸乙酯单独或不同比例混合作为沉淀或萃取试剂[14-18]。经反复试验发现,经乙酸乙酯萃取后,待测物的峰形较为理想且分离度良好,回收率相对较高且稳定,故最终选择乙酸乙酯作为萃取溶剂。方法学考察结果显示,本研究所建HPLC法具有简便、专属性强和灵敏度高的优点,且提取方法不影响待测物的定量分析,符合生物样品定量分析的相关要求[19],可用于血浆样品中青风藤碱含量的测定。此外,本研究所建标准曲线的线性范围虽然较窄(0.1~5.0 mg/L),但由于后续药动学实验给药剂量单一、家兔体内血药浓度变化亦不大,故实用性尚可。
3.3 药动学研究结果分析
本课题组前期研究发现,青风藤碱在大鼠体内存在性别差异,故本研究比较了单次静脉给药后该化合物在雌、雄家兔体内的药动学行为,结果发现两者主要药动学参数并无显著差异。静脉给药后,青风藤碱的平均药-时曲线符合二室模型,t1/2α、t1/2β分别为(10.99±2.52)、(147.08±32.41)min,AUC0-t为(190.82±30.82)mg·min/L,AUC0-∞为(289.82±73.27)mg·min/L,提示青风藤碱在家兔体内分布迅速,且血药浓度下降速度快。关昊等[20]以家兔为对象,考察了静脉给予青藤碱(60 mg/kg)后的体内代谢特征,结果显示,青藤碱的平均药-时曲线符合二室模型,t1/2β为55 min;李鑫等[21]按100 mg/kg的剂量对家兔灌胃青藤碱后,发现其平均药-时曲线符合一室模型,tmax为(1.83±0.33)h,t1/2为(3.27±0.50)h,cmax为(2 867.5±246.76)ng/mL。上述研究提示,青藤碱在体内的消除速度与给药途径、给药剂量等密切相关。青风藤碱与青藤碱结构相近、理化性质相似,适当增加剂量、改变给药途径是否可延长t1/2、是否存在代谢饱和与非线性动力学过程等,尚需后续研究深入探讨。
综上所述,本研究建立的HPLC法操作简便、专属性强、灵敏度高,可用于青风藤碱血药浓度测定和药动学研究。青风藤碱在家兔体内的药动学过程符合二室模型,药动学参数无性别差异,具有分布迅速、消除较快的特点。但所建HPLC法存在分离时间较长、线性范围较窄等不足,有待后续研究予以完善。
参考文献
[ 1 ] 彭扶云.云南地不容的化学成分研究[D].昆明:云南中医学院,2014.
[ 2 ] 董文燊,瞿发林.青风藤药理作用及制剂临床应用研究概况[J].天津药学,2012,24(2):76-78.
[ 3 ] 史克勇.青风藤碱的药物新用途:中国,103417540A[P]. 2013-12-04.
[ 4 ] 汪波.云南地不容化学成分及呵朴菲型生物碱抗心律失常构效关系初步研究[D].昆明:云南中医学院,2013.
[ 5 ] 秦峰,蔡辉.青藤碱药理作用研究进展[J].现代中药研究与实践,2016,30(4):81-86.
[ 6 ] 抗晶晶,刘晓宁.青藤碱抗炎作用的新進展[J].中国野生植物资源,2017,36(6):32-35.
[ 7 ] 陈志杰,莫志贤.青藤碱抗肿瘤作用及机制研究进展[J].中国临床药理学杂志,2018,34(22):2671-2673.
[ 8 ] 朱士龙,陈迪钊,李勇,等.青藤碱最新研究进展[J].吉首大学学报(自然科学版),2011,32(5):95-100.
[ 9 ] 王华洋,李岩,魏海,等.青藤碱的制剂与药代动力学研究进展[J].上海中医药杂志,2010,44(10):84-89.
[10] YAN H,YAO M,LI HD,et al. Pharmacokinetics and penetration into synovial fluid of systemical and electroporation administered sinomenine to rabbits[J]. Biomed Chromatogr,2014,29(6):883-889.
[11] 丁涵滢,单连菊,王锐,等.青藤碱经皮给药制剂药动学及药效学的研究进展[J].中华中医药学刊,2016,34(5):1111-1113.
[12] XIE Y,JING ZH,ZHOU H,et al. The pharmacokinetic study of sinomenine,paeoniflorin and paeonol in rats after oral administration of a herbal product Qingfu guanjiesu capsule by HPLC[J]. Biomed Chromatogr,2014,28(9):1294-1302.
[13] 国家药典委员会.中华人民共和国药典:一部[S]. 2015年版.北京:中国医药科技出版社,2015:195-196.
[14] 谢彤,程学芳.基于HPLC-MS/MS的青风藤生物碱的药物代谢动力学研究[J].中国临床药理学与治疗学,2017,22(9):984-991.
[15] 刘秋梅,田卫伟,喻光燚,等.柱前衍生-HPLC测定白消安在家兔体内的药动学参数[J].中国现代应用药学,2018,35(9):1303-1313.
[16] 张敏,孔令希,罗成,等.山柰酚在家兔体内的药动学研究[J].中国药房,2014,25(43):4040-4042.
[17] 杨辉,周远大,何海霞,等.芳维甲酸乙酯在Beagle犬体内的药动学研究[J].中国药房,2017,28(25):3522-3524.
[18] 王凯,蒋大鹏,张伟,等. UPLC法测定大鼠血浆中那格列奈的浓度及药动学研究[J].中国药房,2017,28(31):4381-4383.
[19] 国家药典委员会.中华人民共和国药典:四部[S].2015年版.北京:中国医药科技出版社,2015:363-368.
[20] 关昊,邵继征.微透析技术研究盐酸青藤碱在家兔体内的药动学[J].今日药学,2017,27(10):666-669.
[21] 李鑫,谢志忻,魏艳霞,等.青藤碱在兔生理状态下血液及关节液的药动学研究[J].中国医院药学杂志,2017,37(14):1357-1360.
(收稿日期:2019-01-21 修回日期:2019-07-14)
(编辑:张元媛)

