心脏手术中皮肤压疮的预防及护理
吴家凤
(佛山市第一人民医院,广东 佛山 528000)
多数心脏手术患者术中需建立体外循环,加上受血流动力学等因素影响,皮肤压疮发生风险较高[1]。既往临床多采用常规皮肤护理预防压疮,但总体效果仍不理想[2]。本研究在36例心脏手术患者中行皮肤压疮预防护理,效果显著,报道如下。
1 资料与方法
1.1 一般资料 随机抽取2018年1月-2019年1月本院72例心脏手术患者,均符合手术指征,年龄≥18岁,且知情同意。摸球法分组:对照组(36例)男19例,女17例;年龄25-75(48.15±12.38)岁;16例瓣膜置换术,12例冠状动脉搭桥术,8例先天性心脏病矫形手术。研究组(36例)男19例,女17例;年龄24-76(47.76±10.23)岁;15例瓣膜置换术,14例冠状动脉搭桥术,7例先天性心脏病矫形手术。两组临床资料保持同质性(P>0.05)。
1.2 方法 对照组行常规皮肤护理,包括协助按摩皮肤、观察皮肤颜色、受压部位应用软枕等。研究组则实施皮肤压疮预防护理,内容包括以下几项内容。
1.2.1 术前 ①筛查皮肤高危人群:采用Barden量表[3]评估皮肤压疮风险,总分值范围6分-23分,以得分≤14分为高危人群;②皮肤准备:除对照组观察皮肤颜色、应用软枕外,还加强早期皮肤干预,如温水坐浴30min,俯卧于床上,轻擦、按摩骶尾部皮肤20 min,涂抹润肤霜等。
1.2.2 术中 ①保护受压皮肤:选择恰当手术床,保持舒适体位,确保肢体被动受限局部皮肤压强最小化;穿刺中心静脉、股动脉等部位时,采用棉垫防护,骶尾部以透明水胶体减压贴保护;②皮肤减压:同一体位下手术>2 h则适当调整体位,以局部皮肤测压仪动态检测压力,进行术中皮肤减压;③保温:合理调整室内温度、湿度,液体、血液输入前加温;密切观察末梢血液循环,一旦血氧饱和度或血压降低,积极处理,防止受压皮肤长时间处于低血氧、低灌注状态;④术毕评估:术毕再次观察受压皮肤,判断压疮发生情况。
1.2.3 术后 ①强化监测:每隔2 h检测1次骶尾部、肩胛部等皮肤;应用约束带或胸部固定带者,每隔4 h评估带下皮肤;②营养:早期给予肠外或肠内营养支持,确保每日热量、蛋白质、水摄入量充足,维持营养指标平衡,必要时行营养科会诊。
1.3 观察指标 比较两组术后压疮发生情况。依据《慢性伤口诊疗指导意见》[4]中压疮标准:无压疮,为正常;皮肤红、热、肿、麻,压力解除30 min皮肤颜色仍异常,为I期;皮肤红肿、硬,呈紫红色,存在表面水泡,为II期;皮肤表面水泡溃破,有黄色渗出液,为III期;坏死组织发黑,存在脓性分泌物,且感染扩展,为IV期。I期-IV期均为压疮。
1.4 统计学分析 以SPSS 20.0软件分析。资料以%和(Mean±SD)表示,以χ2和t检验。P<0.05为差异显著。
2 结果
研究组压疮发生率低于对照组(P<0.05)。见表1。
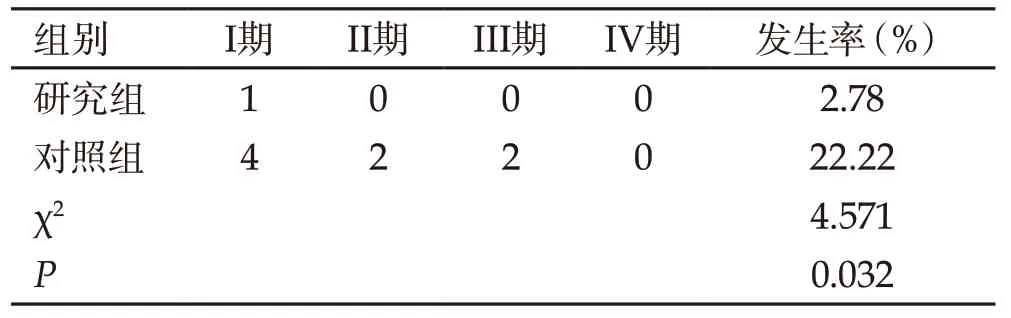
表1 两组压疮发生情况对比(n)
3 讨论
手术患者压疮危险因素较多,包括手术体位、空腹时间过长、受压部位皮肤、肢体活动等[5]。而心血管手术患者为压疮多发人群。陈沅等[6]分析成人心血管手术压疮发生与营养状况、手术时间、体位、体温、皮肤潮湿程度、摩擦力及剪切力等因素有关。但既往常规皮肤护理仅重视皮肤颜色、温度等观察,总体效果不佳。本次研究在研究组中应用皮肤压疮预防护理,自术前、术中、术后三个层面强化预防护理力度,措施更具针对性、客观性。其中,术前积极筛查高危人群,完善皮肤准备,可为压疮预防奠定基础;而术中积极保护受压部位皮肤,进行皮肤减压处理,预防低体温,术毕再次评估皮肤状况,可降低压疮发生风险;术后强化皮肤压疮监测,并进行营养干预,以改善肌肉及皮肤功能。本次研究中,研究组仅出现1例压疮,而对照组出现8例,发生率差异显著,凸显出皮肤压疮预防护理应用的有效性。
综上所述,心脏手术患者中应用皮肤压疮预防护理的效果显著,需引起高度关注。

