Co3O4/CeO2复合氧化物的制备及染料废水处理性能
田志茗,王元春
(齐齐哈尔大学 化学与化学工程学院,黑龙江 齐齐哈尔 161006)
全球工业化对环境产生了不利的影响,纺织品、药品、化妆品等行业把合成的有机染料排放进入环境,污染了地表水和地下水[1-2]。传统的吸附和降沉技术很难消除有毒的物质[3]。CeO2具有丰富的光谱学性质和紫外光吸收能力,因此铈氧化物可作为光催化剂在染料废水处理中得到应用[4-7]。但CeO2可见光吸收能力较弱,在应用中制备成氧化铈基复合材料;Co3O4具有窄带隙,可见光吸收能力强,酸碱性能可控的优点[8-11];Co3O4和CeO2的结合有效地抑制电子和空穴的复合,提高了CeO2的可见光吸收能力和应用范围。本文采用浸渍-焙烧法制备Co3O4/CeO2复合材料,研究降解染料中的催化活性,确定催化降解孔雀石绿染料的优化条件。
1 实验部分
1.1 试剂与仪器
硝酸铈、硝酸钴、氢氧化钠、柠檬酸、孔雀石绿均为分析纯;实验用水均为去离子水。
D8-FOCUS型X射线衍射仪;ESCALAB250Xi型X射线光电子能谱仪;Diamond TG/DTA型热重/差热综合分析仪。
1.2 催化剂的制备
CeO2的制备[12]:在超声的条件下将1.5 g Ce(NO)3·6H2O分散在5 mL去离子水中,得到悬浮液A;在超声的条件下将3.2 g氢氧化钠分散28.5 mL去离子水中,将其加入悬浮液A中,在磁力搅拌下保持15 min后,转移到反应釜中,在80 ℃下晶化10 h;冷却至室温,抽滤,用去离子水洗至中性,在100 ℃下干燥过夜,并在马弗炉中300 ℃下煅烧2 h。制得淡黄色CeO2固体样品。
Co3O4/CeO2复合材料的制备:将0.86 g CeO2和1.92 g柠檬酸在超声条件下分散在50 mL的去离子水中,在磁力搅拌下保持2 h,加入1.45 g 硝酸钴继续搅拌溶解,形成溶胶,将水蒸发得沉淀物。将沉淀物在80 ℃下干燥12 h,然后在马弗炉中500 ℃煅烧 4 h,制得黑色Co3O4/CeO2固体催化剂[13-15]。除不加CeO2外,其余按照上述的步骤制得黑色Co3O4样品。
1.3 催化剂的表征
采用X射线衍射仪对催化剂晶相进行分析;采用X射线光电子能谱仪对元素表面浓度、价态进行分析;TG/DTA型热重/差热综合分析仪对未煅烧样品的热稳定性进行分析。
1.4 催化降解孔雀石绿的实验
取50 mL 10 mg/L的孔雀石绿溶液于烧杯中,加入5 mg Co3O4/CeO2复合催化剂,吸附30 min,在给定的时间内从反应器中取出样品,离心,在620 nm处检测染料吸光度。然后,加入30 mmol H2O25 min后,离心样品,检测吸光度,用300 W氙灯照射样品,每15 min离心样品测定吸光度。根据脱色反应前后吸光度的变化计算孔雀石绿的脱色率,计算公式为:
式中D——孔雀石绿的脱色率,%;
C0——孔雀石绿溶液的初始浓度,mg/L,
A0——测得的孔雀石绿溶液的初始吸光度;
Ct——t时刻孔雀石绿溶液的浓度,mg/L;
At——t时刻孔雀石绿溶液的吸光度。
2 结果与讨论
2.1 表征结果
2.1.1 XRD表征结果 图1为制备的Co3O4、CeO2和Co3O4/CeO2复合材料的X射线衍射图。Co3O4的X射线衍射图与标准PDF卡片对比得知,衍射角为19.02,31.30,36.86,59.38°和65.26°处的衍射峰属于Co3O4尖晶石结构;CeO2的X射线衍射图与标准PDF卡片对比得知,衍射角为28.60,32.99,47.57,56.33,58.94,69.62°和77.36°出现的衍射峰属于CeO2立方体萤石结构。将制备的Co3O4/CeO2的XRD与CeO2相比,CeO2的衍射角28.60,32.99,47.57,56.33°处的衍射峰仍然存在,说明CeO2基体结构并没有因为Co3O4的掺杂而产生影响。将Co3O4/CeO2复合氧化物XRD谱图与Co3O4的XRD对比可知,Co3O4的19.02,31.30,36.86,59.38°和65.26°特征峰均出现,但强度明显变弱,说明在制备的氧化铈基钴复合材料中形成了结晶程度较弱的Co3O4晶体。
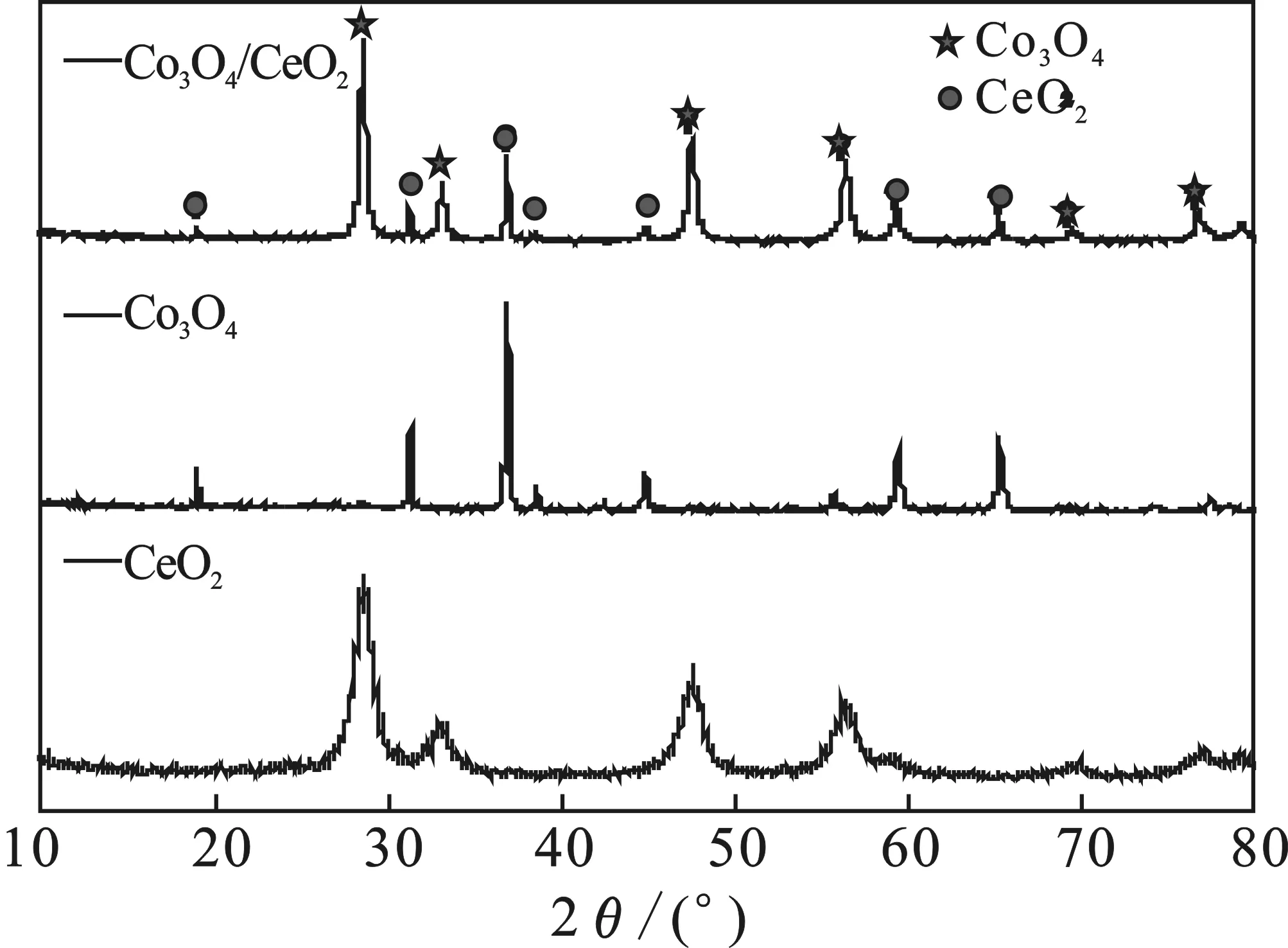
图1 催化剂的XRD谱图Fig.1 XRD patterns of the catalysts
2.1.2 XPS表征结果 图2为复合材料Co3O4/CeO2的XPS谱图。由图2(a)复合材料Co3O4/CeO2的XPS全谱可以看出,复合材料Co3O4/CeO2中存在Na、Ce、Co、O元素,Na元素衍生自CeO2的制备,Ce(OH)3是CeO2的前体,使用NaOH作沉淀剂。图2(b)给出了Ce3d的XPS谱图,在882.88,889.48和898.48处的峰被分配在Ce3d5/2,901.68,910.08和916.98的峰分配在Ce3d3/2。说明在复合材料Co3O4/CeO2中Ce3+和Ce4+都存在。从图2(c)可以看出,典型的Co2p核心能级谱在780.08和795.18 eV出现2个主峰,对应于自旋轨道分裂Co2p3/2和Co2p1/2的双峰接近于Co3O4[13]。

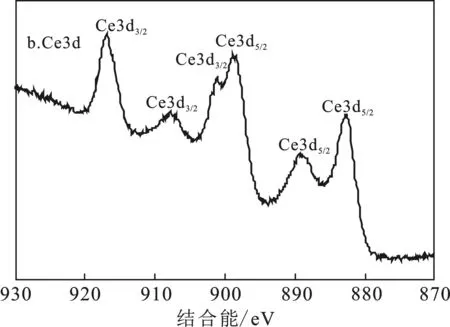

图2 Co3O4/CeO2的XPS谱图Fig.2 XPS spectrum of Co3O4/CeO2 a.Co3O4/CeO2;b.Ce3d;c.Co2p
2.1.3 TG-DTA表征结果 图3为Co3O4/CeO2前体的热重分析曲线,其中DTA曲线在121 ℃和325 ℃具有明显的吸热峰和放热峰,TG曲线有相应的失重区间。0~121 ℃附近的重量损失是由于Co3O4/CeO2前体中的吸附水和结晶水蒸发;121~325 ℃附近的重量损失是柠檬酸钴和柠檬酸铈中化合结晶水受热挥发引起的;325~500 ℃范围内的重量损失是柠檬酸钴和柠檬酸铈中的羧基热解反应及Co3O4和CeO2的生成过程引起的。在500 ℃以后TG曲线趋于稳定,说明生成了Co3O4/CeO2晶粒。因此,确定制备催化剂的焙烧温度为500 ℃。

图3 Co3O4/CeO2前体的TG/DTG曲线Fig.3 TG/DTG spectrum of Co3O4/CeO2 precursor
2.2 降解条件的优化
2.2.1 催化剂中钴铈摩尔比对脱色率的影响 在实验条件下,改变Co3O4/CeO2中钴铈摩尔比对孔雀石绿溶液脱色情况的影响,实验结果见图4。
由图4可知,当钴铈比Co/Ce<1时,染料的脱色率随着钴铈比的增加而增加,当Co/Ce=1时,染料的脱色率达到最大值,当Co/Ce>1时,染料的脱色率逐渐变小,这表明复合氧化物中的钴铈比影响染料的脱色率,当钴铈摩尔比为1∶1时,Co3O4/CeO2复合材料表现高的脱色率。
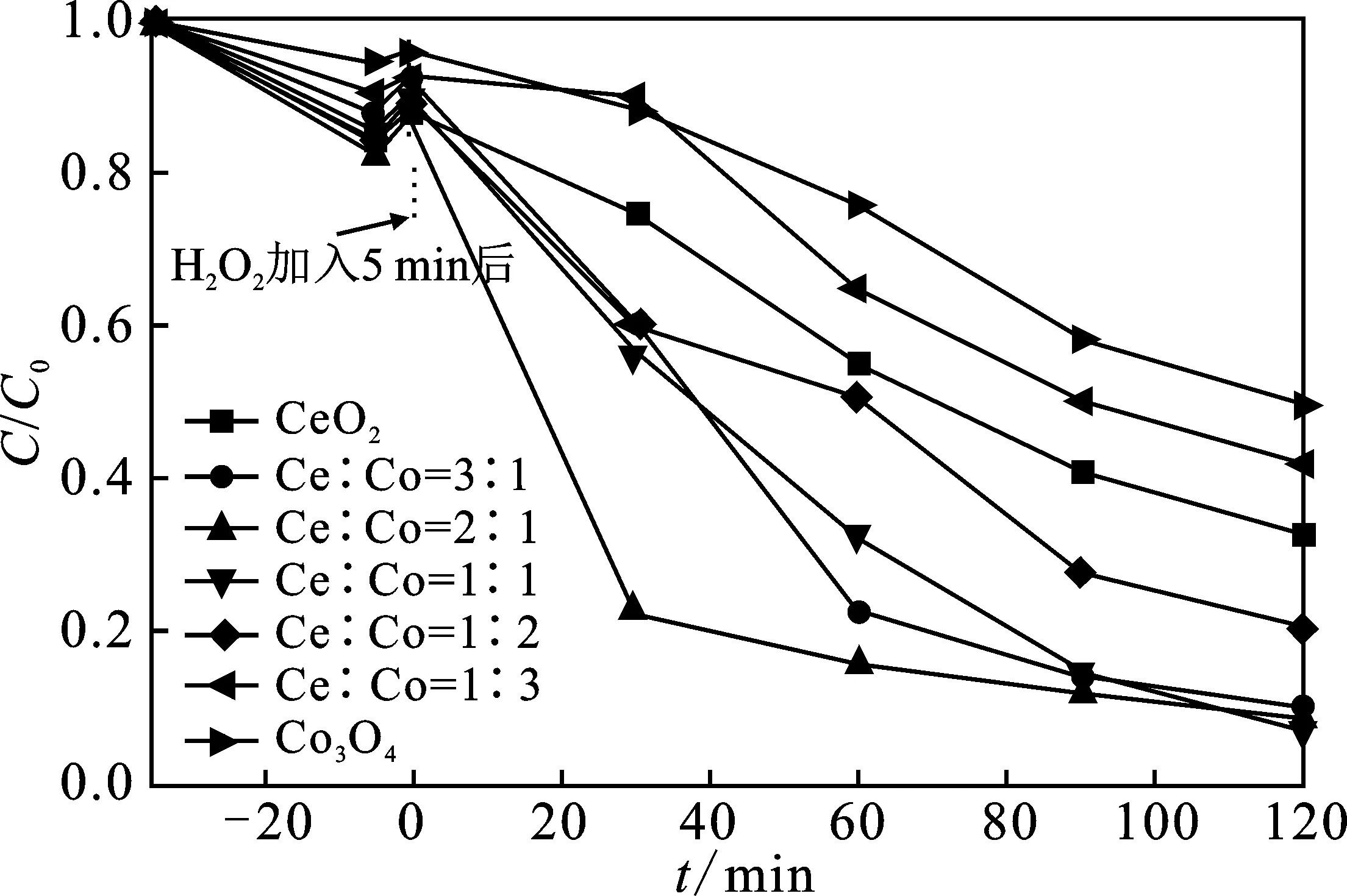
图4 n(Co)∶n(Ce)对孔雀石绿降解性能的影响Fig.4 Effects of n(Co)∶n(Ce) on the degradation of Malachite Green
Co3O4/CeO2对孔雀石绿的脱色作用包括催化剂对染料的吸附作用和催化剂的光催化氧化降解作用。由图4可知,不同比例的催化剂对染料具有不同的吸附容量,钴铈摩尔比为1∶1的Co3O4/CeO2复合材料吸附最强,吸附30 min后染料的吸附率为19.5%。在吸附平衡后,加入H2O2,溶液在最初的5 min吸光度上升,因为H2O2与吸附在Co3O4/CeO2催化剂表面的染料产生竞争吸附,从而将染料置换下来使溶液颜色变深。随着反应时间的增加,溶液颜色逐渐变浅,120 min后达到脱色平衡。因此,后续实验均使用钴铈摩尔比为1∶1的Co3O4/CeO2复合材料[14]。
2.2.2 H2O2用量对脱色率的影响 H2O2的量对孔雀石绿降解性能的影响见图5。

图5 H2O2的量对孔雀石绿降解性能的影响Fig.5 Effects of H2O2 dosage on the degradation of Malachite Green
由图5可知,当H2O2的量增加时,孔雀石绿脱色率先增加然后减小。当H2O2用量达到150 mmol时,脱色率在83%以上;然后继续增加H2O2用量,降解速率下降。这是因为H2O2用量太大时,过量H2O2无效地分解,并且可能与溶液中的·OH竞争,从而孔雀石绿的脱色率下降。
2.2.3 溶液初始pH对脱色率的影响 溶液的初始pH对孔雀石绿降解性能的影响见图6。
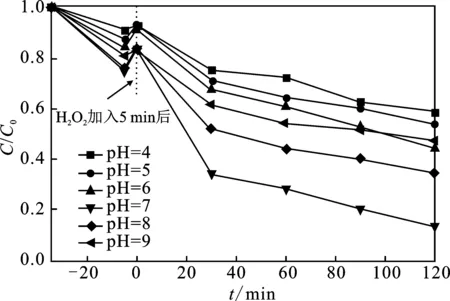
图6 溶液初始pH对孔雀石绿降解性能的影响Fig.6 Effect of initial pH of solution on degradation of Malachite Green
由图6可知,当溶液pH从4增加到7时,孔雀石绿的脱色率随pH的增加而增加;当溶液pH由7增加到9时,孔雀石绿的脱色率降低,因为强酸性抑制了Ce3+和Co3+的生成,使·OH的生成量减少;当溶液为碱性溶液时,较高浓度的OH-也会抑制·OH的生成,这会影响孔雀石绿的氧化降解。
2.3 不同初始浓度染料降解性能的动力学分析
一级、二级动力学模型分别如下:
ln(C0-C)=-k1t
式中,C0和C分别是初始浓度和平衡浓度,k1是一级动力学速率常数(min-1),k2为二级动力学速率常数(g·mg-1·min-1)。
图7表示-ln(C/C0)对时间t绘制的不同染料浓度一级动力学曲线,表1为孔雀石绿降解的一级动力学常数,图8为t/C对时间t绘制的不同染料浓度二级动力学曲线。表2为孔雀石绿降解的二级动力学常数,一级动力学曲线的方差与二级动力学曲线的线性相关系数相比,一级动力学更接近于1[15-16],故可以得出结论,Co3O4/CeO2复合物对孔雀石绿的催化符合一级动力学方程[17]。

图7 不同初始浓度染料降解性能的一级动力学分析Fig.7 First-order kinetics analysis of degradation performance of dyes at different initial concentrations
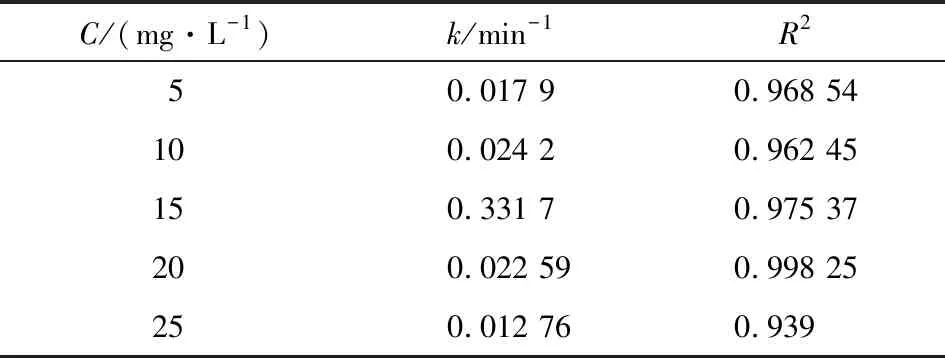
C/(mg·L-1)k/min-1R250.017 90.968 54100.024 20.962 45150.331 70.975 37200.022 590.998 25250.012 760.939

图8 不同初始浓度染料降解性能的二级动力学分析Fig.8 Second-order kinetics analysis of dye degradation performance at different initial concentrations

C/(mg·L-1)k/(g·mg-1·min-1)R254.488 010.871 43104.185 910.857 67155.506 410.898 71201.497 340.901 82250.304 570.871 14
2.4 降解原理
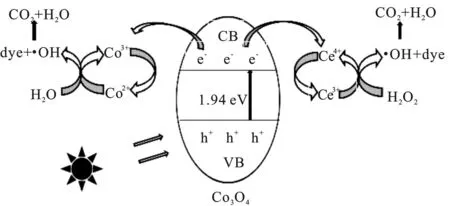
Co3O4吸收高于催化剂禁带宽度的光子能量,使电子被激活,从价带跃迁到导带,在价带和导带上分别形成了带正电的空穴(h+)和带负电的高活性电子(e-),从而形成了电子-空穴对[16]。Ce4+从Co3O4导带获得电子形成Ce3+,电子(e-)与空穴(h+)发生分离,e-与h+的重组受到抑制,从而改善了孔雀石绿的光催化降解;另外,Ce3+把H2O2还原为·OH,同时Ce3+又被氧化为Ce4+[17]。
其结果是,反应体系可稳定供给Co3+和Ce4+,使H2O2分解产生·OH用于孔雀石绿氧化。在反应体系中存在·OH的情况下,孔雀石绿分子的杂环在·OH氧化下形成小分子中间体。这些不稳定的小块碎片更容易降解为CO2,H2O和其它副产物如无机盐[18-19]。
Co3O4+hv→Co3O4(h++e-)
Ce4++e-→Ce3+
2Ce3++H2O2→2·OH+2Ce4+
Co3++e-→Co2+
2Co2++H2O2→2·OH+2Co3+
Co3++H2O2→Co2++·OOH+H+
Co2++H2O2→Co3++·OH+OH-
OH-+h+→·OH
dye+2·OH→CO2+H2O
3 结论
Co3O4的掺杂对CeO2基体的结构未产生影响,制备的复合材料仍具有载体CeO2的立方萤石结构;Co3O4与CeO2的复合改变了CeO2的禁带宽度,光响应波长向可见光区移动,抑制了空穴(h+)和光生电子(e-)的复合,并且光催化活性得到改善。制备的Ce3O4/CeO2复合材料催化剂,对初始浓度为15 mg/L的孔雀石绿具有良好光催化性能。最佳实验条件为:钴铈摩尔比为1,催化剂用量为1.0 g/L,H2O2用量为150 mmol/L,溶液的初始pH=7,在最好的实验条件下孔雀石绿的脱色率达到99.58%。

