乙炔的制备及性质实验改进
余新红 李调霞
甘肃省岷县第一中学(748400) 甘肃省舟曲县第一中学(746300)
1 问题的提出
乙炔是最简单的炔烃,也是炔烃中最具有代表性的物质,在人教版化学选修5“有机化学基础”中,为了更好的理解并掌握乙炔的物理性质和化学性质,课本中专门安排了实验,具体操作是:在圆底烧瓶里放入几小块电石,旋开分液漏斗的活塞,逐滴加入饱和食盐水,便可产生乙炔气体。再将验纯后的气体依次通入盛有高锰酸钾酸性溶液的试管中和盛有溴的四氯化碳溶液的试管中。
在实际的教学中发现该实验存在以下的不足:①所用的实验仪器较多,准备一次实验花费的时间较长,如果要进行学生分组实验,准备起来费时费力,所以很多教师在教学中仅仅进行课堂演示,不利于培养学生的动手能力及化学核心素养;②在实验中制备乙炔气体的目的是验证其化学性质,实验中虽然为了减缓反应速率,用饱和食盐水代替了水,但还是产生了大量的泡沫,影响后续性验的操作。
为了产生平稳、适量的乙炔气体,同时将气体制备及性质验证实验一体化,力求整个装置简单,实验现象明显,笔者设计了如下改进实验装置。
2 改进后的实验装置及操作
2.1 实验仪器和药品
50 mL锥形瓶、10 mL注射器、尖嘴导管、破底试管、双孔橡胶塞1个、单孔橡胶塞1个、输液管1段、棉花、镊子、0.5 g电石、乙醇、饱和食盐水、酸性高锰酸钾溶液、饱和硫酸铜溶液、溴的四氯化碳溶液、滤纸、透明胶带。
2.2 破底试管的准备
提前准备1个底部破裂的试管,在酒精喷灯上预热后加热至玻璃红热,用镊子和锉将试管底部磨平,再在酒精喷灯上圆口,使之光滑。
2.3 实验装置
改进后的实验装置如图1所示。
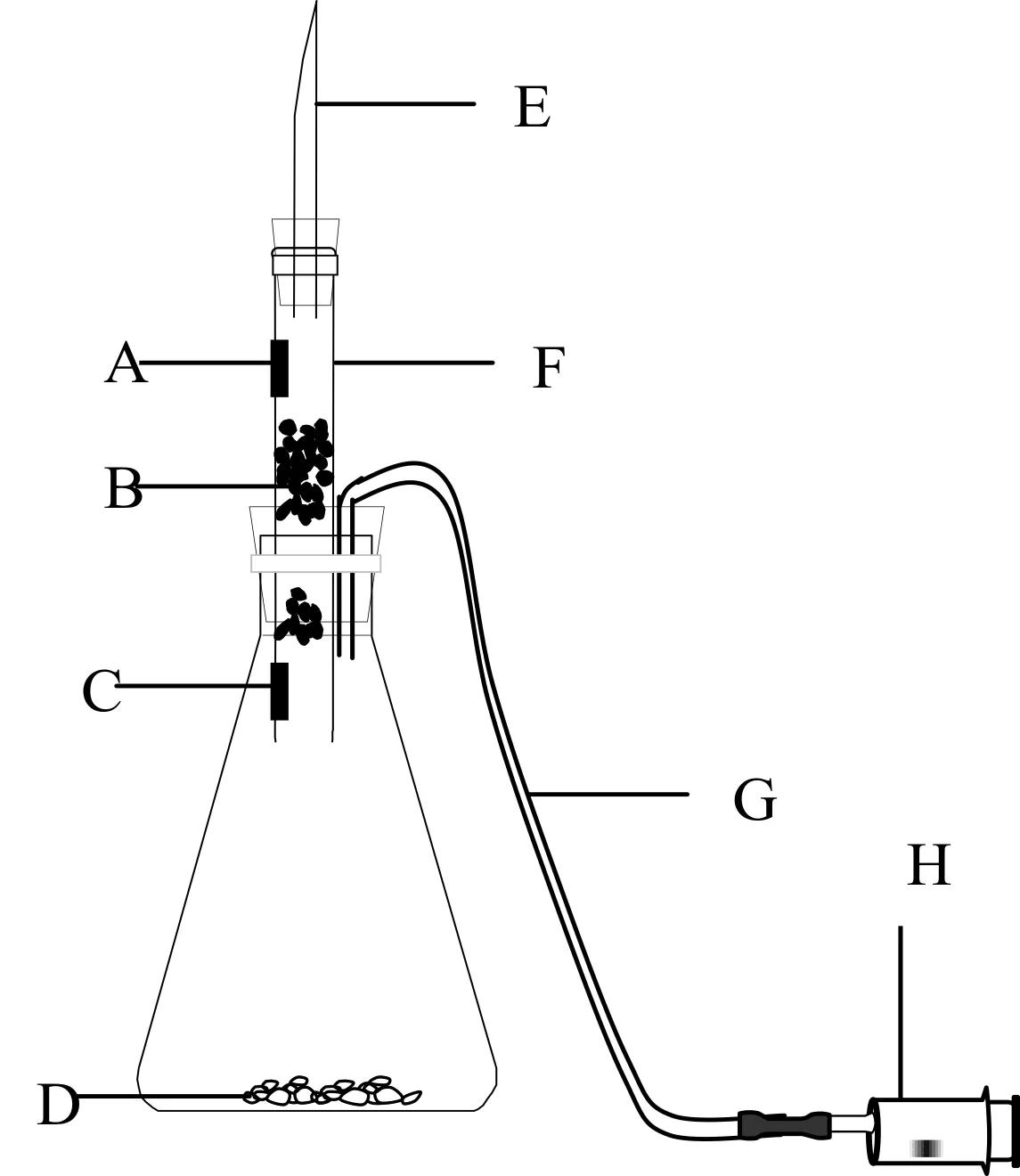
A-蘸有KMnO4(H+)溶液的滤纸;B-蘸有硫酸铜溶液的棉花;C-蘸有溴的四氯化碳溶液的滤纸;D-电石;E-玻璃尖嘴导管;F-破底试管;G-输液管;H-装有乙醇与饱和食盐水混合液(体积比1∶3)的注射器。图1 改进后实验装置图
2.4 实验操作
(1)如图1所示组装好实验装置,检查装置的气密性。
(2)在干燥的50 mL锥形瓶中放入0.5 g电石,用透明胶带将蘸有溴的四氯化碳溶液的滤纸粘在破底试管连有双孔橡胶塞一侧的管口,将双孔橡胶塞塞在锥形瓶瓶口。用镊子将蘸有饱和硫酸铜溶液的棉花疏松地塞在破底试管的中间,在破底试管的最上端管口用透明胶带粘上蘸有酸性高锰酸钾溶液的滤纸,塞上带尖嘴导管的单孔橡胶塞。在注射器中吸入乙醇和饱和食盐水(体积比1∶3)的混合溶液,通过输液管连在双孔橡胶塞另一个孔中的玻璃导管上。
(3)挤压注射器的活塞,使乙醇和饱和食盐水的混合溶液缓慢地滴入锥形瓶中,电石与混合溶液缓慢地开始反应,产生的无色气体使溴的四氯化碳溶液褪色(乙炔和溴发生加成反应生成无色的1,1,2,2—四溴乙烷),蘸有饱和硫酸铜溶液的棉花上有黑色的物质产生(电石中常含有硫化物和磷化物等杂质,这些物质也会和水反应生成硫化氢和磷化氢等气体,该气体与硫酸铜溶液反应生成硫化铜、磷化铜等黑色沉淀),蘸有酸性高锰酸钾溶液的滤纸褪色(乙炔和酸性高锰酸钾发生了氧化反应)。
(4)用手触摸锥形瓶,瓶壁发烫,说明乙炔与水反应放出了大量的热。用火柴点燃尖嘴玻璃导管,乙炔在空气中燃烧,火焰明亮并伴有浓烈的黑烟。
3 实验优点
(1)用乙醇和饱和食盐水按体积比1∶3的混合溶液代替了饱和食盐水,反应液中不会出现大量的泡沫,产生气流平稳、适中的乙炔气体。
(2)改进后的装置将气体的制备、净化、性质验证实验在一个简单的装置中完成,操作简单,现象明显。使用注射器可以控制滴加乙醇和饱和食盐水混合液的体积,从而控制反应的速率,还可控制反应的开始与停止。
(3)将医用注射器、输液管、破底试管应用到改进装置中,培养学生节约资源、废物再利用的意识,装置改进培养了学生的创新意识和动手能力,促进了学生化学学科核心素养的培养。

