MRI在卵巢子宫内膜异位囊肿术前诊断中的应用价值
张 昆,丁长青*,杨 峰,罗 慧
(江苏省丰县人民医院,1.妇产科;2.影像科,江苏 徐州 221700)
卵巢子宫内膜异位症是一种严重影响育龄期妇女的慢性妇科疾病,可能导致盆腔疼痛和不孕[1]。约半数以上不孕妇女存在本症[2]。其特征在于功能性异位子宫内膜腺体和间质在卵巢生长[1]。既往本症的诊断主要依赖于超声,经验丰富的超声科医生可经阴道超声(transvaginal ultrasound,TVUS)较为敏感地检测卵巢子宫内膜异位囊肿[3]。但TVUS严重依赖操作者技能[4]。随着MRI的渐趋普及,其多序列、多方位及优良的软组织分辨力,使其成为评价卵巢子宫内膜异位症较佳的影像学诊断手段。现回顾性2015年1月~2018年5月我院手术病理证实的15例共36个卵巢子宫内膜异位囊肿的临床及影像学资料,旨在探讨MRI在术前诊断及鉴别诊断中的应用价值。
1 资料与方法
1.1 一般资料
15例卵巢子宫内膜异位症女性患者,年龄23~52岁(平均3 4.4 2.7 岁)平。主要就医原因:月经失调(n=14)、痛经(n=13)、下腹痛(n=11)、盆腔包块(n=5)、不孕(n=2)。出现临床检查时间:2 m~3.5 y,MRI检查后均于1 w内完成手术。本组均行肿瘤标记物检查,其中5例CA199增高,10例CA125增高。本研究获得院医学伦理学委员会审查批准及患者本人的知情同意。
1.2 MRI观察指标、手术及病理观察
使用1.5 T高场MRI扫描仪,扫描序列包括T1WI、T 2 W I、脂肪抑制序列(S PA I R)、扩散加权序列(DWI),方位以轴位为主,辅以矢状位及冠状位。重点观察子宫及附件形态大小、病灶形态信号特点、周围情况及盆腔淋巴结及积液情况。
本组均经腹腔镜手术,术中重点观察病灶的形态、大小、位置、周围有无粘连等。对切除的标本内含液进行大体观察,并对囊肿及其已切除的周围组织行镜下观察,并进行MRI与病理对比观察。
2 结 果
2.1 手术病理结果对照
与手术病理结果对照,MRI诸序列均可全部显示36个子宫内膜异位囊肿。与手术病理比较,本组MRI诊断准确率为100%。
2.2 MR表现
囊肿位于两侧卵巢10例,位于左侧3例,右侧2例。36个子宫内膜异位囊肿中,呈类圆形14个、椭圆形9个、葫芦形7个、不规则形6个。囊肿大小:8 mm 7 mm~89 mm 54 mm。呈T1WI低T2WI高抑脂序列高(脂肪抑脂序列可见勾边效应)DWI高28个(见图1),呈T1WI低T2WI高抑脂序列高DWI高5个,诸序列信号混杂3个(T2WI伴黑点征2个),10例伴“卫星囊”,5例囊内伴分隔,4例伴小破口及高信号影外突而呈“尖角征”。
2.3 手术病理所见
术中可见患侧卵巢呈褐色增大,20个囊肿表面较为光滑、36个周围有粘连(其中4例伴小破口者粘连尤为严重)。囊肿大体标本可见囊液多为粘稠的暗红色或咖啡色,呈巧克力状,镜下囊壁为子宫内膜组织。
图1 女性49岁两侧卵巢子宫内膜异位囊肿,可见两侧附件区呈中高信号的囊肿

图1a T1WI
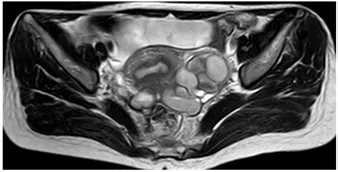
图1b T2WI

图1c 脂肪抑脂序列(SPAIR)

图1d DWI序列
3 讨 论
卵巢子宫内膜异位囊肿系子宫内膜异位于卵巢、反复出血致囊肿形成,其内为巧克力样液体,故又称卵巢巧克力囊肿。可能的机理尚不明确,子宫内膜种植、上皮化生、淋巴及静脉播散、免疫异常等为可能的发病因素[5]。临床上本症主要表现为月经失调(本组93.3%)、痛经(本组86.7%)、下腹痛(本组73.3%)、盆腔包块(本组33.3%)、不孕等。异位子宫内膜可以产生CA125及CA199,故部分患者相应血清学指标可升高。
子宫内膜异位病灶的MRI表现多样,主要取决于出血量、子宫内膜细胞量及基质量、平滑肌增殖及纤维化等。MRI上以囊壁厚薄不均匀、大囊肿周围伴小囊肿的“卫星囊”、多序列中高信号、“囊壁缺口征”为、部分囊肿因反复出血与周围组织粘连而呈现特征性的“尖角征”[5-6]。T2WI序列上的黑点征多为慢性出血的特异性征象,可与功能性出血性囊肿相鉴别[7]。
MRI上主要应与成熟性畸胎瘤、卵巢纤维瘤或卵泡膜细胞瘤、卵巢囊腺瘤或囊腺癌、卵泡膜细胞瘤等鉴别[8-10]:病灶内部出现典型脂肪成分或脂-液平面,则多为畸胎瘤;内含较多纤维成分者多为卵巢纤维瘤或卵泡膜细胞瘤;内部主要为囊性成分且有明显分隔、均匀薄壁可能为囊腺瘤,而壁厚且不均匀,DWI信号明显高,血供丰富且增强呈快进快出等征象则多为囊腺癌;分隔厚且不规则,伴壁结节、双侧、边界不清或浸润性生长的实性或以囊实性肿块,有腹膜、淋巴结及远处转移者,更提示恶性肿瘤。
MRI可对盆腔进行完整的评估,是子宫内膜异位症术前分期的最佳成像技术,有利于指导制定更合适的手术方法计划[1]。
总之,熟悉子宫内膜异位囊肿MRI表现特点,将有助于医师缩小鉴别诊断范围并做出准确诊断,进而指导临床制定合理的治疗计划。

