类Fenton试剂氧化酸性嫩黄染料废水的研究
孙中华 张颖杰
摘要:染料废水可生化性差,色度深,处理难度较大,已成为我国目前主要的有害及难处理的工业废水之一。采用次氯酸钠与Fe2+组成的类Fenton试剂[1]氧化体系对酸性嫩黄模拟染料废水进行处理,利用其超强氧化性实现对染料的深度氧化。通过研究一系列条件试验探求反应过程的最佳操作条件。
关键词:类Fenton试剂;染料废水;研究
中图分类号:X131.2 文献标识码:A 文章编号:2095-672X(2019)05-0-02
DOI:10.16647/j.cnki.cn15-1369/X.2019.05.072
Abstract: Dyestuff wastewater has been one of the main harmful and difficult industrial effluents in China at present. The Fenton reagent oxidation system consisting of sodium hypochlorite and Fe2 + was used to treat the acid yellow dye simulated wastewater, and the deep oxidation of the dye was achieved by using its Super oxidizing properties. The optimal operating conditions of the reaction process are explored through a series of conditional tests.
Keywords: Class Fenton reagent; Dye wastewater; Study
Fenton氧化法[2]处理水中的难降解有机物具有较好的效果,但由于体系中大量的亚铁离子存在,使H2O2[3]的利用效果不高,有机物降解不完全,而且由于H2O2价格昂贵,使用量大,导致Fenton试剂处理染料废水成本较高。HClO[4]比H2O2氧化性更强,在光照条件下可生成HO-和H2O2,可响应的波长范围比H2O2宽。以HClO代替H2O2同样可以与亚铁离子反应生成HO-。介于上面的原因,以Fe2+为催化剂,采用NaClO或Ca(ClO)2为氧化剂生成HClO来代替H2O2的氧化作用[5],对染料废水中难降解有机物进行实验摸索。
1 研究方法
1.1 模拟染料废水的配制
采用酸性嫩黄和蒸馏水配制。在电子天平上称取0.4000g的酸性嫩黄染料,溶解于一个干净的烧杯中,待完全溶解后,将其移入一个干净的1L容量瓶中,定容,摇匀,配制成400mg/L的酸性嫩黄溶液。
1.2 试验方法
取若干份150mL浓度为400mg/L酸性嫩黄溶液放入烧杯中,经充分溶解后,加入FeSO4·7H2O和NaClO溶液,在恒温振荡水槽中反应一段时间后对处理后的水样进行吸光度值的测定,根据标准工作曲线,换算出相应的浓度,求出各影响因素在最佳条件时的对废水的脱色率:
1.3 分析方法
吸光度测定采用分光光度法;溶液浓度测定采用标准工作曲线法。
2 分析结果
2.1 最大吸收波长的确定
采用721分光光度计对溶液进行吸光度分析。用电子天平准确称取0.1000g酸性嫩黄染料,在1000mL容量瓶中配制成100.00mg/L的酸性嫩黄溶液,在可见光波长范围内测得溶液在不同波长处的吸光度。结果见表1所示:
根据表1中数据确定酸性嫩黄染料的最大吸收波长为383nm。
2.2 標准工作曲线的绘制
配制一系列不同浓度的酸性嫩黄标准溶液,用连续扫描法测定各标准溶液在383nm处的一系列吸光度值。根据浓度与相应吸光度制作标准曲线,结果如图1所示:
2.3 对比试验
取2份150mL浓度为400mg/L初始pH为7.13的酸性嫩黄染料溶液,向其中一份加入FeSO4·7H2O 0.3g,充分溶解后加入2mLNaClO,调节溶液初始pH值为7.13,将溶液放入恒温振荡水槽反应;将另一份溶液亦加入2mLNaClO溶液,同样放入恒温振荡水槽反应。每隔一定时间后取出部分溶液静止过滤,取上清液在383nm处测其吸光度值。结果见图2。由图2可以看出:在相同的反应条件下,加入FeSO4·7H2O的水样处理后的脱色率明显高于没有加入FeSO4·7H2O的水样,因此确定FeSO4·7H2O的加入对实验的处理效果有很大影响。
2.4 各因素对脱色率影响的正交实验
结合经济成本和其他因素,列正交试验表。正交试验表如表2所示:
由表2可得:NaClO用量对试验结果的影响最大,pH值和FeSO4·7H2O用量为其次,反应时间的影响最小。以下通过单因素试验确定各因素的最佳值。
2.5 影响因素的确定
2.5.1NaClO投加量对处理结果的影响
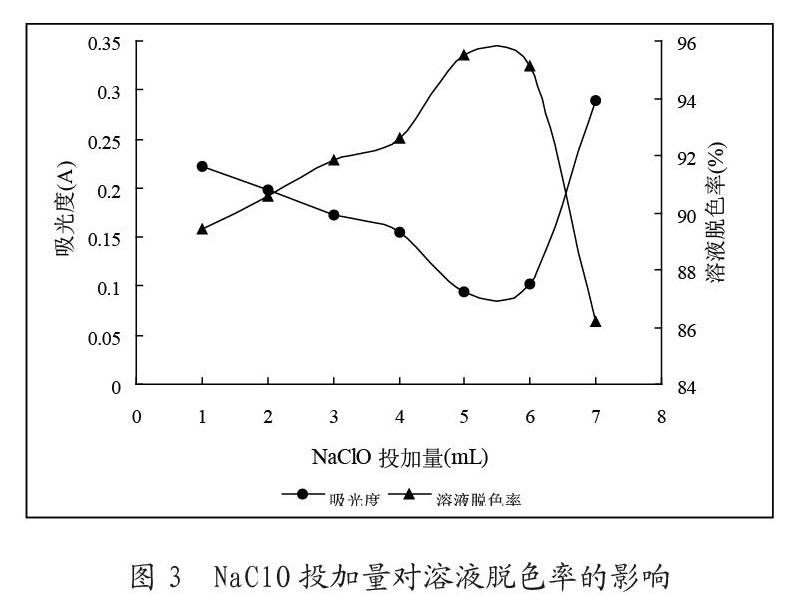
取7份150mL浓度为400mg/L的酸性嫩黄染料溶液,固定FeSO4·7H2O的用量为0.1000g,调节溶液初始pH为7.13,改变NaClO的用量,在恒温振荡水槽中反应30min。反应结束后调节出水pH在8-9之间,静止过滤,取上清液在383nm处测其吸光度值。结果见图3所示。
由图3可以看出:NaClO用量多少对处理效果有显著影响,当NaClO<5mL时,溶液脱色率随NaClO用量的增大而迅速增大,NaClO为5mL时,处理效果最好,溶液脱色率达95.48%,此后,增加NaClO用量,溶液脱色率反而下降,这是因为由于在一定的pH范围内受到[H+]的限制,过多的[ClO-]无益于HClO的生成,影响HClO与Fe2+生成羟基自由基,从而使反应处理效果下降。因此试验确定NaClO投加量为5mL。
2.5.2 FeSO4·7H2O投加量对处理结果的影响
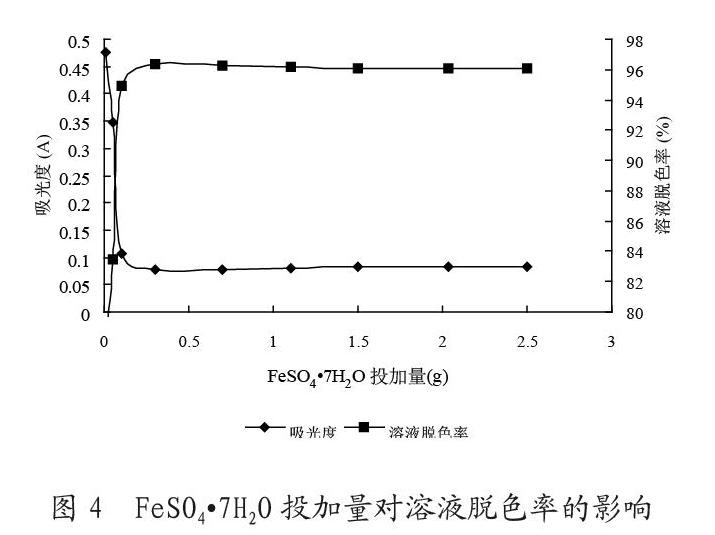
取9份150mL浓度为400mg/L的酸性嫩黄染料溶液,固定NaClO的最佳投加量为5mL,改变FeSO4·7H2O的用量,待溶液充分溶解后调节溶液pH值为7.13,将配置好的9份试样放入恒温振荡水槽反应30分钟。反应结束后调节出水pH在8-9之间,静止过滤,取上清液在383nm处测其吸光度值。结果见图4所示。
由图4可以看出:随着FeSO4·7H2O用量的增加,废水的脱色率随之增加,当FeSO4·7H2O投加量在0.3g左右时,脱色率达到最大值,之后曲线趋于平缓。这是由于Fe2+浓度过高时,多余的Fe2+被HClO氧化为Fe3+,使得Fe2+用量的增多对出水浓度的减少没有实际意义。所以确定FeSO4·7H2O的最佳投加量为0.3000g。
2.5.3 pH值对处理结果的影响
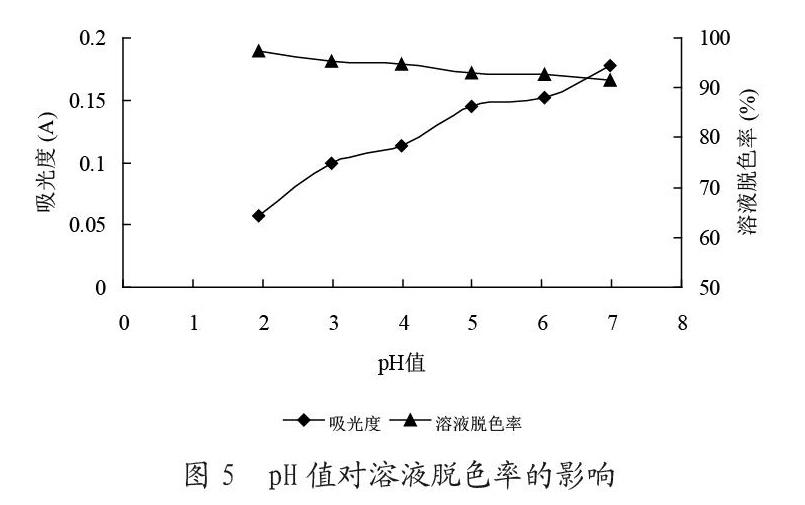
取6份150mL浓度为400 mg/L的酸性嫩黄染料溶液,固定NaClO与FeSO4·7H2O的最佳投加量分别为5mL和0.3000g,调节不同的初始pH值,在恒温振荡水槽中反应30min。反应结束后调节出水pH在8-9之间,静止过滤,取上清液在383nm处测其吸光度值。结果见图5所示。
由图5可以看出:pH值在2~5之间时由NaClO和FeSO4·7H2O组成的氧化体系对水样的处理效果较好,这是因为pH值过高将会导致Fe2+形成沉淀或铁的复杂络合物,使体系中无法进一步产生足够的羟基自由基,导致脱色率降低。因此确定反应最佳pH值为2。
3 结果讨论
根据正交试验结果分析得出,影响Fe2+与NaClO组成的类Fenton试剂氧化酸性嫩黄染料废水脱色率各因素的重要性顺序为:NaClO投加量>pH值>FeSO4·7H2O投加量>振荡反应时间。以Fe2+与NaClO组成的类Fenton试剂氧化处理酸性嫩黄模拟染料废水时,其最佳操作条件为:NaClO投加量为5mL,pH值为2, FeSO4·7H2O投加量為0.3g。此次研究仅为实验室模拟,现实染料废水具有水量大、成分复杂、有机污染物浓度高,可生化性差、色度深且多变、难降解等特点,采用类Fenton试剂氧化处理还需进一步研究考证。
参考文献
[1]崔淑兰,王峰云.铁屑-双氧水氧化法处理染料废水[J].环境保护,1990,(12):10-11.
[2]陈文松,韦朝海. Fenton氧化-混凝法处理印染废水的研究[J].工业水处理,2004,11(5):39-41.
[3]李硕文.活性炭-H2O2催化氧化在染色废水脱色中的应用[J].工业水处理,1989,9(4):25-27.
[4]李绍峰,黄君礼,陶虎春. Fenton试剂降解水中活性染料的研究[J].哈尔滨建筑大学学报,2001,34(5):76-80.
[5]徐向荣,王文华,李华斌.Fenton试剂与染料溶液的反应[J]. 环境科学,1999,20(3):72-74.
收稿日期:2019-03-29
作者简介:孙中华(1985-),男,汉族,环境工程专业,工程师,研究方向为环境工程及环境监测。

