SO32-/HSO5-体系去除印染生化尾水溶解性有机污染物
张昊楠,唐 海,李 强,张 晨,刘桂中
SO32-/HSO5-体系去除印染生化尾水溶解性有机污染物
张昊楠1,唐 海1*,李 强1,张 晨1,刘桂中2
(1.安徽工程大学生物与化学工程学院,安徽 芜湖 241000;2.北京市环境保护科学研究院,北京 100083)
印染废水常规生化处理尾水中仍残余一定浓度的溶解性有机污染物(DOM)和新标准严格管控的苯胺.采用亚硫酸钠活化过硫酸氢钾复合盐(SO32-/HSO5-)产硫酸根自由基(SO4-·)高级氧化体系对尾水进行深度处理,并基于响应面法优化初始pH值、反应温度、SO32-/ HSO5-物质的量比和HSO5-投加量对COD和苯胺去除效果的单独及交互影响.结果表明该体系对苯胺具有非常显著的去除效果,同时对COD亦有一定的降解能力.影响因子对COD和苯胺降解效果贡献排序分别为:温度>(SO32-)/(HSO5-)>(HSO5-)>初始pH值和(HSO5-)>(SO32-)/(HSO5-)/初始pH值>温度.在实验优化后得到的最佳条件下(pH=6.8,温度为53℃,SO32-/HSO5-物质的量比为1.6, HSO5-投加量为37.1mmol/L)反应10min,出水的COD和苯胺去除率分别达到33%和90%.进一步分析了印染生化尾水处理前后DOM的荧光和分子特性,三维荧光光谱(3DEEMs)发现芳香族蛋白质和溶解性微生物代谢产物是原尾水中DOM的主要组分,经不同氧化条件下出水中DOM的荧光强度明显降低且性质发生改变,荧光区域标准体积削减了42.03%~77.67%;同时观察到氧化出水中类色氨酸(x/m=230~225nm/340~330nm)峰值发生了5~10nm的蓝移,推测尾水中稠环芳烃分解为小分子,共轭基团和芳香环数量减少;凝胶渗透色谱(GPC)结果表明DOM中大分子(0.45 μm~100kDa)物质比例为41%,中等分子(12~100kDa)物质的比例为48.9%,峰值分子量(p)为56.324kDa,w/n=2.168,处理后的出水p主要分布在12.28~17.56kDa范围内,小分子物质数量增多,结构和种类发生变化;气相色谱质谱(GC-MS)进一步揭示氧化出水中的烷烃类物质含量明显降低,主要副产物为一些酯类、醇类和脂肪酸物质,为后续进一步生化处理创造了条件.
印染尾水;硫酸根自由基;过一硫酸盐;三维荧光;凝胶色谱
纺织印染行业具有水量大、有机污染物含量高、色度深、碱性大及水质变化大等特点.传统印染废水处理工艺以生化法为主,其生化处理尾水含有的溶解性有机污染物(DOM)是一种高度异质的混合物[1],由各种不同分子量的化合物组成,大部分为难降解有机物.随着印染工艺的发展,新型染料、特别是偶氮染料广泛应用,在生物降解过程中,偶氮染料利用共基质条件下降解释放的电子断裂—N=N—,生成无色芳香胺类化合物,其中代谢产物苯胺是一种有毒物质,不仅会导致人体肝脏和肾受损,也会在水中积累并抑制水生生物的生长[2-3].苯胺被列入我国“十四类环境优先污染黑名单”中,纺织染整企业将执行新的排放标准(GB 4287-2012)[4],规定COD和苯胺的直接排放限值分别为80mg/L和不得检出(实际质量浓度低于0.03mg/L).由于DOM的浓度和组成直接决定了印染废水深度处理工艺和效率,当前主流工艺有铁炭微电解、Fenton氧化、O3氧化、膜分离等[5-9].目前大量的印染企业采用传统方法难以达标排放,因此原有水处理设施提标改造尤为重要.
由于SO4-·相对于羟基自由基(·OH)氧化能力更强(0=+2.5V~+3.1V/NHE),对水中有机物具有无选择性和持续性的氧化,理论上可降解大部分有机污染物,较快的反应速率,并且其氧化产物SO42-不影响后续生物处理等优势,当前过硫酸盐活化产生强氧化性硫酸根自由基(SO4-·)的高级氧化技术受到广泛关注[9].特别是过硫酸盐易储存,环境友好,安全稳定,易于控制,价格低廉,具有很好的商业前景,因此近年来基于硫酸根自由基高级氧化技术成为处理有毒有害废水新途径[10-14].据报道当前过硫酸盐活化技术发展非常迅速,特别以铁氧化物[15-16]、零价金属[17]、碳基材料[18]和亚硫酸根活化[19]以及包括以上述材料为基础改性合成的新型材料等成为国内外的研究热点.
本研究用亚硫酸钠活化过硫酸氢钾复合盐(SO32-/HSO5-体系)产生硫酸根自由基(SO4-·),以实际印染生化尾水为研究对象,使用响应面方法对反应条件进行了优化研究,获得主要影响因素下的最优结果,同时采用凝胶渗透色谱(GPC)结合气相色谱质谱(GC-MS)技术和三维荧光(EEM)光谱技术比较了印染生化尾水处理前后主要有机组分的变化.并对进出水水质的组分进行分离,测量各组分分子质量分布和三维荧光光谱图,旨在为染料废水的深度处理提供可行的解决方案和可靠的技术路线.
1 材料与方法
1.1 废水及试剂
废水取自芜湖某印染废水处理站生化处理出水,其COD=120.2mg/L,TOC=12.28mg/L,苯胺= 3.65mg/L,水样过0.45μm滤膜待用.实验中主要试剂Na2SO3、2KHSO5·KHSO4·K2SO4(PMS)、NaOH和H2SO4均为分析纯,购自阿拉丁药剂有限公司(上海).
1.2 分析方法
COD采用快速消解分光光度法(HJ/T 399- 2007).TOC采用总有机碳测定仪测定(Vario TOC, Elementar,德国).苯胺测定采用N-(1-萘基)乙二胺偶氮分光光度法(GB 11889-89).pH值测定采用pH 计 (PHS-3C,上海雷磁).三维荧光激发-发射光谱(3DEEMs)测定采用荧光分光光度计(Hitachi F- 4500,日本),使用1cm的石英比色皿,150W氙弧灯作激发光源,在室温条件下,x/m为200~500nm/ 220~600nm,扫描速度1200nm/min,扫描间距5nm,狭缝宽带为5nm,三维荧光图形处理使用软件Origin 7.0完成,拉曼和瑞丽散射影响用Matlab软件编程予以消除.
分子量分布采用凝胶渗透色谱分析仪(GPC, Waters 2695,美国),使用水溶性色谱柱Ultrahydrogel 1000, 250, 120,以0.1mol/L NaNO3溶液作为流动相对仪器进行进样,进样时柱温为35℃,速率控制在1mL/min,进样体积为50μL.标样均采用聚乙二醇(PEG).气相色谱质谱(GC-MS)(日本岛津GCMS- QP2010)的色谱柱为HPS石英毛细管柱((30m× 0.25mm i.d.×0.25μm),以He作为载气,流量为1mL/ min,柱温为60℃,保持2min,以10℃/min的速度升温至250℃,保持5min,终温保持3min;进样量为0.2μL,分流比为35:1;质量扫描范围:15~500amu;电离方式EI,电子轰击能量为70eV,倍增电压2400V,离子源温度250℃.根据美国环保署(EPA)对工业废水的取样和分析方法进行水样预处理:将废水水样pH值依次调至中性、酸性和碱性,利用二氯甲烷萃取后合并,至旋转蒸发器在43℃下浓缩至1mL,加少量无水硫酸钠干燥.
1.3 试验步骤
反应所用仪器为数显恒温磁力搅拌器,设定温度和搅拌数值,用0.1mol/L NaOH和H2SO4调节反应体系初始pH值至设定值,确定并加入所需Na2SO3和PMS进行活化及氧化,反应10min后迅速收集出水测定COD和苯胺.去除率通过公式(1)计算:
=(0-e)/e×100% (1)
式中:为降解率;0和e分别为印染尾水初始COD和苯胺浓度以及反应结束时COD和苯胺浓度, mg/L.
采用Design Expert V8.0进行响应面优化分析,以物质的量比(SO32-)/(HSO5-)、HSO5-投加量、初始pH值和反应温度为自变量,COD和苯胺降解率为响应值,根据Box-Behnken中心组合原理,设计实验.因素设置与水平见表1.

表1 Box-Behnken实验设计因素水平
2 结果与讨论
2.1 响应面分析
响应面法具有试验次数少、精密度高、预测性能好等优点,广泛应用于寻找最佳工艺参数[20].根据前期研究成果[19]和单因素筛选,确定Box-Behnken模型较优化水平为:(SO32-):(HSO5-)为1.0~2.0,(HSO5-)为5.0~50.0mmol/L,初始pH值为2.0~11.0,反应温度为20~60℃.试验设计和COD及苯胺降解率见表2,根据BBD统计学要求,对COD和苯胺回归模型进行方差分析(表3).可以看出该回归模型均具有显著性(<0.05),COD模型拟合较好,失拟项不显著(>0.05),而苯胺回归模型具有极其显著性(<0.0001),说明模型拟合很好.COD的复相关系数2=0.7283,相关性一般,校正决定系数adj2= 0.4567,而苯胺复相关系数2=0.9298,相关性良好,校正决定系数adj2=0.8595,说明该模型能解释85.95%的苯胺去除响应值的变化.
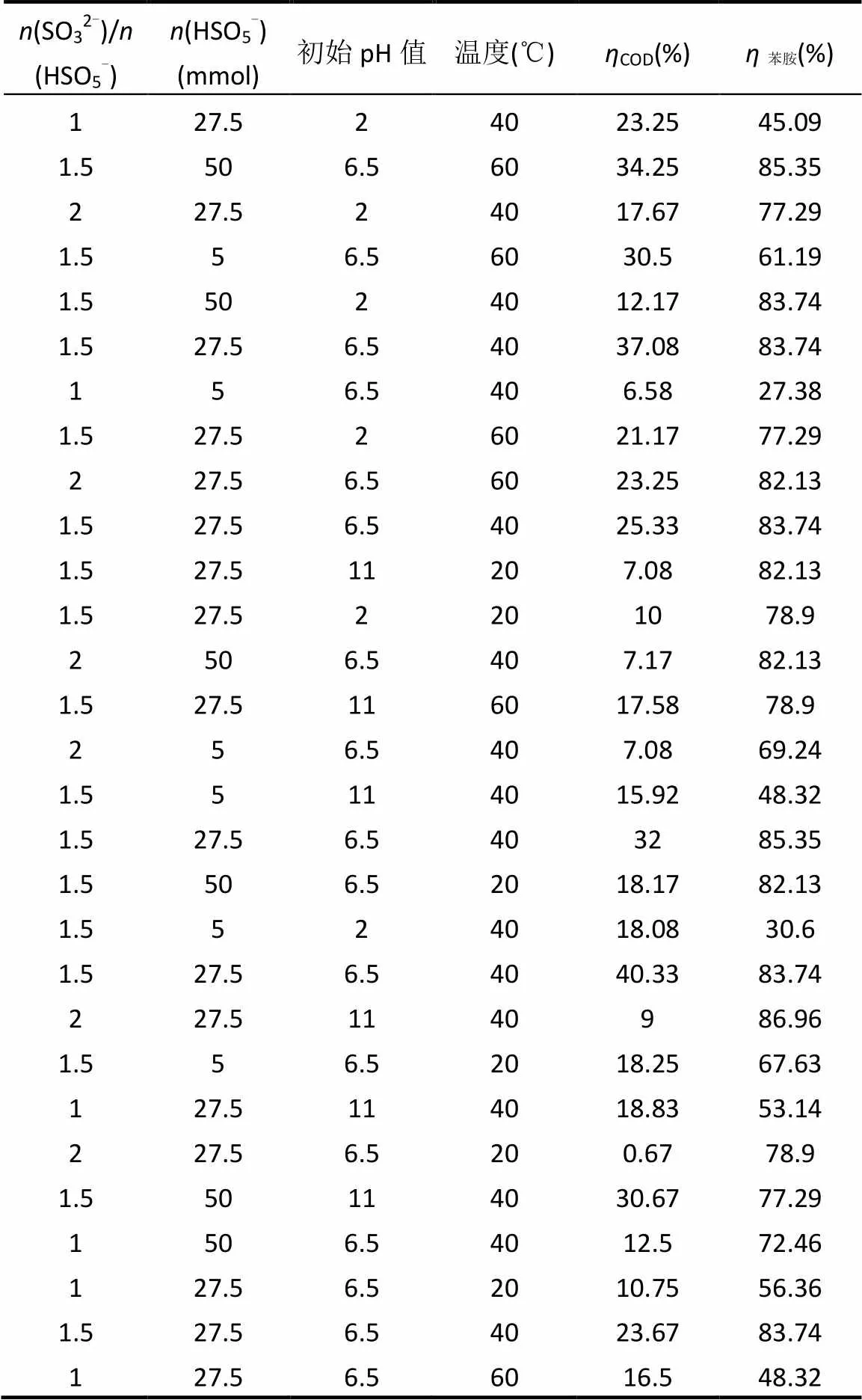
表2 Box-behnken试验设计和结果
其中COD自变量的一次系数(温度)显著(<0.05),二次项22显著(<0.05),根据值分析,对COD去除率影响大小的排列顺序依次为:温度>(SO32-)/(HSO5-)>(HSO5-)>初始pH值;对于苯胺,自变量的一次系数极显著(<0.0001),二次项222(<0.05)显著,同样由值分析得出对苯胺去除率影响大小的排列顺序依次为:(HSO5-)>(SO32-)/(HSO5-)/初始pH值>温度.在实验优化得到的最佳条件下:pH=6.8、温度为53℃、SO32-/HSO5-物质的量比为1.6、HSO5-投加量为37.1mol/L,出水的COD和苯胺去除率分别为33%和90%,待进一步优化之后可预期达到(GB 4287-2012)[4]排放标准.
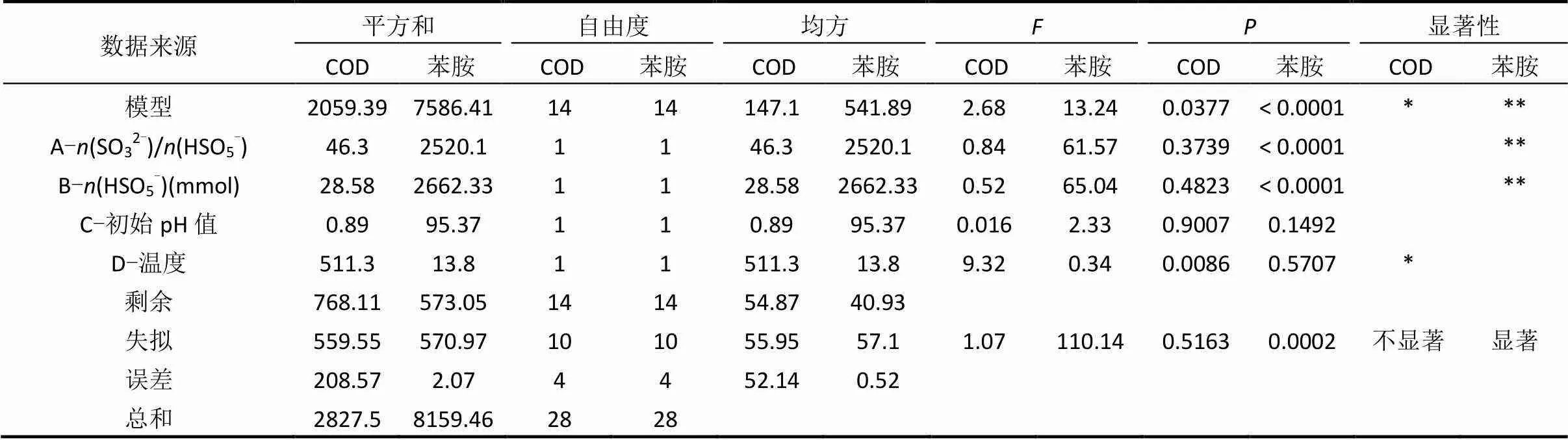
表3 COD和苯胺回归方差分析
注: **差异极显著(<0.0001),* 差异显著(<0.05).
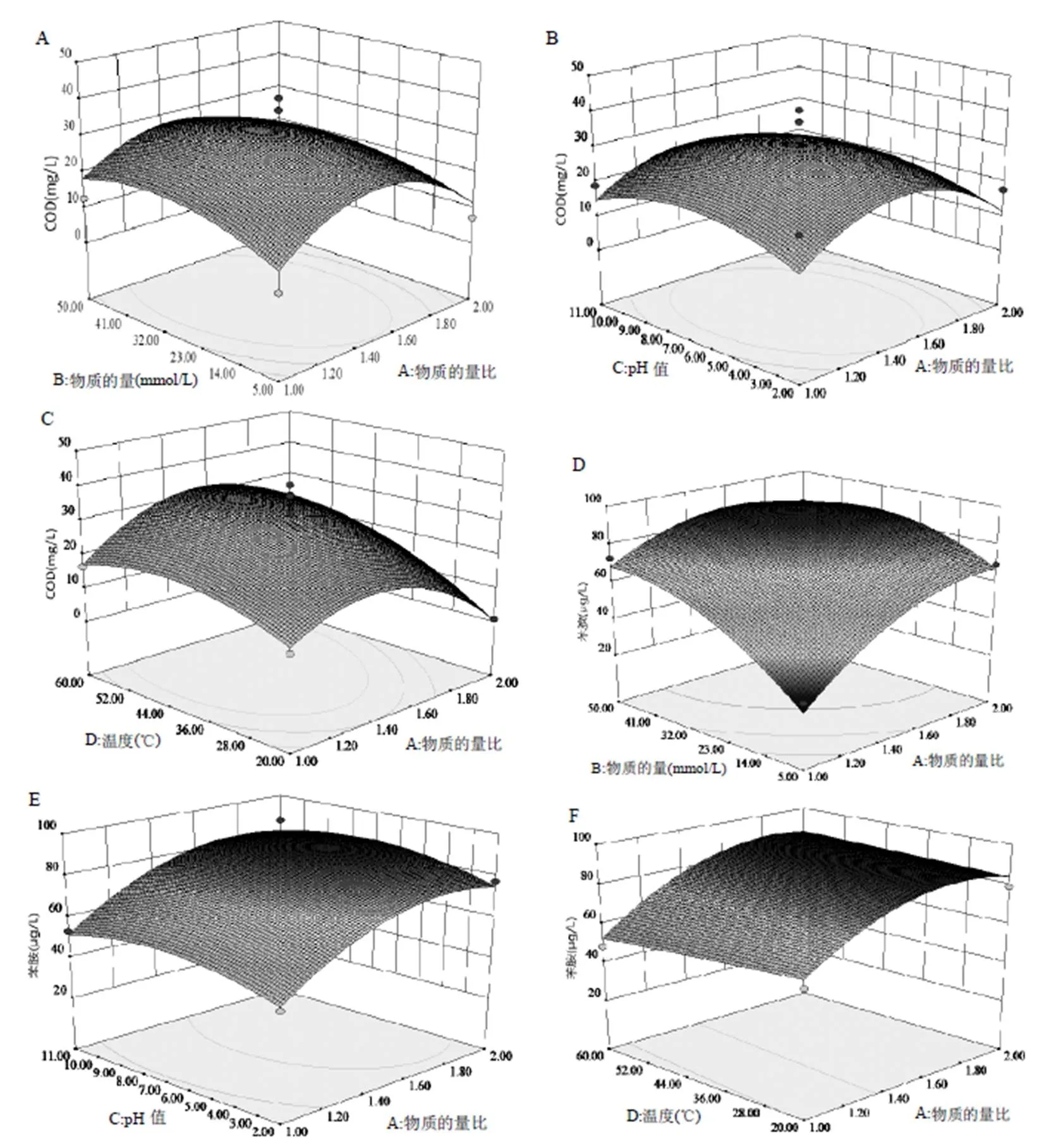
图1 COD和苯胺的去除等高线图
A:物质的量比和物质的量对COD降解的影响;B:物质的量比和初始pH值对COD降解的影响;C:物质的量比和反应温度COD降解的影响;D:物质的量比和物质的量对苯胺降解的影响;E:物质的量比和初始pH值对苯胺降解的影响;F:物质的量比和反应温度对苯胺降解的影响
同时基于Box-behnken设计响应面模拟和方差分析得到二次响应曲面模型,结果如图1所示.三维响应曲面图,颜色越深表明降解效果越显著,去除效果越好[21].结果表明,温度是影响SO32-/HSO5-处理生化尾水效果的重要参数,温度升高加速了SO4-·产生速率.在相同温度下HSO5-浓度越大,COD和苯胺降解率越高,尤其是pH值在6.5,温度在40℃,物质的量比为1.5,HSO5-浓度为27.5mmol/L时,曲面颜色最深,COD去除效果最好.而对于苯胺来说,降解率可以达到83.74%以上,这归因于反应体系中产生的SO4-·具有强氧化性,对苯环的进攻使苯胺发生开环反应,导致大部分的苯胺被降解为对苯醌.此外,物质的量比对SO32-/HSO5-活化体系降解印染生化尾水COD和苯胺亦有显著影响,与前期报道结果类似[19].从结果看出,适量的SO32-会促进HSO5-的活化,增强印染尾水中残余有机污染物的降解效果.当HSO5-过量时,会对COD和苯胺降解起到抑制作用,这是由于活化分解HSO5-产生一定稳态浓度的SO4-·氧化降解COD和苯胺时,如果HSO5-浓度较高,产生的SO4-·同时会与溶液中存在的HSO5-发生淬灭[公式(2)],导致消耗了部分SO4-·[22].同时在这一过程中,苯胺与SO32-对SO4-·产生了竞争作用,也抑制了印染尾水小分子有机物的降解.最后,初始pH值与(HSO5-)或者物质的量比这2个因素的交互作用表现不明显,对响应值的影响不显著.
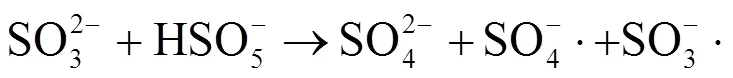
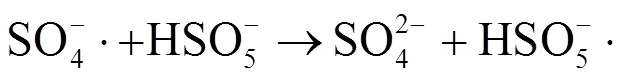
2.2 EEM分析
EEM光谱分析是鉴定各种水样中腐殖质和蛋白质类荧光信号的一种简单快捷方法[23].染料大都含有多重苯环,苯系物含有π-π共扼双键,能够发出较强的荧光,为了更好的解释印染生化尾水在SO32-/HSO5-体系氧化前后DOM的组成、分布及其变化规律,运用EEM技术对其进行解析,结果如图2所示.图2为原水和不同氧化条件下出水消除瑞丽和拉曼散射后的三维荧光光谱图.根据分类方法[24],将三维荧光光谱图分为5个区域,每个区域均代表着不同类型的有机物.其中,I~II区代表芳香蛋白类(类酪氨酸和类色氨酸)、III区代表富里酸类物质、IV区代表溶解性微生物代谢产物和V代表腐殖酸类物质.如光谱图所示,印染生化尾水荧光主要分布在2个区域(图2A),区域IVx/m=280/320nm具有最高的荧光强度,区域IIx/m=230/340nm次之,这表明2个区域的污染有机物浓度较高,而区域I、III和VI荧光强度较小.通过比较三维荧光光谱谱图可以推测[25],它可能来源于印染废水生物处理过程中产生的蛋白质和溶解性微生物代谢产物[26].也有文献报道多种苯系物的荧光也在x/m=280/340nm和240/340nm附近,推测与DOM中的芳环氨基酸结构和芳香性蛋白类结构有关.
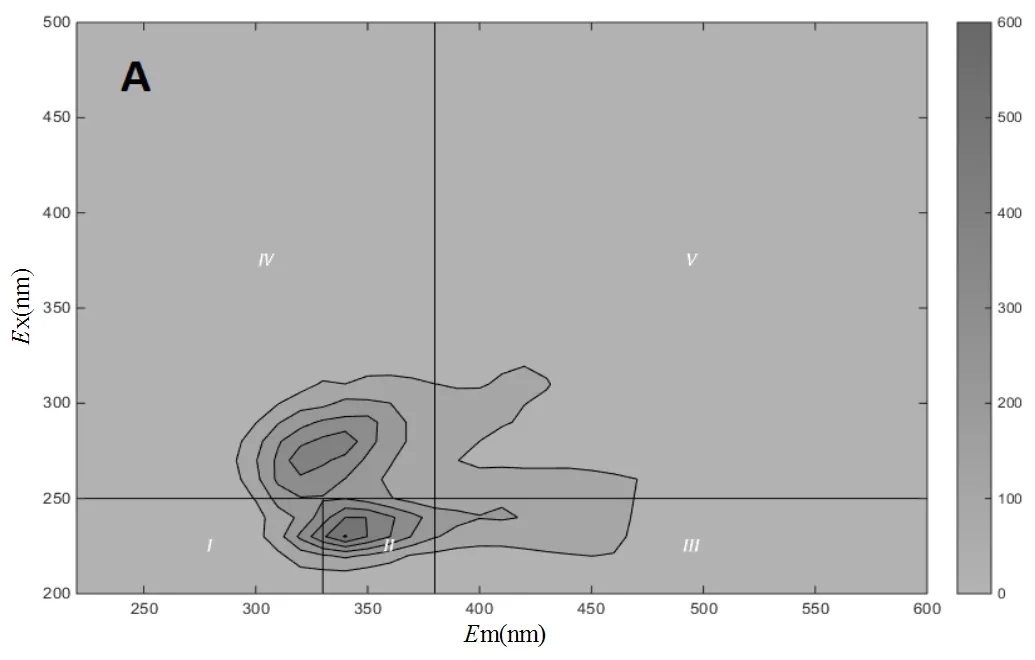
A:原水;B:Na2SO3:PMS=50mmol/L:50mmol/L,30℃;C:Na2SO3:PMS=100mmol/L: 50mmol/L,30℃
采用能定量区分EEM细微变化的FRI法(Fluorescence regional integration,荧光区域综合指数法)分析EEM数据[27-28],通过计算特定区域标准体积(Φ,n)和各区域标准体积百分比(P=100×Φ)反映对应区域具有特定结构荧光物质的含量和相对含量.不同条件下的荧光区域积分标准体积Φ,n和荧光区域体积组成变化百分比分别见表4和图3.原水中的芳香性蛋白类物质(区域Ⅱ)为主要污染物,荧光区域标准体积为1.08×107au·nm2,其次是溶解性微生物代谢产物(区域VI),荧光区域标准体积为1.21× 107au·nm2.此外,芳香性蛋白类物质(区域Ⅰ) 和富里酸类物质在原水水体中也占有一定的比例,荧光区域标准体积分别为5.11×106和4.90×106au·nm2.然而,腐殖酸类物质在原水中含量较低,荧光区域标准体积只有2.02×106au·nm2.经过SO32-/HSO5-体系产硫酸根自由基氧化处理之后,可以看出,当物质的量比(SO32-):(HSO5-)分别为50mmol/L:50mmol/L和100mmol/L: 50mmol/L时,水样的荧光区域标准体积均有较大程度的减弱,从3.49×107au·nm2分别下降到2.02×107和7.80×106au·nm2,相比原水分别降低了42.03%和77.67%.各区域所代表的有机物被氧化的程度也各不相同,当SO32-和HSO5-物质的量比为50mmol/L:50mmol/L时,区域I~V分别减少了23.52%、50.01%、48.11%、39.62%和45.94%.区域II、III、V标准体积百分比有所下降,而区域Ⅰ和Ⅳ标准体积百分比却有所上升,可能是由于芳香性蛋白类物质(区域II)、富里酸类和腐殖酸类物质的去除率高于芳香性蛋白类物质(区域I)和溶解性微生物代谢产物,导致最终出水中芳香性蛋白类物质(区域I)和溶解性微生物代谢产物的相对比例增加.而当SO32-和HSO5-物质的量比为100mmol/L: 50mmol/L时,区域I~V分别减少了66.32%、80.38%、64.56%、88.30%和60.10%.区域II、Ⅳ标准体积百分比有所下降,而区域Ⅰ、III、V标准体积百分比却有所上升,原因可能是芳香性蛋白类物质(区域II)和溶解性微生物代谢产物在水体中相对浓度较高,属于SO32-/HSO5-体系首要的去除对象,导致其他区域相对浓度有所上升.
各荧光区域积分标准体积间接表征了水体中有机污染物的相对含量,由此说明SO32-/HSO5-氧化体系对于蛋白质和芳香族化合物具有良好的去除能力.经过处理后,印染尾水中大分子氧化分解成小分子、芳香族缩聚、共轭生色团水平显著降低,因此,印染尾水的生物降解性得以显著提高.同时发现出水中色氨酸(x/m=230nm~225nm/340nm~330nm)峰值发生了5~10nm的蓝移,峰强亦均有所降低.通过对比可以推测,蓝移现象的产生,可能是在硫酸根自由基的强氧化作用下导致色氨酸类蛋白质的结构发生改变.研究表明,这种蓝移现象主要是由于水体中腐殖酸类物质被大量去除,溶解性有机物(DOM)分子共扼效应降低,色氨酸类蛋白质中的共轭基团、稠环芳烃多环结构开环及数量减少,或者是与物质结构中羟基、羧基、氨基等官能团的降解有关[29-30].
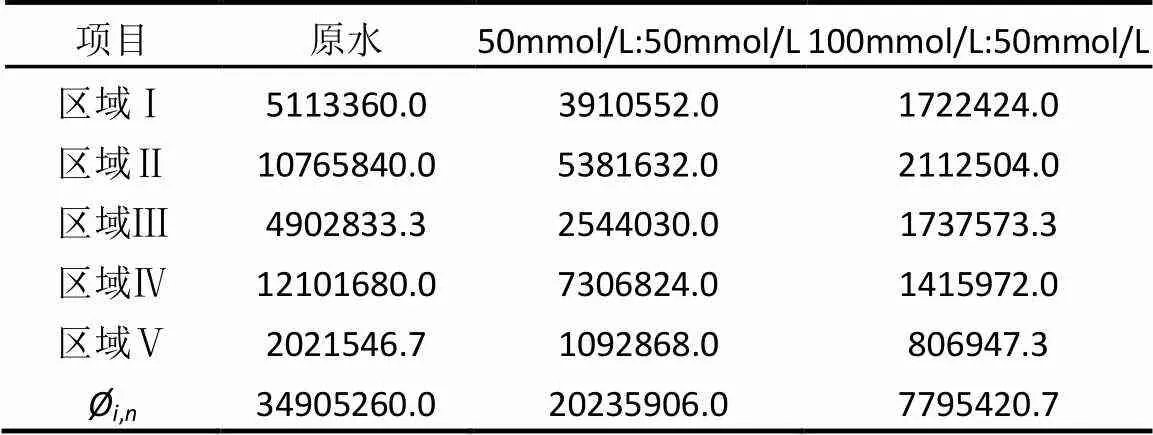
表4 不同条件下的荧光区域积分标准体积Øi,n

图3 不同条件下荧光区域体积组成变化
2.3 GPC/GC-MS分析
污水处理中分子质量分布的测定多采用滤膜过滤法,而近年来发展起来的凝胶渗透色谱(GPC)法可以简单方便的测定有机物分子量分布(MWD),因此被广泛运用到有毒有害污染物的检测分析中[30]. GPC主要参数有峰值分子量(p),重均分子量(w)以及数均分子量(n),w和n分别以分子重量的百分比和分子数量的百分比进行统计作为半定量分析,在分子质量和物质结构变化等方面解释有机污染物去除的机理.采用MWD分析考察了SO32-/ HSO5-体系对印染生化尾水残余有机物的去除效果及机理,并进一步验证EEM光谱分析的结果.n、w和以w/n表示的MW分布见表5.图4表示印染生化处理出水和物质的量比(SO32-):(HSO5-)为50mmol/L:50mmol/L、100mmol/L:50mmol/L条件下处理出水的MWD.
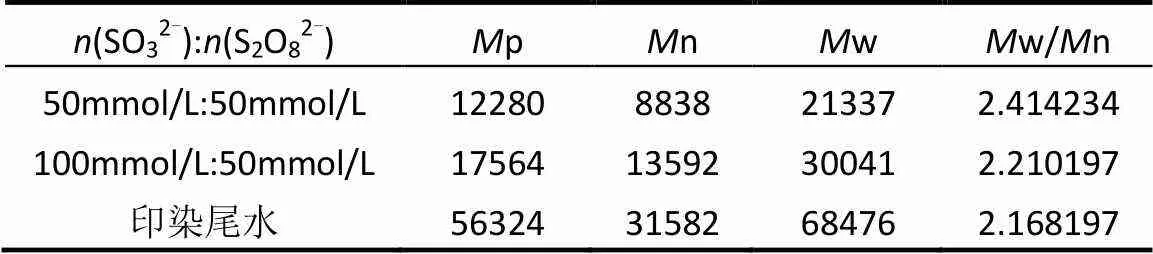
表5 水样分子量分布数据
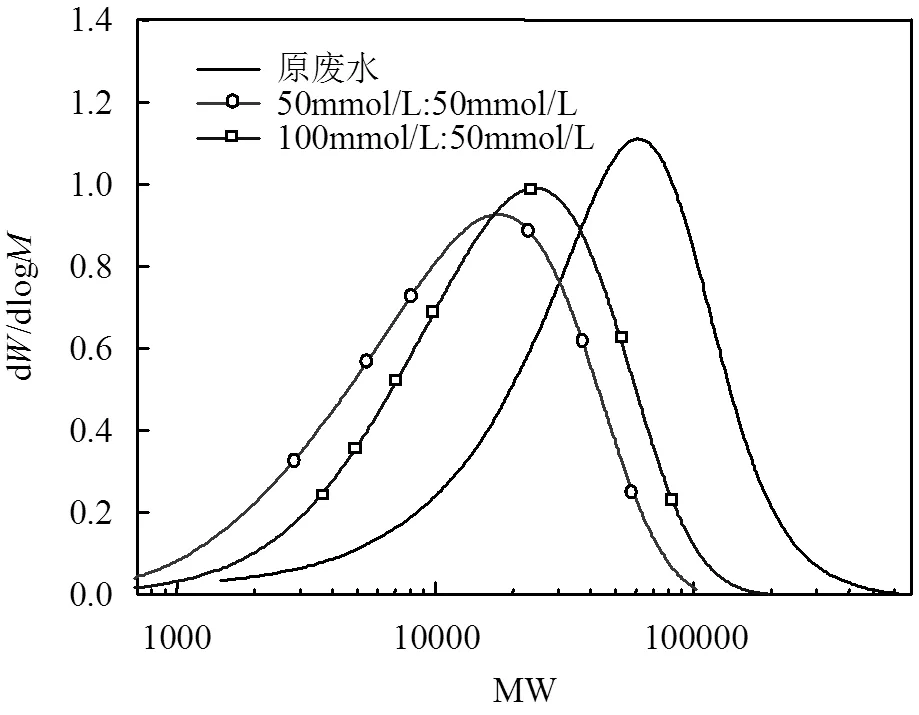
图4 水样的分子量分布拟合曲线
图4和图5分别表示水样的分子量分布拟合曲线图和水样的分子量分布统计,结果表明,生化尾水中p为56.324kDa,n为31.582kDa,w为68.476kDa,w/n为2.168197.w/n的值表示分子量的分散性,其值恒大于1,越接近1就表明有机物的大部分组成都是同源或特征属性相似[31]. DOM是指能通过0.45μm滤膜的有机物[32],印染生化尾水中的DOM主要分布在10kDa以上,其中>100kDa占41.8%,12~100kDa占54.2%,表明在印染生物处理尾水之中高分子量的有机物较多.推测大部分大分子应为蛋白质、多糖、分子量在100~ 10kDa腐殖酸类物质、芳香族有机物、氨基有机物和脂肪族有机物等.

图5 水样的分子量分布统计
经过硫酸根自由基高级氧化处理之后,表4中结果显示当(SO32-):(HSO5-)增加到50mmol/L: 50mmol/L和100mmol/L:50mmol/L时,p显著降低分别为12.28,17.564kDa,表明出水中有机物的分子量进一步减小,其峰面积值也逐渐降低;w/n值分别为2.414234,2.210197,与原水几乎相同,表明尾水中有机物整体分子量的减少.其中分子量>100kDa的有机物分布显著减少,从41.8%分别下降到1.1%和18.2%,而12~100Kda增多,分别为71.4%和67.7%, 8~12kDa为4.1%和11.9%,5~8kDa分别为2.9%和8.7%,2~5kDa分别为2.8%和8.4%,表明大分子DOM(0.45 μm~ 100 kDa)在硫酸根自由基氧化后有效地降解为小分子有机物(1~10 kDa).残留在水中的小分子有机质的数量增多,这是由于含芳香族氨基酸的蛋白质类物质或酚类物质的不饱和键断裂,引起废水中DOM (溶解性有机物)结构和种类发生改变,还原性物质减少,使大分子物质变成小分子物质[33].进一步发现,在氧化处理之后DOM的种类开始大幅度增加,且具有同源性或特征性质相似,这是因为低分子量(0.2~0.5kDa)的有机质具有生物不稳定性,腐殖酸被氧化成脂肪族和短链有机酸物质[34-35],同时,硫酸根自由基极易攻击简单芳香族化合物的不饱和键,从而发生断裂和开环,特别是含C=C双键或苯环的有机物易被快速氧化降解[36].
进一步结合GC-MS结果,如图所示,经过硫酸根自由基氧化处理之后,根据官能团分类有机物种类,并通过其峰面积计算各物质的去除率.结果发现,印染尾水中成分非常复杂,主要污染物质为苯胺、长链的烷烃类(大多为链式烷烃)、含氮杂环化合物等苯系物和杂环类有机物,还含有一定量的脂类、少量苯类、脂肪酸及醇类等物质.经过硫酸根自由基氧化之后,(SO32-):(HSO5-)增加到50mmol/L:50mmol/L和100mmol/L:50mmol/L条件下峰面积分别减少了36.2%和30.1%,原水中大量存在的烷烃类和脂类物质大多被部分去除,出水中的有机物含量显著降低.由此表明,硫酸根自由基对烷烃类物质的氧化较为彻底,相比之下,脂类物质的去除并不彻底,表明即使是SO32-/HSO5-工艺仍然无法对这两类物质进行彻底的氧化,一些脂类在经过硫酸根自由基氧化之后仍然残存在出水中.推测TOC的下降(从12.283mg/L到6.913~ 6.330mg/L)主要归因于硫酸根自由基的氧化下,烷烃碳链断裂生成低碳化合物,同时,又被氧化成有机酸和醇,继而发生水解生成酯类.

图6 水样GC-MS的总离子流图
3 结论
3.1 基于响应面法优化,该体系对有机物有一定的去除率,特别是对苯胺去除效果尤为显著,影响因子对COD和苯胺处理效果的贡献排序分别为:温度>(SO32-)/(HSO5-)>(HSO5-)>初始pH值;(HSO5-) >(SO32-)/(HSO5-)/初始pH值>温度.在实验最佳条件:pH=6.9,温度为53℃,SO32-/HSO5-物质的量比为1.6, HSO5-投加量为37.1mmol/L,该条件下反应10min时出水COD和苯胺去除率分别为33%和90%.
3.2 EEM结果发现,印染尾水氧化出水中荧光性DOM含量显著降低,并且性质发生改变.芳香性蛋白类物质(区域Ⅱ)是原废水中DOM的主要组分,在(SO32-):(HSO5-)为100mmol/L:50mmol/L时,类色氨酸荧光区域标准体积削减了80.38%,溶解性微生物代谢产物荧光区域标准体积被削弱了88.30%,说明硫酸根自由基对大分子有机污染物可以有效去除;类色氨酸峰发生了5~10nm的蓝移,推测尾水中稠环芳烃分解为小分子,共轭基团和芳香环数量减少.
3.3 GPC结果发现,DOM中大分子(0.45μm~ 100kDa)物质比例为41%,中等分子(12~100kDa)物质的比例为48.9%,峰值分子量(p)为56.324kDa,w/n=2.168,处理后的出水p主要分布在12.28~ 17.56kDa范围内,小分子物质数量增多,结构和种类发生改变.GC-MS结果同步揭示,氧化出水中的烷烃类物质显著减少,主要副产物为一些酯类、醇类和脂肪酸物质,为后续进一步生化处理创造了条件.
[1] Lou T, Xie H. Photochemical alteration of the molecular weight of dissolved organic matter [J]. Chemosphere, 2006,65(11):0-2342.
[2] Eldesoky H S, Ghoneim M M, Elsheikh R, et al. Oxidation of levafix CA reactive azo-dyes in industrial wastewater of textile dyeing by electro-generated Fenton's reagent [J]. Journal of Hazardous Materials, 2010,175(1–3):858-865.
[3] Oon Y L, Ong S A, Ho L N, et al. Up-flow constructed wetland- microbial fuel cell for azo dye, saline and nitrate remediation and bioelectricity generation: from waste to energy approach [J]. Bioresource Technology, 2018,266:97-108.
[4] GB4287-2012 纺织染整工业水污染物排放标准 [S]. GB4287-2012 Discharge standard of water pollutants in textile dyeing and finishing industry [S].
[5] Dulekgurgen E, Doğruel S, Karahan O, et al. Size distribution of wastewater COD fractions as an index for biodegradability [J]. Water Research, 2006,40(2):273-282.
[6] Huang C, Peng F, Guo H J, et al. Efficient COD degradation of turpentine processing wastewater by combination of Fe-C micro- electrolysis and Fenton treatment: long-term study and scale up [J]. Chemical Engineering Journal, 2018,351:697-707.
[7] Chung M H, Wang C T, Wang J W, et al. Application of response surface methodology on COD removal from textile wastewater by anodic chlorination and cathodic electro-Fenton process [J]. Desalination & Water Treatment, 2018,108:144-151.
[8] 陈思莉,江 栋,刘 永,等.臭氧-MBR工艺深度处理印染废水中试研究[J]. 环境科学与技术, 2012,35(12J):259-261.Chen S L, Jiang D, Liu Y, et al. Pilot plant research of dyeing wastewater by ozone/membrane bioreactor [J]. Environmental Science & Technology 2012,35(12J):259-261.
[9] Tan Y J, Sun L J, Li B T, et al. Fouling characteristics and fouling control of reverse osmosis membranes for desalination of dyeing wastewater with high chemical oxygen demand [J]. Desalination, 2017,419:1-7.
[10] 何洋洋,唐素琴,康婷婷,等.响应面法优化硫酸根自由基高级氧化深度处理渗滤液生化尾水[J]. 中国环境科学, 2015,35(6):1749-1755.He Y Y, Tang S Q, Kang T T, et al. Optimization of sulfate radical-based advanced oxidation process using response surface methodology for treating effluent from biological treatment of landfill leachate. [J]. China Environmental Science, 2015,35(6):1749-1755.
[11] Zhang B T, Zhang Y, Teng Y, et al. Sulfate radical and its application in decontamination technologies [J]. Critical Reviews in Environmental Science & Technology, 2015,45(16):1756-1800.
[12] 唐 海,徐建平,安 东,等.TiO2/ZSM-5m光催化耦合过硫酸盐降解焦化尾水的研究[J]. 中国环境科学, 2015,35(11):3325-3332.Tang H, Xu J P, An D, et al. Studies on the TiO2/ZSM- 5mphotocatalyst and combination with persulfate for the degradation of coking wastewater [J]. China Environmental Science, 2015,35(11): 3325-3332.
[13] 朱思瑞,高乃云,鲁 仙,等.热激活过硫酸盐氧化降解水中双酚A [J]. 中国环境科学, 2017,37(1):188-194. Zhu S R, Gao N Y, Lu X, et al. Degradation of bisphenol A in aqueous solution by thermally activated sulfate oxidation China Environmental Science, 2017,37(1):188-194.
[14] Zhu L, Ai Z, Ho W, et al. Core–shell Fe–Fe2O3nanostructures as effective persulfate activator for degradation of methyl orange [J]. Separation & Purification Technology, 2013,108(16):159-165.
[15] Xie P, Ma J, Liu W, et al. Removal of 2-MIB and geosmin using UV/persulfate: contributions of hydroxyl and sulfate radicals [J]. Water Research, 2015,69:223.
[16] Lei Y, Chen C S, Tu Y J, et al. Heterogeneous Degradation of Organic Pollutants by Persulfate Activated by CuO-Fe3O4: Mechanism, Stability, and Effects of pH and Bicarbonate Ions [J]. Environmental Science & Technology, 2015,49(11):6838-6845.
[17] Li H, Guo J, Yang L, et al. Degradation of methyl orange by sodium persulfate activated with zero-valent zinc [J]. Separation & Purification Technology, 2014,132:168-173.
[18] Yang M M, Zhou S Q, Liu D, et al. Degradation kinetics of activated carbon catalyzed persulfate oxidation orange G [J]. Environmental Science, 2013,34(3):962.
[19] 唐 海,张昊楠,段升飞,等.SO32-活化S2O82-降解偶氮染料废水的机制研究[J]. 中国环境科学, 2018,38(3):959-96.Tang H, Zhang H N, Duan S F, et al.Mechanism research for degradation of azo dying wastewater based on persulfate activated by sulphite [J]. China Environmental Science, 2018,38(3):959-96.
[20] 王文啸,卞 伟,李 军,等.响应面法优化解体好氧颗粒污泥的修复方式[J]. 中国环境科学, 2018,38(1):161-168.Wang W X, Bian W, Li J, et al. Optimizing the repairing method of decomposition aerobic granular sludge by response surface methodology [J]. China Environmental Science, 2018,38(1):161-168.
[21] Hazime R, Nguyen Q H, Ferronato C, et al. Optimization of imazalil removal in the system UV/TiO2/K2S2O8using a response surface methodology (RSM) [J]. Applied Catalysis B Environmental, 2013, 132-133(1):519-526.
[22] Matzek L W, Carter K E. Activated persulfate for organic chemical degradation: A review [J]. Chemosphere, 2016,151:178-188.
[23] 宿程远,郑 鹏,卢宇翔,等.海泡石与生物质炭强化厌氧处理养猪废水[J]. 中国环境科学, 2017,37(10):3764-3772.Su C Y, Zheng P, Lu Y X, et al. Enhanced efficiency of an anaerobic reactor containing sepiolite or biochar for treatment swine wastewater [J]. China Environmental Science, 2017,37(10):3764-3772.
[24] Bridgeman J, Baker A, Carliell-Marquet C, et al. Determination of changes in wastewater quality through a treatment works using fluorescence spectroscopy [J]. Environmental Technology, 2013, 34(21-24):3069.
[25] Sun W L, Ni J R, Xu N, et al. Fluorescence of sediment humic substance and its effect on the sorption of selected endocrine disruptors [J]. Chemosphere, 2007,66(4):700-707.
[26] Lai P, Zhao H Z, Zeng M, et al. Study on treatment of coking wastewater by biofilm reactors combined with zero-valent iron process [J]. Journal of Hazardous Materials, 2009,162(2/3):1423- 1429.
[27] Wu H, Zhou Z, Zhang Y, et al. Fluorescence-based rapid assessment of the biological stability of landfilled municipal solid waste. [J]. Bioresource Technology, 2012,110(2):174-183.
[28] Chen W, Westerhoff P, Leenheer J A, et al. Fluorescence excitation- emission matrix regional integration to quantify spectra for dissolved organic matter [J]. Environmental Science & Technology, 2015,37(24): 5701-5710.
[29] 唐书娟,王志伟,吴志超,等.膜-生物反应器中溶解性有机物的三维荧光分析[J]. 中国环境科学, 2009,29(3):290-295.Tang S J, Wang Z W, Wu Z C, et al. Excitation-emission matrix fluorescence spectra analysis of dissolved organic matter in membrane bioreactor [J]. China Environmental Science, 2009,29(3):290-295.
[30] Yan H, Nian Y, Zhou Y, et al. A detailed dissolved organic matter characterization of starch processing wastewater treated by a sedimentation and biological hybrid system [J]. Microchemical Journal, 2017,130:295-300.
[31] Meng L, Huang M, Bi L, et al. Performance of simultaneous wastewater reuse and seawater desalination by PAO-LPRO process [J]. Separation and Purification Technology, 2018,201:276-282.
[32] Liu L, Song C, Yan Z, et al. Characterizing the release of different composition of dissolved organic matter in soil under acid rain leaching using three-dimensional excitation–emission matrix spectroscopy [J]. Chemosphere, 2009,77(1):0-21.
[33] 张定定,马冬梅,汤志涛,等.印染废水深度处理过程中有机污染物分子量的分布变化[J]. 环境化学, 2014,33(7):54-60.Zhang D D, Ma D M, Tang Z T, et al. Molecular weight distribution and variations of organic pollutants in advanced treatment processes of biological treatment effluent of dyeing wastewater [J]. Environmental Chemistry, 2014,33(7):54-60.
[34] Jarusutthirak C, Amy G. Understanding soluble microbial products (SMP) as a component of effluent organic matter (EfOM) [J]. Water Research, 2007,41(12):2787-2796.
[35] 彭华平,吴彦瑜,周少奇,等. Fenton法氧化/混凝作用去除腐殖酸的研究[J]. 环境科学, 2010,31(4):996-1001.Peng H P, Wu Y Y, Zhou S Q, et al. Removal of humic acids by oxidation and coagulation during fenton treatment [J]. Environmental Science, 2010,31(4):996-1001.
[36] Kun-Chang H, Zhiqiang Z, Hoag G E, et al. Degradation of volatile organic compounds with thermally activated persulfate oxidation [J]. Chemosphere, 2005,61(4):551-560.
Removal of soluble organic containments from dyeing biochemical effluent by SO32-/HSO5-system optimized.
ZHANG Hao-nan1, TANG Hai1*, LI Qiang1, ZHANG Chen1, LIU Gui-zhong2
(1.School of Biochemical Engineering, Anhui Polytechnic University, Wuhu 241000, China;2.Beijing Municipal Research Institute of Environmental Protection, Beijing 100083, China)., 2019,39(7):2854~2863
The conventional biochemical treatment effluent of dyeing wastewater (BREDW) still contains a certain concentration of dissolved organic pollutants (DOM) and Aniline strictly controlled by the new standard. Sodium bisulfite-activated potassium bisulfate complex salt (SO32-/HSO5-) advanced oxidation system was used to produce sulfate radical (SO4-·) for the advanced treatment of BREDW. The effects of initial pH value, reaction temperature, SO32-/ HSO5-molar ratio and HSO5-dosage on the removal of COD and aniline were optimized based on response surface methodology. COD and aniline can be removed by the system remarkably. The contribution order of influencing factors to COD and aniline treatment were as follows: temperature>(SO32-)/(HSO5-)>(SO32-)>initial pH value and(HSO5-)>(SO32-)/(HSO5-)/initial pH value>temperature. The removal rates of COD and aniline were 33% and 90% respectively under the experimental conditions by the experiment optimization : pH of 6.8, temperature of 53℃, concentration molar ratio SO32-to HSO5-of 1.6 and HSO5-dosage of 37.1mmol/L. Further studies were made on the changes of fluorescence and molecular properties of the main DOMs before and after dyeing effluent treatment. 3DEEMs found that aromatic proteins and soluble microbial metabolites were the main components of DOM in the BREDW. The fluorescent DOM content in the oxidized effluent decreased significantly under different conditions, and the fluorescent area volume was reduced by 42.03%~77.67%. At the same time, the peak value of tryptophan (x/m=230~225nm/ 340nm~330nm) in the oxidized effluent was observed to blue shift of 5~10nm. Polycyclic aromatic hydrocarbons in BREDW are decomposed into small molecules, the number of conjugated groups and aromatic rings decreases; GPC revealed that the proportion of macromolecules (0.45μm~100kDa) was 41%, that of medium molecules (12~100kDa) was 48.9%, that of peak molecular weight (p) was 56.324kDa, and that ofw/n = 2.168. After treatment, the effluentp mainly distributes in the range of 12.28~17.56kDa, with more small molecular substances, more structures and species. GC-MS synchronously reveals that the alkanes in the oxidized effluent are greatly reduced, and the main by-products are esters, alcohols and fatty acids, which can create conditions for further biochemical treatment.
the effluent of dyeing wastewater by biological treatment;sulfate radical;peroxymonosulfate;Excitation— Emission—Matrix Spectra;Gel Permeation Chromatography
X703.5
A
1000-6923(2019)07-2854-10
张昊楠(1994-),女,安徽蚌埠人,安徽工程大学硕士研究生,主要从事水的深度处理技术研究.发表论文4篇.
2018-12-20
国家重点实验室开放课题(PCRRF17016);安徽省自然科学基金资助项目(1608085ME118);安徽省优秀人才基金资助项(gxyqZD2016120)
* 责任作者, 教授, tanghai@ahpu.edu.cn

