高血压患者心外膜脂肪组织厚度对心脏结构及心功能的影响
刘卫华 黄群英 赵印平 莫江英
(桂林市第二人民医院,广西桂林541001)
1 资料与方法
1.1 一般资料
选择2015年1月至2016年5月100例健康体检者,符合2010年中国高血压防治指南高血压患者150例,其中女性115例,男性135例,平均(65.7±12.3)岁。
1.2 临床资料
1.2.1 超声心动图测量 (1)EAT测量与分组:采
用东芝Aplio 400型多普勒显像仪,探头频率3.0MHz,研究对象取左侧卧位,在胸骨旁左心室长轴检查,以主动脉瓣环为定位标识,显示右心室游离壁前方的EAT,在舒张期末冻结图像,垂直主动脉瓣环,测量右心室游离壁EAT厚度,测量5个周期,取平均值。根据EAT值分为低值(1.96mm-7.12mm)、中值(7.13mm-11.68mm)、高值(11.69mm-16.37mm)3组。
(2)心脏结构和心功能指标:采用德东芝Aplio 400型多普勒显像仪,探头频率3.0MHz,测量心脏结构:①舒张末室间隔厚度(IVST)和(或)左心房后壁厚度(PWT);②左心房前后径;③左心室舒张末期(LVDd)。
左室重量(LVM)(g)=0.8×10.4[(IVST+PWT+LVDd3-LVDd3]+0.6
左室重量指数(LVMI)(g/m2)=LVM/BSA(体表面积)
测量心功能包括(1)以二尖瓣舒张早期血流峰值(E峰)与舒张早期二尖瓣环速度(Em峰)的比值(E/Em 比值);(2)左室射血分数(LVEF)。
1.2.2 常规生化测定 (1)空腹血糖(FBG):东芝TBA-120FP全自动生化分析仪使用GOD-PAP法测定。
(2)空腹胰岛素(FINS):采用HPLC法采用化学发光法。
(3)胰岛素抵抗指数(HOMA-IR):HOMA-IR=FINS(μU/ml)×FBG(mmol/L)/22.5超敏C反应蛋白(hs-CRP):东芝TBA-120FP全自动生化分析仪使用免疫比浊法测定。
1.3 统计方法
统计分析应用SPSS11.0 for Windows软件包进行,计量资料以±s表示,以t检验进行两组资料间的显著性检验;计数资料用χ2检验,P<0.05为差异有统计学意义。
2 结 果
2.1 两组患者临床资料的比较
高血压组与健康组除性别和体表面积、甘油三酯差异无统计学意义外,年龄、体重指数、吸烟、合并糖尿病、总胆固醇、低密度脂蛋白、高密度脂蛋白、hs-CRP、HOMA-IR差异有统计学意义(P<0.05)。见表1。
2.2 不同厚度的EAT与血压、心脏结构、心功能的关系
三组不同厚度EAT组与血压差异有统计学意义(P<0.05)。三组不同厚度 EAT与 hs-CRP、HOMA-IR、LA、LVMI、EF、E/Em 比值差异有统计学意义(P<0.05)。见表 2。
表1 健康组与高血压组一般临床资料比较(±s)
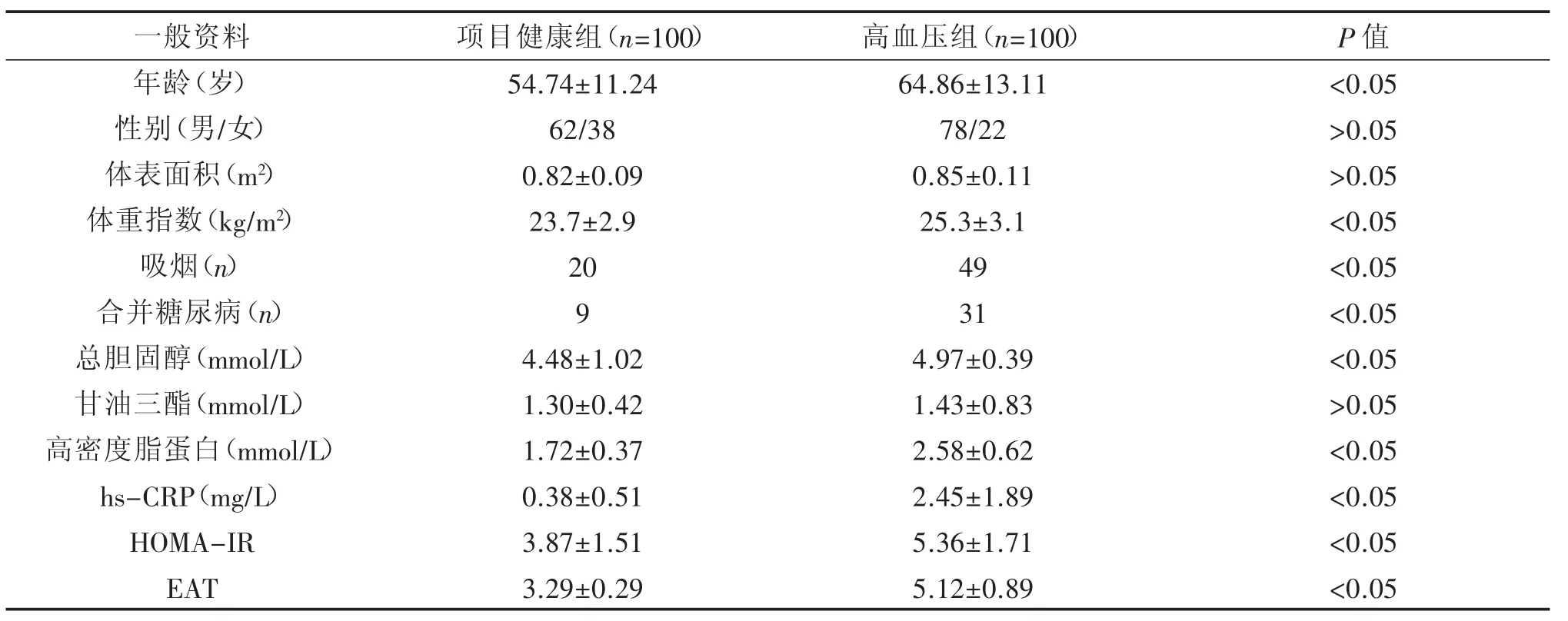
表1 健康组与高血压组一般临床资料比较(±s)
一般资料年龄(岁)性别(男/女)体表面积(m2)体重指数(kg/m2)吸烟(n)合并糖尿病(n)总胆固醇(mmol/L)甘油三酯(mmol/L)高密度脂蛋白(mmol/L)hs-CRP(mg/L)HOMA-IR EAT项目健康组(n=100)54.74±11.24 62/38 0.82±0.09 23.7±2.9 20 9 4.48±1.02 1.30±0.42 1.72±0.37 0.38±0.51 3.87±1.51 3.29±0.29高血压组(n=100)64.86±13.11 78/22 0.85±0.11 25.3±3.1 49 31 4.97±0.39 1.43±0.83 2.58±0.62 2.45±1.89 5.36±1.71 5.12±0.89 P值<0.05>0.05>0.05<0.05<0.05<0.05<0.05>0.05<0.05<0.05<0.05<0.05
表2 EAT三组结果比较(±s)
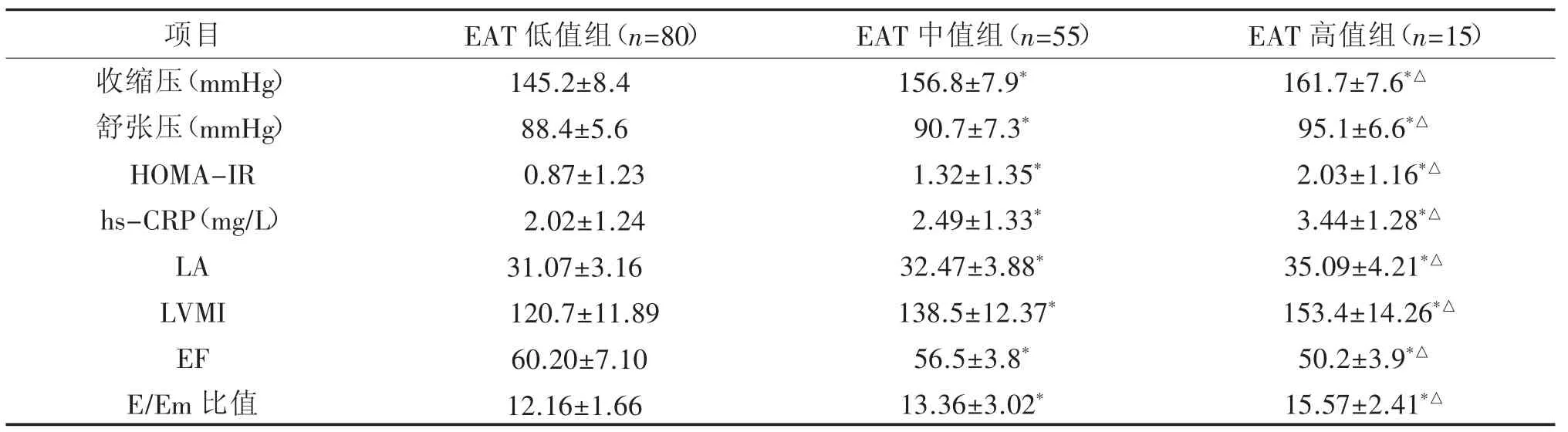
表2 EAT三组结果比较(±s)
注:与 EAT低值组比较,*P<0.05;与 EAT中值组比较,△P<0.05。
项目收缩压(mmHg)舒张压(mmHg)HOMA-IR hs-CRP(mg/L)LA LVMI EF E/Em比值EAT低值组(n=80)145.2±8.4 88.4±5.6 0.87±1.23 2.02±1.24 31.07±3.16 120.7±11.89 60.20±7.10 12.16±1.66 EAT中值组(n=55)156.8±7.9*90.7±7.3*1.32±1.35*2.49±1.33*32.47±3.88*138.5±12.37*56.5±3.8*13.36±3.02*EAT高值组(n=15)161.7±7.6*△95.1±6.6*△2.03±1.16*△3.44±1.28*△35.09±4.21*△153.4±14.26*△50.2±3.9*△15.57±2.41*△
3 讨论
临床研究表明长期和持续的高血压由于一系列神经内分泌因子激活产生心肌重构,导致心脏结构改变和收缩舒张功能障碍。EAT影响心脏结构,心功能的可能的机制:(1)EAT的增加机械性限制了心脏扩张和充盈;(2)EAT分泌一些如病毒、抵抗素、内毒素、肿瘤坏死因子等一些促炎症脂肪和细胞。这些炎症因子通过渗透作用进入冠状动脉到达心肌各层,影响心肌功能。另一方面这些炎症因子也可引起冠状动脉自身的病变,并与全身高游离脂肪酸血症协同作用,导致胰岛素介导的内皮依赖性血管舒张功能障碍,可能成为粥样硬化病变的基础。本研究中高血压患者的EAT厚度与胰岛素抵抗、超敏C反应蛋白之间有统计学差异,提示EAT可能参与体内炎症过程,影响胰岛素抵抗、超敏C反应蛋白。
本研究局限性在于样本数量较小,且有些高血压患者病情相对复杂,影响心功能因素也较多,EAT也受到多种因素影响,故还有许多与EAT的关系还有待研究。但综合上述,EAT与高血压有关,高血压EAT厚度增加影响患者心脏结构的大小,也影响了心脏收缩、舒张功能,若能通过各种方式积极干预治疗EAT,将有利于高血压及并发症管理。

