大剂量甲氨蝶呤不同输注方案治疗骨肉瘤疗效和安全性的Meta分析Δ
黄振城,宋再伟,赵荣生(1.北京大学第三医院药剂科,北京100191;2.北京大学药学院药事管理与临床药学系,北京 100191;3.北京大学医学部药物评价中心,北京 100191)
骨肉瘤是儿童和青少年中最常见的原发性恶性骨肿瘤,治疗难度较大,目前的治疗方案多以外科治疗为主,化疗或其他治疗为辅[1]。最新的许多骨肉瘤相关指南均推荐甲氨蝶呤(Methotrexate,MTX)作为骨肉瘤的一线化疗药物,包括美国国家综合癌症网络(National Comprehensive Cancer Network,NCCN)制订的《骨肿瘤临床实践指南》[2]、欧洲肿瘤内科学会(European Sarcoma Network Working Group,ESMO)制订的《骨肉瘤诊断、治疗和随访指南》[3]、我国的《中国骨肉瘤临床循证诊疗指南(2018)》[4]。大剂量甲氨蝶呤(High-dose methotrexate,HDMTX)是指MTX静脉给药剂量>500 mg/m2[5]。全身性化疗已成为骨肉瘤的治愈性治疗中必不可少的一部分,大多数骨肉瘤化疗方案中包含剂量范围为8~12 g/m2的HDMTX。由于MTX在骨肉瘤患者中用药剂量非常大,血液浓度往往较高,在提高疗效的同时也导致血液毒性、肝毒性、肾毒性等毒性反应的发生率增加,可导致化疗中断、肿瘤复发等[6],因而HDMTX用于治疗骨肉瘤时如何设计输注方案是受到广泛关注的临床问题。不同的给药剂量和输注时间均可能对HDMTX的血药浓度、安全性和有效性造成影响。
目前关于HDMTX用于治疗骨肉瘤的最佳输注方案尚无共识。因此,本研究采用Meta分析方法,系统评价HDMTX不同输注方案治疗骨肉瘤的疗效和安全性,为临床治疗提供循证参考。
1 资料与方法
1.1 纳入与排除标准
1.1.1 研究类型 国内外公开发表的观察性研究、随机/非随机对照试验。语种限定为中文和英文。
1.1.2 研究对象 接受HDMTX化疗的骨肉瘤患者。患者种族、性别、年龄均不限。
1.1.3 干预措施 不同的输注方案,包括不同的给药剂量、不同的输注时间。
1.1.4 结局指标 A.血液毒性/骨髓抑制;B.严重血液毒性/骨髓抑制;C.白细胞减少;D.血小板减少;E.肝毒性;F.严重肝毒性;G.肾毒性;H.严重肾毒性;I.口腔黏膜炎;J.严重口腔黏膜炎;K.消化道毒性;L.皮肤毒性;M.严重皮肤毒性;N.疾病进展;O.持续无病生存(Continuously disease-free survival,CDFS);P.血药浓度。其中A~M为不良事件的发生率,为安全性指标;N、O为疗效指标;P为MTX 的血药浓度(c0h、c24h、c48h等,如c0h指MTX输注完毕时,立即取血测得的血清药物浓度)。HDMTX的疗效参照欧洲肿瘤年会(European cancer conference,ECCO)的实体瘤疗效评价标准(Response evaluation criteria in solid tumors,RECIST)1.1[7],不良事件分级参照世界卫生组织(WHO)抗癌药物毒副作用分级[8]、美国国家癌症研究所常见不良反应评价标准(Common terminology criteria for adverse events,CTCAE)[9]或其他通用标准。
1.1.5 排除标准 ①非中、英文文献;②重复文献;③无法获取全文的文献。
1.2 检索策略
计算机检索Medline、Embase、clinicaltrial.gov、中国期刊全文数据库、万方数据和中国生物医学文献数据库,检索时限均从建库截至2018年3月。英文检索词包括 :“Bone marrow Cancer”“Osteosarcoma”“Methotrexate”“Drug dose”“Infusion”等;中文检索词包括:“甲氨蝶呤”“大剂量”“骨肉瘤”“给药方式”“不同剂量”“输注”等。英文和中文数据库的详细检索策略分别见图1(以Medline为例)和图2(以中国期刊全文数据库为例)。同时手工检索纳入文献的参考文献。本研究已在PROSPERO注册(注册号:No.CRD42018098976)。

图1 英文数据库检索策略(以Medline为例)Fig 1 Search strategy of English database(take Medline as example)
1.3 文献筛选、资料提取和质量评价
1.3.1 文献筛选 由2名研究者独立筛选文献并交叉核对,若遇分歧则咨询第三方协助判断。筛选文献时按题目、摘要和全文的顺序进行筛选。

图2 中文数据库检索策略(以中国期刊全文数据库为例)Fig 2 Search strategy of Chinese database(takingCJFD as example)
1.3.2 资料提取 由2名研究者提取资料并交叉核对,提取内容包括:① 纳入研究的基本信息,包括题目、第一作者、文献发表年份、种族/人群、患者数、性别、年龄、含HDMTX化疗方案的例次、给药方案、结局指标等;② 所关注的结局指标的结果测量数据。缺乏的资料尽量与作者联系以补充。
1.3.3 质量评价 由2名研究者独立采用纽卡斯尔-渥太华量表[10-11](the Newcastle-Ottawa scale,NOS)、Cochrane协作网提供的5.1.0偏倚风险评估工具[12]和非随机对照试验方法学评价指标(Methodological index for non-randomized studies,MINORS)[13]分别对观察性研究、随机对照试验和非随机对照试验进行偏倚风险评价。NOS量表共8个评价条目(满分为9分),其中研究人群选择方面有4个条目、组间可比性方面有1个条目、结果测量方面有3个条目,7~9分为高质量研究,4~6分为中等质量研究,1~4分为低质量研究。Cochrane偏倚风险评估工具主要从选择(包括随机序列产生和分配隐藏)、实施(包括对研究者和受试者施盲)、测量(研究结局盲法评价)、随访(结局数据的完整性)、报告(选择性报告研究结果)及其他(其他偏倚来源)这6个方面总计7个条目对偏倚风险进行评价。对每个条目依据偏倚风险评估准则做出“低风险偏倚”“高风险偏倚”和“不清楚”的判定结果。MINORS共12条评价指标,每条0~2分,前8条针对无对照组的研究;后4条与前8条一起针对有对照组的研究。遇到分歧时通过讨论解决或征求第三方意见。
1.4 统计学方法
应用Microsoft Excel 2016软件建立数据库,双人录入,并进行校对。采用Rev Man 5.3软件进行统计分析。计数资料和计量资料分别采用比值比(OR)和均数差(Mean difference,MD)为效应指标,各效应量均给出其点估计值和95%置信区间(CI),统计学差异性的检验水准设为0.05。所有定量合并都用固定效应模型进行分析。纳入研究间的异质性用χ2检验及I2进行分析,当Phet>0.10或I2≤50%时,研究结果间不存在异质性。若存在明显异质性(Phet≤0.10且I2>50%)[12],排除数据提取错误后,可作亚组分析或敏感性分析,分析异质性来源。若异质性过大或未能明确异质性来源,用随机效应模型进行合并或仅进行描述性分析。无法合并的结局指标用描述性方法分析。发表偏倚采用Egger's检验(研究数>10时有效),P<0.05说明存在发表偏倚。
2 结果
2.1 纳入研究基本信息
初检共获得相关文献3 093篇,手工补充检索0篇。经过逐层筛选,最终纳入5项研究[14-18],其中3项[14-16]用于Meta分析,另外2项[17-18]仅用作描述性分析。文献筛选流程见图3。
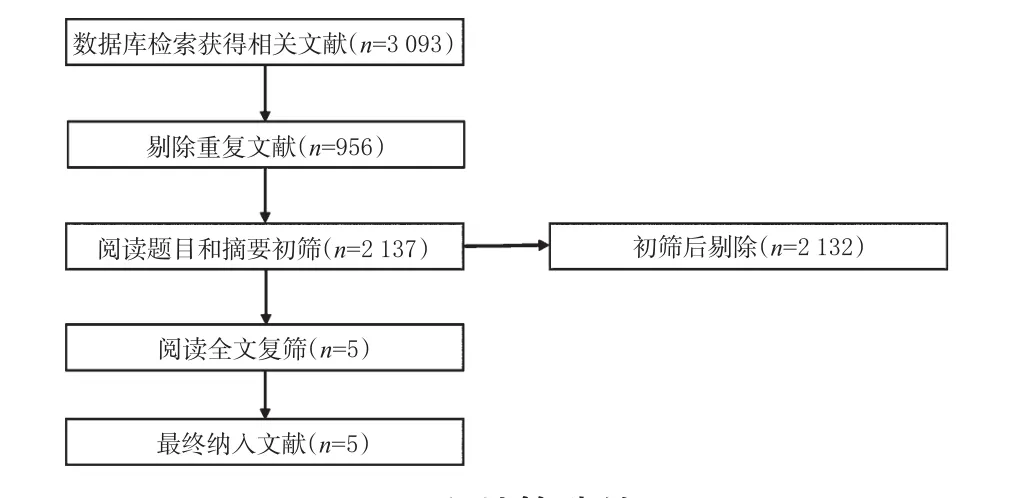
图3 文献筛选结果Fig 3 Result of literature screening
纳入的5项研究中4项为队列研究[14-17],1项为非随机对照试验[18]。3项研究亚洲人群的相关性[14-16],1项研究高加索人群[18],1项研究高加索人群和非洲人群[17]。1项研究纳入了儿童[16],4项同时纳入了儿童与成人[14-15,17-18]。输注方案方面,剂量包括0.7、2.5、5、7.5、8、10 g/m2,输注时间包括0.5、2、4、6、4~6 h。纳入研究的基本信息见表1。

表1 纳入研究基本信息Tab 1 General information of included studies
2.2 方法学质量评价结果
纳入的4项队列研究[14-17]的NOS平均得分为7.75分,均属于高质量研究。纳入1项非随机对照试验[18],根据MINORS评价指标,满足针对无对照组研究的其中7个指标(得分为13分)和针对有对照组研究的其中3个指标,总得分为18分,属于高质量研究。队列研究的方法学质量评价结果见表2。
2.3 Meta分析结果
2.3.1 不同输注方案与MTX血药浓度关系 共纳入3项队列研究[14-16],均在亚洲人中进行,其中2项[14-15]调查了儿童和成人,1项[16]仅调查了儿童。3项研究[14-16]均报道了当剂量不同时的c0h、c24h、c48h、c72h,1项[15]报道了当输注时间不同时的c0h、c24h、c48h、c72h、c96h。Meta分析结果详见表3、森林图见图4~图5。

表2 纳入的队列研究的NOS质量评价结果Tab 2 NOS quality evaluation of included cohort studies
由表3及图4~图5可知,8 g/m2组患者c0h[MD=-240.11,95%CI(-271.47,-208.75),P<0.001;图4]、c24h[MD=-0.09,95%CI(-0.11,-0.08),P<0.001;图5]、c48h[MD=-0.07,95%CI(-0.10,-0.05),P<0.001]、c72h[MD=-0.05,95%CI(-0.06,-0.03),P<0.001]均低于 10 g/m2组,但c0h、c24h、c48h的结果存在较大异质性。亚组分析结果提示,除c48h(I2=82%)外,异质性可能来源于年龄。用随机效应模型对c48h再次进行分析,效应值发生改变,但异质性大小仍不变。进行敏感性分析仍无法确定异质性来源,故对c48h这一结局指标的结果作描述性分析:3项研究的结果均提示8 g/m2组患者c48h显著低于10 g/m2组。
栗怀广等[15]报道了输注时间与MTX浓度的关系,故仅进行了描述性分析。结果表明,与6 h组比较,2 h组[MD=1.54,95%CI(0.32,2.76),P=0.01]、4 h组[MD=0.54,95%CI(0.17,0.91),P=0.004]患者给药结束后第24 h血药浓度可能更高。其他结局指标的定性分析均未发现相关性。
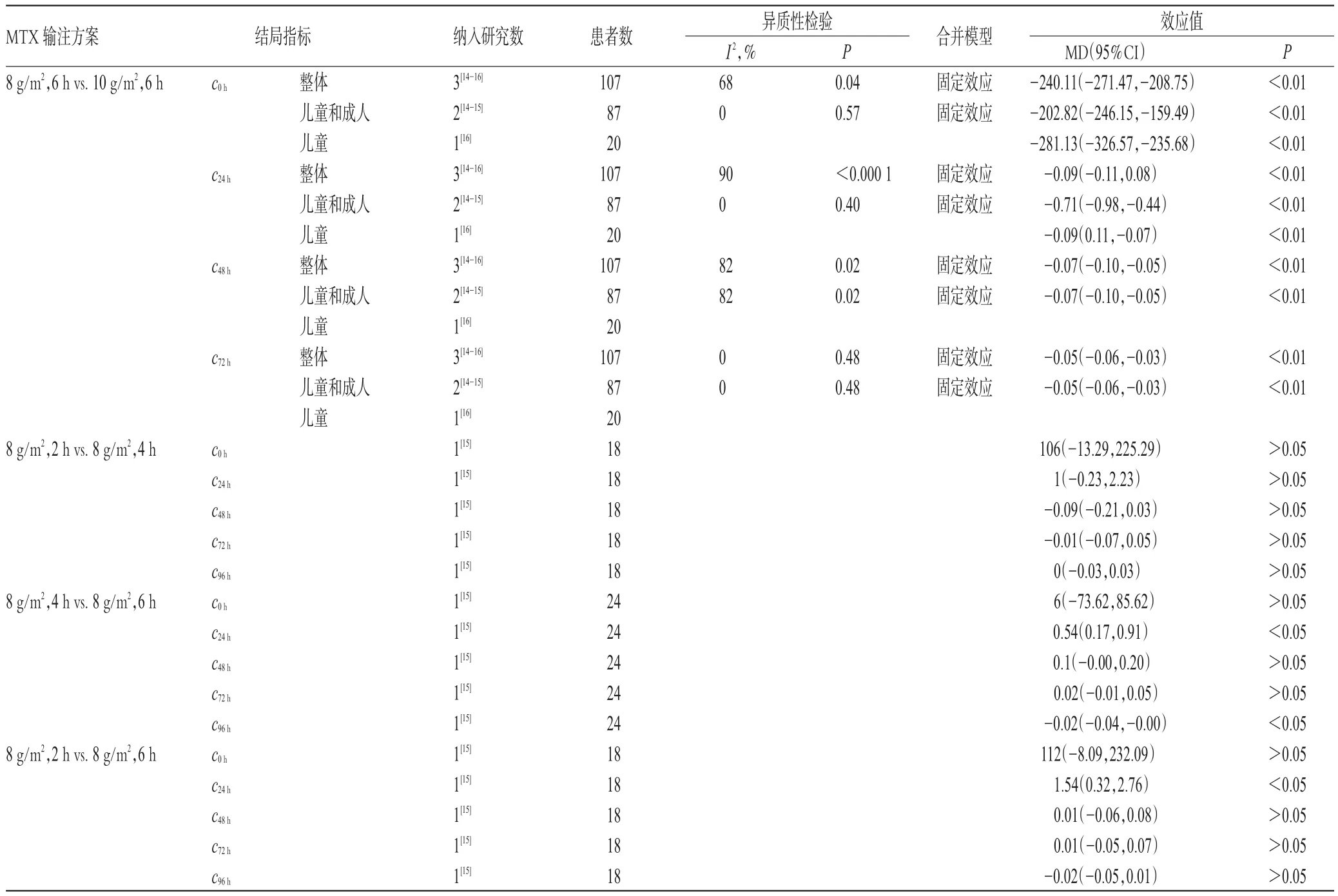
表3 骨肉瘤患者中HDMTX输注方案与MTX血药浓度的关系Tab 3 Relationship between infusion scheme of HDMTX and plasma concentration of MTX in patients with osteosarcoma
2.3.2 不同输注方案与HDMTX相关毒性的关系 仅2项研究[14,16]报道了HDMTX相关毒性,且均研究了剂量与HDMTX毒性的相关性。2项研究同时报道了肝毒性、口腔黏膜炎、胃肠道毒性、皮肤毒性,Meta分析结果见表4,森林图见图6。
由表4及图6可知,8 g/m2组肝毒性发生率[OR=0.26,95%CI(0.10,0.67),P=0.005]比10 g/m2组显著降低,且未观察到研究间异质性。按年龄进行亚组分析,结果表明儿童与成人混合组的肝毒性发生率在给药剂量为8 g/m2时显著低于10 g/m2,差异有统计学意义[OR=0.31,95%CI=(0.11,0.84),P<0.05]。其他指标的比较均未观察到显著相关性。
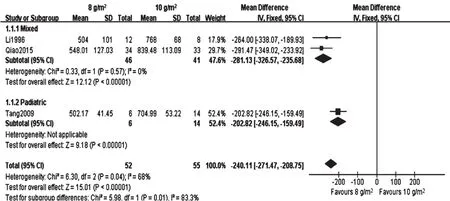
图4 两组患者c0 h的Meta分析森林图Fig 4 Forest plot of Meta-analysis for c0 hof patients in 2 groups
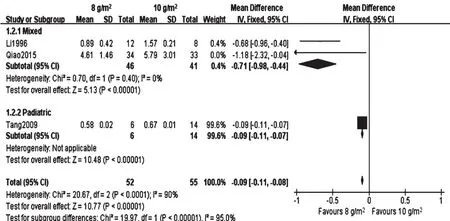
图5 两组患者c24 h的Meta分析森林图Fig 5 Forest plot of Meta-analysis for c24 hof patients in 2 groups

表4 骨肉瘤患者HDMTX输注方案与不良反应发生率的关系Tab 4 Relationship between infusion schemes of HDMTX and the incidence of ADR in patients with osteosarcoma

图6 肝毒性发生率的Meta分析森林图Fig 6 Forest plot of Meta-analysis of the incidence of liver toxicity
乔小云等[14]还报道了骨髓抑制、严重血液毒性(G3~G4)、白细胞减少症、血小板减少症、严重肝毒性(G3~G4)、肾毒性、严重口腔黏膜炎(G3~G4)、严重胃肠道毒性(G3~G4)、严重皮肤毒性(G3~G4),描述性分析结果显示,8 g/m2组白细胞减少[OR=0.05,95%CI(0.00,0.66),P=0.02]和血小板减少[OR=0.02,95%CI(0.00,0.48),P=0.02]的发生率可能比10 g/m2组更低。HDMTX与其他毒性则不显著相关。
2.3.3 不同输注方案与HDMTX疗效的关系 仅2项研究[17-18]报道了HDMTX的疗效,但2项研究的输注方案不同,只能进行描述性分析,结果见表5。

表5 骨肉瘤患者HDMTX输注方案与疾病进展的关系Tab 5 Relationship between infusion schemes of HDMTX and disease progress in patients with osteosarcoma
Pratt CB等[17]仅报道了疾病进展这一指标,描述性分析结果提示,MTX的剂量与疾病进展可能不显著相关。Bacci G等[18]报道了疾病进展和CDFS两个指标,描述性分析结果提示,MTX的输注方案可能与疾病进展无关,700 mg/m2,30 min方案的CDFS(51%)比7 500 mg/m2,6 h的(42.4%)高,但由于缺乏相关数据,无法计算输注方案与CDFS的关系。
3 讨论
骨肉瘤是儿童和青少年中发病率最高的原发性骨肿瘤和发病率排第3位的肿瘤类型,其特征是恶性肿瘤细胞产生类骨质或不成熟骨,治疗难度较大,目前的治疗方案包括新辅助化疗、手术切除、术后辅助化疗等[19-20]。自从20世纪70年代开始在肿瘤切除术后引入辅助化疗以来,患者的10年生存率从30%提高到了50%[21]。骨肉瘤化疗常用化疗药物包括HDMTX(加亚叶酸钙用于解毒)、阿霉素、顺铂和异环磷酰胺、依托泊苷等[22]。MTX是一种拮抗叶酸代谢的化疗药物,其结构与叶酸类似,主要通过竞争性抑制细胞中二氢叶酸还原酶的活性而使二氢叶酸不能还原成具有生理活性的四氢叶酸,从而使嘌呤核苷酸和嘧啶核苷酸的生物合成过程中碳基团的转移作用受阻,导致DNA的生物合成明显受抑制[23]。
本系统评价纳入4项队列研究和1项非随机对照试验,合计310例患者。Meta分析结果显示,输注时间相同或相近,MTX给药剂量为8 g/m2时c0h、c24h、c48h、c72h均比10 g/m2组显著更低,但研究间的异质性较大。亚组分析结果提示,异质性可能源于年龄的差异,年龄有可能与血药浓度存在某种关系。安全性方面,8 g/m2组患者的肝毒性发生率也显著低于10 g/m2组,但MTX输注方案与其他不良反应之间暂未发现关系。疗效方面也暂未发现关系。对单一研究的描述性分析结果提示,8 g/m2组的白细胞减少和血小板减少的发生率可能比10 g/m2组更低,2 h组和4 h组c24h可能比6 h组高。结果表明,相对于10 g/m2,给药剂量为8 g/m2时血药浓度更低,肝毒性发生率可能更低,安全性方面可能更优,但疗效方面尚不确切。输注时间和是否给予负荷剂量与疗效和安全性之间是否具有相关性则暂时无法得知。
本研究严格遵守系统评价步骤,制定了严格的纳入、排除标准,剔除了无对照的研究,并且对纳入的文献进行了方法学评价,保证了本研究结果的可靠性,但仍存在以下局限性:(1)纳入的研究数量和样本量较少;(2)各研究间年龄分布、病程、随访时间等存在差异;(3)不同研究间可用于合并的结局指标和数据都较少,有可能存在一定偏倚;(4)仅分析了MTX的剂量、输注时间与血药浓度,剂量与毒性、部分疗效指标的相关性的研究;受限于现有研究数量有限,尚未探讨是否给予负荷剂量与血药浓度、安全性、有效性,输注时间与疗效,以及输注方案与其他疗效指标的相关性,所以结论不全面。
综上所述,当前证据表明,HDMTX用于治疗骨肉瘤,给药剂量降低时,给药后血药浓度降低、肝毒性发生率可能降低,安全性可能更优,但疗效的相关性尚不明确;输注时间相对较长时,给药结束后第24 h血药浓度可能更低、安全性可能更优,但疗效的相关性尚不明确。因此,适当降低给药剂量(如8 g/m2)和适当延长输注时间(如6 h)有可能获得更好的治疗结局。但受纳入研究数量的限制,上述结论尚需要大样本、高质量的研究进一步验证。

