NaCl溶液中回收AZ31镁合金的腐蚀和电化学特性
李贺超, 祝向荣,b, 汤文,王金敏,b,张 娅,陈秋荣
(1.上海第二工业大学a.环境与材料工程学院;b.资源循环科学与工程研究中心,上海201209;2.中国科学院 上海微系统与信息技术研究所,上海200050)
0 引言
近年来,由于各项独特的性能,镁及其合金在工业领域中得到了广泛的应用[1-3]。作为轻合金结构材料,镁合金不仅可以大量应用于飞机、汽车等交通运输设备中[4-5],而且因为其具有较高的理论比容量和较小的标准电极电位,它也可应用于化学电源的负极材料中[6-7]。
随着镁合金的广泛应用,产生了大量的废弃镁合金材料。尽管镁资源在地球上具有较高的丰度,但过度开采镁矿石会破坏地球环境,造成镁资源枯竭;另一方面废弃镁合金的堆积会占用宝贵的土地资源并造成环境污染,而且相比于初始镁合金的冶炼,回收利用废弃镁合金材料所需消耗的能源大为降低[8-10],因此废弃镁合金材料的回收及利用值得重视。
目前,应用非常广泛的一类镁合金是以Al、Zn元素作为主要添加合金元素的AZ系列镁合金,比如AZ31、AZ91等。有关这类合金的研究主要集中于合金的机械特性、腐蚀等方面[11-14]。由于镁合金在化学电源方面的应用前景,近年来有关镁合金电化学特性方面的研究报道日益增多。影响镁合金的电化学特性因素非常复杂,最主要的是与材料的显微组织特征有关,而这又与合金元素的添加、材料的制备和加工工艺密切相关[11-16]。研究表明,AZ系列的镁合金如AZ31镁合金具有较好的抗腐蚀特性和电化学特性[11]。
因此本文采用熔炼工艺,按照AZ31镁合金的组分配比,将废弃的镁合金型材重新加工成回收镁合金(recycled magnesium alloy,RMA),研究了RMA在NaCl溶液中的腐蚀和电化学特性,并与商业化镁合金(commercial magnesium alloy,CMA)的腐蚀和电化学特性进行了比较。
1 实验
本文中所用的CMA样品为铸态。RMA采用熔炼法自行制备,初始合金组分按国家标准中AZ31镁合金的成分设计。先将废弃的镁合金型材经过机加工成块、清洗,然后在中频感应炉中进行熔炼,熔炼过程中需要通入氩气作为保护气体。为了调节Al、Mn的含量,期间添加适量的Al、MnCl2等原料。出炉冷却后得到了RMA铸锭,尺寸为120 mm×400 mm。利用电感耦合等离子光谱仪(ICP)测定CMA与RMA的成分,同时对比了国家标准中AZ31的金属含量(见表1)。ICP结果表明,RMA成分符合国家标准AZ31镁合金成分范围;与CMA相比,RMA中的Al含量较高,Fe、Cu、Ni的杂质含量也有所偏高。

表1 不同镁合金中各元素所占的质量分数Tab.1 The mass fraction of each element in different magnesium alloys
利用金相显微镜(OM)观察样品的表面形貌特性。利用X射线衍射仪(XRD)表征样品的晶体结构,XRD型号为Rigaku D/max2200vpc,扫描角度范围为 10◦∼ 100◦,扫描速率为 2◦/min。
腐蚀和电化学特性实验在NaCl电解质溶液中进行。NaCl溶液的浓度分别为0.6 mol/L和0.9 mol/L。首先进行腐蚀实验,样品经24 h腐蚀后,从NaCl溶液中取出,用250 g/L的铬酸溶液进行清洗,干燥后对样品进行称重。根据样品腐蚀前后的质量变化来求取样品的腐蚀速率,其计算公式为:

样品的电化学特性实验在标准三电极体系中进行。将样品加工成10×10×3 mm的片状,作为工作电极;Pt电极作为对电极;饱和甘汞电极作为参考电极。工作电极浸没在NaCl溶液中,持续900 s,采用AutolabAT302N电化学工作站获得样品的极化曲线和电化学阻抗谱(EIS)。测试极化曲线时,扫描速率为1 mV/s;EIS测试的频率范围为0.1 Hz∼100 kHz。
最后利用样品制作了镁电池原型器件。电池的负极为镁合金样品,电极尺寸加工成40 mm×50 mm×3 mm;电池的正极由MnO2、乙炔炭黑、石墨、N-甲基吡咯烷酮(NMP)和聚偏氟乙烯(PVDF)按一定比例混合制成。在恒电流50 mA,截止电压0.8 V的测试条件下,利用LAND CT2001A电池测试系统测试了原型电池的放电特性。
2 结果和讨论
图1所示为RMA和CMA的XRD图谱。由图可知,RMA和CMA具有相同的晶体结构和物相特征,一方面,两种样品主要都由六方结构的Mg基底(α相)组成。另一方面,除了Mg基底之外,还有少量的第二相Mg17Al12(相)。
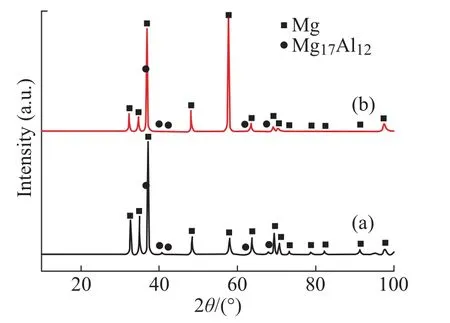
图1 两种镁合金样品的XRD图谱Fig.1 XRD patterns of the two as-cast magnesium alloys
图2 所示为两种镁合金样品的OM形貌。由图可见,材料显微组织主要是由10∼100µm的晶粒组成,晶粒为图1中的α相,其中,RMA样品的晶粒平均尺寸要小于CMA样品。这可能是由于RMA中Al含量略高,在熔炼过程中有助于晶粒的细化。另外,主要沿着晶界,分布有少量的β相。其中RMA样品中的β相分布比CMA样品要多,这也与RMA样品中较多的Al含量有关。且图1和图2显示的样品结构特性与其他文献报道结构类似[13-14].
表2为样品在不同浓度NaCl溶液中腐蚀24 h后获得的腐蚀速率数据。根据表2,当溶液浓度为0.6 mol/L时,RMA样品的腐蚀速率略高于CMA样品。当溶液浓度增加至0.9 mol/L时,CMA和RMA样品的腐蚀速率均上升,且RMA上升的幅度更大,说明RMA耐腐蚀性较差。这与前人已有的Al元素较高的合金具有较高的耐腐蚀性[17]的研究结果相反。可能是源于RMA中形成了较多的第二相,一方面,第二相在晶界的分布,更容易形成晶间腐蚀;另一方面,第二相的形成降低了Mg基底中的Al含量,不利于表面钝化膜的形成,从而降低抗腐蚀特性。从OM观察来看,RMA样品晶粒的平均尺寸要小于CMA样品。这也意味着RMA具有更多的晶界,而晶界处比较容易发生腐蚀。同时,RMA中Fe杂质含量高于CMA,这也不利于材料抗腐蚀。
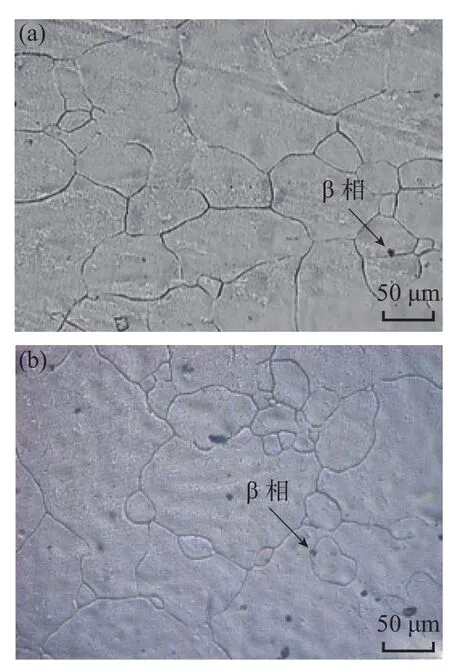
图2 两种镁合金样品的OM形貌 (a)RMA,(b)CMAFig.2 OM photos of the as-cast magnesium alloy samples(a)RMA,(b)CMA

表2 样品在不同浓度NaCl溶液中的腐蚀速率Tab.2 Corrosion rate of as-cast alloys in NaCl solutions with different concentrations
图3所示为样品在不同浓度NaCl溶液中腐蚀得到的极化曲线图。从图中可以看出,不同的样品在不同浓度溶液中,各极化曲线平滑且形状相似,但抗腐蚀能力不完全相同。表3为样品在不同浓度NaCl溶液中获得的腐蚀电位和腐蚀电流密度。由表3可知,当溶液浓度相同时,RMA样品的腐蚀电位略低于CMA样品的腐蚀电位;相应地,前者的腐蚀电流密度比后者略高,进一步表明RMA的抗腐蚀特性略差。从表3还可以看出,当溶液的浓度升高时,腐蚀电位更低一些;腐蚀电流密度明显增加。这是因为NaCl溶液浓度升高时,更多的Cl−会破坏表面形成的氧化膜,从而导致腐蚀速率上升[11]。

图3 样品在不同浓度NaCl溶液中的极化曲线Fig.3 Polarization curves of as-cast alloys in NaCl solutions with different concentrations

表3 样品在不同浓度NaCl溶液腐蚀后的腐蚀电位和腐蚀电流密度Tab.3 Corrosion potentialand corrosion currentdensity of ascast alloys in NaCl solutions with different concentrations
利用金相显微镜拍摄了样品在NaCl溶液中腐蚀24 h后的形貌特征,如图4所示。各样品经24 h腐蚀后,表面被腐蚀产物覆盖。但随着溶液浓度的增加,腐蚀产物也增加,如图4(b)、(d)所示。该结果与文献[9]中报道的AZ91腐蚀实验类似。由图4进一步看出,RMA样品表面形成的腐蚀孔和腐蚀产物要多于CMA。
图5所示为各样品在不同浓度NaCl溶液中腐蚀的EIS,其中每条谱线包含了高频容抗谱和低频感抗谱。高频部分的圆弧直径反映了样品的抗腐蚀特性,直径越大,抗腐蚀特性越好[11]。低频感抗谱与镁合金电极溶解过程形成的中间产物有关。由图5可知,当溶液浓度为0.6 mol/L时,CMA样品对应的高频部分直径大于RMA样品;当溶液浓度上升到0.9 mol/L时,CMA样品对应的高频部分直径仍旧大于RMA样品,表明CMA的抗腐蚀特性高于RMA。

图4 OM下各样品腐蚀后的表面形貌CMA(a)和RMA(b)在0.6 mol/L NaCl中,CMA(c)和 RMA(d)在 0.9 mol/L NaCl中Fig.4 OM images after corrosion for the two as-cast alloysCMA(a)and RMA(b)in 0.6 mol/L NaCl,CMA(c)and RMA(d)in 0.9 mol/L NaCl

图5样品在不同溶液中腐蚀后的EISFig.5 EIS of the as-cast alloys with corrosion in different solutions
图6 所示为两种合金作为负极材料在镁电池原型器件中的放电曲线。表4为RMA和CMA在NaCl电解质溶液中放电特性的相关数据。由图6可知,在放电初始,合金放电电压较高,随着放电时间延长,电压逐渐下降。另外,当电解质溶液浓度为0.9 mol/L时,放电时间较0.6 mol/L时大大延长。由表4可知,在0.9 mol/L溶液中,RMA和CMA的放电容量分别为24.4 Ah/m2和20.8 Ah/m2,RMA的放电容量略高于CMA。当溶液浓度降低到0.6 mol/L时,RMA和CMA的放电容量分别降低到18.9 Ah/m2和12.1 Ah/m2,RMA明显优于CMA。通常放电特性与材料的腐蚀电位有关,材料的腐蚀电位越偏负,其放电容量越大[11]。正如前面分析的,RMA的腐蚀电位较CMA偏负,因此其放电容量越大。总体而言,适度增加电解质溶液的浓度,有利于增加放电容量和延长放电时间。
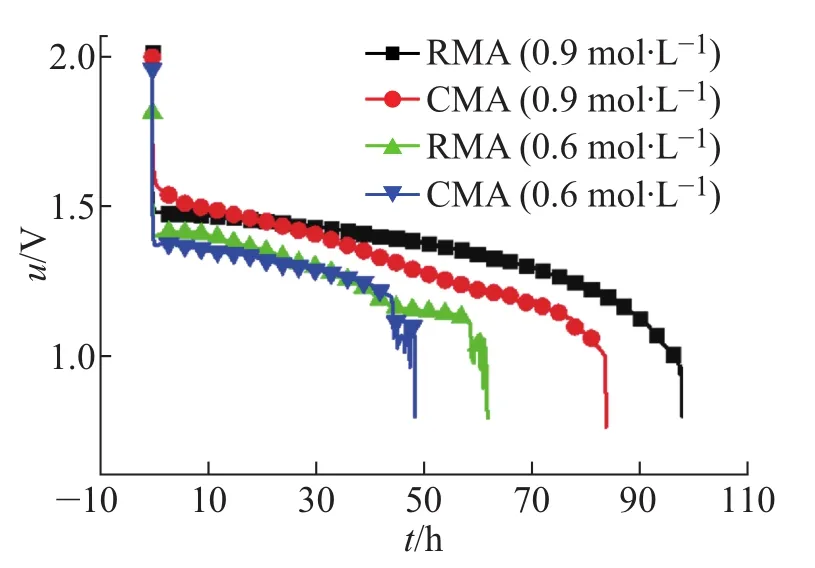
图6 RMA和CMA作为镁电池负极材料时的放电曲线Fig.6 Discharge capacity patterns of RMA and CMA as the cathode material of magnesium battery
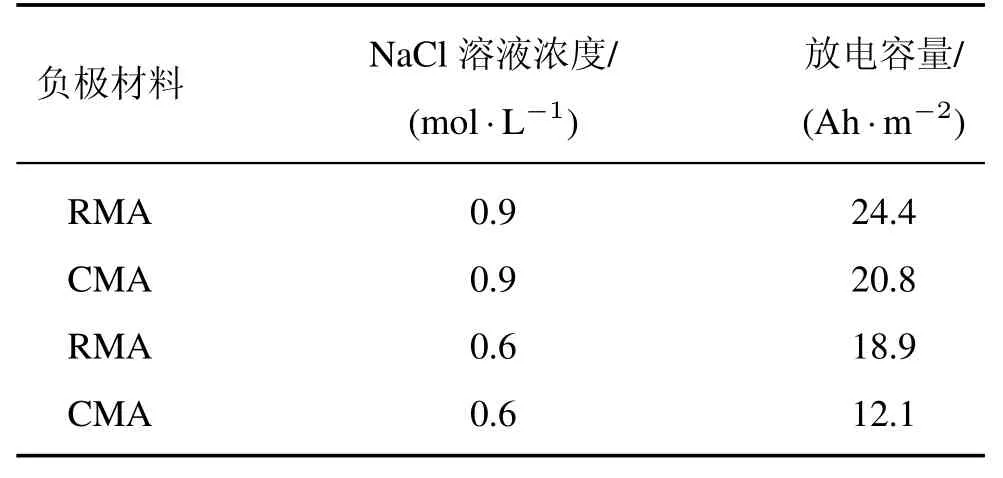
表4 RMA和CMA在NaCl电解质溶液中的放电容量Tab.4 Discharge capacity of RMA and CMA in NaCl electrolyte solutions
3 结论
利用熔炼工艺和废旧镁合金型材,按照AZ31合金组分范围制备了RMA。研究了RMA的结构及其在NaCl电解质溶液中的腐蚀和电化学特性,并与CMA进行了对比。
(1)RMA与CMA具有相似的晶体结构特征,并且两者物相组成相似,都是由相和相组成。OM观察显示,RMA中相数量略多于CMA。
(2)RMA的抗腐蚀特性低于CMA,表现为前者的腐蚀速率较快,腐蚀电流密度较大和较低的EIS。当电解质溶液浓度从0.6 mol/L增加至0.9 mol/L时,RMA和CMA的抗腐蚀特性均降低。
(3)两种合金作为镁电池负极材料的放电特性实验表明,RMA的放电特性优于CMA。并且,当电解质溶液浓度从0.6 mol/L增加至0.9 mol/L时,有利于增加材料的放电容量和延长放电时间。

