FOLFOX方案与XELOX方案治疗中晚期结肠癌患者疗效和安全性的meta分析
陈进宝,邱艳艳,徐 可,贺 雪,吴宏磊,曾亦军,殷佩浩
上海中医药大学附属普陀医院普外科,上海 200062
结肠癌(colon cancer)作为常见的恶性肿瘤之一,其发病率仅低于肺癌与胃癌,常见于中老年人群,且发病人群的年龄逐渐年轻化,严重威胁着人类身心健康[1]。目前,结肠癌的治疗主要是一种以手术治疗为主,放化疗、生物治疗、靶向治疗以及中医药治疗为辅的综合治疗。现阶段,手术仍然是根治结肠癌的主要手段,而Ⅱ/Ⅲ期结肠癌患者往往有微小转移灶的存在,手术不能彻底清除,术后出现病灶转移、复发的可能性较高。因此,术后的有效化疗是结肠癌患者获得长期生存的必要条件。临床实践发现,针对Ⅱ/Ⅲ期结肠癌患者应用全身辅助化疗杀灭远处潜在的微小转移灶的同时可杀死血液中残留的微小转移灶,能够降低病灶转移和复发的概率,提高治疗效果、延长无病生存期,具有较高的应用价值[2-5]。目前,5-氟尿嘧啶(5-FU)/甲酸四氢叶酸(LV)联合奥沙利铂(OXA)组成的FOLFOX方案与卡培他滨(CAP)联合OXA组成的XELOX方案被广泛用于Ⅱ/Ⅲ期结肠癌辅助化疗中。虽然化疗在肠癌复发和转移方面发挥着重要作用,但是化疗也常常带来许多不良反应,如神经毒性、胃肠道反应、骨髓抑制以及免疫抑制等[6]。本研究主要对已发表的有关FOLFOX方案与XELOX方案治疗结肠癌的临床试验,采用RevMan 5.3软件进行评估,为中晚期结肠癌的治疗提供一定的循证医学证据以及相关研究思路。
1 资料与方法
1.1 文献来源与检索
通过检索中国知网、中国生物医学文摘数据库、维普数据库、万方数据以及PubMed数据库,下载有关FOLFOX方案与XELOX方案治疗中晚期结肠癌患者疗效与安全性的随机对照临床研究。中文检索词:FOLFOX方案、XELOX方案、奥沙利铂、氟尿嘧啶、卡培他滨、结肠癌;英文检索词:FOLFOX, XELOX, oxaliplatin, 5-fluorouracil, capecitabine, colon cancer, colonic neoplasm, sigmoid neoplasm。检索时间为各数据库建库至2019年3月。检索条件:题名、主题词、关键词。
1.2 纳入标准与剔除标准
1.2.1 纳入标准 (1)纳入文献类型:要符合随机对照临床研究,任何评论、综述、指南类文章均未纳入。(2)研究对象:中晚期结肠癌患者。(3)研究内容:FOLFOX方案与XELOX方案治疗中晚期结肠癌术后患者疗效及安全性比较。(4)两组组间均衡性较好,具有一定的可比性。(5)患者治疗后疗效评定符合公认的疗效评定标准。
1.2.2 剔除标准 (1)非随机临床对照研究。(2)研究对象非中晚期结肠癌术后患者。(3)治疗组或对照组含研究以外的联用药物(可能对结果有重要影响)。(4)试验数据有一定缺漏和错误、病例资料相对不完整。
1.3 干预措施
治疗组主要是FOLFOX方案:5-FU/LV+OXA;对照组则是XELOX方案:CAP+OXA 。
1.4 结局指标
结局指标:总体应答率、完全应答率、部分应答率、总体生存率、无病进展存活率、不良反应,按照世界卫生组织(WHO)毒性反应分级标准分为0~Ⅳ级。本研究主要探讨Ⅲ/Ⅳ级不良反应。
1.5 文献质量评价
本研究文献质量评价主要采用改良Jadad量表法,主要从随机序列的产生、随机化隐藏、盲法、退出和失访4个方面进行评价。其中1~3分为低质量文献,4~7分为高质量文献。如果产生分歧,则通过相互讨论或者由第三位研究者进行协助解决。
1.6 统计学分析
本研究采用RevMan 5.3软件进行分析。二分类变量指标选用相对危险度(RR),并计算95%可信区间(95% CI)表示,当P<0.05时认为组间差异明显。采用χ2检验分析考察异质性情况,并主要用I2来评价异质性大小。检验结果P>0.1,且I2<50%时,采用固定效应模型,否则采用随机效应模型。若研究过程中存在疗程、剂量等临床或方法学异质性,则需要采用亚组分析或敏感性分析。另外,如果纳入的研究满足了一定的数量,则需要对潜在的发表偏倚进行漏斗图分析。
2 结果
2.1 检索及筛选结果
我们初步检索得到文献136篇,通过阅读标题,排除不相关文献60篇,重复32篇及综述11篇,之后精读文献,剔除联合其他药物实验10篇,剔除同源或无数据文献5篇、剔除非治疗效果(成本分析)比较以及不存在相关结局指标比较6篇,最终纳入了文献12篇[7-18]。主要包括1 614例结肠癌患者,其中FOLFOX组801例,XELOX组813例。文献检索的流程见图1。
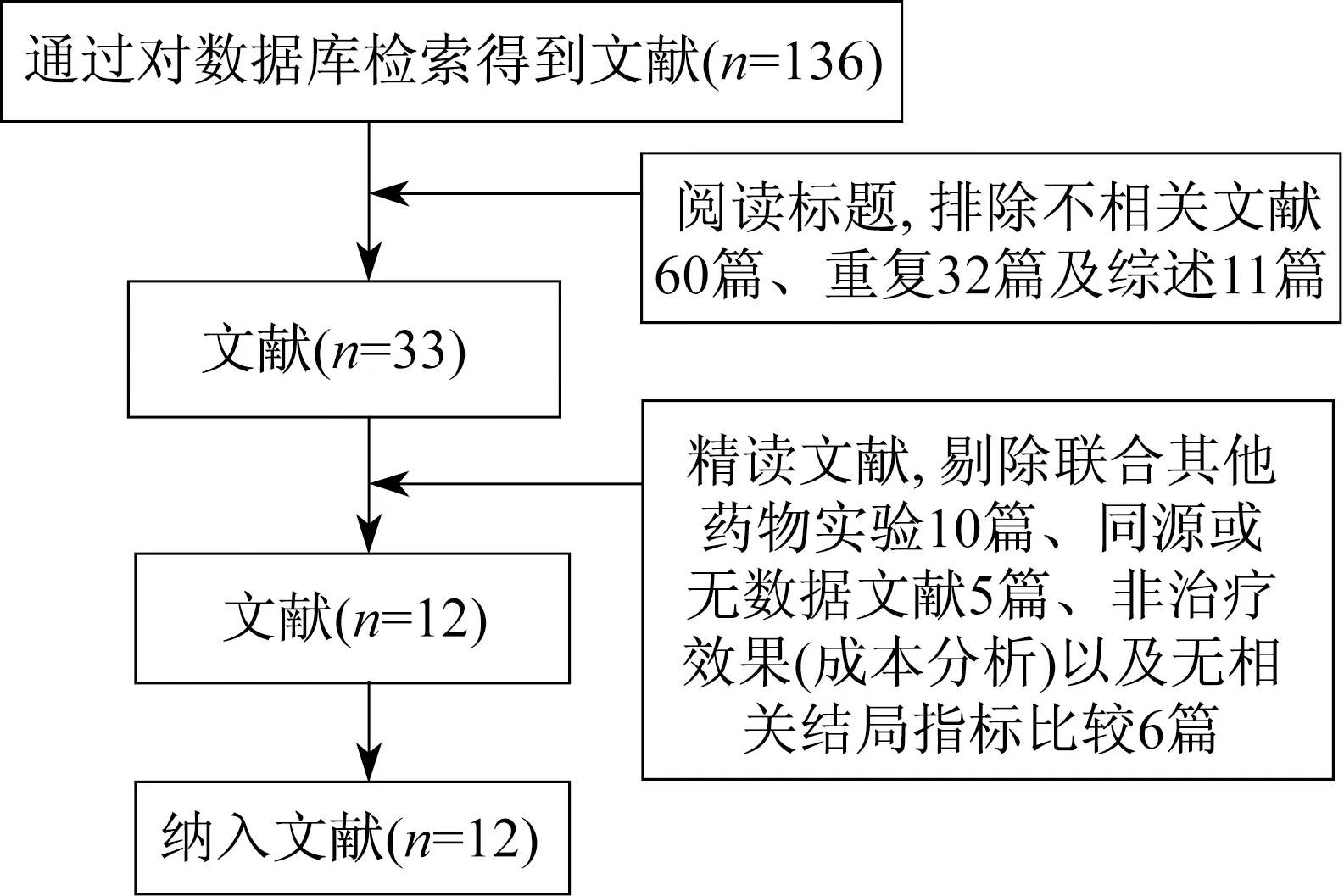
图1 文献检索流程及结果

表1 纳入文献一般情况
续表1

作者 年份病例数(FOLFOX组/XELOX组)干预措施FOLFOX组XELOX组结局指标Jadad评分杨兰[13] 201448/475-FU、LV 联合OXA方案化疗,OXA 85 mg·m-2,iv gtt, LV 200 mg·m-2,第1~2天,iv gtt 2 h后+ 5-FU 400 mg·m-2,静脉推注,后续600 mg·m-2持续iv gtt 22 h,第1~2天,2周重复,4周为1个疗程,共2个疗程CAP联合OXA方案化疗,CAP 1 000 mg·m-2,po,bid,1~14 d+ OXA 130 mg·m-2,iv gtt,第1天;3周重复,为1个疗程,共2个疗程①②③1陈倩雅[14] 201767/67第1天,OXA注射液 iv,130 mg·m-2,注射用LV 200 mg·m-2,第1~2天,注射用5-FU1.2 mg·m-2,持续iv 48 h,总量2.4 g·m-2,每2周为1个周期,连续治疗12个周期第一天OXA注射液iv,130 mg·m-2,CAP 1.0 g·m-2,bid,po,连续应用2周,每3周为1个周期,连续治疗8个周期④⑤⑥4马妮娜[15] 201440/40LV iv gtt,5-FU,第1天,300 mg·m-2;5-FU 静脉推注,第1天,400 mg·m-2,2 400 mg·m-2 iv gtt 46 h; OXA iv gtt,第1天,持续3 h,100 mg·m-2。14 d为1个治疗周期CAP餐后30 min p.o,bid,100 mg·m-2,第1~14天;OXA iv gtt,第1天持续3 h,130 mg·m-2。21 d为1个治疗周期①②③⑥0苏雪清[16] 201330/27治疗第1天静脉滴注85 mg·m-2 OXA;在第1-2天iv gtt 200 mg·m-2LV,2 h后,对患者静脉推注400 mg·m-25-FU,之后持续22 h iv gtt 600 mg·m-2 5-FU,每2周重复,以4周为1个治疗周期治疗第1天iv gtt 85 mg·m-2 OXA;在第1~2天iv gtt 200 mg·m-2LV,2 h后,对患者静脉推注400 mg·m-25-FU,之后持续22 h ivgtt 600 mg·m-2 5-FU,每2周重复,以4周为1个治疗周期①②③⑥2孙雅萌[18] 2014103/112OXA 85 mg·m-2,iv gtt 2 h,第1天,LV 200 mg·m-2 iv,第1-2天,5-FU 400 mg·m-2iv,然后600 mg·m-2持续iv gtt 22 h,第1、2天,每2周为1个周期,共12周期OXA 130 mg·m-2,iv gtt,第1天,CAP 1 000 mg·m-2从第1天晚上到第15天早晨,po,bid,休息7 d,每3周为1个周期,共8周期④⑥0潘海燕[17] 201626/29OXA 130 mg·m-2 iv gtt 2 h,第1天;LV 200 mg·m-2静脉输注2 h,第1~5天;5-FU 500 mg·m-2iv gtt 4~6 h,第1~5天,21 d为1个周期,共2个周期以上CAP 1 000 mg·m-2,po,bid,第1~14天;OXA 130 mg·m-2,iv gtt,第1天;21 d为1个周期,共2个周期上⑥1Comella[7] 2009164/158CAP1 000 mg·m-2,po,bid,第1~11天;OXA 100 mg·m-2,iv,2 h,第1天(2周1次,12个周期)OXA 85 mg·m-2,iv,2 h,第1天;LV 250 mg·m-2,iv,2 h,第1~2天;5-FU 850 mg·m-2,iv,第2天(2周1次,12个周期)①②③④⑤⑥1
2.2 纳入研究的基本特征
纳入研究的基本特征见表1。其中结局指标:①代表总体应答率;②代表完全应答率;③代表部分应答率;④代表总体生存率;⑤代表无病进展存活率;⑥代表不良反应。
2.3 纳入研究的质量评价
所选文献采用Jadad改良7分法进行质量评价,评分结果见表1。
2.4 Meta分析结果
2.4.1 总体应答率 总共有8篇文献[7-10,12-13,15-16]报道了总体应答率,8个研究之间无统计学异质性(P=0.92,I2=0%),需选用固定效应模型分析,结果显示两种方案在总体应答率方面差异无统计学意义(RR=1.01,95%CI 0.90~1.13,P=0.91),见图2。
2.4.2 完全应答率 共有8篇文献[7-10,12-13,15-16]报道了完全应答率,各个研究之间无统计学异质性(P=0.93,I2=0%),选用固定效应模型分析,结果显示两种方案在完全应答率方面差异无统计学意义(RR=0.85,95%CI 0.63~1.13,P=0.27),见图3。
2.4.3 部分应答率 总共有8篇文献[7-10,12-13,15-16]报道了部分应答率,各个研究之间均无统计学异质性(P=0.90,I2=0%),因此选用固定效应模型进行分析,研究结果显示两种方案在部分应答率方面差异无统计学意义(RR=1.06,95%CI 0.92~1.24,P=0.42),见图4。
2.4.4 总体生存率 共有5篇文献[7-8,11,14,18]报道了总体生存率,几个研究之间无统计学异质性(P=0.98,I2=0%),选用固定效应模型进行分析,结果显示两种方案在总体生存率方面差异无统计学意义(RR=1.01,95%CI 0.93~1.09,P=0.82),见图5。
专名屈折变化之非本真性的意义在于殊相相对于语言的独立性:虽然我们对语言的不同使用方式创造了各种不同的对象,然而在某种意义上,殊相可以被视为语言不得不原封不动地接纳的前语言“自在客体”,而作为其语言上的对应物,本真专名在充当句子之专名时在很多语言中都不经历变化。
2.4.5 无病进展存活率 总共4篇文献[7-8,11,14]报道了无病进展存活率,各研究之间无统计学异质性(P=0.16,I2=42%),采用固定效应模型分析显示,两种方案在无病进展存活率方面差异无统计学意义(RR=1.00,95%CI 0.94~1.06,P=0.99),见图6。
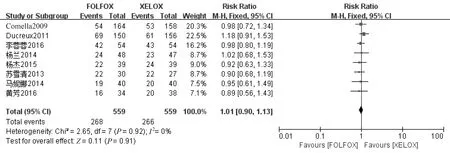
图2 总体应答率meta分析
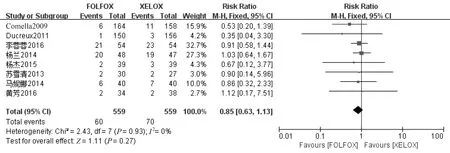
图3 完全应答率meta分析
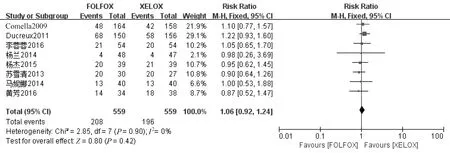
图4 部分应答率meta分析

图5 总体生存率meta分析
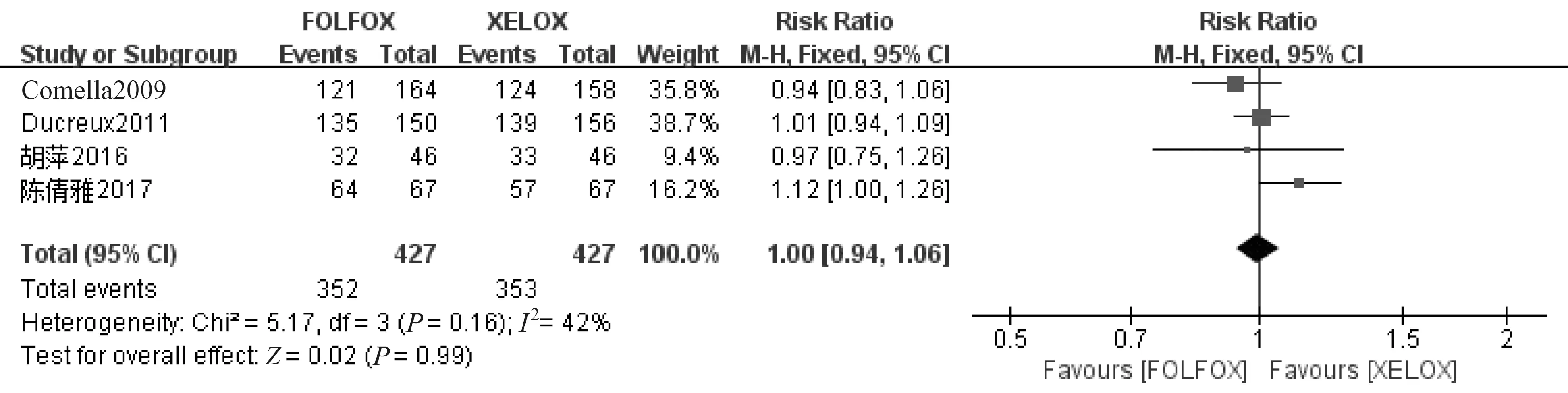
图6 无病进展存活率meta分析
2.4.6 安全性(不良反应) 所有文献均提供了患者出现的一系列不良反应的数据,本文主要比较了Ⅲ/Ⅳ级不良反应的发生率。总共有8篇文献[7-10,13,15-17]报道了患者治疗期间Ⅲ级以上不良反应发生情况,此次meta分析结果显示XELOX方案的手足综合征发生率高于FOLFOX方案(RR=0.20,95%CI 0.08~0.51,P=0.000 8);而中性粒细胞减少症的发生率低于FOLFOX方案(RR=5.05,95%CI 1.76~14.53,P=0.003);此外Ⅲ/Ⅳ级腹泻 (P=0.05)在两种方案中可能存在显著性差异,也可能不存在显著差异,因此可以在以后的研究中扩大样本量进一步求证。两种方案的其他不良反应发生率相似(如白细胞减少症、周围神经病变等),研究发现无显著性差异,结果见图7~15、表2。
2.4.7 敏感性分析 经过分析显示,在纳入研究的12篇文献中均没有采用随机化隐藏、盲法及撤出与退出情况,Jadad评分显示大多为低质量文献,故未进行低质量研究的敏感性分析。
2.4.8 文献发表偏倚评价 用漏斗图衡量文献的发表偏倚,选取总体应答率、完全应答率以及部分应答率指标进行“倒漏斗图”分析来衡量文献的发表偏倚。结果发现,“倒漏斗图”的分布均在区间的范围内,但图中的点在中线两侧的分布数量并不对称,提示本次纳入的研究可能存在一定的发表偏倚,也可能存在未发表阴性结果的研究等原因。见图16~18。
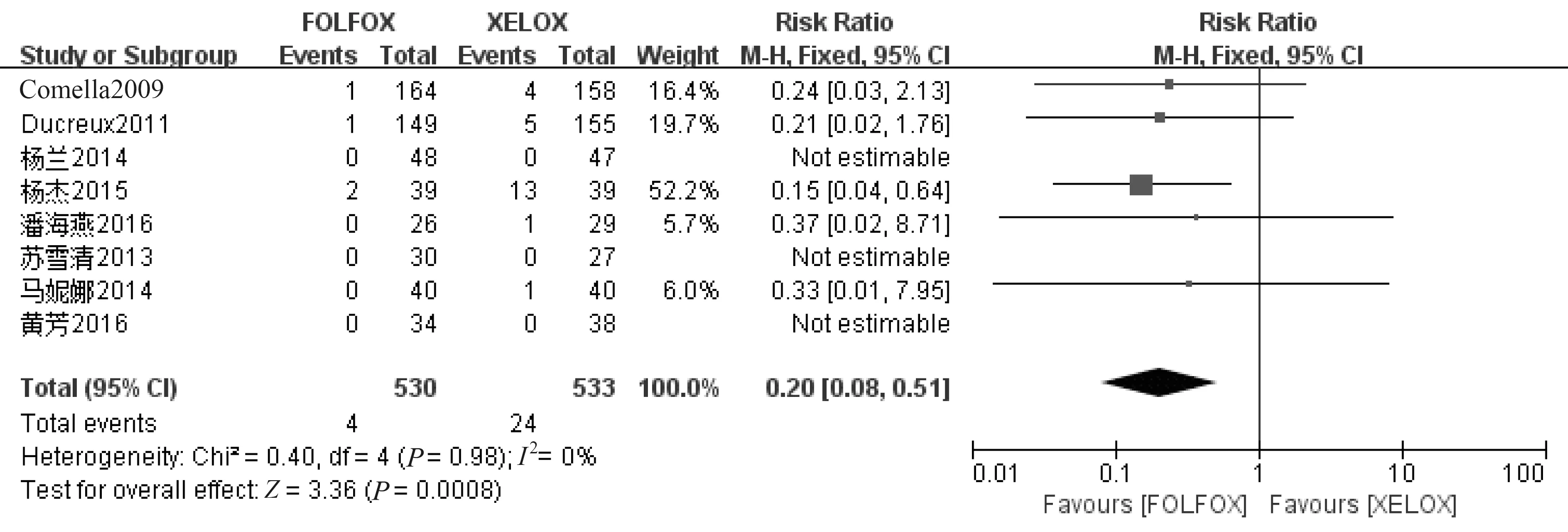
图7 手足综合征的meta分析

图8 中性粒细胞减少症的meta分析

图9 周围神经病变的meta分析

图10 白细胞减少症的meta分析
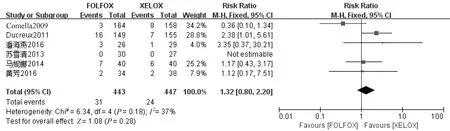
图11 恶心呕吐的meta分析
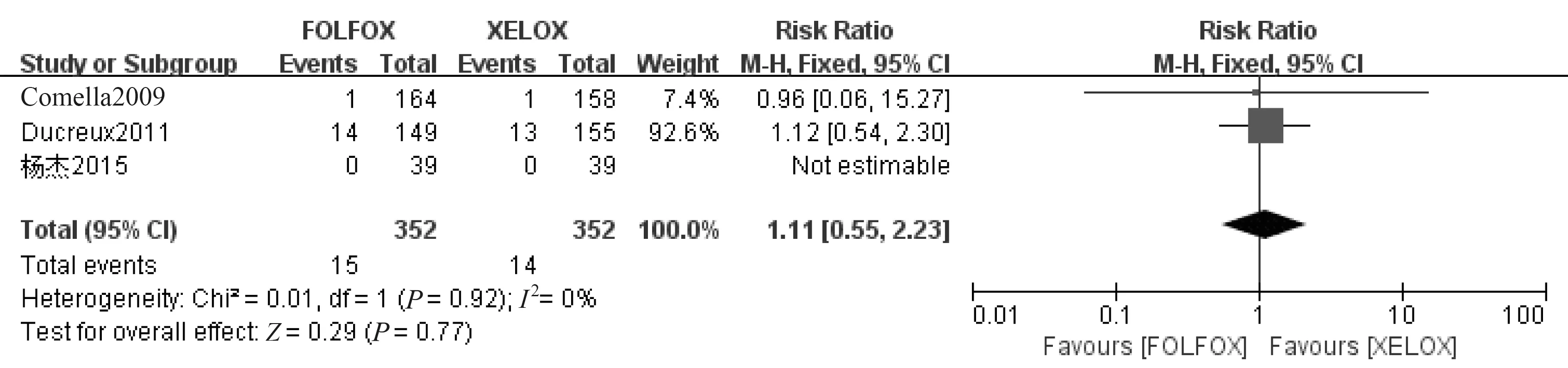
图12 乏力的meta分析
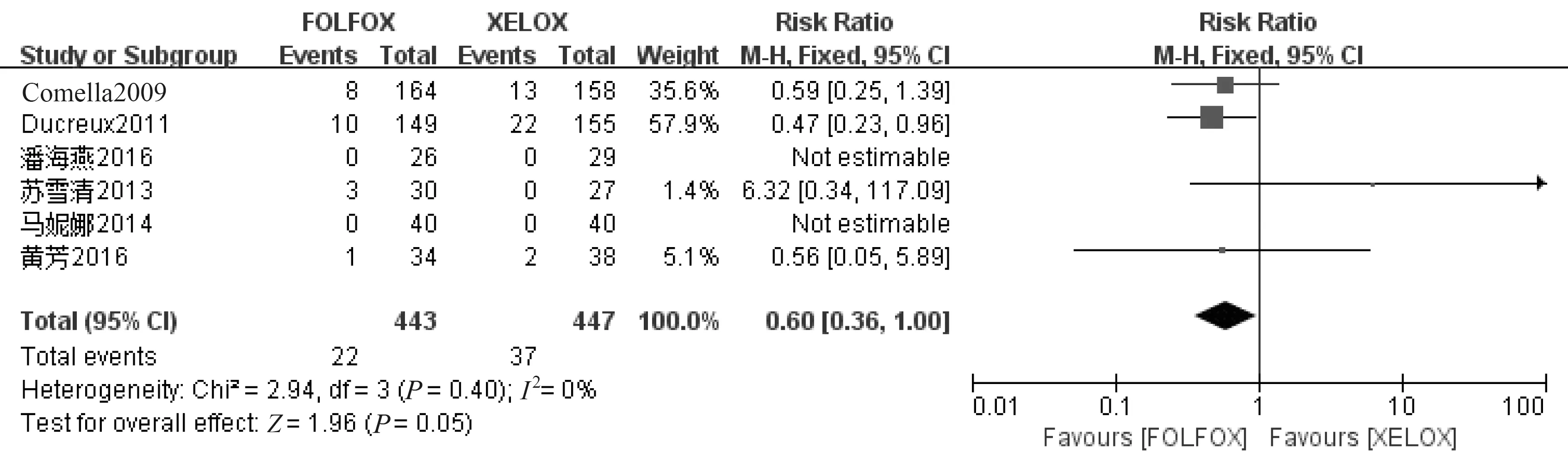
图13 腹泻的meta分析

图14 贫血的meta分析

图15 血小板减少症的meta分析

不良反应纳入研究个数FOLFOX组(n/N)XELOX组(n/N)统计模型RR(95%CI)P值手足综合征84/53024/533固定效应模型0.20(0.08~0.51)0.0008中性粒细胞减少症4100/39218/392随机效应模型5.05(1.76~14.53)0.003周围神经病变748/49132/494随机效应模型1.13(0.47~2.72)0.79白细胞减少症49/1475/153固定效应模型1.88(0.68~5.17)0.22恶心呕吐631/44324/447固定效应模型1.32(0.80~2.20)0.28乏力315/35214/352固定效应模型1.11(0.55~2.23)0.77腹泻622/44337/447固定效应模型0.60(0.36~1.00)0.05贫血49/3957/398固定效应模型1.29(0.50~3.33)0.59血小板减少症713/50023/506固定效应模型0.59(0.31~1.13)0.11
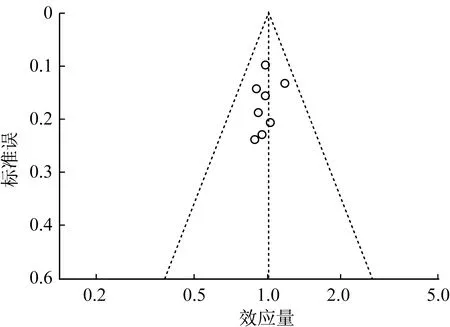
图16 总体应答率文献发表偏倚漏斗图
3 讨论
目前,5-FU/LV联合OXA组成的FOLFOX方案与卡培他滨(CAP)联合奥沙利铂(OXA)组成的XELOX方案被广泛用于Ⅱ/Ⅲ期结肠癌辅助化疗中。虽然化疗在结肠癌复发和转移方面发挥着重要作用,但是化疗也常常带来许多不良反应,如神经毒性、胃肠道反应、骨髓抑制以及免疫抑制等。Meta分析可以解决一些研究结果的不一致性,它主要是通过增加样本的含量进而增加结论的可信性。本研究主要收集目前已发表的有关FOLFOX方案与XELOX方案治疗结肠癌方面的临床试验,主要针对这两种方案的利弊进行meta分析,旨在为中晚期结肠癌的治疗提供循证医学证据。
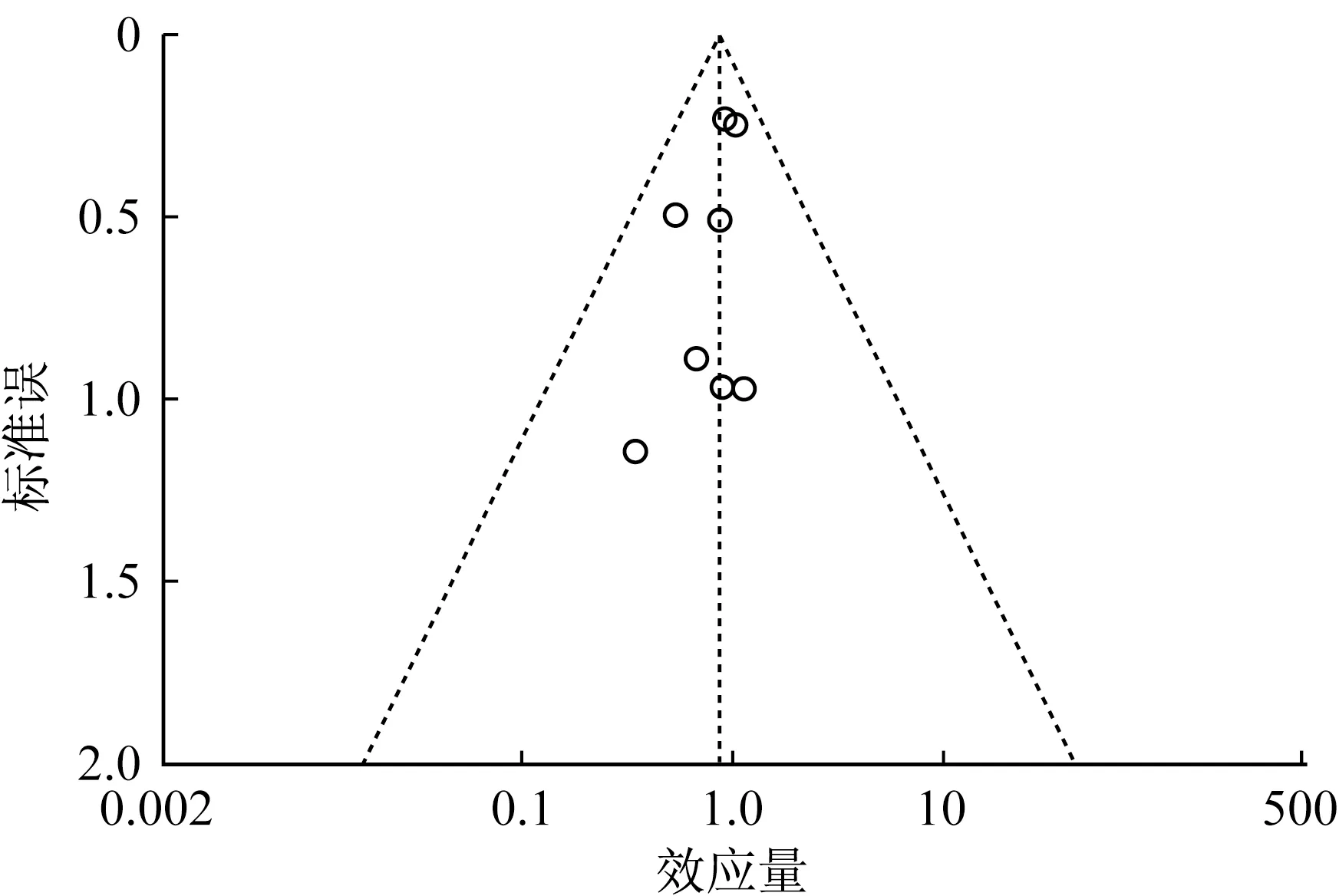
图17 完全应答率文献发表偏倚漏斗图

图18 部分应答率文献发表偏倚漏斗图
3.1 有效性分析
本次研究结果显示,两种方案在完全应答率、总体应答率、部分应答率、无病进展存活率以及总体生存率方面差异均无统计学意义,FOLFOX方案与XELOX方案在治疗中晚期结肠癌方面可以取得较为相似的疗效。
3.2 安全性分析
不良反应的分析结果显示,XELOX方案造成的患者Ⅲ/Ⅳ级手足综合征发生率要高于FOLFOX方案,而FOLFOX 方案导致的Ⅲ/Ⅳ级中性粒细胞减少症的发生率高于XELOX方案。另外,Ⅲ/Ⅳ级腹泻(P=0.05)在两种方案中可能存在显著性差异,也可能是无显性著差异,因此可以在以后的研究中扩大样本量进一步求证。而在Ⅲ/Ⅳ级血小板减少症、贫血、腹泻、 恶心呕吐、白细胞减少症以及周围神经病变方面FOLFOX方案与XELOX方案未表现出显著性差异。
3.3 研究局限
本次研究总共纳入了12篇文献,仅有4篇文献[8,10,12,14]具体描述了随机方法,其余均未对所用随机方法进行具体描述;另外,纳入文献均未描述分配隐藏的实施与否,提示研究可能具有一定选择性偏倚;所有纳入文献[7-18]均未提到是否采用了盲法,提示本次纳入的研究可能存在一定的实施偏倚;此外,3篇文献[8,14,16]对患者退出/失访原因进行了描述,而其余研究均并未作出情况说明,提示可能存在测量偏倚。本研究主要使用改良Jadad评分对纳入文献进行质量评价,其中2篇文献[8,14]评分为4分,属于高质量研究,其余评分均不高于3分,属于低质量研究。另外,本次研究所涉及到的两种方案的用药剂量和具体使用情况并不完全一致,疗效可能受到一定程度的影响。
综上所述,FOLFOX方案与XELOX方案在治疗中晚期结肠癌方面的疗效相似,但需要特别注意FOLFOX方案具有较易发生Ⅲ/Ⅳ级中性粒细胞减少症的风险,而采用XELOX方案的患者具有更易发生Ⅲ/Ⅳ级手足综合征的风险。

