血压变异干预策略对高血压脑白质疏松、预后卒中及认知的影响
方立,袁学谦,张莉峰,尹所,滕军放
(郑州人民医院 1.神经内科二病区,2.影像科,河南 郑州 450003;3.郑州大学第一附属医院 神经内科,河南 郑州 450052)
脑白质疏松症(Leukoaraiosis,LA),也称为脑白质高信号(white matter hyperintensities,WMHs),多见于高血压病患者[1]。可增加痴呆、卒中等的发病率及病死率[1]。研究发现,血压变异性(blood pressure variablility,BPV)及昼夜血压节律紊乱(如非杓型)可能是较收缩压更强的LA 进展危险因素[3]。收缩压变异性独立于收缩压,与认知功能障碍相关[4]。通常用血压标准差(standard deviation SD)、变异系数(variation coefficien CV)来反映血压随着时间的推移所发生的变异性,即BPV。创新和发展新的药物,改善动脉僵硬度,可抑制脑小血管疾病的进展[5]。一些抗高血压药物预防中风的作用机制中可能部分是由于减少BPV[6]。以上研究多见于国外报道,国内鲜有报道。本研究通过分析LA 与BPV 关系,进而提前采取干预策略影响BPV,以观察和证实对LA 病变进展以及卒中血管事件和认知功能的影响,并分析其机制。
1 资料与方法
1.1 研究对象
选取2013年1月—2016年12月郑州人民医院确诊的资料完整的高血压患者275 例,其中不配合回访2 例,拒绝单药治疗而退出试验4 例,最终纳入统计分析269 例。同意1年内单药治疗高血压的患者180 例。将269 例患者分为无或轻度LA 组(111 例)和中重度LA 组(158 例)。
1.2 诊断及排除标准
所有患者均符合世界卫生组织和国际高血压联盟(WHO/ISH,1999年)高血压诊断标准,认知能力无缺陷,能完成量表测评。排除标准:①影像学检查排除皮层或皮层下梗死、脑出血、蛛网膜下腔出血、硬膜内外血肿等;②存在各种明确病因导致的脑白质病变,如一氧化碳中毒、缺氧性脑白质病、多发性硬化等;③心肝肾衰竭者或肿瘤转移;焦虑症、抑郁症,或正在服用抗焦虑、抗抑郁类药物;④不能配合完成量表测评者。
1.3 方法
1.3.1 流行病学调查问卷调查包括人口学资料、吸烟史、饮酒史、糖尿病、冠状动脉粥样硬化性心脏病(以下简称冠心病)、卒中史、高血压等脑血管危险因素。
1.3.2 生化指标检测入院次日晨起空腹抽取肘静脉血5 ml,分离并提取血清用于生化指标的检测。生化指标的检测采用日本日立公司的7600 型自动生化分析仪,实验室指标包括血糖、血脂、同型半胱氨酸、肝功能、肾功能、碱性磷酸酶、尿常规初筛尿蛋白等。
1.3.3 卒中事件统计首次入院后根据服药习惯,分为单药治疗氨氯地平组、依那普利组、普萘洛尔组和未用药组。同时,在药物剂量允许范围内,2 周内调整血压至140/90 mmHg 内;随访1年,统计患者单药治疗期间是否发生卒中事件(包括缺血性和出血性卒中)。
1.3.4 认知功能的评价首次入院后第1 天及1年后复诊随访均采用简明精神状态量表(mini-mental state examination,MMSE)[7],对研究对象进行认知功能状态的评分。其主要包括7 个方面:时间向力、地点向力、即刻记忆、注意力及计算力、延迟记忆、语言及视空间。共30 题,每项正确回答得1 分,回答错误或不知道得0 分,量表总分范围为0 ~30 分。该量表的最终评分均由专人计算汇总。
1.3.5 BPV 计算首次入院时及复诊随访均行动态血压监测。采用Tele.ABP 型动脉血压监测仪。在血压监测过程中嘱患者尽量避免剧烈运动,以轻体力或安静状态为主,自动测压时保持静止,放松上臂并使之保持与心脏在同一水平。首次入院后降压药物暂不调整,继续既往服药习惯、服药种类及剂量;除非收缩压(systolic blood pressure SBP)≥220 mmHg 或者舒张压≥120 mmHg。因高血压患者多是以SBP 增高为主,因此以SBP 为指标,计算CV 及SD。根据夜间血压下降百分率的幅度分为:非杓型血压(<10%或>20%)和杓型血压(10%~20%)[8]。
1.3.6 入院时及1年后随访复诊均采用德国西门子3.0 T 超导MR 扫描仪行颅脑T1WI、T2WI、FLARE、MRA、DWI 序列(b 值=1 000s/ram2)扫描。由2 位不知晓临床资料的影像科高年资医师观察MR 结果并评分。根据FAZEKAS 量表[9]对LA 严重程度进行评分。评分0 ~3 分为无或轻度组,量表评分> 3 分为中重度组。最低分0 分,最高分6 分。
1.4 统计学方法
数据分析采用SPSS 19.0 统计软件。计量资料以均数±标准差(±s)表示,满足正态分布的两组间比较采用t检验,多组间比较采用方差分析,在方差分析有意义的基础上,两两比较采用LSD-t检验,计数资料以例(%)表示,组间比较应用Fisher 确切概率法,并用Bonferroni 法校正检验水平,采用多因素Logistic 回归模型计算LA 的影响因素及值。多组计数资料间的比较以双侧P<0.0167 为差异有统计学意义,余均以双侧P<0.05 为差异有统计学意义。
2 结果
2.1 基本情况
无或轻度脑白质疏松患者111 例。其中,男性60 例,女性51 例,中位年龄57 岁;中重度脑白质疏松患者158 例。其中,男性83 例,女性75 例,中位年龄68 岁。中重度LA 患者中,高CV 者132 例,占45.57%;高SD 者100 例,占63.30%;非杓型特点者82 例,占84.81%;应用单一降压药物者180 例。氨氯地平组84 例,其中中重度LA 11 例,占13.11%;依那普利组60 例,其中中重度LA 20 例,占33.33%;美托洛尔组36 例,其中中重度LA 32 例,占88.89%。
2.2 两组患者一般资料的比较
两组患者比较,年龄、卒中史、冠心病史、糖尿病史、24 h SBP 分级、高CV、高SD、非杓型之间比较,差异有统计学意义(P<0.05)。见表1。

表1 两组患者一般资料的比较 例(%)
2.3 多因素Logistic 回归分析
将年龄、卒中史、糖尿病史、冠心病史、24 h SBP分级、CV、SD、杓型分型等变量纳入Logistic 回归分析,采用逐步向前法,结果显示,24 h SBP 分级、高SD、非杓型、糖尿病史、卒中史、年龄均为LA 的独立危险因素(P<0.05)。其中,高SD 患者的LA 风险升高2.168 倍。非杓型患者LA 风险升高2.764 倍。见表2。
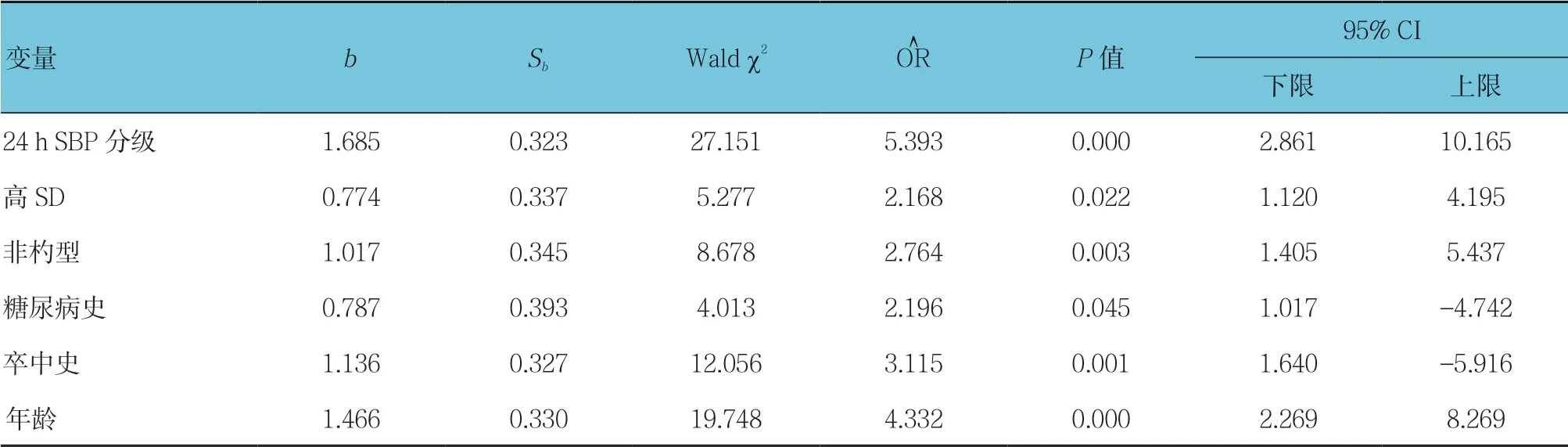
表2 多因素Logistic 回归分析参数
2.4 随访及卒中事件
1年后随访,发现氨氯地平组的中重度LA 比例13.1%,低于依那普利组33.33%与美托洛尔组88.89%,组间比较,差异有统计学意义(P<0.0167);氨氯地平组的卒中事件发生率30.95%,低于依那普利组51.67%与美托洛尔组63.89%,组间比较,差异有统计学意义(P<0.0167)。见表3。
2.5 随访BPV 与MMSE 评分
首次入院时氨氯地平、依那普利、美托洛尔3 组间的BPV、MMSE 评分比较,差异无统计学意义(P> 0.05);1年后随访发现氨氯地平组的BPV 降低明显,而依那普利组与美托洛尔组的BPV 均升高,组间比较,差异有统计学意义(P<0.05);用药后,依那普利组与美托洛尔组的MMSE 评分降低,而氨氯地平组的MMSE 评分降低不明显,组间比较,差异有统计学意义(P<0.05)。见表4。
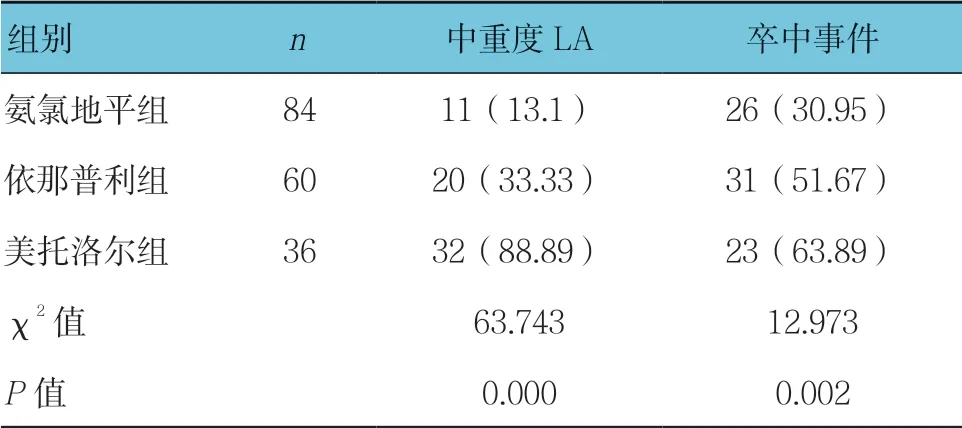
表3 不同降压药物应用后LA 及卒中事件比较 例(%)
表4 不同降压药物应用后BPV 及MMSE 评分 (±s)
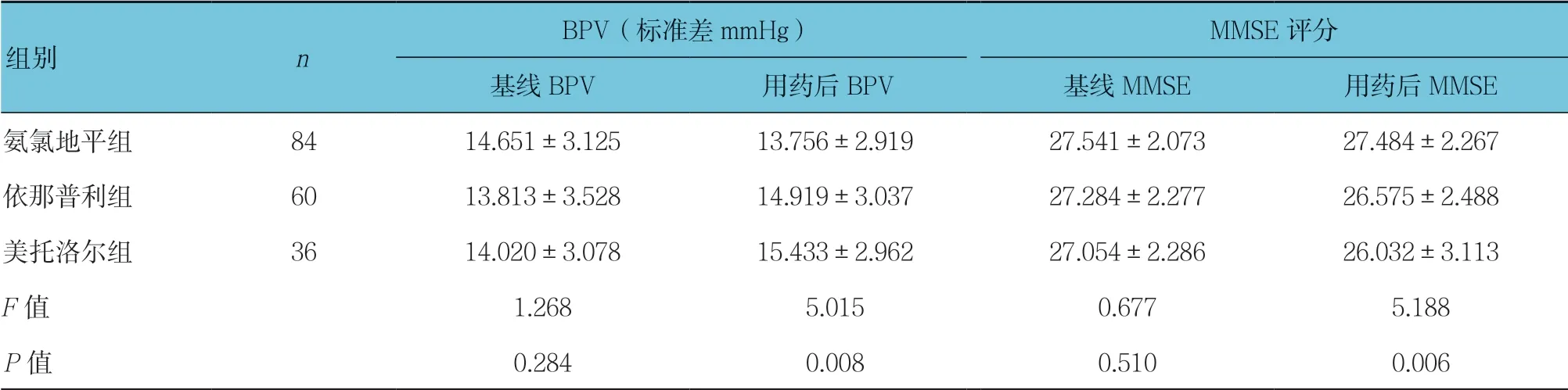
表4 不同降压药物应用后BPV 及MMSE 评分 (±s)
BPV(标准差mmHg)MMSE 评分基线BPV 用药后BPV 基线MMSE 用药后MMSE氨氯地平组 84 14.651±3.125 13.756±2.919 27.541±2.073 27.484±2.267依那普利组 60 13.813±3.528 14.919±3.037 27.284±2.277 26.575±2.488美托洛尔组 36 14.020±3.078 15.433±2.962 27.054±2.286 26.032±3.113F值 1.268 5.015 0.677 5.188P值 0.284 0.008 0.510 0.006组别 n
3 讨论
JOSEFINA 等[10]发现平均收缩压变异性与WMH进展程度相关。本研究显示,高血压患者的收缩压变异性与LA 相关;且收缩压CV 及标准差为影响LA进展独立危险因素。高血压可导致动脉硬化。研究发现动脉粥样硬化能够导致脑白质血管发生透明样变性,加重脑白质血流动力学障碍[11]。SLOTEN 等[12]研究发现,动脉硬化可导致脉动压力和血压变异性增加。由于大脑微循环的特点是低阻抗,使脉动负载压力深入其微血管床,进而损伤微循环。在大脑中,微循环损伤特征性表现即WMHs。
研究指出昼夜血压节律紊乱是较夜间收缩压更强的LA 危险因素[3]。本研究发现,非杓型血压也是LA 的独立危险因素。超杓型血压患者可因血压大幅度波动引起脑实质内小血管调节功能丧失,从而无法应对夜间显著的血压降低,造成脑白质区脑血流量下降出现慢性缺血的改变[13]。
WEBB 等[14]发现BPV 与卒中复发风险高度相关,是其独立影响因素。ASCOT-BPLA 试验纳入19 257 例高血压患者,发现BPV 与脑卒中风险呈正相关,且以氨氯地平为主的治疗方案能显著减少心脑血管病[15]。WEBB 等[16]发现ACEI 类药物未减少BPV。GORELICK等[17]指出,钙离子拮抗剂和β 受体阻滞剂在降低卒中方面差异主要基于两者对BPV 作用效果不同。WIJSMAN 等[18]发现,钙离子拮抗剂应用者认知功能改善明显,而ACEI 和β 受体阻滞剂应用者的认知功能减退明显本研究发现,较之依那普利和美托洛尔,氨氯地平能明显降低BPV,延缓LA 及其预后认知障碍的发生,并减少卒中发生。
对钙离子拮抗剂预防LA、痴呆与卒中机制的研究。O'ROURKE 等[9]发现,重复脉动引起中心动脉弹力层疲劳并断裂进而动脉硬化,脉动影响进一步延伸到脑小血管,导致对脑实质损伤。而BPV 增高时,反复剧烈的血压波动可导致上述变化进一步加重。由于动脉粥样硬化引起的血管狭窄并发的动脉僵硬度增加可以加速脉冲波。脉动压力或血压变异性会对脑实质产生“海啸效应”,导致脑小血管病变[5]。而脑小血管病明显增加痴呆发生率[2]。理想的降压药物降低血压的同时还应该降低BPV[17]。氨氯地平半衰期较长,能明显降低BPV,减少血压波动,且具有扩张脑动脉改善血管狭窄,增加供血作用,这可能是其效果明显的原因。
本研究的意义在于前瞻性的给予干预措施,探索不同降压方案对LA 预后的影响。探索不同降压药物改变BPV 的差异,以及对卒中和认知功能影响的差异为本研究提供新的预防和阻止LA 进展的策略,应用长效并能够减少BPV 的降压方案,可能更有利于阻止LA,预防可能发生的卒中及认知功能障碍。但缺陷是调查的样本量太小,及患者服药依从性未严格控制(可能存在间断漏服药物),以后还需多中心、大样本及更严格的实验控制来证实。

