磷石膏常压酸化法制备无水硫酸钙晶须的实验研究
谢 晴,蒋美雪,彭同江,2,国佳豪
(1.西南科技大学固体废物处理与资源化教育部重点实验室,绵阳 621010; 2.西南科技大学分析测试中心,绵阳 621010)
1 引 言
磷石膏是湿法磷酸生产过程中产生的固体废弃物,主要成分为二水硫酸钙(CaSO4·2H2O)。我国磷石膏堆存量已超过3亿吨,不仅占用大量土地,又对环境造成污染。资源化利用主要集中在石膏建材[1]、土壤改良剂[2]、水泥缓凝剂[3]、制取硫酸联产水泥[4]等方面,但由于产品附加值低、处理工艺能耗大等原因,磷石膏的综合利用率仅为10%~30%[5-6]。利用磷石膏制备无水硫酸钙晶须是高附加值利用的途径之一。
因结晶水含量的不同硫酸钙晶须可分为二水、半水和无水硫酸钙晶须,其制备方法主要有水热法和常压酸化法。二水硫酸钙晶须由于结晶水脱失温度较低限制了其应用;半水硫酸钙晶须极易水化为二水硫酸钙,可用作高强石膏原料;无水硫酸钙晶须性能稳定,晶体结构致密,力学性能优异[7-8],是一种绿色环保型增强材料[9-11]。经过表面改性后,无水硫酸钙晶须具有良好的促结晶作用,已有研究表明,无水硫酸钙晶须能够提高复合材料和PP的结晶速率、成核速率,起到异核相和的作用[12]。目前,无水硫酸钙晶须的制备一般采用水热-灼烧法,在水热条件下合成半水硫酸钙晶须,然后在600 ℃以上高温灼烧得到无水硫酸钙晶须[13]。秦军等[14]研究考察了磷石膏为原料,采用水热法制备硫酸钙晶须,反应温度、料浆初始pH、反应时间、料浆浓度及磷石膏粒度对生成硫酸钙晶须的影响。结果表明,在最佳反应条件下可制备出平均直径为2 μm,长径比为42的硫酸钙晶须产品。耿庆钰等[15]研究考察了磷石膏为原料,采用常压酸化法制备硫酸钙晶须,反应温度、料桨含固量、反应时间和盐酸质量分数对产物的影响。结果表明,在最佳反应条件下可制备出外观均匀、长径比达到138.46且纯度在99.8%以上的二水硫酸钙晶须产品。吕智慧等[16]研究考察了生石膏为原料,采用常压酸化法制备无水硫酸钙晶须,反应温度、反应时间、浓盐酸与水的体积比对产物的影响。结果表明,在最佳反应条件下可制备出长度为10~20 μm、直径为0.1~0.3 μm的无水硫酸钙晶须。但常压酸化法制备半水和无水硫酸钙晶须的研究在工业上更具实用性。
本文基于磷石膏的属性,采用常压酸化法一步合成无水硫酸钙晶须,并与其他可溶硫酸盐杂质分离开来。通过单因素条件实验,探究溶剂浓度、反应温度、反应时间以及固液比对硫酸钙晶须结晶形态的影响,并结合X射线物相分析、显微形貌分析等手段,从晶体生长的角度探索了制备条件对晶须属性的影响。
2 实 验
2.1 原料、试剂与装置
原料:磷石膏样品采自四川广元某磷酸生产厂家,外观呈粉状、灰黑色,经50 ℃干燥至恒重、研磨并经100目标准检验筛筛分后,密封保存在干燥器中备用,样品编号:P。
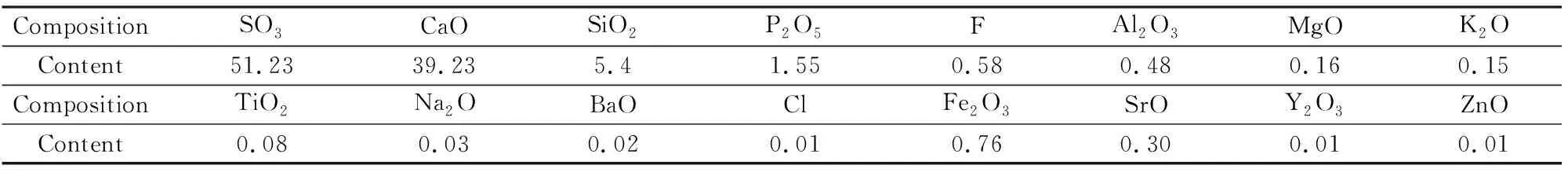
表1 磷石膏样品P的X射线荧光光谱化学成分分析结果Table 1 Chemical composition analysis of phosphogypsum sample P by X-ray fluorescence spectrometry /wt%

图1 磷石膏样品P的XRD图谱Fig.1 XRD pattern of phosphogypsum sample P
表1为磷石膏原料样品P的X射线荧光光谱化学成分分析结果。由表1,原料中主要组分SO3的质量分数为51.23%,CaO的质量分数为39.23%,二者质量分数之和为90.46%;次要组分包括SiO2、P2O5;含微量Fe2O3、F、Al2O3等。
图1为磷石膏样品P的XRD图谱。可以看出,原料中主要矿物相为石膏(CaSO4·2H2O),含少量石英(SiO2),未见其他成分的物相出现。
试剂:盐酸,质量分数36%~38%,分析纯(AR),购自成都科龙化工试剂厂;实验室自制去离子水,电阻率>18.2 MΩ·cm。
装置:101A-2型数显电热鼓风干燥箱,电子天平(精度0.1 mg,上海舜宇恒平科学仪器有限公司生产),DF-101S集热式恒温加热磁力搅拌器。

表2 实验方案Table 2 Text scheme
2.2 实验方案与步骤
采用单因素实验方法,参照文献[16]重点考察了盐酸浓度、反应温度、反应时间、固液比4个因素对磷石膏制备无水硫酸钙晶须的影响,以确定优化的工艺技术条件。具体实验方案如表2所示。
将磷石膏样品P与不同浓度的稀盐酸按设定的固液比(磷石膏质量和溶液体积之比)置于100 mL烧杯中混合均匀,形成灰黑色浆料,用磁力搅拌器搅拌升温至所设定的温度进行溶解,达到所设定的反应时间后,将灰白色的悬浊液趁热过滤,滤渣用蒸馏水洗涤3次,在烘箱中60 ℃下干燥12 h即得到晶须产物的样品。

图2 不同盐酸浓度下制备的晶须产物样品的XRD图谱Fig.2 XRD patterns of whisker product samples at different hydrochloric acid concentrations
2.3 样品测试
采用帕纳科Axios型X射线荧光光谱仪(XRF)对磷石膏样品进行化学成分分析,陶瓷X射线光管(Rh靶),分析元素范围为9F到92U,含量范围0.01~100%;采用帕纳科X'pertPRO型X射线衍射仪(XRD)对磷石膏样品和晶须产物样品进行物相分析,陶瓷X射线管,Cu靶;采用德国Carl zeissNTS GmbH公司的高分辨冷场发射扫描电子显微镜分析系统对晶须样品进行微观形貌分析,能谱分辨率优于127 eV(MnKα处);谱峰漂移<1 eV(MnKα处),电子背散射空间分辨率0.1 μm,角分辨率0.5度。
3 结果与讨论
3.1 盐酸浓度对产物物相和形貌的影响
图2为在不同盐酸浓度下获得的晶须产物样品的XRD图谱。分析可知,当盐酸浓度为3 mol/L时,产物主要物相为石膏(二水硫酸钙),此外还检测到较弱的硬石膏(无水硫酸钙)的特征峰和石英的特征峰。当盐酸浓度达到5 mol/L,产物为无水硫酸钙和少量石英,说明原料中二水硫酸钙已完全转化为无水硫酸钙。盐酸浓度为7 mol/L和9 mol/L时,产物为无水硫酸钙和少量石英。由于石英不溶于盐酸,因此原料中的石英在实验过程中没有产生变化。

图3 不同盐酸浓度下制备的晶须产物样品表面形貌Fig.3 Morphology of whisker product samples prepared at different hydrochloric acid concentrations (a)C=3 mol/L; (b)C=5 mol/L; (c)C=7 mol/L; (d)C=9 mol/L
图3为在不同盐酸浓度下获得的晶须产物样品的SEM照片。从图3a中可以看出,当盐酸溶液浓度为3 mol/L时,所形成的石膏样品的显微形貌呈板状、板条状,长径比为3~5。从图3b~3d,当盐酸浓度为5 mol/L、7 mol/L、9 mol/L时,所制备的硬石膏呈柱状、棒状或晶须状,对应样品的直径分别为1~3 μm、0.5~2 μm和0.2~3 μm,长径比分别为4~12、2~13和6~12,各样品大小分布较为均匀,长径比变化不明显,以盐酸浓度为7 mol/L时晶须的均匀性最好。因此,在较高盐酸浓度条件下可以制备长径比大、形貌均匀的无水硫酸钙晶须;而在较低盐酸浓度条件下制备的样品为长径比小、板状的二水硫酸钙晶须。
3.2 温度对产物物相和形貌的影响

图4 不同温度下制备的晶须产物样品的XRD图谱Fig.4 XRD patterns of whisker product samples at different temperatures
图4为在不同温度下制备的晶须产物样品的XRD图谱。分析可知,当温度为70 ℃时,产物主要为二水硫酸钙,没有新的物相生成;温度为80 ℃时,产物主要为二水硫酸钙,并检测到较弱的无水硫酸钙特征峰,说明原料中二水硫酸钙开始转化为无水硫酸钙,二水硫酸钙的特征衍射峰强度相对70 ℃有所减弱,表明二水硫酸钙的溶解度随温度的升高而增大,二水硫酸钙溶解并转化为无水硫酸钙表现为特征峰强度减弱;当温度达到90 ℃,产物全部为无水硫酸钙,说明原料中二水硫酸钙已完全转化为无水硫酸钙,因为在更高温条件下无水硫酸钙的溶解度小于二水硫酸钙[17],无水硫酸钙结晶析出,进一步导致二水硫酸钙的溶解,直到二水硫酸钙完全转化为无水硫酸钙。温度为100 ℃时,产物也全部为无水硫酸钙。

图5 不同温度下制备的晶须产物样品表面形貌Fig.5 Morphology of whisker product samples prepared at different temperatures (a)T=70 ℃; (b)T=80 ℃; (c)T=90 ℃; (d)T=100 ℃
图5为在不同温度下制备的晶须产物样品的SEM照片。由图5(a),当T=70 ℃时,所形成的二水硫酸钙样品的显微形貌呈板状、板条状,直径为6~9 μm,长径比为2~10。由图5(b),当T=80 ℃时,所形成的二水硫酸钙样品的显微形貌呈棒状、晶须状或板状,直径为1~4 μm,长径比为2~13。由图5(c)和5(d),当T=90 ℃和T=100 ℃时制得的无水硫酸钙样品的直径分别为1~3 μm和3~7 μm,长径比分别为4~12和1~12,以温度为90 ℃时晶须的均匀性最好。因此,在较高的反应温度条件下可以制备形貌均匀的无水硫酸钙晶须,提高溶解温度会导致所制备的晶须直径增大,形貌均匀性变差;而在较低的温度条件下制备的样品为分散性较差的二水硫酸钙晶须,降低溶解温度会导致所制备的晶须呈板状、板条状。
3.3 反应时间对产物物相和形貌的影响

图6 不同反应时间下制备的晶须产物样品的XRD图谱Fig.6 XRD patterns of whisker product samples at different reaction time
图6为在不同反应时间下晶须产物样品的XRD图谱。分析可知,当反应时间为2 h时,产物主要物相为烧石膏(半水硫酸钙)和硬石膏,是半水硫酸钙晶须和无水硫酸钙晶须的混合物,说明反应还未达到平衡。当反应时间达到3 h,产物为无水硫酸钙,说明半水硫酸钙已完全转化为无水硫酸钙。当反应时间为4 h和5 h,产物为无水硫酸钙。
图7为在不同反应时间下晶须产物样品的SEM照片。由图7(a),当t=2 h时,所形成的半水硫酸钙晶须和无水硫酸钙晶须的混合物样品的显微形貌呈柱状或棒状,直径为0.5~2 μm,长径比为2~11,晶体生长均匀性较差。由图7(b)、7(c) 和7(d),可以看出当t=3 h、t=4 h、t=5 h时制得的无水硫酸钙晶须直径分别为1~4 μm、1~3 μm和2~5 μm,长径比分别为3~8、4~12和5~6,各样品尺寸变化不大,晶体生长均匀性好,以反应时间为4 h和5 h时晶须的均匀性最好。因此,在较高的反应时间条件下可以制备结晶均匀的无水硫酸钙晶须,提高反应时间会导致所制备的晶须直径增大,结晶均匀性变差;而在较低的反应时间下制备的样品为结晶均匀性较差的半水和无水硫酸钙晶须的混合物。

图7 不同反应时间下制备的晶须产物样品表面形貌Fig.7 Morphology of whisker product samples prepared at different reaction times (a)t=2 h; (b)t=3 h; (c)t=4 h; (d)t=5 h

图8 不同固液比制备的晶须产物样品的XRD图谱Fig.8 XRD patterns of whisker product samples at different solid-liquid ratios
3.4 固液比对产物物相和形貌的影响
图8为不同固液比制备的晶须产物样品的XRD图谱。分析可知,当固液比为0.06 g/mL时,产物主要为无水硫酸钙,且无水硫酸钙结晶性较差,强度较弱。当固液比为0.10 g/mL时,产物为无水硫酸钙,且较0.06 g/mL无水硫酸钙强度明显增强,说明体系中越来越多的无水硫酸钙结晶析出,且结晶性较好。当固液比为0.14 g/mL,产物主要为无水硫酸钙和半水硫酸钙,说明无水硫酸钙开始向半水硫酸钙转化。当固液比0.18 g/mL,无水硫酸钙开始向半水硫酸钙和二水硫酸钙转化,且较固液比0.14 g/mL,半水硫酸钙强度增强,还出现了二水硫酸钙。
图9为不同固液比时制备的晶须产物样品的SEM照片。由图9(a),当固液比为0.06 g/mL时,所形成的无水硫酸钙样品的直径为1~ 3 μm,长径比为2~8,晶体生长均匀性较差;由图9(b),当固液比0.10 g/mL时,所形成的无水硫酸钙样品的直径为1~4 μm,长径比为3~8,晶体生长均匀性好;由图9(c),当固液比0.14 g/mL时,所形成的无水硫酸钙和半水硫酸钙样品的直径为2~4 μm,长径比为3~7,晶须样品长径比有所降低;由图9(d),当固液比0.18 g/mL时,所形成的二水、半水和无水硫酸钙样品的直径为1~5 μm,长径比为11~24,晶须样品长径比大,但含有细小的粒状晶体。因此,在较低的固液比条件下可以制备结晶均匀的无水硫酸钙晶须,降低固液比将导致所制备的样品结晶性变差;而在较低的固液比下制备的样品为结晶均匀性较差的半水硫酸钙晶须和无水硫酸钙晶须的混合物,提高固液比所制备的样品为长径比大的二水、半水和无水硫酸钙的混合物。

图9 不同固液比制备的晶须产物样品表面形貌Fig.9 Morphology of whisker product samples prepared by different solid-liquid ratio (a)S=0.06 mg·L-1; (b)S=0.10 mg·L-1; (c)S=0.14 mg·L-1; (d)S=0.18 mg·L-1
表3为优化反应条件下合成产物的化学成分分析结果。可以看出,主要组分SO3为52.96%,CaO为40.35%,二者质量分数之和为93.31%;次要组分SiO2为5.92%;其它组分含量都很低。相较于磷石膏原料(表1),主要组分SO3和CaO及次要组分SiO2含量有所增加,Al2O3、P2O5、MgO和SrO等含量明显降低。表明在常压酸化法制备无水硫酸钙晶须过程中,产物得到了进一步纯化。

表3 优化反应条件下合成产物的化学成分分析结果Table 3 The chemical composition of the product was optimized by X-ray fluorescence spectrometry /wt%
3.5 盐酸体系中无水硫酸钙晶须的形成机理
二水硫酸钙是微溶电解质,在水中溶解度很低。根据文献[18]及相关溶解度数据可知,在盐酸体系中,二水硫酸钙溶解度大幅度提高,电离出钙离子和硫酸根离子,为无水硫酸钙的成核提供必要的过饱和度,即二水硫酸钙不断溶解、无水硫酸钙过饱和结晶,反应式如下:
(1)
(2)
当盐酸浓度逐渐增大时,盐酸电离产生的氢离子与二水硫酸钙溶解产生的硫酸根离子结合生成硫酸氢根(酸效应),可进一步促进二水硫酸钙的溶解。当溶液中钙离子和硫酸根离子的浓度大于无水硫酸钙的过饱和度时,溶液中就会有无水硫酸钙晶核形成,进而生长成形貌较均匀和长径比较大的棒状、柱状或晶须状无水硫酸钙晶体。无水硫酸钙的结晶析出,会促进二水硫酸钙的进一步溶解,与此循环,直至二水硫酸钙晶体完全转化为无水硫酸钙晶体。当反应温度较低时,体系中达到反应活化能的分子数较少,因此二水硫酸钙的溶解量较少,随着反应温度的升高,二水硫酸钙溶解度增加,当体系中的钙离子和硫酸根离子浓度达到无水硫酸钙过饱和度时,开始形成无水硫酸钙晶核,并逐渐生长为完善的无水硫酸钙晶体。
4 结 论
(1)在磷石膏制备无水硫酸钙晶须的过程中,盐酸的浓度、反应温度、反应时间和固液比都对形成产物的物相和形貌产生较大的影响;
(2)制备无水硫酸钙晶须的优化反应条件为:盐酸浓度为5 mol/L、反应温度为90 ℃、反应时间为3 h和固液比为0.10 g/mL;
(3)本文所采用的无水硫酸钙晶须的工艺为一步法,工艺流程短,反应条件可控性强,所制备的晶须直径为1~4 μm,长径比为3~8,均匀性好;
(4)在盐酸水体系中,存在二水硫酸钙的溶解和无水硫酸钙晶核形成与生长两种作用过程,在合适的反应条件下,当二水硫酸钙溶解产生的钙离子和硫酸根离子达到无水硫酸钙的过饱和度时,即有无水硫酸钙结晶形成。

