多层螺旋CT对肺部空洞性病变中癌性空洞和结核性空洞的诊断价值
戴晗光,张景峰
(1.宁波市北仑区人民医院 放射科,浙江 宁波 315800;2.浙江大学医学院附属第一医院 放射科,浙江 杭州 310013)
肺部组织出现坏死后经引流支气管排出并吸入空气填充形成的空洞即为肺部空洞性病变[1],其中以结核性空洞和癌性空洞最为常见[2],根据数目不同又可分为单发性空洞和多发性空洞[3]。对于多发性空洞,部分患者仅靠实验室检查难以获得确切诊断结果,通常需依靠影像学检查辅助确诊[4]。肺结核空洞和肺癌空洞因其病因不同,在影像学表现上,亦呈现不同的形态特征[5]。多层螺旋CT因其经济、简便、准确度高、重复操作性强等优势,已广泛应用于各类型肺部病变的临床诊断中[6-7],本研究回顾性分析我院收治的经多层螺旋CT诊断的肺结核空洞和肺癌空洞患者的临床资料,探讨多层螺旋CT对肺部空洞性病变中癌性空洞和结核性空洞的诊断价值,以期为临床上肺部空洞性病变的影像学检查提供参考。
1 资料和方法
1.1 一般资料 收集2016年1月—2018年2月我院收治的55例肺结核空洞和50例肺癌空洞患者的临床资料,患者均行多层螺旋 CT检查,并经术后病理、经皮穿刺活检、痰菌阳性或抗结核治疗等确诊。 全部105例患者中男58例,女47例,年龄29~75岁,平均59.6±7.3岁,临床均表现为发热、咳嗽、呼吸困难、咳痰、痰中带血等,部分无症状表现。肺结核空洞组和肺癌空洞组患者的一般资料比较,差异无统计学意义(P>0.05),见表1。
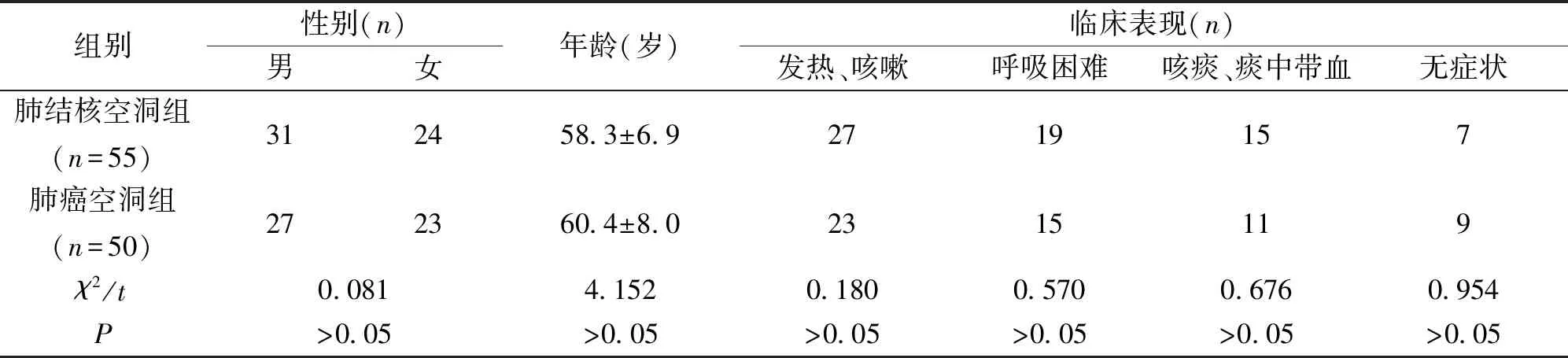
表1 两组一般资料的比较
1.2 CT检查 采用PHILIPS LightSpeed VCT(64层螺旋CT)对患者肺部进行扫描。患者取仰卧位,双手举至头顶,屏气状态下行连续扫描,扫描范围为从肺尖至肺底的全部区域,包括两侧胸壁至腋窝。扫描参数:电压120 kV,电流250 mA,螺距1.0 mm,矩阵512×512,采用多平面重建,重建层厚0.8 mm,层间隔0.8 mm。分别进行横轴位、冠状位和矢状位成像,由2位具有5年以上阅片经验的放射科医师进行图像处理和分析。
1.3 观察指标 分析并比较空洞大小、位置、洞壁厚度、空洞特点(壁钙化、壁强化、壁结节、偏心空洞等)以及周围组织结构特点(胸膜增厚粘连、胸膜凹陷、卫星病灶、周围炎症等)[8]。空洞大小取最大内径值,洞壁厚度取最大厚度值,均以PACS专业工作软件进行测量。
1.4 统计学方法 应用SPSS 19.0统计软件进行数据分析,计数资料比较采用χ2检验,计量资料比较采用t检验;P<0.05表示差异具有统计学意义。
2 结果
2.1 空洞大小、位置、洞壁厚度的比较 CT图像分析结果显示,肺结核空洞组的空洞大小(24.52±8.93 mm)与肺癌空洞组(39.06±10.54 mm)差异无统计学意义(P>0.05);两组的空洞位置、洞壁厚度比较,差异有统计学意义(P<0.05),见表2。
2.2 空洞的特点 肺结核空洞组中,出现壁钙化的数量显著高于肺癌空洞组,而出现壁强化、壁结节、偏心空洞和气液平面的数量则显著低于肺癌空洞组;差异均有统计学意义(P<0.05)。两组中壁密度均匀和空洞边缘清晰的出现率比较,差异无统计学意义(P>0.05),具体见表3。

表2 两组空洞位置、洞壁厚度的比较

表3 两组空洞特点的比较[n(%)]
2.3 两组空洞周围组织结构特点的比较 肺结核空洞组中,空洞周围组织结构出现卫星病灶、周围炎症和纵膈淋巴结钙化的数量显著高于肺癌空洞组,出现纵膈淋巴结肿大和血管集束征的数量则显著低于肺癌空洞组;差异均有统计学意义(P<0.05)。两组的空洞周围组织结构中胸膜增厚粘连和胸膜凹陷的出现率比较,差异无统计学意义(P>0.05)。见表4。

表4 两组空洞周围组织结构特点的比较[n(%)]
3 讨论
结核性空洞是由于结核杆菌引起肺部慢性感染,进而引发肺组织干酪样坏死、液化经引流支气管排出后形成空洞,癌性空洞则是由于肺部癌性肿块内部的供血不足,进而引发肿块组织坏死、液化,经支气管引流排出后形成空洞[9],两者的形成机制不同,因而,在影像学上亦呈现各自的不同表现。有报道证实[1,10-11],多层螺旋CT在检测肺部空洞的特征和周围组织异常改变方面,有着较好的诊断效果。
结核性空洞好发于上叶尖后段和下叶背段部位,空洞周围常见有卫星病灶,在空洞与肺门之间亦较常见到与胸膜粘连的引流支气管[12-13],这些均可作为结核性空洞的典型特征。结核性空洞洞壁一般较薄,内缘光滑且规则,少见壁结节,多数可见钙化灶征象,空洞周围时常可见炎性病灶渗出而呈现的片状浸润影像;而癌性空洞壁多由缺血坏死的肿瘤组织构成,洞壁一般较厚且薄厚不均匀,尤以血液供应丰富的邻近肺门部位洞壁最厚,同时洞壁多表现为粗糙不光滑,大多可见明显的壁结节,并呈现偏心性空洞征象[1]。癌性空洞因其洞壁较厚,大部分可见强化征象,而结核性空洞壁多不强化或仅可见外周薄层强化[9]。还需要注意的是,肺癌病灶周围的血管大多呈现明显的增粗和僵直征,同时向病灶组织方向聚拢,进而形成较为明显的“血管集束征”表现,但该表现易与结核性炎症引发的局部充血相混淆,需要仔细加以鉴别[14]。本研究结果显示,肺结核空洞位置位于肺上叶尖后段或下叶背段的占比81.8%,显著高于肺癌空洞的44.0%;肺结核空洞的洞壁厚度>3 mm的占比21.8%,显著低于肺癌空洞的94.0%;肺结核空洞组的壁钙化数量和周围卫星病灶、炎症、纵膈淋巴结钙化数量均显著高于肺癌空洞组,而壁强化、壁结节、偏心空洞和血管集束征的数量则显著低于肺癌空洞组,该结果与上述论断基本一致。在气液平面表现上,一般认为癌性空洞较多见气液平面征象,而结核性空洞无气液平面表现,但也有报道指出,肺结核空洞合并感染及出血时,亦可见气液平面征象,但仅有少于20%的结核性空洞可见该征象表现[5]。 本研究中,肺结核空洞组的气液平面征象数量显著低于肺癌空洞组,与上述论断一致。此外,肺癌病灶还可表现为小叶间隔串珠样改变、分叶征、细毛刺、胸膜尾征以及纵膈淋巴结明显肿大等CT影像学表现,均可用于癌性空洞的辅助鉴别诊断[15-16]。
终上所述,多层螺旋CT对肺部空洞性病变中癌性空洞和结核性空洞的诊断具有重要的参考价值。如CT表现为厚壁且厚薄不均匀空洞,并伴有明显壁结节、壁强化及偏心空洞表现,同时可见气液平面、分叶、毛刺、血管集束征象,则可高度怀疑为癌性空洞;如CT表现为空洞壁薄、壁钙化明显,周围多见卫星病灶、炎症、纵膈淋巴结钙化表现,则倾向诊断为结核性空洞。当然,在实际临床工作中,还需要结合患者的年龄、病情、临床表现、实验室指标等进行综合诊断,必要时还需要进行肺组织穿刺活检进行确诊。

