CD30在外周T细胞淋巴瘤-非特指型中的表达与预后的相关研究
杨笋 张明智
外周T细胞淋巴瘤-非特指型(peripheral lymphoma T cell lymphoma,unspecified,PTCL-U)是一种需要排除间变大细胞淋巴瘤(anaplastic large cell lymphoma,ALCL)、血管免疫细胞性T细胞淋巴瘤(angioimmunoblastic T-cell lymphoma,AITL)等的外周T 细胞淋巴瘤(peripheral lymphoma T cell lymphoma,PTCL),为PTCL中最常见亚型,在欧美国家约占非霍奇金淋巴瘤(non-Hodgkin's lymphoma,NHL)的7%,在亚洲国家占NHL的15%~22%[1]。发病时多为晚期、无特征性的临床表现,通常为淋巴结增大及结外疾病(常见于脾脏、骨髓、皮肤),严重者可出现噬血细胞综合征,侵袭性强、预后差,5年生存率为25%~45%[2]。CD30 抗原是肿瘤坏死因子受体(tumor necrosis factor receptor,TNFR)超家族的跨膜糖蛋白,刺激后CD30对细胞生长和存活发挥较多作用,为目前临床上诊断霍奇金淋巴瘤(Hodgkin's lymphoma,HL)和ALCL 重要的组织化学标记。2011年美国食品和药物监督管理局(FDA)根据临床试验数据批准CD30单抗brentuximab vedotin 用于HL 和ALCL,数据显示疗效较好[3]。CD30 在PTCL-U 表达的生物学意义逐渐被关注[4]。本研究通过回顾性分析CD30在PTCL-U中的差异及表达情况,分析CD30与临床生存预后的相关性。
1 材料与方法
1.1 病例资料
选取2013年1月到2017年12月郑州大学第一附属医院初治的56 例PTCL-U 患者的病例资料。所有患者均行骨髓穿刺、浅表淋巴结超声、胸腹部CT和PET-CT等检查结果。
1.2 方法
1.2.1 标本获取 CD30为郑州大学第一附属医院病理科的常规诊疗在确诊时已完成,本研究对淋巴结活检或手术标本病理切片进行重新阅片,回顾每例患者免疫组织化学检测CD30 表达情况。CD30 产物表达于细胞膜及核旁点状阳性,显色均呈棕黄色,不着色为阴性,计数10 个具有代表性的高倍视野(×400),每个视野计100 个细胞,CD30 阳性细胞数/1 000个肿瘤细胞≥20%视为阳性。
1.2.2 诊断与疗效标准 所有患者均采用2008年世界卫生组织(WHO)造血与淋巴组织肿瘤分类标准经病理及免疫组织化学法诊断。疗效评估标准参考2015年美国国立综合癌症网络(National Comprehensive Cancer Network,NCCN)发布的NHL指南标准[5]。完全缓解(complete response,CR)及部分缓解(partial response,PR)患者占全部病例数的百分率称为客观缓解率(objective response rate,ORR)。
1.2.3 治疗方法 56 例患者中接受CHOP 方案治疗为28例,接受GDPT方案为28例。
1.2.4 随访 通过查阅病例及电话进行随访,时间截至2018年12月或患者死亡时间。随访内容包括总生存时间(overall survival,OS)、无进展生存时间(progression-free survival,PFS)。OS定义为从确诊到患者死亡或末次随访的时间;PFS定义为从确诊开始到发生疾病进展、复发或死亡的末次随访时间。截至随访结束,56 例患者中33 例死亡,19 例生存,4 例失访,失访率为7.14%。
1.3 统计学分析
采用SPSS 17.0软件进行统计学分析。分类变量进行Chi-square 检验,生存分析采用Kaplan-Meier法,生存率比较采用Log-rank 检验;对影响生存的临床及病理指标进行单因素Logistic 回归分析。以P<0.05为差异具有统计学意义。
2 结果
2.1 临床特征
56例PTCL-U患者中男性35例、女性21例,男女比例为1.7∶1,中位年龄为60(16~76)岁;年龄≥60岁为27例(48.2%),临床分期Ⅰ期6例、Ⅱ期12例、Ⅲ期16 例、Ⅳ期22 例。38 例(67.9%)患者诊断时为晚期疾病,53 例(94.6%)患者存在淋巴结增大,结外病变数目≥2个部位12例(21.4%)病变,22例(39.3%)伴随B 症状,10 例(17.9%)存在骨髓浸润,ECOG 评分2 分10 例(17.9%)。实验室结果显示:LDH 水平升高29例(51.8%),β2-MG 升高24 例(42.9%),Ki-67≥80%为12 例(21.4%),EBER 阳性13 例(23.2%),EBER 阴性26例(46.4%),EBER未查17例(30.4%)。IPI/aaIPI评分中低-中危组(IPI评分0~2分或aaIPI评分0~1分)27 例(48.2%),中-高危组(IPI 评分3~5 分或aaIPI评分2~3分)29例(51.8%);PIT中低-中危组(0~1 分)30 例(53.6%),中-高危组(2~4 分)26 例(46.4%)。在54 例可评估初治效果的病例中32 例(59.3%)初治有效,15例(27.8%)达CR。
2.2 CD30表达与各因素的关系
比较CD30 表达与患者临床特点、病理学指标及初治效果的关系(表1)。CD30 阳性表达在晚期患者、LDH水平升高、结外病变数目≥2个部位、中-高危患者更为多见(P<0.05),CD30 阳性患者初治效果不佳(P=0.027);在性别、年龄、B症状、体力状况、Ki-67(80%)、骨髓、β2-MG、EBER 方面比较,差异无统计学意义(P>0.05)。

表1 CD30表达与临床特点、病理学指标及初治效果的关系
2.3 CD30对PTCL-U预后的影响
56例患者的3、5年OS率分别为42.2%和20.4%,3、5年PFS率分别为32.1%和17.8%(图1)。CHOP与GDPT方案的患者3、5年OS及PFS比较,差异无统计学意义(OS:P=0.971,图2A;PFS:P=0.962,图2B)。根据CD30 表达情况,将56 例患者分为CD30 阳性组和CD30阴性组,CD30阳性20例,CD30阴性36例,阳性率为35.7%。3年OS 分别为16.5%和54.9%(P=0.001,图3A)。3年PFS 分别为11.2%和44.5%(P=0.016,图3B)。

图1 56例PTCL-U患者的OS和PFS
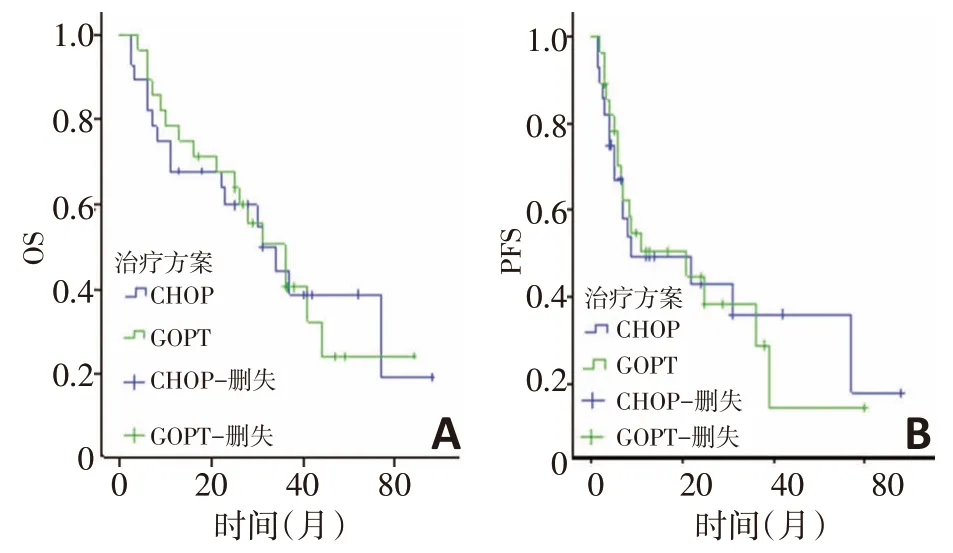
图2 CHOP与GDPT方案患者OS与PFS的比较
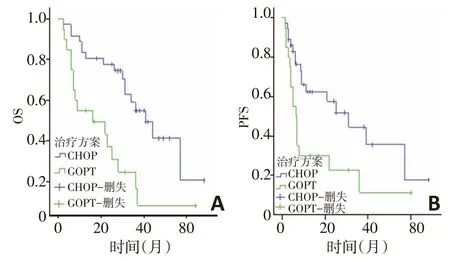
图3 CD30表达对PTCL-U患者OS与PFS的影响
2.4 PTCL-U患者的生存预后分析
对可能影响PTCL-U 患者生存的临床及病理因素进行单因素Logistic回归分析,PTCL-U患者的生存与临床分期、IPI/aaIPI 评分、PIT 及CD30 表达相关(P<0.05,表2)。在单因素分析中对(P<0.05)的变量进行Cox 回归模型多因素分析,分期及PIT 为影响患者OS的危险因素,IPI/aaIPI评分及CD30是否表达及对OS 的影响,差异无统计学意义;PIT 为影响PFS 的唯一危险因素(表3)。
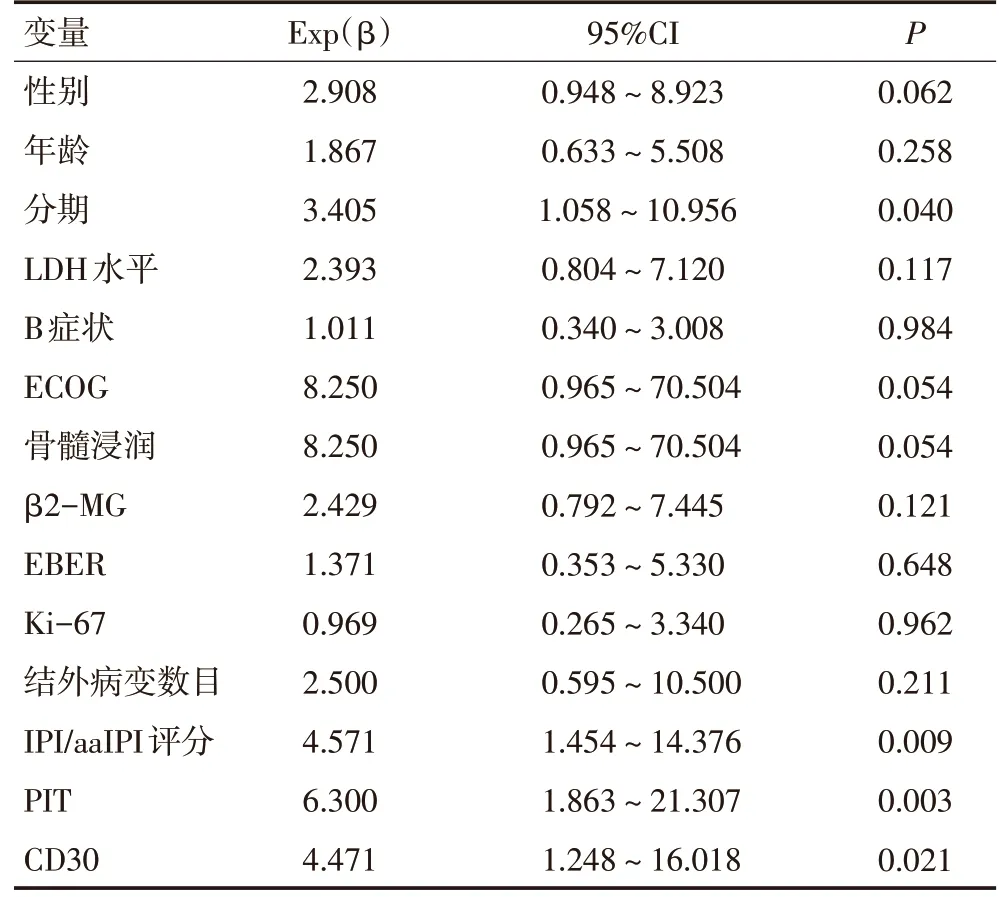
表2 PTCL-U患者的单因素分析
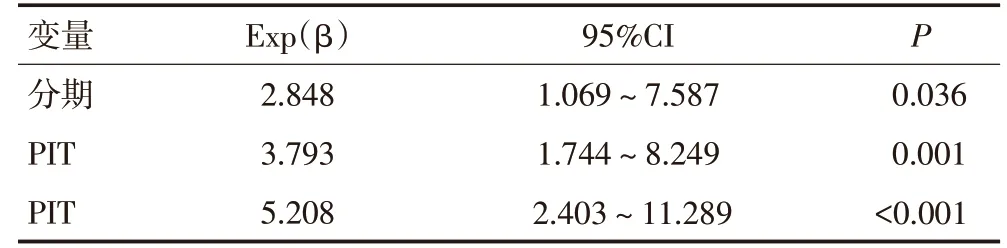
表3 PTCL-U患者的多因素分析
3 讨论
PTCL-U 为一种需要排除特定PTCL 亚群、异质性强的成熟T 细胞淋巴瘤,目前尚无标准的化疗方案,生存预后不佳,本研究中患者3、5年OS 分别为42.2%和20.4%。PTCL-U 采用含蒽环类药物的治疗效果欠佳,既往报道对含吉西他滨的化疗方案反应较好[6]。本研究中CHOP 和GDPT 方案对患者的OS影响差异无统计学意义。本研究发现,患者诊断时均存在淋巴结肿大,中位年龄为60 岁,男性占优势,67.9%患者诊断时为晚期,易结外受累、51.8%患者LDH水平升高,与之前的研究相一致[7],提示PTCL-U易转移、侵袭性强和肿瘤负荷高。骨髓受累比弥漫性大B 细胞淋巴瘤更为常见[8],本研究中17.0%患者存在骨髓浸润,较既往研究20%~30%略低,可能与病例数较少相关。EBER 阳性占33.3%,使该病更具有侵袭性,Aneja 等[9]研究表明,在EB 病毒感染时,CD30在PTCL-U中表达较EB病毒未感染时更高。
CD30 为肿瘤坏死因子受体超家族的成员,在人体正常条件下,通常不表达[10]。病理状态下在肿瘤、感染和自身免疫性疾病中均可表达,阳性率可以提示肿瘤的恶性程度和炎症的活动[11-13]。CD30 在10%~20%B 淋巴恶性肿瘤和30%T 淋巴恶性肿瘤中表达,HL 和ALCL 为最常见的CD30 阳性恶性肿瘤。CD30单抗在HL和ALCL中疗效显著,CD30在PTCL-U中的表达情况及单抗能否为PTCL-U 患者带来获益为关注的热点。本研究发现,当Ki-67 为20%时,阳性患者20 例(35.7%)。与既往报道不一致,2016年Céline 等[14]分析141 例PTCL-U 患者,当Ki-67 为5%时,CD30 阳性率为58%;当Ki-67 为25%时,CD30 阳性率为32%。CD30 在PTCL-U 预后中的意义,报道较少。本研究中CD30 阳性组较阴性组预后更差,3年OS 分别为16.5%和54.9%,与2015年美国的报道相仿[15],其通过对纳入的340 例PTCL-U 患者分析得出,CD30表达为预后不佳的危险因素。Bisig 等[16]研究表明,CD30 表达可能为有价值的标准,可以把PTCL-U 定义为两个不同的生物亚群CD30(+)和CD30(-)。BV为一种CD30抗体药物偶联物,在HL与ALCL中疗效显著,但在PTCL-U 中疗效欠佳[17],可能与其阳性表达率偏低有关。
综上所述,PTCL-U为一种尚无标准治疗方案且预后较差的异质性疾病。CD30在PTCL-U中的阳性表达率偏低,CD30阳性患者预后较差。本研究的56例患者均来自同一所医院,存在样本地域的偏倚,CD30 是否能作为判断PTCL-U 预后的独立参数,亟需多中心、大样本的研究来验证。

