我国华中地区大气PM2.5 长期暴露与成人血压水平的相关性分析
宋佳丽,胡爽,唐桂刚,张迪,张文博, 严小芳,杨静玮,高岩,李静,李希,郑昕
大气颗粒物污染是全球首要的环境危险因素[1],也是我国面临的重大公共卫生问题之一,为仅次于饮食、高血压和吸烟的第四大致死危险因素[2]。高血压是我国最重要的心血管病危险因素[3],目前我国高血压患病人数已达2.7 亿[4],但控制率仅约7%[5]。大气颗粒物污染,特别是PM2.5污染,可显著增加心血管病死亡与入院风险[6-7],PM2.5暴露后引起的血压升高可能是潜在的生物学机制之一。多项研究表明,PM2.5短期暴露可引起一过性的血压升高,但PM2.5长期暴露与血压的相关性尚无定论[8-12]。
本文将基于我国心血管病高危人群队列的华中地区横断面调查数据,研究PM2.5长期暴露与血压(收缩压、舒张压、平均动脉压、脉压)的相关关系,从而为我国华中地区PM2.5健康效应评价以及预防策略制定提供科学依据。
1 对象与方法
1.1 研究设计
心血管病高危人群早期筛查与综合干预项目是2014 年启动的国家重大公共卫生服务项目,其研究方案已先期发表[13]。本文根据行政区划纳入华中地区河南、湖北、湖南三省。年龄在35~75 岁的初筛对象共264 749 例,在此基础上排除20 423 例空气污染暴露水平以及研究分析所用变量缺失的对象。为进一步减小血压测量误差对结果的影响,排除了422 例收缩压>190 mmHg(1 mmHg=0.133 kPa)或<90 mmHg以及舒张压>120 mmHg 或<60 mmHg 的调查对象,最终研究共纳入243 904 例调查对象的数据。
1.2 人群数据收集及变量定义
心血管病高危人群早期筛查与综合干预项目在华中地区河南、湖北、湖南三省,综合考虑地理环境、城乡人口分布等因素在每个省选取6 个区(县)作为项目点。每个项目点依据人口规模选择3~5 个乡镇或街道进行社区宣传动员,邀请当地常驻居民参与该项目。统一培训的现场调查人员对符合入选标准的调查对象进行信息采集,并根据标准操作流程进行血压、身高、体重等指标测量。收集的信息包括:人口学特征(如年龄、性别、居住地址、民族、职业、教育程度、家庭年收入、婚姻状况、有无医疗保险)、疾病史(如心肌梗死、脑卒中)、心血管病危险因素[如糖尿病、吸烟、饮酒、体重指数(BMI)]等。血压测量采用统一的电子血压计(Omron HEM-7430),调查对象静坐5 min 后测量右上臂血压两次取均值。如果两次收缩压差值大于10 mmHg,则测量第三次,最终血压值通过计算后两次血压平均值得到。脉压为收缩压与舒张压的差值,平均动脉压为舒张压与1/3 脉压的和。体重指数定义为体重(kg)除以身高(m)的平方;超重定义为体重指数≥25 kg/m2。对于被问及“目前是否服用降压药物?”,且回答为“是”的调查对象则被认为正在服用降压药。与《2014 美国成人高血压管理指南(JNC8)》和2010 年《中国高血压防治指南》的定义一致,平均收缩压≥140 mmHg 或平均舒张压≥90 mmHg,或自报在过去两周内服用降压药物的人群定义为高血压人群。
1.3 空气污染暴露测量
研究时段内河南、湖北、湖南三省的18 个城市(郑州市、洛阳市、平顶山市、鹤壁市、新乡市、濮阳市、漯河市、武汉市、宜昌市、孝感市、荆州市、咸宁市、长沙市、株洲市、湘潭市、岳阳市、常德市、湘西州)PM2.5的日均浓度监测资料来源于中国环境监测总站“全国城市空气质量实时发布平台”,其空气质量监测方法和评价方法均依据我国相关标准[14-15]。以某市一年内逐日所有有效PM2.5日均浓度的平均值作为该市污染物年均值,从而计算出每位调查对象参加信息采集前一年的年均PM2.5暴露水平。
1.4 统计学方法
所有数据分析使用SAS 9.4 以及R 3.5.2 完成。连续变量利用均值和标准差描述,分类变量利用频数和百分比描述。连续变量组间比较采用Kruskal-Wallis 检验,分类变量组间比较采用卡方检验。首先,按PM2.5年均暴露的四分位数间距描述暴露于不同PM2.5水平的调查对象社会经济学特征以及健康特征。其次,为探究PM2.5长期暴露与血压水平间的相关关系,建立了多水平的线性混合模型,模型纳入的混杂因素为通过文献回顾事先确定,为了同时评估调查对象的人口学特征、社会经济学特征以及心血管病危险因素等对于此相关关系的影响,模型1 仅纳入年龄和性别,模型2 在模型1 基础上纳入家庭年收入、教育程度和婚姻状态,模型3 在模型2 基础上纳入心血管病危险因素,如体重指数、吸烟情况、糖尿病患病情况,模型4 在模型3 基础上纳入降压药使用情况。关注的血压水平指标除收缩压和舒张压外,还有反映血管弹性的脉压以及反映心输出量以及体循环血管阻力的平均动脉压。最后,按照研究对象的基本特征,如年龄(≥60 岁和<60 岁)、性别(男性和女性)、体重指数(≥25 kg / m2和<25 kg / m2)等进行分层分析,并在模型中引入PM2.5年均暴露与个体特征的交互项以评估个体特征与PM2.5暴露的交互作用。此外,为减少降压药服用情况对PM2.5与血压水平间的相关关系的影响,仅纳入未服用降压药调查对象进行敏感性分析。统计学推断均采用双侧检验,P<0.05 认为具有统计学意义。
2 结果
2.1 调查对象基本特征
按调查对象PM2.5年均暴露的四分位数间距划分的社会经济学(表1)以及健康特征(表2)描述。研究共纳入243 904 例对象,92 819 例 (38.1%)为男性。高血压患者119 282 例(48.9%),服用降压药的调查对象27 289 例(11.2%)。平均收缩压为(136.3±19.8)mmHg,平均舒张压为(80.8±11.1) mmHg。
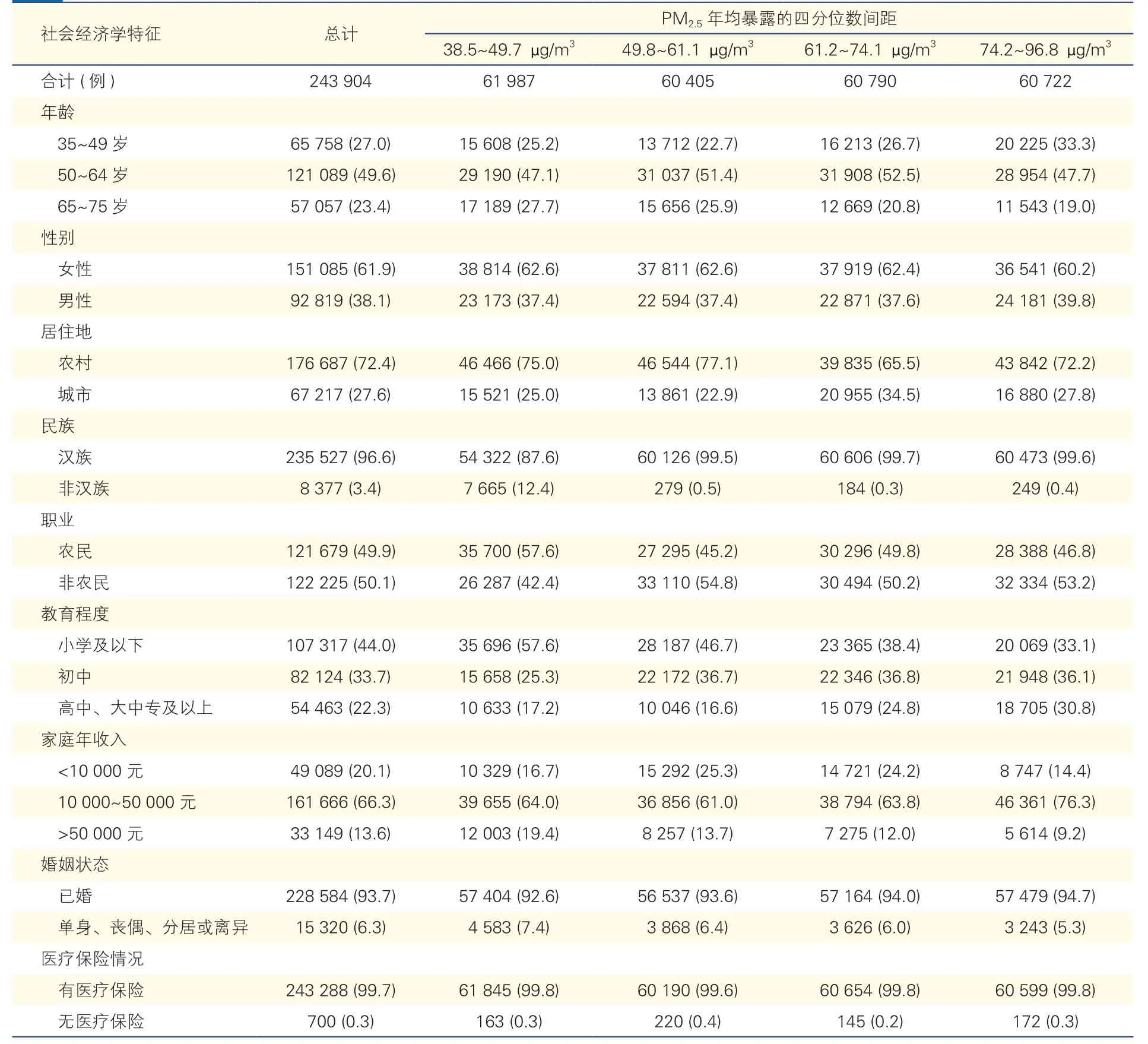
表1 按PM2.5 年均暴露的四分位数间距划分的调查对象社会经济学特征 [例 (%)]
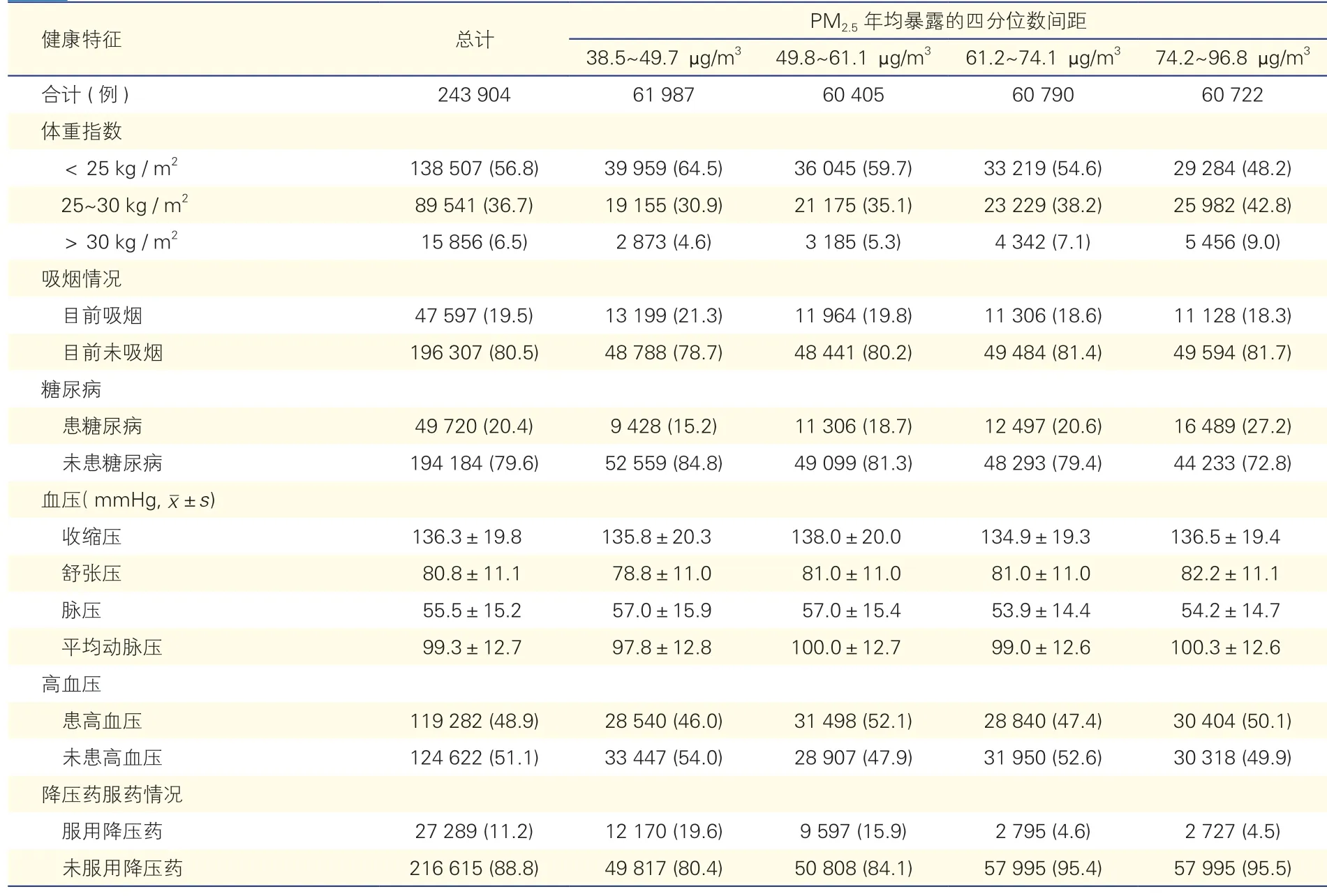
表2 按PM2.5 年均暴露的四分位数间距划分的调查对象健康特征 [例 (%)]
2.2 PM2.5 与成人血压水平的相关关系
在调整了人口学特征(年龄、性别)、社会经济学特征(教育程度、家庭年收入、婚姻状态)、心血管病危险因素(体重指数、吸烟情况、糖尿病史)以及降压药服用情况后,PM2.5浓度每增高10 μg/m3,收缩压、舒张压、脉压及平均动脉压分别增加2.47(95%CI:2.34~2.61)mmHg、0.69(95%CI:0.62~ 0.77)mmHg、1.79(95%CI:1.68~ 1.89)及1.28(95%CI:1.19~ 1.37) mmHg。
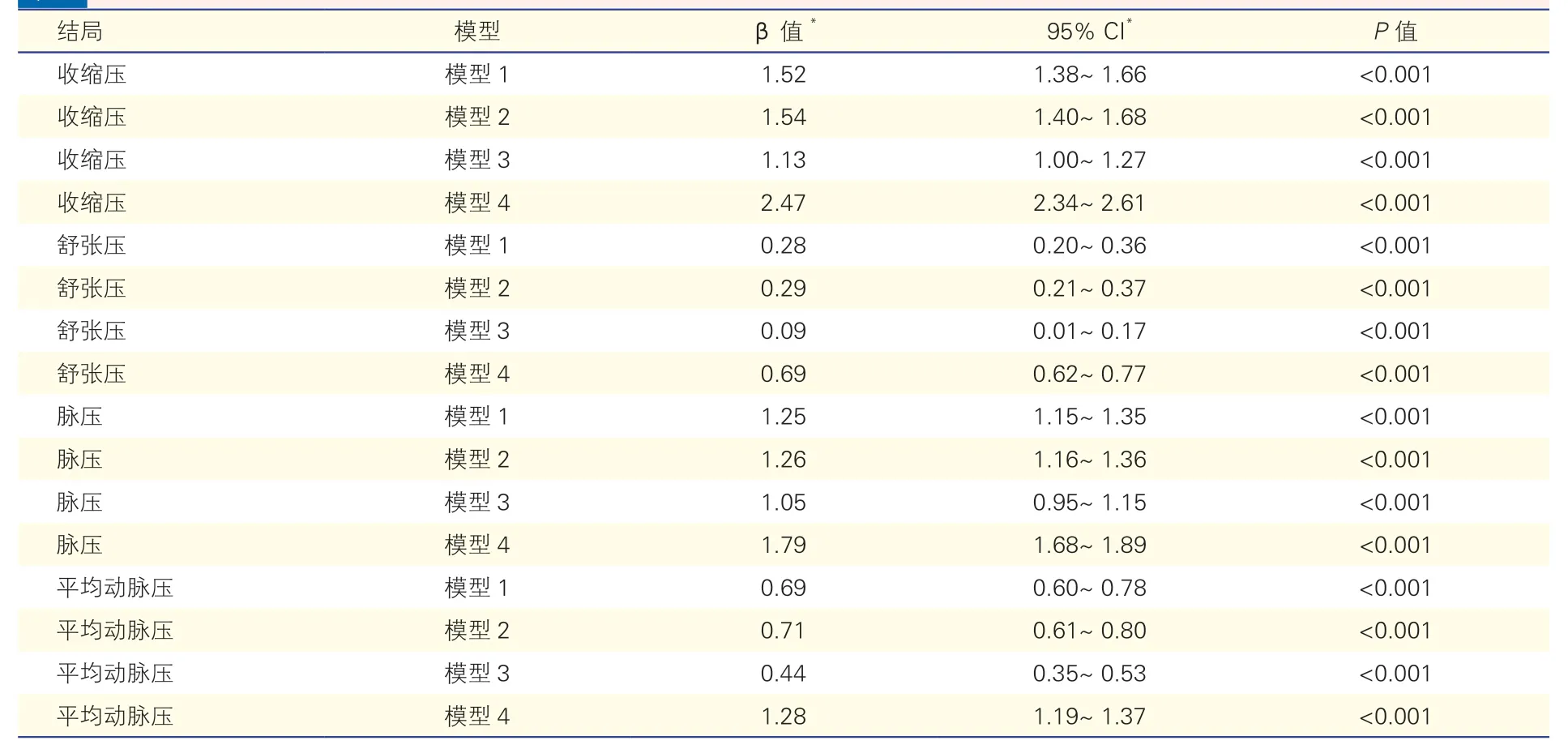
表3 PM2.5 与所有调查对象血压水平的相关关系(mmHg,n=243 904)
调整心血管病危险因素(模型2 vs 模型3)及降压药服用情况后(模型3 vs 模型4),PM2.5暴露与成人血压水平的相关关系效应量(β 值)变化较大(表3)。当仅纳入未服用降压药的调查对象时,最终的(表4 模型3)β 值与纳入所有调查对象最终的β 值(表3 模型4) 相似。
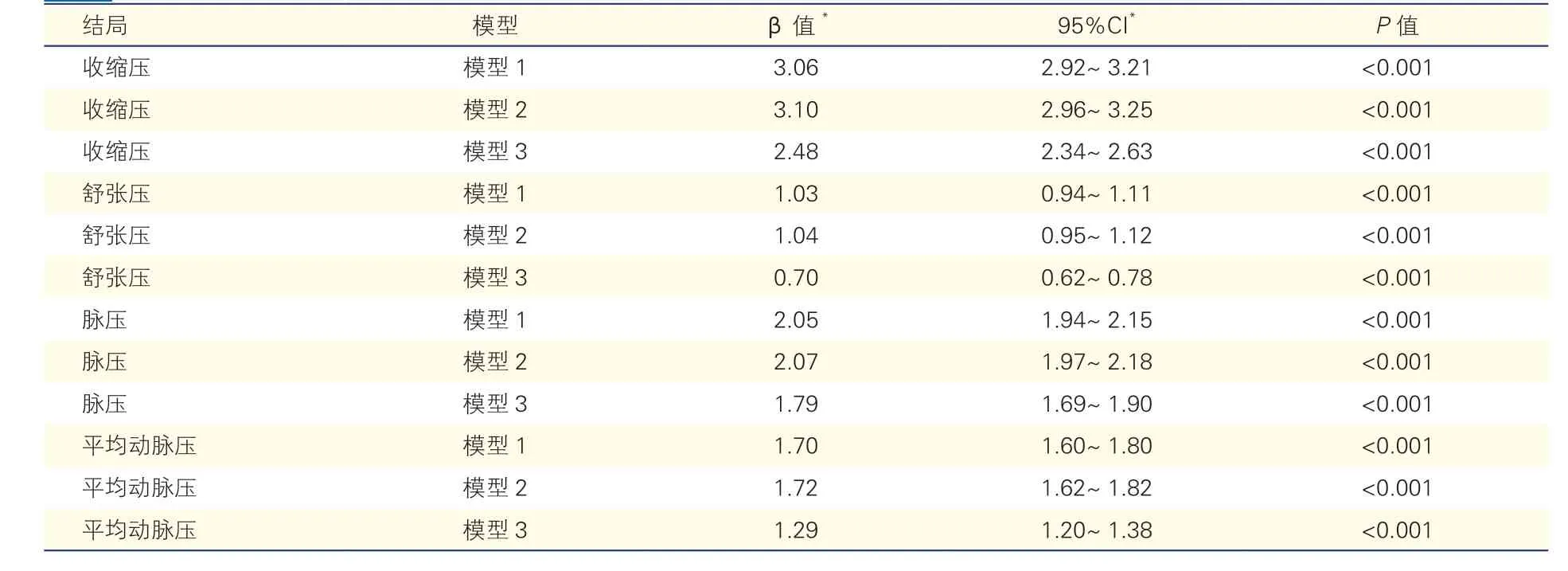
表4 PM2.5 与未服用降压药调查对象血压水平的相关关系(mmHg,n=216 615)
2.3 个体特征对PM2.5 与收缩压相关关系的影响
根据调查对象的人口学特征(年龄、性别)、心血管病危险因素(高血压患病情况、体重指数、吸烟情况、糖尿病患病情况)进行PM2.5与收缩压的相关关系的分层分析显示,老年人(年龄≥60岁)、男性、未吸烟、患糖尿病、超重(体重指数≥25kg/m2)、患高血压的调查对象,PM2.5每增加10 μg/m3收缩压增加更多。PM2.5暴露与年龄、性别、高血压患病情况均存在交互作用,老年人(年龄≥60 岁)、男性、患高血压的调查对象PM2.5长期暴露与收缩压升高的关联程度更高(P交互<0.05)(图1)。
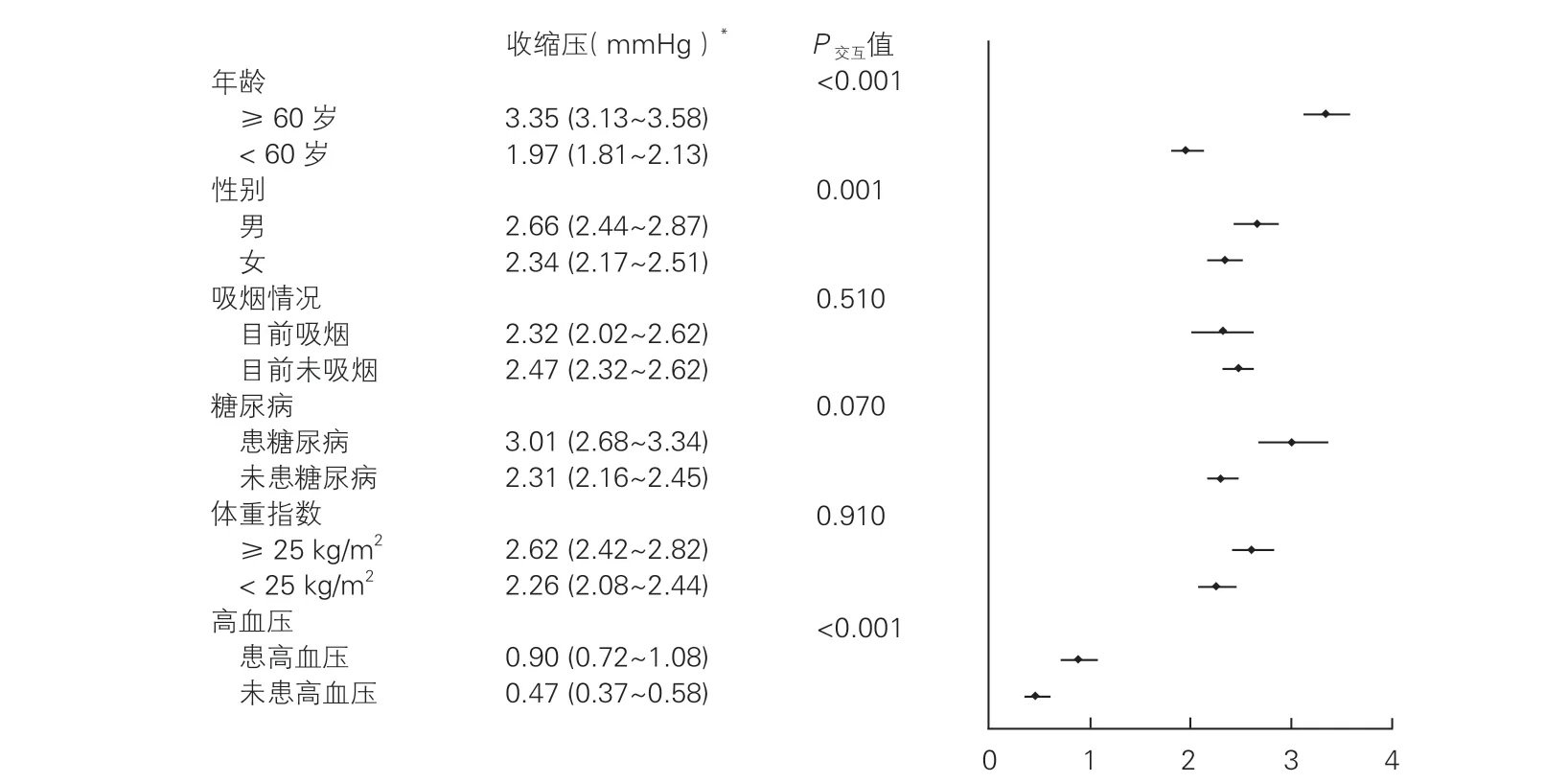
图1 个体特征对PM2.5 与收缩压相关关系的影响(n=243 904)
3 讨论
研究通过华中地区大样本的典型性人群横断面调查数据发现PM2.5长期暴露与个体的收缩压、舒张压、脉压与平均动脉压的升高相关,其中对于收缩压的影响最大。在老年人、男性、高血压患者中收缩压增加更为显著。
研究发现,PM2.5长期暴露与血压(收缩压、舒张压、脉压、平均动脉压)升高密切相关,与既往几项研究结果基本一致[9-10,16]。但目前PM2.5的长期暴露与血压的相关关系尚无定论,一项基于我国7省代表性人群的相关性分析结果显示,PM2.5浓度每增加10 μg/m3,收缩压增加1.30 mmHg,舒张压增加1.04 mmHg[16],本研究结果与此类似。然而,一项基于65 岁以上27 752 例我国台湾居民的分析结果显示,PM2.5的长期暴露可增加舒张压水平,但不增加收缩压水平[17]。而另一项基于我国28 省35 岁以上代表性人群的研究结果显示PM2.5与收缩压存在关联,但与舒张压无关[18]。这些分析结果的不一致性可能与不同地区人群生活习惯、空气污染暴露测量方法、大气污染物的载带组分及其时空分布特征不同等因素有关。而本研究利用局部地区大样本的人群数据,人群特征变异性较小,可在一定程度上降低地域差异对结果的影响。此外,降压药的使用情况为PM2.5暴露与血压相关关系的重要中介因素[19],既往部分研究用药信息缺失[17-18],限制了降压药使用对相关性影响的探讨。本研究观察了调整降压药使用前后的相关关系效应量(β 值)变化,并在未使用降压药的人群中进行了敏感性分析,使得PM2.5暴露与血压相关性的分析更加全面和客观。
PM2.5暴露引起血压升高的生物学机制可能包括自主神经系统功能紊乱、系统炎症及氧化应激反应和内皮功能损伤[20]。吸入PM2.5数分钟到数小时内,其即可通过影响自主神经系统引起副交感神经张力的降低以及交感神经活动增加,引起急性血压升高。而慢性血压升高则可能主要由系统炎症反应介导[20]。目前已有研究证实大气颗粒物长期暴露与中性粒细胞比例以及白介素-6 等炎症标记物之间的关联[9]。同时,PM2.5长期暴露还与空腹血糖、糖化血红蛋白以及总胆固醇水平升高相关,引发的代谢紊乱与系统炎症及氧化应激反应等可一同加速动脉粥样硬化进程[21],进而导致血管重塑、外周血管阻力增加-这与本研究发现PM2.5长期暴露与脉压以及平均动脉压升高相关相互印证。
PM2.5长期暴露对收缩压影响最为显著,进一步分析结果显示老年人、男性、患高血压者PM2.5长期暴露后收缩压升高更为显著,与既往研究基本一致[22-23]。由于老年人呼吸道颗粒物清除等生理机能的减退以及心血管、呼吸系统合并症的增加,使其更易受到外界大气颗粒物污染的影响[24]。而相较于女性而言,男性户外活动频率及强度更高[25],因此PM2.5长期暴露后血压升高更为显著[22,26]。高血压患者已有一定的自主神经系统功能紊乱以及内皮功能损伤,在此基础上PM2.5暴露所致的负性健康效应会进一步加强[27],Auchincloss 等[23]的研究也显示了相似的结果。
本研究为华中地区乃至全国的大气污染治理以及个人防护提供了启示。本研究显示PM2.5长期暴露浓度每增加10 μg/m3,个体水平上血压仅上升1~2 mmHg,但这一微小的改变在人群水平上具有重要的公共卫生意义——环境中每立方米空气中的PM2.5减少几微克,其对人群血压影响与采取减少钠盐摄入以及限制饮酒等高血压非药物干预措施的影响类似[28]。因此,空气质量持续改善将进一步对心血管健康带来有益影响。在个体层面上,特别是老年男性、高血压患者等敏感人群,在污染天气需采取个人防护措施,从而降低PM2.5的不利影响。
本研究仍存在一定的局限性。首先,本研究为基于人群横断面调查的相关性分析,未报告大气颗粒物长期暴露前后的血压变化,无法证实大气颗粒暴露与血压升高的因果关联。第二,使用调查对象所在城市1 年的PM2.5均值代表其PM2.5长期暴露水平,未考虑城市内部个体PM2.5暴露的差异性(如个体户外暴露时间不同),对人群大气污染暴露的测量可能存在误差。第三,每个个体仅取其一次体格检查中的血压测量值。尽管采用了统一的标准操作流程以及仪器,但缺少多次连续追踪的血压测量,对血压实际水平的估计可能存在误差。第四,本研究以PM2.5为主要污染物进行分析,仅建立了PM2.5单污染物模型,未考虑PM10、二氧化氮(NO2)、臭氧(O3)等其他污染物的协同效应对血压的影响,一定程度上可能会造成PM2.5对血压水平影响的高估。
综上所述,PM2.5长期暴露与人群血压水平存在相关性,且这种相关关系受年龄、性别、是否合并高血压的影响, 其内在的机制有待于进一步研究。本研究为大气污染治理相关的政策制定、深入理解空气质量与健康的相关性及其机制,从而进一步改善我国居民健康水平提供了科学依据。

