锁骨下/颅外椎动脉狭窄的处理:中国专家共识
中国医疗保健国际交流促进会血管疾病高血压分会专家共识写作组
1 前言
锁骨下动脉狭窄(subclavian artery stenosis, SS)和椎动脉狭窄(vertebral artery stenosis, VAS)在临床上并非少见,随着我国人口老龄化趋势的加剧,其患病率逐年增高,但该病临床上往往无明显症状,常被忽视。椎动脉往往是锁骨下动脉的一个分支,绝大数发自锁骨下动脉近中段,故本共识一并阐述。
脑卒中已成为当今全球致残和死亡最重要的病因之一,其中缺血性脑卒中占50%以上。流行病学调查结果显示,我国每年新发脑卒中患者超过200 万,死于脑卒中的人群约150 万[1]。研究表明,约25%~40%的短暂性脑缺血发作(transient cerebral ischemic attack, TIA)或者脑卒中发生在后循环[2-3]。锁骨下动脉和椎动脉是后循环系统的重要供血血管,同时也是后循环缺血性脑卒中的重要起源部位,其中约20%的后循环卒中是由颅外椎动脉狭窄(extracranial vertebral artery stenosis, ECVAS)或SS引起[4-5]。VAS 可直接影响后循环的灌注,狭窄部位的易损斑块或血栓也有可能脱落进入椎基底动脉,导致TIA 或脑卒中。有研究显示,症状性动脉粥样硬化性后循环缺血发生致命性反复性脑卒中的风险很高,特别是在后循环TIA/脑卒中发生后20~30 天内。症状性后循环缺血(包括ECVAS, SS)患者一年后发生脑卒中或者死亡的风险高达5%~11%[5-6]。SS 还会影响同侧上肢的血液供应,从而引发一系列症状或综合征,导致患肢功能障碍甚至截肢。由于这两支血管狭窄各自或并存均可能导致严重后果,临床上需要予以重视。
近年发表的相关指南已开始关注这一问题,认识、加强并规范SS 和ECVAS 的处理是预防脑卒中发病重要且有效的措施之一[7]。目前SS 和ECVAS 的治疗包括药物治疗、外科手术及经皮腔内介入治疗三种方法。近20 年来,随着介入技术进步和器械的不断改进,经皮腔内介入治疗正逐步被作为有指征的SS和ECVAS 患者的首选治疗方式。尽管如此,国内外相关研究有限,对其处理措施也无统一意见[8-10],指南和临床实践之间仍有分歧,一些重要的临床问题仍有待解决,因此迫切需形成共识,指导临床实践。
2 流行病学和筛查人群
2.1 锁骨下动脉狭窄的患病率
国外社区老年SS 患病率约2%,且随年龄增长而升高,70 岁以上人群约占9%[11]。上海社区老年人中(3 133 例,平均年龄69 岁),臂间收缩压差值≥15 mmHg(1 mmHg=0.133 kPa)的人数占1.7%[12],提示患病率与西方国家类似。老年人SS 常合并其他动脉疾病,合并冠状动脉、颈动脉、下肢动脉疾病的比例分别高达50%、29%和27%[13]。老年人SS 往往提示合并心脑血管病,对心血管事件和死亡有预测价值[12, 14-15]。
2.2 颅外椎动脉狭窄的患病率
国外研究表明,在动脉粥样硬化性心血管疾病(ASCVD)患者中(3 717 例,平均年龄60 岁),超声诊断近段VAS >50%的患者达7.6%[16]。一小样本研究表明,在既往发生后循环小脑卒中的患者中,颅脑磁共振血管成像(MRA)发现26.2%的患者椎基底动脉狭窄>50%[3]。有研究对连续2 490 例门诊老年心血管患者的超声检查发现:存在至少一侧椎动脉开口狭窄或闭塞的比例为8.2%,双侧均存在狭窄或闭塞比例为1.4%[17]。因此,在老年人群,尤其是患ASCVD 的人群中,估计ECVAS 的患病率较高,且与后循环脑卒中相关。国内外在这方面的大样本人群数据缺乏,需要尽快开展研究。
2.3 建议筛查人群
基于SS 和VAS 患病人群的特征,本共识不推荐在普通人群中开展筛查。依据已有的指南或者共识推荐,结合临床实践,本共识建议SS/ECVAS 的筛查人群如下:
SS/ECVAS 筛查人群建议
具备以下任何一条的人群,建议作进一步的专业检查。
(1) 有上肢缺血症状,或查体发现左右侧肱/桡动脉搏动明显不对称,或锁骨上窝闻及明显血管杂音,或两侧肱动脉收缩压差值≥10 mmHg;
(2) 有后循环缺血相关神经系统症状或体征的患者;
(3) 40 岁以上ASCVD 患者。
3 临床表现和病理生理学机制
锁骨下动脉主要为上肢供血,左侧锁骨下动脉往往直接起源于主动脉弓,右侧往往起源于无名动脉。椎动脉大部分起源于锁骨下动脉近段,左右二支入颅后汇集到基底动脉,与Willis 环相连并发出大脑后动脉,主要为小脑半球和脑干供血。因此SS主要引起患侧上肢缺血和(或)后循环缺血的相应症状和体征。由于锁骨下动脉与颈外动脉可形成侧支循环,还与椎动脉-基底动脉-Willis 环连接,故慢性闭塞过程中往往侧支循环代偿较好,发生明显症状的少见,但急性闭塞和侧支循环代偿不良者往往导致明显症状和严重临床后果。
SS 好发于左侧,左右侧患病比例约为3:1[18],原因可能系左锁骨下动脉开口与主动脉弓血流方向呈近似直角,血流正面冲击血管壁,容易产生涡流,进而损伤这部分血管。SS 因部位不同所致缺血症状有所差别。狭窄位于椎动脉起源的近心段时,主要表现为上肢缺血和锁骨下动脉窃血综合征,狭窄部位在椎动脉起源的远心段时主要表现为上肢缺血。上肢缺血主要表现为与上肢运动相关的跛行症状,一般表现为患肢运动耐力差,运动时加重,休息后缓解;缺血加重时出现患肢发凉或肩周部位酸胀不适,严重缺血发生时患肢远段苍白、冰冷、麻木、无力,晚期可出现静息痛和局部组织坏死[19]。
锁骨下动脉窃血综合征指SS 近段狭窄所引起的椎基底动脉缺血的临床症候群。当位于椎动脉起源近心段的锁骨下动脉出现严重狭窄或者闭塞时(图1),狭窄远段管腔压力显著下降,椎动脉正向血液停止,由于虹吸作用,后循环的血液通过同侧的椎动脉逆流向锁骨下动脉,导致后循环供血的小脑或脑干有不同程度缺血,如果后循环供血下降超过了对侧椎动脉和颅脑Willis 环后交通支循环的代偿能力,尤其是当上肢活动增加而要求供血增加时,就会出现后循环缺血症状,表现为头晕/眩晕、呕吐、头痛、复视、视觉障碍、肢体/头面部麻木或感觉异常、构音/吞咽障碍、肢体无力或瘫痪、行走不稳或跌倒、短暂意识丧失、Horner 综合征等临床表现。
随着心外科冠状动脉旁路移植术的普及,临床使用起源于锁骨下动脉的左侧内乳动脉作为桥血管日益增多,在这些患者中SS 的患病率大约为5%[19],如果病变未能在冠状动脉外科手术前治疗,或者术后发生了锁骨下动脉近段的狭窄,患者可能会发生冠状动脉-锁骨下动脉窃血,即冠状动脉的血液经内乳动脉桥逆流向锁骨下动脉,导致内乳动脉桥供血区域的心肌缺血,引发心绞痛甚至心肌梗塞。同样,因腹主动脉远段和(或)髂动脉闭塞行腋股动脉旁路外科手术的患者也可能由于近段SS 导致移植血管血流无法维持而跛行加重。另外肾功能衰竭患者使用前臂动静脉瘘行血液透析,如果同侧存在严重SS,则通道血流量不足甚至废用。

图1 锁骨下动脉窃血综合征示意图
椎动脉一般起源于锁骨下动脉近中段,约5%的个体左侧椎动脉直接从主动脉弓发出。两侧椎动脉大小大多不一致,50%个体左侧椎动脉直径大于右侧,25%个体左右椎动脉直径相当,25%个体右侧椎动脉直径大于左侧[20]。椎动脉解剖上一般分为四段,V1~V4 分别为颈段、椎间段、枕段和颅内段,其中V1 段是VAS 的常见受累部位。颈椎关节横向增生及椎间盘组织退行性改变等亦可累及椎动脉,造成椎动脉中段血流受阻,当患者转头时可诱发症状发作[10]。VAS 可直接影响后循环的灌注,并且狭窄部位的易损斑块或血栓也有可脱落进入椎基底动脉,导致TIA 或脑卒中。
4 诊断
全面准确的诊断是选择合理治疗的前提和关键。SS/ECVAS 的诊断应该包括:(1) 病因诊断;(2)解剖诊断;(3)病理生理诊断。
4.1 病因诊断
SS 和VAS 最常见的病因是动脉粥样硬化,其它病因包括血管炎(大动脉炎、巨细胞动脉炎以及其它炎性血管疾病)、先天性畸形、纤维肌性发育不良(fibromuscular dysplasia, FMD),神经纤维瘤病、放射线损伤、血栓形成或栓塞、以及机械性原因(胸廓出口综合征、外伤、主动脉夹层、覆膜支架覆盖等)[11,21-24]。
阜外医院回顾性分析了1999~2017 年连续1 793 例诊断为SS 住院患者的病因构成,动脉粥样硬化、大动脉炎以及其它病因的患者分别为1 543例(86.1%)、232 例(12.9%)和18 例(1.0%)。发病年龄>40 岁的患者中(n=1 594)动脉粥样硬化占95.9%;而在年龄≤40 岁的患者中(n=199)大动脉炎占 90.5%[25]。该研究表明,大动脉炎是国人SS 的重要病因,尤其在年青患者中占很高比例,这与西方国家有明显差别,需要予以重视。
因此,临床上必须鉴别上述病因,尤其是动脉粥样硬化性和大动脉炎性SS/ECVAS。
4.1.1 动脉粥样硬化性病变
动脉粥样硬化性病变诊断标准
需要综合临床病史以及影像学检查结果。如果满足以下至少两项,则考虑患者病因为动脉粥样硬化:
(1) 至少存在1 个动脉粥样硬化的危险因素,包括年龄>40 岁、高血压、糖尿病、高脂血症、吸烟。
(2) 至少符合2 条动脉粥样硬化的影像学特征,包括① 斑块状不规则性狭窄;② 偏心狭窄;③锥形病变;④ 血管钙化;⑤ 病变主要位于动脉开口或近段;⑥ 其他外周动脉粥样硬化的证据[25-26]。
4.1.2 大动脉炎性病变诊断标准
2011 年中华医学会风湿病学分会制定了中国的“大动脉炎诊断及治疗指南”[27],采用了1990年美国风湿病学会的诊断标准。在此基础上日本、欧盟等推出了更新的大动脉炎诊断标准,但在临床实践中发现,如果照搬这些标准,尤其是1990 年的美国标准用于中国患者有一定局限性。我们回顾分析了近半个世纪上千例的临床病例,提出了大动脉炎诊断的阜外标准及综合分型[28](表1),该标准诊断敏感度很高,几乎可以包括所有形式的大动脉炎病损,甚至对超急性期无血管腔影像改变的大动脉炎也可做出诊断。如果大动脉炎诊断成立,受累部位包括SS/ECVAS,可诊断为大动脉炎性病因。
大动脉炎诊断的阜外标准
需满足以下三项,每项须符合其中至少一条:
(1) 发病年龄≤40 岁,女性多见;
(2) 具有血管受累部位的症状和(或)体征(受累器官供血不足、病变血管狭窄相关体征、急性期可出现受累血管疼痛和炎症指标明显升高);
(3) 发现特征性的病变影像,这种病变影像综合分型包括病变部位和病变性质的组合,即任何一型或多型的病变部位加任何一型或多型的病变性质组合,需排除动脉粥样硬化、FMD、先天性动脉畸形、结缔组织病或其他血管炎等所致。
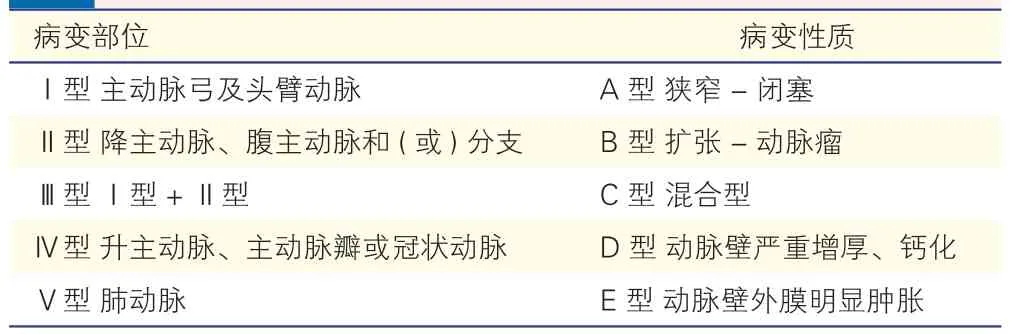
表1 大动脉炎病变综合分型
4.1.3 其他病因
如主动脉夹层、主动脉覆膜支架置入、放射治疗、外伤、血栓等,主要依据相关特征性的临床病史和典型的影像学改变。
4.2 解剖诊断
4.2.1 无创四肢动脉血压检测
同时测量两侧上肢血压是筛查SS 的一个简单、无创、经济的方法。两侧上肢收缩压差值在10 mmHg 以上,提示有上肢动脉病变可能,荟萃分析显示其诊断SS 的敏感度为31%,特异度为91%[15];如果收缩压差值在15 mmHg 以上,其诊断SS 的阳性预测价值和阴性预测价值为100%[18,29]。较低血压一侧一般为患侧,但是双侧病变时两侧血压也有可能差值不大,需结合波形上升加速度和峰值时间延迟诊断[30]。这种无创方法的缺点是敏感度较低。一般下肢收缩压比上肢血压高20~40 mmHg,如果升高大于40 mmHg,伴上肢压力波升支振幅低,波谷至波峰时间延迟,需要警惕双上肢动脉严重狭窄。该方法无法对病变的部位进行准确定位。
4.2.2 双功能超声
超声可观察血管管腔、管壁和血流速度,结合血流频谱进行综合分析和判断,可作为SS 和ECVAS 筛查的首选方法[8,31]。根据管腔大小、狭窄处湍流、流速及患侧椎动脉血流方向,可判断SS 程度,是否存在锁骨下动脉窃血。椎动脉较细小,行程分为多段,彩色多普勒超声探查V1 段相对容易,但V2 段及以上显示困难,对于这些部位的VAS 需要联合其他方法进行诊断。超声检查经济、方便、无创、可反复检查,但高度依赖操作者的技术。
4.2.3 磁共振血管成像或计算机断层血管成像
MRA 或者计算机断层血管成像(CTA)能提供锁骨下动脉及椎动脉的高分辨率图像,和直接动脉内造影相比,对SS 和VAS 的检测敏感度和准确特异度高达90%以上[8,20,29],是常用而可靠的方法。MRA 的优势在于结合脑实质MRI 可以更敏感地检测到后循环的小梗死灶,且不需要复杂的后处理技术。对比剂增强的MRA 对动脉的显影更清楚,能动态显示血流方向,对侧支和窃血显示更直观。MRA 的缺点是放大狭窄程度、无法判断支架再狭窄、幽闭恐惧症、慎用于肌酐清除率低于30 ml/min 等。CTA 可以显示血管腔大小、形态、血流及管壁特征。应用多种后处理技术可以多角度旋转,多方位观察血管的形态、管壁、斑块的性质、狭窄的部位与程度、管腔闭塞及侧支血管,清晰直观地显示血管树与周围组织的关系,对鉴别胸廓出口综合征有重要作用。CTA 的缺点是有放射性、对严重钙化的狭窄判断准确性欠佳、使用碘对比剂对肾功能不全者有顾虑等。
4.2.4 数字减影选择性动脉造影
数字减影选择性动脉造影(digital subtraction angiography, DSA)仍是目前诊断血管狭窄的金标准方法[8],可提供血管狭窄程度、部位、形态、范围等信息,并动态观察椎动脉血流方向, 但DSA 对于管壁病变如斑块成分、附壁血栓等无法准确显示,并且有创,使用碘对比剂有相应的风险,一般在考虑同期行经皮腔内介入治疗时才选用。
4.3 病理生理诊断
4.3.1 具备对应症状或体征
SS/ECVAS 需具备对应狭窄动脉供血区域的症状或者体征,表现为相关区域上肢缺血、后循环缺血或者窃血综合征等,已如前述。
4.3.2 病理生理评估
应用DSA、CTA、MRA、经颅彩色多普勒超声检查、同位素灌注成像和(或)同位素代谢成像等有助于评估狭窄供血区域缺血程度、侧支循环代偿及脑血流储备,确定缺血区或症状是否与狭窄相关[32]。例如,冠状动脉旁路移植术使用左侧内乳动脉桥的患者,出现同位素运动心肌显像前壁缺血性改变,患者左上肢收缩压较对侧低15 mmHg 以上,影像检查发现左锁骨下动脉近端严重狭窄,这种情况的病理生理很可能系内乳动脉桥-锁骨下动脉窃血。由于目前尚无病理生理评估的统一标准,临床实践中需根据患者症状和医院拥有的设备,选择相应的评估方法。
5 治疗
5.1 药物治疗
药物治疗需要依据SS/ECVAS 的病因、并存临床疾病以及血运重建方案的选择而定。
5.1.1 动脉粥样硬化性病变的药物治疗
必须在戒烟、合理膳食、适当运动、减肥等非药物治疗基础上进行,主要针对危险因素,包括降脂、控制血压和降糖治疗等,重点是降脂治疗。依据《中国成人血脂异常防治指南(2016 年修订版)》指导降脂治疗[33]。SS/ECVAS 应归属为极高危人群,建议强化降脂,目标为低密度脂蛋白胆固醇≤1.8 mmol/L。其他危险因素的防治应遵循相应的最新国内外指南。
5.1.2 大动脉炎性病变的药物治疗
主要针对血管壁非特异性炎症,本病在就诊时应该评价炎症是否处于活动期。如果临床上处于活动期,尤其是在急性期,一般主张积极抗炎治疗[34]。多数指南推荐初始治疗为糖皮质激素[27],其剂量及疗程文献推荐并不一致,强烈需要有说服力的循证医学证据。
基于阜外医院几十年的观察研究,我们推荐以下经验供临床参考:醋酸泼尼松初始治疗推荐剂量为每天0.5 mg/kg,或30 mg/d,若一周内C反应蛋白(CRP)和血沉降至正常,炎症症状缓解,则继续维持;如果不达标,剂量可在一周后增至每天1 mg/kg。如仍不能控制炎症,需要联合应用免疫抑制剂。维持治疗一般2 个月以上,随后每个月查CRP 和血沉,如果在正常范围,可以每月减量2.5~5 mg,至10~15 mg/d 时,维持观察3~6 个月。如果CRP 和血沉仍在正常范围,可以考虑继续每个月减量2.5 mg 至5.0~10 mg/d 低剂量维持,小部分患者甚至可以停药,但仍有复发可能[28]。也有研究主张大动脉炎活动期起始治疗即联合应用免疫抑制剂和糖皮质激素来诱导和维持炎症缓解,常用的免疫抑制剂有甲氨蝶呤、硫唑嘌呤、环磷酰胺等[27]。临床上处于非活动期的年轻患者,是否需要予以低剂量维持抗炎治疗有争议,如行血运重建建议适量使用糖皮质激素来降低再狭窄的风险[35-36]。
5.1.3 抗栓治疗
血栓/栓塞是导致SS/VAS 的少见原因之一,急性缺血症状多与之有关,来源于心房颤动的栓塞是主要病因之一。临床上对于这部分患者,如CHA2DS2-VASc 抗凝评分在2 分及以上,应该给予系统性的抗凝治疗,华法林口服维持目标国际标准化比值(INR)2~3[37],或者服用新型口服抗凝药物,如利伐沙班或者达比加群酯等。缺血急性期可给与溶栓治疗,溶栓治疗的方案需遵循相应指南或者共识。
5.1.4 抗血小板治疗
抗血小板治疗是改善ASCVD 预后的根本治疗措施之一,但是目前对于SS/ECVAS 的抗血小板治疗循证医学证据较少,因此临床上一般是基于冠状动脉、颈动脉或者下肢动脉疾病治疗的经验实施抗血小板治疗。对于有症状的患者建议给予积极抗血小板治疗,长期口服阿司匹林(100 mg/d)或者氯吡格雷(75 mg/d)。对于TIA 或者小的缺血性脑卒中,应该在24 小时内给予双联抗血小板治疗,至少维持1 个月[38]。对于动脉粥样硬化性SS/ECVAS 支架治疗的患者常规予以双联抗血小板治疗(阿司匹林100 mg/d + 氯吡格雷75 mg/d)。双联抗血小板治疗术前3~5 天开始,如急诊或术前服用时间不够,可酌情在术前6 ~24 h 内顿服阿司匹林300 mg 和氯吡格雷300 mg。目前大部分SS 患者使用裸支架,一般主张双联抗血小板治疗维持至术后1~3 个月,随后使用一种抗血小板药物长期维持;行椎动脉支架患者大多选用药物支架,一般建议双联抗血小板治疗6 个月以上,最好9~12 个月[39]。大动脉炎性病变的介入治疗以经皮腔内血管成形术(percutaneous transluminal angioplasty, PTA)为主,术后抗血小板治疗一般建议选用一种抗血小板药物即可,维持3~6 个月以上[40-41]。如果这类患者因病情需置入支架,可给予规范的双联抗血小板,注意部分患者术后血压控制不良,或维持使用泼尼松20 mg/d 以上,双联抗血小板有增加出血的风险,要谨慎使用。
5.2 血运重建治疗
血运重建主要包括经皮腔内介入治疗和外科手术治疗,其选择需要根据病因、病情和病变解剖学特点而定。
5.2.1 锁骨下动脉狭窄的血运重建
5.2.1.1 动脉粥样硬化性锁骨下动脉狭窄的血运重建
血运重建策略包括介入治疗和外科手术。介入治疗包括PTA、支架置入术、旋切/旋磨术等,PTA 联合支架置入是最常见的介入方式,术后再狭窄发生率低于单纯PTA[44],应作为粥样硬化性SS 的一线血运重建方案。外科手术策略包括:颈-锁骨下动脉搭桥术、腋-腋动脉搭桥术、颈-腋动脉搭桥术等[45],其中颈-锁骨下动脉搭桥术最常用。外科手术治疗创伤大,需要全麻,适合手术中低危、介入治疗失败的患者。
动脉粥样硬化性锁骨下动脉狭窄的血运重建建议
对于SS 直径狭窄≥70%和(或)跨狭窄收缩压差≥20 mmHg 者,如伴有下述情况时,建议行血运重建治疗[8,10,42-43]:
(1) 有症状;
(2) 无症状但伴有如下任一项者:①计划使用患侧内乳动脉行冠状动脉旁路移植术;②已使用患侧内乳动脉行冠状动脉旁路移植术,如锁骨下动脉近段狭窄导致心肌相应部位缺血;③血液透析患者使用患侧人工动静脉瘘进行透析治疗;④双侧SS 无法通过上肢血压测量准确反映中心动脉实际血压。
介入治疗路径选择方面,股动脉是最常用路径,路径动脉走行迂曲、Ⅲ型主动脉弓患者可选择患侧上肢路径或联合上下肢路径。对于锁骨下动脉近段和开口完全闭塞性病变,经患肢肱/桡动脉路径的成功率明显高于股动脉路径,因为经股动脉路径操作距离较长,导管头端无锚定区,稳定性和支撑力低,导丝常难以通过较硬的纤维帽。支架类型选择上,严重钙化开口处病变应置入支撑力强、定位精确的球囊扩张支架,中远段、长段、尤其病变累及椎动脉和(或)内乳动脉应选择自膨胀支架。如果病变有闭塞时间较长(2 年以上)、闭塞面平坦、闭塞段钙化严重等特征,则介入治疗失败的可能性增加[35]。对这类慢性病变闭塞,如患者有意愿,也符合外科手术适应症,建议改行外科手术治疗。
目前尚缺乏随机临床研究比较介入和外科手术治疗SS 的安全性和中远期临床结果。有研究显示介入治疗狭窄病变和闭塞病变的成功率分别为100%和80%~95%,2 年随访累积通畅率可达90%以上[46]。外科治疗5 年通畅率可达90%以上[47]。围手术脑卒中发生率介入治疗为0.1% ~2.6%,外科治疗为0.9%~2.4%[47-49]。另外,介入治疗可重复多次,但再次外科开放手术往往难度很大。
5.2.1.2 大动脉炎性锁骨下动脉狭窄的血运重建
炎症活动期不宜实施血运重建,一般使用糖皮质激素和(或)免疫抑制剂治疗后炎症活动控制2 个月以上方可考虑血运重建[35-36]。介入治疗适合节段性病变和外科手术高危患者,首选单纯PTA[50-51],支架置入治疗仅适用于PTA 术后反复再狭窄或出现明显影响血流的夹层患者。外科手术自体血管移植管腔通畅率高于介入治疗,但人工血管的中远期通畅率明显低于自体血管移植,手术创伤大,并发症(包括吻合口动脉瘤、脑卒中和心力衰竭等)发生率较高。
5.2.1.3 其他原因锁骨下动脉狭窄的血运重建
如先天性畸形、FMD、放射线损伤以及机械性原因(胸廓出口综合征、外伤、主动脉夹层、覆膜支架覆盖等),如满足上述血运重建指征,应考虑行血运重建治疗。
5.2.2 颅外椎动脉狭窄的血运重建
5.2.2.1 动脉粥样硬化性颅外椎动脉狭窄的血运重建
粥样硬化性ECVAS 程度≥70%,如果给予药物治疗后仍出现缺血事件,或者有后循环缺血症状的患者,建议血运重建。而对于无症状患者,是否进行血运重建尚存在较大争议。如ECVAS 严重影响优势侧椎动脉/孤立椎动脉血供,或者合并严重的前循环动脉狭窄闭塞病变,提供给后循环侧支可能失代偿,对这些无症状患者可考虑进行血运重建治疗[8,16,52-55]。血运重建主要包括外科手术和经皮腔内介入治疗,目前尚缺乏随机对照研究比较两种方法治疗VAS 的安全性和有效性。
ECVAS 腔内介入主要包括PTA 和支架置入术。支架置入术较单纯PTA 能减少血管夹层和急性血管闭塞的发生率,且远期通畅率明显升高[52,56-57],应作为粥样硬化性ECVAS 介入治疗的首选。介入治疗安全性似乎较外科手术好。一项包含27 项ECVAS研究系统分析[56]表明:993 例患者行腔内介入治疗,术后30 天内脑卒中发生率为1.1%,TIA 发生率为0.8%。另外一项囊括1981 ~2011 年42 项VAS 研究的系统分析[52]显示:1 099 例ECVAS 患者中84例接受PTA 治疗,1 015 例接受支架治疗,围术期TIA 和脑卒中发生率分别为1.5%和0.5%,30 天脑卒中和死亡联合发生率为1.1%,死亡率为0.5%(6/1 099),其中仅4 例死亡与脑卒中相关。动脉粥样硬化性ECVAS 支架治疗选用裸支架还是药物涂层支架是临床关注的问题之一。已有多个研究显示药物涂层支架较裸支架中远期通畅率高[52,56-57],应作为首选。裸支架可用于不能耐受较长时间双联抗血小板治疗患者的替代选择。栓塞保护装置的脑保护作用不明确,并且可能增加椎动脉介入治疗中血管痉挛、斑块脱落、血栓形成等的发生风险,因此,除非病变椎动脉管径较大且狭窄处斑块不稳定,否则不推荐应用栓塞保护装置[58-59]。
外科重建方法包括椎动脉内膜剥脱术、椎动脉移位术(移植到颈总动脉、颈内动脉,少部分至甲状颈干和锁骨下动脉)、椎动脉搭桥术、邻近小血管重建椎动脉术及静脉移植重建术等。外科手术并发症包括Horner 综合征、淋巴瘘、喉返神经损伤及切口感染、脑卒中、死亡等,其围手术期并发症发生率报道为2.5%~25.0%,围手术期死亡率为0~4.0%[60-61]。因其创伤较大,并发症发生率高,目前仅推荐作为介入治疗失败的备选方案。
5.2.2.2 大动脉炎性颅外椎动脉狭窄的血运重建
血运重建时的指征选择参照上述动脉粥样硬化性ECVAS。在策略选择方面,顾虑到外科手术治疗创伤较大和炎性疾病本身容易出现并发症[62],介入治疗应作为首选,一般在炎症活动控制2 个月以上方可实施。多数研究表明,PTA 应为首选介入方式。支架系异物,有激活或加重炎症反应可能,再狭窄率较高,支架置入一般仅用作PTA 后夹层严重限制血流、弹性回缩严重或反复再狭窄的替代选择。近年来推出的药物涂层球囊可能有助于降低再狭窄率[41,63]。
少数患者(约6%)椎动脉直接起源主动脉弓或颈总动脉,如狭窄病变满足上述血运重建指征,应考虑行血运重建,术前影像学评估血管开口的解剖特征尤为重要,有利于手术操作、降低并发症发生率。
6 并存冠心病或颈动脉狭窄的处理原则
SS/ECVAS 患者并存冠心病、颈动脉狭窄和其他外周动脉狭窄的患者随着衰老越来越多,心脑血管事件也明显增多。既往脑缺血事件、冠心病、血肌酐升高、间歇性跛行、糖尿病等是并存多发狭窄的主要危险因素。SS/ECVAS 并存冠状动脉或颈动脉狭窄的患者往往表现出相应血管各自狭窄程度相关的缺血症,部分患者症状与严重程度相关。因此,临床上一旦具备相关症状或者体征表现时应该完善影像学检查进一步明确病情,进而指导下一步治疗策略的选择。
并存多发狭窄的处理时机是一个非常重要的问题,需要全面权衡患者身体状况和各方面机能,各器官并存狭窄的风险评分可用来进行各自的病情严重程度评估,然后将所有的评估结果进行综合比较,选择对患者获益最大的、最危急的狭窄先进行干预,然后根据患者情况决定是否需要进行其他并存狭窄的处理。如果并存狭窄有相应的处理指南,则应遵循该指南,避免冲突。并存狭窄的处理分为同期和分期处理,同期处理要充分评估获益与风险的掌控。如果患者状态不稳定,或者使用过多碘对比剂等,潜在并发症发生率会增多,则建议分期处理,先处理症状明显,危害大的病变,再处理症状稳定、危险小的病变。
7 介入治疗围术期管理
介入治疗是目前SS/ECVAS 血运重建治疗的主要手段,除掌握规范的介入操作技术外,也要做好围术期的管理,其核心就是为介入治疗提供保证,并有效降低相关并发症带来的健康损害。SS/ECVAS介入治疗围术期处理与其他血管介入治疗类似之处不再赘述,主要阐述其特殊部分。
术前建议完善弓上动脉的影像学检查和四肢血压的检测,影像学包括超声检查评估狭窄后血流情况(是否有窃血综合征),对于无禁忌证的患者行弓上动脉CTA 或MRA 检查,了解主动脉弓和病变程度、长度、位置以及其他解剖特点,有助于术者制定合适的介入治疗策略。建议术前行颅脑CT平扫或者MRA,明确颅脑是否合并影响介入治疗的疾病,并可为围术期出现可疑的神经系统并发症提供背景对比资料。主管医生病史采集应关注相关缺血症状,体格检查应重点关注上肢桡/肱动脉搏动、锁骨上窝的血管杂音、双上肢的血压差等,可以为病情有变化时术前术后对比提供有价值的临床信息。
规范的药物治疗是介入治疗的前提和保证,详细的论述可以参见本文的药物治疗部分。另外,围术期要做好血压管理,因为SS/ECVAS 介入治疗操作过程中,血流的变化直接影响到后循环的灌注。一般情况下,无明显后循环缺血症状的患者,目标血压维持140/90 mmHg 以下为宜;有后循环缺血症状的患者血压在以不诱发症状的情况下尽量维持至140/90 mmHg 以下[64],介入术前最好不超过150/90 mmHg。建议介入术后血压维持不高于术前水平,波动幅度不超过25%,但不应低于90/60 mmHg。
围术期管理中必须重视介入治疗并发症的识别和处理,除和其他部位介入治疗面临同样的并发症风险外,SS/ECVAS 介入治疗应该关注脑栓塞和高灌注并发症,在SS/ECVAS 介入治疗过程中发生脑栓塞的几率较小,通常在1%以下[65-66],主要是由于介入过程中栓子掉落造成。具体诊治可参考《中国缺血性脑血管病血管内介入诊疗指南2015》[67]。SS/ECVAS 解除后发生脑高灌注综合征罕见,如果出现头痛、恶心、呕吐等症状,尤其是合并收缩压超过150 mmHg 时,建议即刻启动静脉药物降压和脱水降颅压处理,症状不能很快缓解者,需行颅脑CT平扫排除脑出血。
8 随访
研究显示,SS/ECVAS 介入术后再狭窄主要发生于术后1 年内[18,68],建议术后1、3、6 和12 个月随访,随后建议每半年进行1 次随访,以评估有无再狭窄发生。随访时建议常规询问有无患肢和神经系统缺血的症状,检查桡动脉搏动,听诊锁骨上窝血管杂音,如有阳性发现,进一步测量同步双上肢血压和双功能超声、必要时行CTA 或MRA,如需行再次介入治疗的患者可行选择性血管造影检查。合并冠心病和(或)颈动脉狭窄的患者应依据相关指南定期进行相应部位血管的评估。
随访时还应强调生活方式管理和其它ASCVD危险因素的全面控制。生活方式管理包括戒烟限酒、健康饮食、规律运动、控制体重。此外,对非动脉粥样硬化因素引起的SS/ECVAS 的患者,需继续原发病的治疗和进行疗效评估。
学术顾问:高润霖(中国医学科学院阜外医院),杨跃进(中国医学科学院阜外医院),乔树宾(中国医学科学院阜外医院),王继光(上海交通大学附属瑞金医院),王焱(厦门市心血管病医院),李拥军(北京医院),邹英华(北京大学第一医院),董会卿(首都医科大学宣武医院)
专家共识写作组成员(按姓氏拼音排序):车武强(中国医学科学院阜外医院),程康(西安市第三医院),董徽(中国医学科学院阜外医院),董一飞(南昌大学第二附属医院),宫海滨(徐州市心血管病研究所),黄晶(重庆医科大学附属第二医院),贾楠(深圳市人民医院),蒋雄京(中国医学科学院阜外医院),李燕(上海交通大学附属瑞金医院),刘新文(浙江医院),罗建方(广东省人民医院),彭猛(郑州大学第一附属医院),唐礼江(浙江医院),田红燕(西安交通大学第一附属医院),王效增(北部战区总医院),许建忠(上海交通大学附属瑞金医院),杨滨(山西省心血管病医院),余静(兰州大学第二医院),张英(大连医科大学附属第一医院),邹玉宝(中国医学科学院阜外医院)
执笔:蒋雄京,邹玉宝

