蓝桉树皮化学成分及其液化工艺分析
刘勇军,史洪洲,汪扬媚,文 静
(1.凉山州林业科学研究所,四川 凉山 615000;2.凉山州林业和草原局,四川 凉山 615000; 3.凉山州西昌农业科学研究所,四川 凉山 615000)
蓝桉(Eucalyptusglobulus),为桃金娘科(Myrtaceae)桉属(Eucalyptus)植物,高大常绿乔木,树皮灰蓝色,片状剥落,嫩枝略有棱。幼态叶对生,叶片卵形,基部心形,无柄,有白粉,主要生长在我国西南地区(四川、重庆、贵州、广西、云南、西藏)的高原上。阳性生长,适应性强,生长快,耐湿热性较差,能抗污染。多用作行道树、造林树种。不适于低海拔及高温地区,能耐零下低温,木材用途广泛,但略扭曲,抗腐能力强,尤适于造船及码头用材;花是蜜源植物;叶含油量0.92%,制作白树油,供药用,有健胃、止神经痛、治风湿、扭伤等效用;也做杀虫剂及消毒剂,有杀菌作用[1]。
数据表明,到21世纪中叶,世界将发生化石能源危机,利用现代高新生物质能开发利用技术,将环境友好性的生物质材料转化为清洁、经济性和可再生性的生物质能源有着巨大的意义[2]。我国桉树分布广,人工种植林面积已达170万hm2,作为生物质材料的重要组成部分,其生长速度极快,是很好的可再生资源,作为优良的能源树种,有“石油植物”之称。桉树用途广泛,但其加工的综合水平较低,生产中有大量的桉树加工剩余物被直接扔掉或烧掉,不但造成了环境污染,同时也浪费了大量的生物质资源。本文对蓝桉树皮的液化工艺进行了基础探究,将废弃的蓝桉树皮经过液化工艺转化为可再次利用的生物小分子物质,不仅有利于缓解能源危机,保护环境,减少浪费,同时也可为生物质材料的工业应用奠定基础。液化是充分利用天然木质原料潜在价值的一个有效途径,液化产物可用于燃料油、胶粘剂[3-6]、泡沫和模塑材料[7-10]等领域,应用前景十分广阔。本研究以甘油为液化剂,浓硫酸、浓磷酸为催化剂,探讨了温度和催化剂用量对桉树树皮液化行为的影响,得出了蓝桉树皮的最佳液化工艺及其对液化产物主要化学成分的影响。
国内外学者在液化这方面也做了一些研究,有学者用苯酚作为液化剂,如白石信夫、林珍兰、Alam、Doh等,也有学者采用多羟基醇作为液化剂,如Kurimoto、李文昭、Yamada等[11]。他们均采用PEG为液化剂,液化工艺参数,本研究选择甘油作为液化剂,考虑其为农作物秸秆生产酒精的副产品,价格低廉,经济适用。
1 实验材料
取生长于四川农业大学校园内胸径均一的5年生蓝桉5株,取树皮若干,打粉,过标准样筛,保留40~60目样品。制备好的样品放置于电热烘干箱中(103±2 ℃)干燥48 h,待烘干后,装入密闭自封袋备用。
2 实验方法
2.1 苯醇抽提
采用GB 2677.6-1994所述方法,配制苯醇混合液(甲苯:95%乙醇=1:2备用。称取2.00 g~2.005 g(m0)绝干试材,采用定量滤纸包好,放入索氏提取器,加入225 mL苯醇混合液,索氏提取器下接250 mL圆底烧瓶,从沸腾开始计时,抽提4 h至提取仪内苯醇变为无色后取出,将烧瓶内的混合物通过旋转蒸发回收苯醇,再将烧瓶放入烘箱103 ℃±2 ℃烘干称重(m1),烧瓶质量(m2)。将抽提过后的试材收集备用。
(1)
2.1.1 硝酸-乙醇纤维素含量测定法
①硝酸-乙醇的配置:采用浓硝酸、无水乙醇,按1:4的体积比例,先将400 mL的乙醇加入1000 mL的烧杯,再将100 mL的浓硝酸分10次加入,每次加入过程中不断搅拌。
②采用硝酸乙醇法测定纤维素含量,G4玻璃砂芯漏斗于500 ℃烧至质量恒定;精确取绝干样品1.000~1.005 g(m0);放入250 mL洁净干燥的圆底烧瓶中,加入25 mL硝酸-乙醇混合溶液,放入恒温水浴锅,上置回流冷凝管,沸水浴加热1 h,取出溶液用G4砂芯漏斗通过真空水循环抽滤去溶剂,重复三到五次,直至纤维变白,用10 mL硝酸乙醇混合液洗涤,再用热水洗涤至不呈酸性为止,最后用无水乙醇洗涤两次,抽干滤液,将盛有残渣的G4砂芯漏斗放入烘箱,在103±2 ℃烘干至质量恒定,称质量(m1),然后将砂芯漏斗放置于马沸炉在500 ℃下灼烧至质量恒定称量(m2)。

(2)
2.1.2 半纤维素含量测定
根据GB 2677.5-1991所述方法,采用固体烧碱为化学试剂,同通过质量分数配置。
实验步骤:称取苯醇抽提后绝干材料1.000 g~1.005 g(m0),放入250 mL圆底烧瓶,加入150 mL 2%NaOH溶液,放进恒温水浴锅,80 ℃加热3.5 h取出,用布氏漏斗进行抽滤,水洗至无色,后用去离子水进行冲洗,将残渣取出至培养皿放入烘箱,在103±2 ℃下进行烘干m3。滤纸质量m1,培养皿质量m2。

(3)
2.1.3 木质素含量测定
根据GB 2677.8-1993所述方法,采用浓硫酸、蒸馏水为试剂,通过体积比进行配置。
实验步骤:取1.000 g~1.005 g(m0)苯醇抽提后的绝干材料,放入50 mL锥形瓶,加入72%的浓硫酸15 mL,加入磁力转子,后将锥形瓶放在磁力搅拌器上,充分搅拌2 h,将液体用560 mL蒸馏水洗出至 1 000 mL的圆底烧瓶,在加热套上煮沸,上置冷凝回流管,4h后用布氏漏斗真空抽滤,再用500 mL热水洗涤,将残渣移入培养皿,放进鼓风干燥箱103±2 ℃干燥至绝干称重m1,培养皿质量m2,滤纸质量m3。
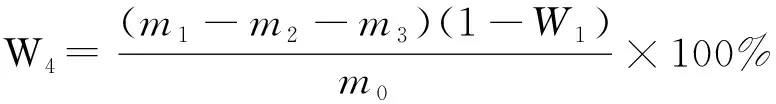
(4)
2.1.4 1%NaOH抽提物
根据GB 2677.5-1991所述方法,配置质量分数为1%的NaOH,称取2.000 g~2.010 g(m0)绝干材料,放入250 mL的平底烧瓶,加入100 mL氢氧化钠溶液,在恒温水浴锅里沸水浴1 h,取出真空抽滤,加入100 mL蒸馏水抽干后再加入50 mL10%的冰乙酸,再次用蒸馏水抽滤至无色无味,转入培养皿放入鼓风干燥箱,103±2 ℃烘干12 h称重得到(m1),滤纸重量(m2),培养皿(m3)。

(5)
2.1.5 热水抽提物
根据GB 2677.4-1993所述方法,取2.000~2.010 g(m0)绝干材料,放入索氏抽提器后加入225 mL蒸馏水,上置循环冷凝装置,下放250 mL圆底烧瓶,在加热炉上煮沸4 h至失去颜色。将残渣放入培养皿烘干称量得(m1),培养皿质量(m2),滤纸质量(m3)。
(6)
2.1.6 灰分含量测定
根据GB 2677.3-1993所述方法,取坩埚洗净,放入马沸炉灼烧至质量恒定,冷却称量记数(m1),取2.000 g~2.010 g(m0)绝干材料,放入坩埚,放进马沸炉在600 ℃保温0.5 h灼烧至恒定质量,称量得(m2)。
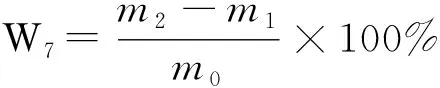
(7)
2.1.7 液化方法
化学药剂:浓硫酸(质量浓度为98%;优质纯GR;四川西陇化工有限公司);甲醇(分析纯AR;成都市新都区木兰镇工业开发区);甘油(分析纯AR;成都市科龙化工试剂厂);二甲基硅油(分析纯AR;成都市新都区木兰镇工业开发区)。
仪器设备:DF-101S集热式恒温加热磁力搅拌器(巩义市予华仪器有限责任公司);101A-3电热鼓风干燥箱(上海实验仪器厂有限公司);电子天平(e=10 d;北京赛多利斯仪器系统有限公司);150 mm规格布氏漏斗,SHZ-Ⅲ循环水真空泵(浙江黄岩黎明实业有限公司)。
实验步骤:称取50 g甘油放入圆底烧瓶,加入1.5 g浓硫酸/浓磷酸作催化剂,待油浴锅温度达到理想温度,放入烧瓶,瓶内放有转子,等甘油到达需要温度时,取10.000 g~10.010 g(m0)绝干材料放入烧瓶,待材料完全湿润开始计时。时间达到后取出烧瓶,将液化物用甲醇转入烧杯,放在磁力搅拌器上搅拌。待搅匀后,用布氏漏斗抽滤,甲醇洗涤至溶液无色,转移残渣至培养皿,质量(m1),滤纸质量(m2),放入烘箱103±2 ℃烘干得到m3。抽滤瓶的滤液通过旋转蒸发仪回收甲醇和分离多元醇液化产物。

(8)
3 实验设计
为了分析液化时间、催化剂、对蓝桉树皮化学成分的影响,设置液化实验的温度分别为80 ℃、100 ℃、 120 ℃、140 ℃、 160 ℃ 和180 ℃,催化剂分别为浓硫酸和浓磷酸,对比分析在相同温度条件下,不同催化剂对蓝桉树皮液化率及其液化残渣化学成分的影响,以探究最佳的液化工艺条件。
4 结果与分析
4.1 桉树树皮化学成分分析
对蓝桉树皮纤维素、半纤维素和木质素等木材主要成分进行测定。实验结果如表1所示,比较蓝桉树皮中纤维素、半纤维素和木质素的含量,蓝桉树皮中木质素的含量最多,占45.37%,其次是纤维素和半纤维素,含量分别为35.65%和18.98%;蓝桉树皮1%NaOH抽提物和灰分含量分别为23.64%和7.50%;蓝桉树皮中苯醇抽提物含量高于热水抽提物含量。
表1蓝桉树皮主要化学成分分析

Tab.1 Analysis of chemical components of Eucalyptus globulus’s bark
4.2 温度对蓝桉树皮液化率的影响
从图1中可知,以浓硫酸为催化剂,蓝桉树皮的液化率随液化温度的升高而增加;在温度为80 ℃时,蓝桉树皮的残渣率为70.6%,当温度升高到180 ℃时,残渣率为17.8%,液化率为82.2%。液化温度在160 ℃时,蓝桉树皮的残渣率为18.52%,温度在180 ℃下的液化残渣率与160 ℃下的残渣率相比,残渣率仅下降了0.72%,说明在160 ℃时的蓝桉树皮的液化率已经较稳定,考虑到试验的经济性,最佳的液化温度为160 ℃。。实验结果表明,最佳液化工艺参数为:液化温度160 ℃,3%的浓硫酸,固液比为1:5,时间为60 min,液化率可达到81.48%(图1)。在浓磷酸的催化下,温度越高残渣率越低,液化率越高,最高出现在1800C,液化时间为60分钟,固液比为1:5,液化率可达50.736%
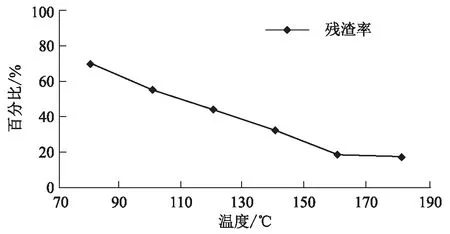
图1 浓硫酸作催化剂时不同液化温度下的液化残渣率Fig.1 Liquefaction residue rate at different liquefaction temperatures with concentrated sulfuric acid as catalyst
由图1可以看出,以浓硫酸作为催化剂,液化温度为80 ℃时,蓝桉树皮液化残渣率为70.60%, 80 ℃后,温度每升高20 ℃,残渣率都下降10%以上,经回归方程分析(回归方程y=-0.6366x+120.53,R2=0.9976)),液化温度在80 ℃到160 ℃区间呈现出一次函数性的特征,温度为160 ℃到180 ℃区间时的液化率相差不大,原因可能是在80 ℃到160 ℃,主要是木质素和半纤维素的降解和液化,纤维素由于其本身的空间结构,很难与化学试剂接触并发生降解反应,当半纤维素和木质素降解到一定程度后,其温度又没达到纤维素的降解条件时,液化率就呈现一个较稳定的状态。
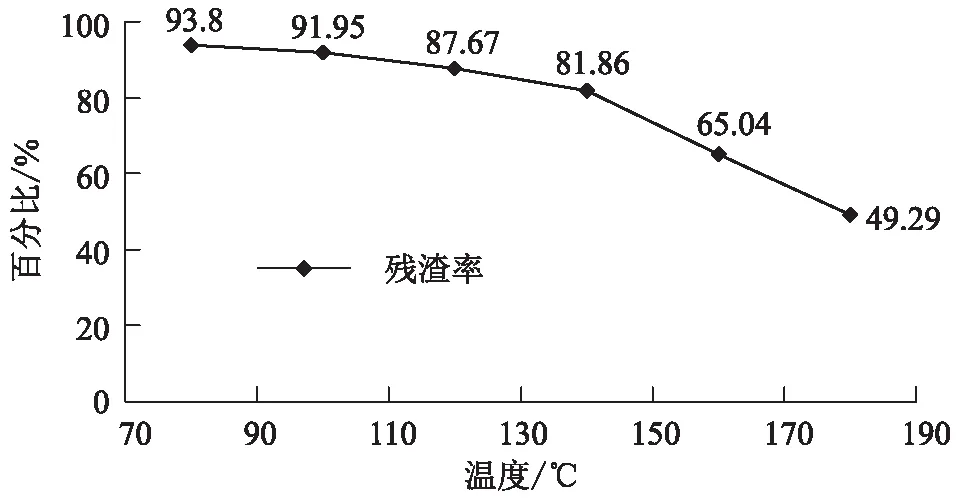
图2 浓磷酸作催化剂时的不同液化温度下的液化残渣率Fig.2 Liquefaction residue rate at different liquefaction temperatures with concentrated phosphoric acid as catalyst
从图2中可知,在浓磷酸的催化下,温度越高残渣率越低,液化率越高,最佳工艺条件为:液化温度180 ℃,液化时间为60 min,固液比为1∶5,液化率可达50.736%。以浓磷酸作为催化剂,温度为80 ℃时,蓝桉树皮的液化残渣率为93.8%,当液化温度增加到100 ℃时,残渣率减少了不到2%,说明在低温范围的时候,温度的增加对其液化率影响不大。直到液化温度增加到140 ℃时,液化残渣率才开始明显下降,在液化温度为180 ℃时液化率刚好达到50%左右。

图3 两种催化剂在不同温度下的液化残渣率对比Fig.3 Comparison of liquefaction residue rates on Eucalyptus globulus bark with two kinds of catalysts at different liquefaction temperatures
实验对两种催化剂在不同温度下的液化残渣率进行对比,从图3中可知,浓硫酸的催化效果明显优于浓磷酸。在液化的开始温度80 ℃时,以浓硫酸作为催化剂的液化效果明显高于浓磷酸,两者残渣率分别为70.6%和93.8%,以浓硫酸为催化剂的蓝桉树皮液化残渣率比以浓磷酸作为催化剂的液化残渣率低23.20%。在实验的各个温度下浓硫酸作催化剂的液化率都优于相同条件下的浓磷酸的催化效果,在160 ℃条件下,浓硫酸作催化剂的残渣率比浓磷酸低46.52%,原因可能是在浓硫酸的催化下,液化产物发生了聚合,由小分子又开始变成大分子化合物,由此可以猜想,假如温度继续升高,有可能残渣率会开始逐渐变大。
4.3 液化对蓝桉树皮化学成分的影响
4.3.1 不同催化剂液化后蓝桉树皮的纤维素含量对比

图4 两种催化剂在不同温度液化后对蓝桉树皮纤维素含量的影响Fig.4 Effect of two kinds of catalysts on cellulose content of Eucalyptus globulus bark at different liquefaction temperatures
由图4可知,经过不同温度液化后,在浓硫酸和浓磷酸催化的条件下,蓝桉树皮中纤维素的含量呈现减小趋势。在液化温度为80 ℃时,以浓磷酸作催化剂液化后,蓝桉树皮液化后纤维素含量为33.42%,以浓硫酸作催化剂液化后,蓝桉树皮液化后纤维素含量为25.69%,与以浓磷酸作催化剂液化相比,浓硫酸催化液化后纤维素含量更低。液化温度从80 ℃上升到180 ℃时,两种催化剂液化后纤维素含量都呈现逐渐下降的趋势并在180 ℃时趋于平缓,这可能说明在此温度区间,蓝桉树皮中纤维素还在逐渐被降解,且在液化温度达到180 ℃时,液化残渣的纤维素含量下降速度明显减少,这说明可能液化产物中纤维素的非结晶区已经逐渐被降解完,剩下的是结构排列紧密的、有规则的结晶区域。
4.3.2 不同催化剂液化后蓝桉树皮的半纤维素含量对比

图5 两种催化剂在不同温度液化后对蓝桉树皮半纤维素含量的影响Fig.5 Effect of two kinds of catalysts on hemicellulose content of Eucalyptus globulus bark at different liquefaction temperatures

图6 两种催化剂在不同温度液化后对蓝桉树皮木质素含量的影响Fig.6 Effect of two kinds of catalysts on lignin content of Eucalyptus globulus bark at different liquefaction temperatures
4.3.3 不同催化剂液化后蓝桉树皮的木质素含量对比
从图5和图6中可知,液化温度从80 ℃上升到180 ℃,以浓磷酸和浓硫酸作为催化剂液化后的蓝桉树皮的木质素含量变化都较小,以浓磷酸作为催化剂液化后蓝桉树皮的木质素含量从34.29%下降到了32.58%,总下降量为1.71%,以浓硫酸作为催化剂液化后的蓝桉树皮的木质素含量从31.41%下降到了27.84%,总下降量为3.57%;实验结果说明浓硫酸作为催化剂对蓝桉树皮的催化作用要优于浓磷酸。木质素含量的总下降量较小的原因是木质素本身紧密的苯环结构,木质素是由愈创木基、紫丁香基和对羟基丙烷基3种主要结构单元通过醚键、C-C键等联接构成的三维网状的复杂聚合物,在液化过程中,其结构很难被打开并和化学试剂发生反应。
4.3.4 液化前后蓝桉树皮主要化学成分对比
在液化温度为160 ℃时,相比于液化前,蓝桉树皮液化后的化学成分发生了较大的变化,蓝桉树皮残渣的纤维素含量减少了17.90%,木质素含量减少了15.99%,半纤维素含量减少了9.19%。由此表明,蓝桉树皮的纤维素含量受液化的影响最为明显,而木质素含量受液化的影响最小。
表2 160℃液化前后主要化学成分的对比
Tab.2 Comparison of chemical components before and after liquefaction of bark at 160℃

成分液化前/%液化后/%差值/%纤维素35.6517.7517.90 木质素45.3729.3815.99半纤维素18.98 9.78 9.19
5 结论
蓝桉树皮纤维素含量为36.65%,半纤维素含量为18.98%,木质素含量为45.37%,苯醇抽提物含量为10.30%,热水抽提物占7.15%,1%NaOH抽提物占23.64%,灰分含量为7.49%;浓硫酸催化效果明显比浓磷酸好;本研究的单因素实验结果得出的较优液化工艺为:以3%浓硫酸为催化剂,液化温度为160 ℃、固液比为1:5,液化率可达82.8%;在该工艺条件下,蓝桉树皮纤维素含量减少了17.90%,木质素含量减少了15.99%,半纤维素含量减少了9.19%。

