IMR重建与iDose4迭代重建技术对肠系膜动脉图像质量影响的对比研究
王帅,李剑,石明国,陈寒,姜文龙,吴志斌,刘从伟,石磊
空军军医大学西京医院 a. 放射科;b. 骨科,陕西 西安 710032
引言
肠系膜动脉等细小动脉CT血管成像已在临床上广泛应用[1],如何在更低辐射剂量的同时获得更高的图像质量一直是人们关注的焦点,以往在肠道CTA成像方面的研究更多是关于扫描参数的优化以及部分迭代重建算法的应用,而全模型迭代重建(Whole Model Iterative Reconstruction,IMR)技术在肠系膜动脉CTA鲜为应用。IMR技术是新一代的迭代重建算法,具有降低图像噪声和提高图像分别率的优点[2],本研究旨在探讨在相同扫描参数以及注射方法情况下,IMR与iDose4技术对肠系膜动脉图像质量影响。
1 资料与方法
1.1 一般资料
将2017年10月至12月在本院Philips Brilliance 256 iCT行肠道CTA扫描的60例患者的动脉期扫描数据纳入本次研究,其中男36例,女24例,年龄34~75岁,扫描结束后对60例患者的动脉期原始扫描数据分别进行IMR重建和iDose4重建。排除标准:碘对比剂过敏者,妊娠及哺乳期妇女,体质量指数BMI>25 kg/m,严重心肝肾功能不全者,有明显呼吸运动伪影者。本次研究经本院伦理委员会同意,所有患者检查前均签署知情同意书。
1.2 仪器与方法
所有患者均用Philips公司的Philips Brilliance 256 iCT螺旋CT扫描仪,患者取仰卧位,扫描范围由膈顶至耻骨联合下方,扫描参数:管电压80 kV,管电流为自动管电流调制技术(Dose Right,Philips Healthcare),球管旋转速度0.75 s/rot,准直128×0.625 mm,矩阵512×512,螺距0.798。扫描技术采用对比剂推送跟踪技术,监测层面为腹主动脉,阈值150 HU,经外周注射对比剂70 mL,流速3.5 mL/s,注射前后分别以3.5 mL/s流速注射40 mL盐水。扫描结束后分别采用IMR和iDose4两种重建算法对动脉期的原始数据进行重建,重建层厚1 mm,层间距0.5 mm,IMR重建Level为1,iDose4重建Level为3。
1.3 图像评价
由两名具有10年以上影像诊断经验的放射科医生在不知实验分组情况下分别对轴位软组织图像、肠系膜上动脉、肠系膜下动脉的最大密度投影(Maximum Density Projection,MIP)和VR图像进行双盲评估,评估内容包括主观评分,数据计算以及客观测量。
1.3.1 主观评分
采用相同的窗宽、窗位,对肠系膜上动脉、肠系膜下动脉的VR、MIP图像进行评估,评价内容包括图像噪声、血管分支显示、血管平滑度、组织结构显示[2]。综合以上图像情况,以4分法对图像质量进行评分,评分标准:1分(差)图像噪声大,肠系膜动脉血管分支显示不佳,血管边缘不光滑,组织结构显示不清,不能满足诊断要求;2分(一般)图像噪声较大,肠系膜动脉血管分支显示能显示清楚,血管边缘欠光滑,组织结构显示欠佳,基本能满足诊断要求;3分(良好)图像噪声尚可,能清晰显示肠系膜动脉血管主干以及分支,血管边缘光滑,组织结构显示清楚,完全能满足诊断要求;4分(优秀)图像噪声小,能够清晰显示肠系膜动脉主干以及细小分支,血管边缘光滑,组织结构显示清晰,对比度好,完全能满足诊断要求。
1.3.2 客观评价
将两组重建后的图像传至Philips IntelliSpace Portal v7.0.6.40181后处理工作站,对动脉期薄层数据进行后处理,测量肠系膜上动脉、肠系膜下动脉CT值,SD噪声以及同层面肌肉CT值,肌肉噪声SD值,以及肌肉的SD值作为背景噪声,测量标记的ROI统一为15 mm2,置于肠系膜上动脉、肠系膜下动脉和同层肌肉层面的中心位置,避开钙化、斑块以及密度不均匀区域,取三次测量平均值,所有数据的测量都在重建图像的相同层面,相同位置进行。计算肠系膜上动脉信噪比(Signal Noise Ratio,SNR)=肠系膜上动脉CT值/肠系膜上动脉噪声SD,对比噪声比(Contrastto-Noise,CNR)=肠系膜上动脉CT值-肌肉CT值/肌肉SD;肠系膜下动脉SNR=肠系膜下动脉CT值/肠系膜下动脉噪声SD,CNR=肠系膜下动脉CT值-肌肉CT值/肌肉SD。
1.4 统计学分析
采用SPSS 19.0统计学软件进行统计学分析,符合正态分布的剂量用表示,不同重建方法图像质量评价内容比较采用配对样本t检验P<0.05为差异有统计学意义。采用Kappa检验观察不同医生间评分结果一致性[3](Kappa值0~0.20一致性低,0.21~0.40一致性一般,0.41~0.6一致性中等,0.61~0.80一致性较高,0.81~1.0一致性高)。
2 结果
本次研究IMR重建组和iDose4重建组患者的一般状况(年龄、BMI、性别)均来自相同的60例肠系膜动脉血管成像的患者。
2.1 图像质量的主观评价结果
两组轴位、冠状位软组织MPR、MIP、VR图像以及组织结构、血管平滑度主观评价,见表1。两名医师对评价一致性中等以上,两组医师对图像质量的主观评分均值IMR重建组高于iDose4重建组,经秩和检验,两名医师对两组图像质量评分差异有统计学意义(P<0.05),见表2。
2.2 两组图像客观评价
所有客观测量数据除肠系膜下动脉SNR外,方差均具有齐性,肠系膜下动脉SNR数据经过校正t检验。采用IMR和iDose4重建算法得到的两组图像在血管强化CT值无明显统计学差异(P>0.05),肠系膜上动脉、肠系膜下动脉,图像噪声IMR重建组<iDose4重建组,IMR重建相对于iDose4重建图像噪声下降,差异有统计学意义(P<0.05),IMR重建组图像噪声相比较iDose4重建组减少47.8%,肠系膜上动脉、肠系膜下动脉SNR,对比噪声比CNR,IMR重建组均大于iDose4重建组,其中肠系膜上动脉SNR,IMR重建组提高49.1%;对比噪声比提高49.4%,肠系膜下动脉SNR,IMR重建组提高52.3%,对比噪声比提高50.9%,差异有统计学意义(P<0.05),详细测量分析数据,见表3。

表1 两名医师对IMR重建组,iDose4重建组两组图像主观质量评价结果一致性检验
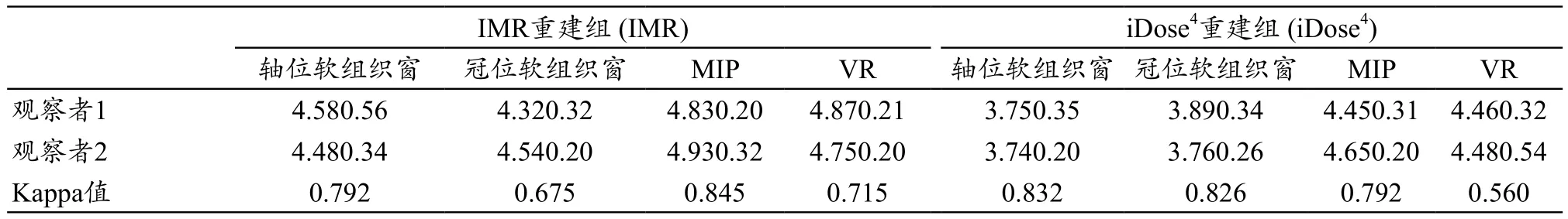
表2 两名医师对IMR重建组,iDose4重建组两组图像主观质量评分结果比较
肠系膜动脉CTA的IMR重建图像和iDose4重建图像,见图1,可以明显看出IMR重建图像噪声小于iDose4图像噪声。IMR全模型迭代重建的肠系膜上动脉、肠系膜下动脉MIP,VR图像,见图2。iDose4迭代重建的肠系膜上动脉、肠系膜下动脉MIP,VR图像,见图3。IMR重建图像远端血管的显示,血管平滑度均高于iDose4重建图像,和两名诊断医生判断相符,符合诊断要求。
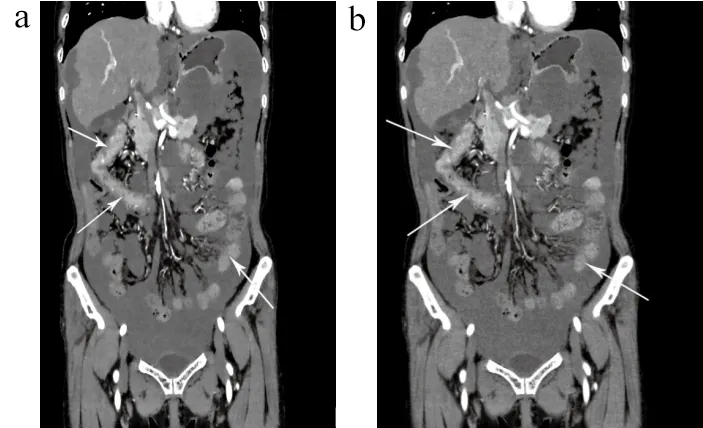
图1 肠系膜动脉CTA的IMR重建图像(a)和iDose4重建图像(b)
3 讨论
肠系膜动脉(SMA,IMA)CT血管成像已在临床上广泛应用,他既可以清晰地显示肠系膜动脉病变管腔内结构特征,还可清晰显示管腔外的解剖结以及闭塞段远端的管腔结构。然而基于CT技术的原因肠系膜CT血管成像的效果依然不能完全满足临床的需求,其中在成像技术方面影响肠系膜动脉CTA图像质量的因素很多,如:对比剂用量、浓度、注射流速、延迟时间、CT扫描及原始数据的重建参数和血管成像的后处理方法等。本次研究固定CT扫描参数、对比剂用量、浓度和注射流速、使用相同的重建层厚和重建间隔,主要探讨基于原始数据的不同重建算法(IMA重建和iDose4重建)对肠系膜动脉(SMA,IMA)图像质量的影响。
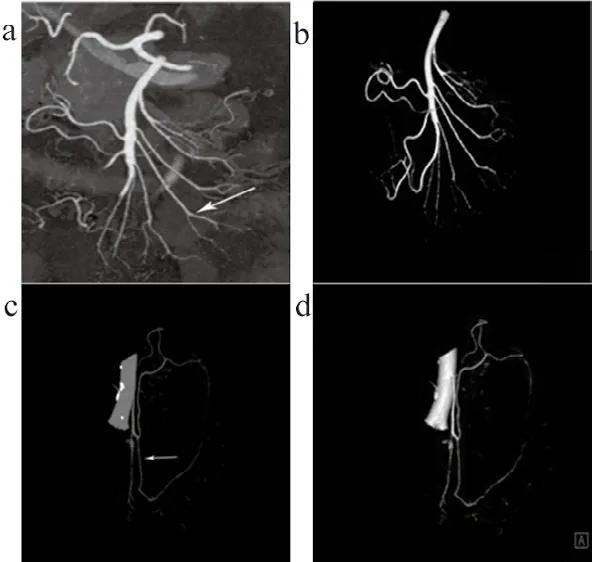
图2 IMR全模型迭代肠系膜重建图像
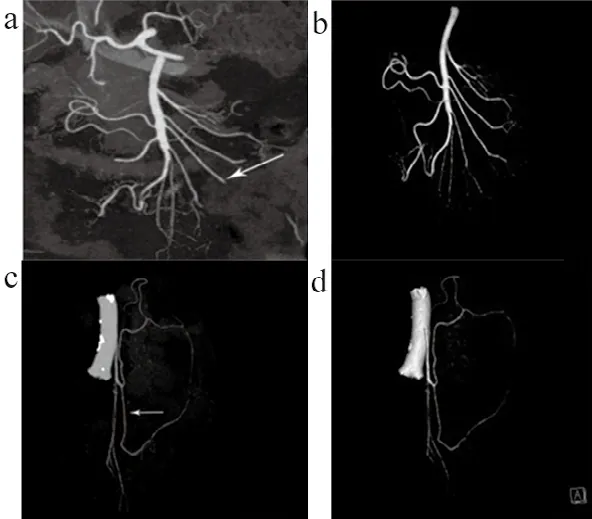
图3 iDose4迭代重建的肠系膜重建图像
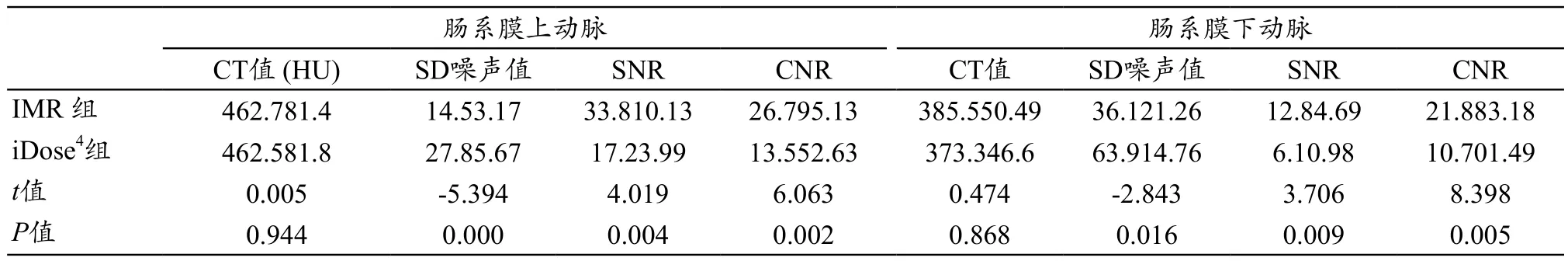
表3 不同重建算法客观评价数据测量结果
本次实验中iDose4重建图像的平均噪声(以肠系膜上动脉为例)为(27.85.67),图像质量噪声明显高于IMR全模型迭代重建组,众所周知,降低kV,CT扫描会导致射线穿透能力减弱[2-3],如果管电流不相应增加,势必会导致图像质量下降[4-5],如何在固定管电压,管电流基础上得到更好的图像质量成为人们关注的焦点,IMR迭代重建技术可以有效解决这一问题。IMR技术是一种结合了三维微平板探测器和Knowledge-based多模型重建算法[6-8],具有强大的降噪功能,以结构化模型为基础,在重建过程中准确建立数据统计模型以及图像统计模型,可在重建过程中准确建立数据统计模型和图像统计模型,通过反复减少原始数据与采集数据间的差异来显示图像[9]。目前常用的iDose4重建技术仍基于滤波反投影法(Filtering Back Projection,FBP)图像进行迭代计算,不可避免地具有FBP重建算法的局限性,降噪能力有限[11-12]。在本次研究中,相同扫描参数情况下,IMR重建组噪声SD值明显低于iDose4重建组,噪声下降百分之47%,而SNR、CNR以及SMA、IMA的VR图像质量评分明显高于iDose4重建组,SNR提高49%,CNR提高48%,提示IMR重建不仅能降低图像噪声,同时能提高图像质量分辨率,与已有报道的IMR重建技术可以提高图像空间分辨率一致[13-16]。
本研究的局限性:① 本次研究在客观评价未计算图像优良指数;② 纳入本次研究的对象均为标准BMI指数患者,未考虑高BMI指数和低BMI指数患者的重建方案的可行性;③ 本次研究未对除肠系膜上动脉、肠系膜下动脉以外的细小动脉如空肠动脉、回肠动脉、胰十二指肠动脉进行评价,因此不能良好展示全肠道动脉系统的重建效果,有待进一步研究。
综上所述在进行肠系膜动脉CTA时,扫描参数、注射方案一致情况下,IMR全模型迭代重建技术相比于iDose4重建可以降低图像噪声,提高图像空间分别率,提高图像质量,满足临床诊断需求。

