IgA肾病伴血脂异常的临床与病理分析
赵圆圆,周广宇*,温 蕊,郭建蕾,王化英,郭硕杰,王雪婷,吴 晨
(1.吉林大学中日联谊医院 肾内科,吉林 长春130033;2.长春市人民医院;3.徐州市第一人民医院 肾内科)
免疫球蛋白A肾病(IgAN)简称为IgA肾病,随着肾活检的广泛开展,发现该病的发病率并不低,占中国原发性肾小球疾病的36.6%[1],既往普遍认为IgA肾病是一种良性病变,随着对该病认识的进一步加深,发现其是一种进展性疾病,大多数患者呈慢性进行性发展,大约有36%的中国成年患者在20年内发展为终末期肾病[2]。研究表明,蛋白尿,低蛋白血症,肾功能下降和高尿酸血症与肾脏疾病进展和预后显著相关[3],国外有文献报道高TG血症,高TC血症是IgA肾病进展的危险因素[4,5],然而,关于不同类型的血脂异常与患者临床表现和病理改变之间关系的报道较少。本文主要通过分析不同类型的血脂异常与IgA肾病患者一般临床资料和Lee氏病理分级的关系,进而探讨血脂异常与IgA肾病预后的关系。
1 资料与方法
1.1 一般临床资料收集2014年6月1日至2018年6月1日入住于我院肾脏病内科,并通过肾活检明确诊断为IgA肾病的患者72例,其中男39例,女33例,平均年龄为37.68±11.30岁。排除标准:①系统性红斑狼疮、过敏性紫癜、肝硬化、乙型肝炎等继发性IgA肾病;②肾组织活检结果提示肾小球数目少于8个的患者;③一般临床资料及肾活检病理资料不全的患者;④肾活检时已行降脂、降尿酸、降尿蛋白治疗的患者。
1.2 方法
1.2.1分组方法 根据中国成人血脂异常预防和治疗指南[6],以满足总胆固醇(TC)≥6.22 mmol/L,甘油三酯(TG)≥2.26 mmol/L,低密度脂蛋白胆固醇(LDL-C)≥4.14 mmol/L和高密度脂蛋白胆固醇(HDL-C)≤1.04 mmol/L中任何1项者定义为血脂异常。将72例患者分为血脂异常组44例和血脂正常组28例;高TG组15例和TG正常组57例;高TC组13例和TC正常组59例。
1.2.2临床资料 收集患者的一般资料:性别、年龄、体重指数,体重指数即体重(单位:kg) 与身高(单位:m) 平方的比值。实验室指标:甘油三酯,胆固醇,高密度脂蛋白,低密度脂蛋白,血尿素氮,血肌酐,血尿酸,24 h尿蛋白定量,血清白蛋白,估算的肾小球滤过率(使用改良的简化MRDR方程计算)。
1.2.3病理学资料 所有肾活检标本均行光镜,免疫荧光和电子显微镜检查,病理分级为Lee氏分级[7]。分别统计各不同分组中病理分级Ⅰ级、Ⅱ级-Ⅲ级、Ⅳ级-Ⅴ级患者的病例数量。
1.3 统计学处理
所有数据用SPSS 22.0统计学软件分析,符合正态分布的计量资料,用均数±标准差来表示,计量资料之间比较采用t检验。计数资料采用百分比表示,计数资料之间比较应用χ2检验。以P<0.05提示为差异有统计学意义。
2 结果
2.1 一般临床资料及指标的比较血脂异常组与血脂正常组相比,血肌酐,血尿酸,血尿素氮,24 h尿蛋白定量,体重指数均一定程度的增高,肾小球滤过率下降,差异有统计学意义(P<0.05);两组在年龄,性别和血白蛋白之间比较差异无统计学意义(P>0.05),见表1。与TG水平正常组相比,高TG血症组血肌酐,血尿酸,血尿素氮,24 h尿蛋白定量和体重指数均增高,肾小球滤过率下降,差异有统计学意义(P<0.05);而两组在年龄、性别、血清白蛋白之间差异无统计学意义(P>0.05),见表2。与TC水平正常组相比,高TC血症组的血肌酐,血尿酸,血尿素氮,24 h尿蛋白定量,肾小球滤过率,年龄,性别和血清白蛋白之间差异无统计学意义(P>0.05),而两组在体重指数之间比较差异有统计学意义,见表3。
2.2 不同分组之间病理分级的比较卡方检验显示IgA肾病血脂异常组与血脂正常组相比较、高TG血症组与TG水平正常组比较、高TC血症组与TC水平正常组比较,Lee氏分级Ⅱ级-Ⅲ级、Ⅳ级-Ⅴ级所占比例高,且其构成比差异有统计学意义(P>0.05)见表4。
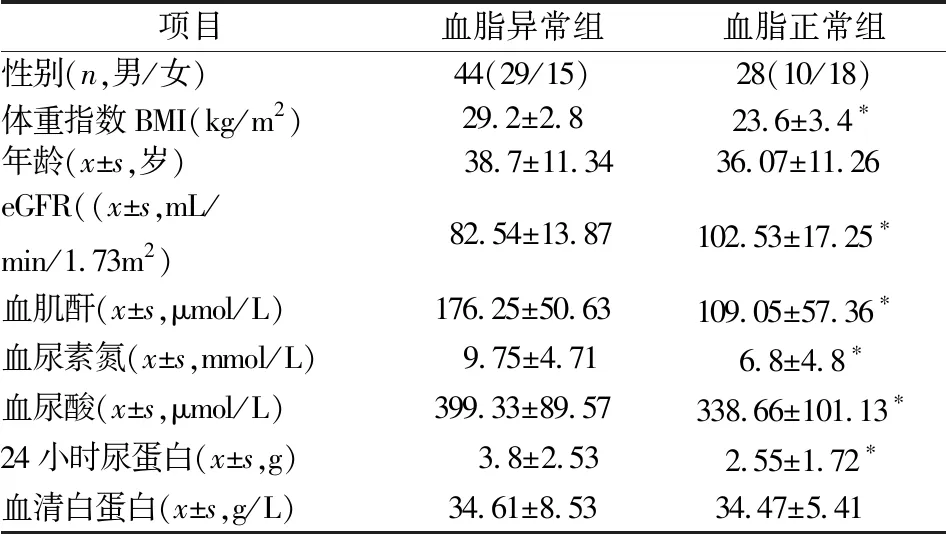
表1 血脂正常组与血脂异常组IgA肾病患者的临床指标比较
注:与血脂正常组比较,*P<0.05
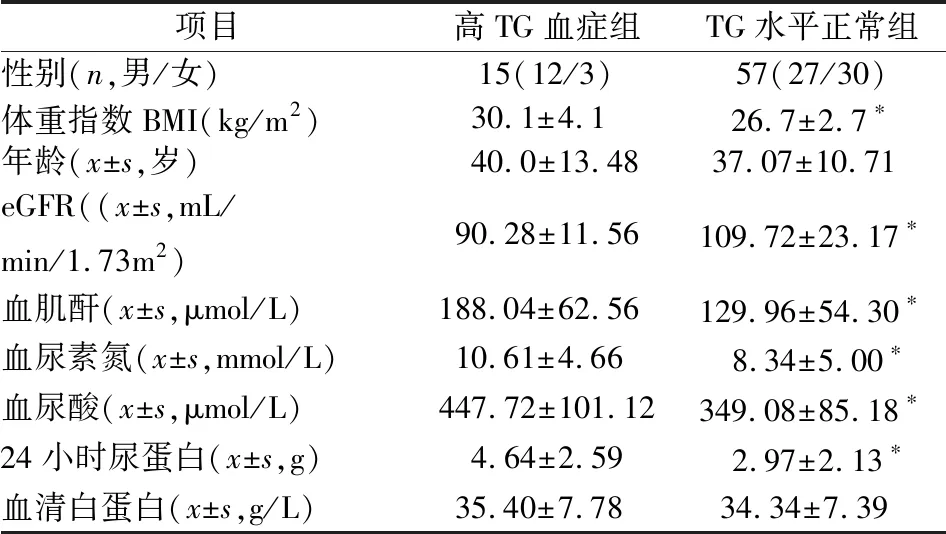
表2 高TG血症组与TG水平正常组IgA肾病患者的临床指标比较
注:与TG水平正常组比较,*P<0.05
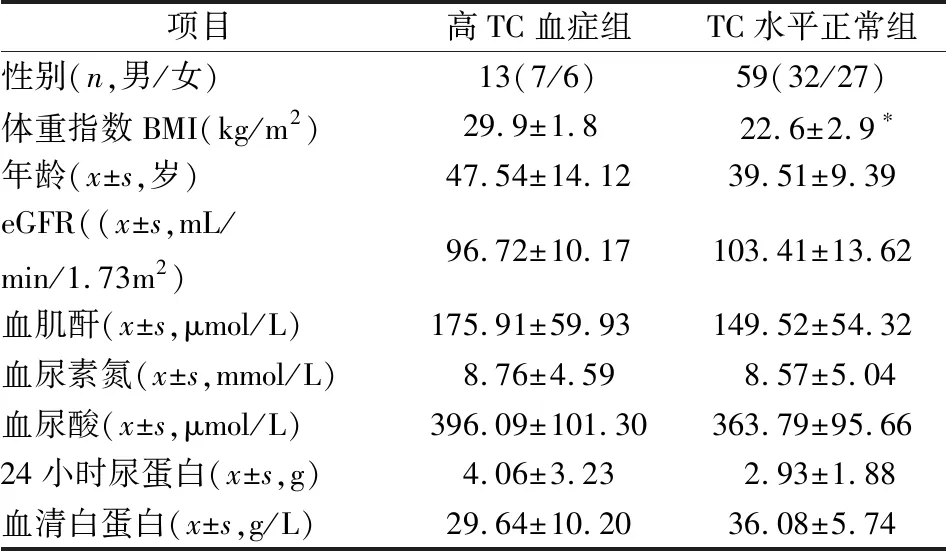
表3 高TC血症与TC水平正常组IgA肾病患者的临床指标比较
注:与TC水平正常组比较,*P<0.05
3 讨论
IgA肾病是循环免疫复合物沉积于肾小球的一种自身免疫性疾病,是我国青年人发生慢性肾衰竭的最常见病因[8]。目前为止,关于IgA肾病的发病病因及发病机制仍然不清,其诊断的唯一标准是肾活检,临床多表现为无症状性血尿和蛋白尿。病理学表现从轻度系膜增生性病变,到大量新月体形成、广泛球性硬化等都可发生。高脂血症在肾脏疾病发生发展中起重要作用[9],是肾小球硬化和小管纤维化的重要原因[10]。研究表明IgA肾病患者合并血脂异常时的肾功能更差,血尿酸和24 h尿蛋白定量更高,而且病理改变的严重程度更重[11]。所以尽早对IgA肾病患者血脂水平的进行干预,可延缓患者疾病进展。
本研究回顾性分析了72例经肾活检确诊的IgA肾病患者的一般临床资料和肾脏病理学资料。结果显示,血脂异常组的体重指数,血尿酸,血尿素氮,24 h尿蛋白和血肌酐均较高,eGFR较低。还发现高TG血症组也有较高的体重指数,血尿酸,血尿素氮,24 h尿蛋白和血肌酐以及较低的eGFR。然而,高TC血症组的患者在血尿酸,血尿素氮,24 h尿蛋白,血肌酐和eGFR与TC水平正常组之间差异无统计学意义。上述结果表明高甘油三酯血症可能与IgA肾病的不良预后关系更密切。Syrjänen[12]等在对IgA肾病患者的随访研究中发现,初次肾活检时高TG血症是IgA肾病的不良预后因素,其可能机制为TG可通过分解成游离脂肪酸,过高的脂肪酸可导致毒性代谢产物的积累,进而引起肾小管上皮细胞及肾小管间质病变。
该研究发现,任何类型的血脂异常与正常血脂水平之间的体重指数存在统计学显著差异。Bonnet[13]等人报道,高体重指数是IgA肾病进展的独立危险因素,会使IgA肾病患者CKD的进展速度增加3倍。然而,高体重指数与肾脏疾病之间强烈的流行病学联系的机制仍不清楚。而BMI的异常升高又是成人血脂异常的独立危险因素[14]。所以,对于IgA肾病患者,可以通过对自我体重的严格控制,降低BMI,从而改善IgA肾病的预后。
研究还发现,血脂异常组与血脂正常组相比,高TG血症组与TG水平正常组相比较,高TC血症组与TC水平正常组相比,Lee氏分级Ⅱ级-Ⅲ级、Ⅳ级-Ⅴ级患者所占比例均较高。这与廖莹[15]等的研究结果一致。Ruan[16]等的研究认为肾小球的硬化与脂质代谢异常有关,脂质能直接引起肾小球硬化和肾小管、肾间质损伤。Frimat[17]等通过对66例IgA肾病患者的随访发现,IgA肾病患者lee氏病理分级I/II级时100%无终末期肾病;Ⅲ、Ⅳ级时14.3%发生终末期肾病,Ⅳ级时66.7%发生终末期肾病;Ⅴ级时87.5%发生终末期肾病。也就是说IgA肾病病理分级越高,预后越差。该研究表明,无论是哪种类型的血脂异常均与不良的IgA肾病预后相关。血脂异常,尤其是高甘油三酯血症时可通过促进肾脏大血管和微血管的硬化而引起肾功能损害。在动物模型,血脂异常可导致肾小球损伤及肾小球滤过率的下降[18]。大鼠经过80周的高胆固醇饮食后可以诱导肾脏间质纤维化[19]。血脂异常引起肾损伤的病理机制主要包括增加LDL在血管内皮的沉积和氧化加速,氧化的LDL被巨噬细胞摄取,在病变区域形成泡沫细胞,泡沫细胞形成后,可产生多种炎性因子、细胞趋化因子以及生长因子,从而引起多种细胞损伤反应[20]。动物实验[21]表明,他汀类药物可以延缓肾间质纤维化程度和肾小球硬化的数量。因此,IgA肾病患者应通过积极改善与疾病相关的脂质代谢异常,进而延缓IgA肾病患者向终末期肾脏病进展。
IgA肾病发病率高,且30%以上的IgA肾病患者在20年内可进展至终末期肾病,中国一项透析移植登记报告的数据显示,中国行血液透析的终末期肾病患者中,有一半以上死于心血管并发症,慢性肾脏病患者并发严重心血管事件的危险性远远超过了肾脏疾病本身所带来的危险。而血脂异常是心血管事件发生的独立危险因素。他汀类药物是最经典有效的降脂药物,一方面可以降低心血管疾病的风险,另一方面可以延缓慢性肾脏疾病的进展。有观察性研究表明,对于终末期肾脏病患者,他汀类药物可以独立地降低全因死亡率和心血管相关死亡率[22],因此对于合并血脂异常的IgA肾病患者应尽早应用他汀类降脂药。
综上所述,血脂异常尤其是高TG血症与较差的IgA肾病预后相关,所以应重视对IgA肾病患者的血脂管理,及时有效的降脂治疗,以改善IgA肾病患者的预后,并延缓其进展为终末期肾脏病,降低心血管事件的死亡率。

