一株黄芪内生真菌甾醇类代谢产物的分离和鉴定
刘 瑞,张弘弛,安志鹏,李 慧
(大同大学生命科学学院,大同大学应用生物技术研究所,山西大同 037009)
甾醇类代谢产物广泛分布于真菌细胞膜中,其化学骨架结构环由26~28个碳原子组成,相对于甾体类化合物,甾醇多了一个饱和或不饱和的仲醇。在自然界中既可以游离态形式存在,也可以结合态形式存在,不同真菌中甾醇的种类与含量不尽相同,主要区别在于C17所连的基团R3不同[1]。
目前生物活性研究发现,甾醇具有降低胆固醇、抗菌、抗肿瘤、调节兔疫系统、抗氧化作用等多种生物学功能。因其特有的生物学性质和物化特点,在医药、食品、化妆品、化工、纺织等行业中都被广泛应用[2]。随着生物技术的进步和天然产品市场的扩大,对甾醇及其衍生物的研究开发将持续扩大,利用真菌提取、分离以及生物合成甾醇及其衍生物的收到很大关注[3]。因而寻找含有丰富的甾醇类物质的新的真菌资源,并从新的真菌资源中提取甾醇及其衍生物有很大的基础理论研究价值和商业价值。
课题组在对黄芪内生真菌代谢产物的系统研究中,发现了多株可产生甾醇类化合物的内生真菌[4-6],前期预实验通过HPLC-MS分析,发现其中一株黄芪内生真菌AR-17-S03,其色谱特征峰密集地出现甾醇类化合物的特征峰,因而,我们对这株内生真菌进行了大量固体发酵,期望寻找到甾醇的新的内生真菌来源。
1 材料与方法
1.1 材料与仪器
内生真菌AR-17-S03[4-6]分离自黄芪根部,纯化菌种保存于大同大学应用生物技术研究所;D101大孔吸附树脂 天津市光复精细化工研究所;硅胶制备型预制板 青岛海洋化工股份有限公司,Sephadex LH-20葡聚糖凝胶 美国GE Healthcare公司;乙腈试剂 色谱纯,德国Sccbayer公司;石油醚、乙酸乙酯、甲醇、氯仿试剂 化学纯,天津博迪试剂厂;改良大米固体培养基 发酵瓶中含大米基质100 g,NaCl 3 g,KNO31 g,谷氨酸钠0.5 g,酵母浸粉10 g,水100 mL,pH7.0。
Waters 600分析高效液相色谱仪 美国Waters公司;Agilent 1200型半制备高效液相色谱 美国惠普公司,Welch material XB-C18柱(4.6 mm×250 mm,5 μm);全自动熔点仪SMP40 英国Bibby-Stuart公司;Bruker maXis 4G UHR-TOF质谱仪 美国安捷伦公司;Bruker ADVANCE 400 MHz核磁共振仪 德国布鲁克公司。
1.2 实验方法
1.2.1 内生真菌的分离和鉴定
1.2.1.1 内生真菌的分离纯化 采用组织学法[7],具体步骤:取黄芪根,无菌水冲洗并晾干水分,用灭菌的剪刀将根部剪成0.5 cm×1 cm节段。表面消毒程序如下:75%乙醇消毒30 s,2%次氯酸钠消毒10 s,75%乙醇润洗20 s,无菌水冲洗2次,然后将组织材料纵切成4~5段,置于已制备的PDA培养基上,放置在28 ℃培养7 d后,观察皿中材料切口处长出菌丝(菌落),采用顶端菌丝挑取法,挑取不同形态的菌落,连续接代几次,即得内生真菌[5],经过HPLC-MS分析,其中一株AR-17-S03可产生大量甾醇类化合物,因此对AR-17-S03进行后续实验。
1.2.1.2 内生真菌的鉴定 将分离到的内生真菌,接种于PDA平板上,27 ℃暗箱培养,从第2 d开始记录生长形态和外观培养性状菌落的大小、颜色、质地、有无气生菌丝体、渗出物等)以及色素产生情况;采用玻片培养法,显微观察孢子梗的分枝状况和孢子形态等情况。DNA提取方法和分子鉴定方法同文献[8],内生真菌平板培养10~15 d后,刮取内生真菌菌落,抽干水分得干燥的菌丝块,液氮中将菌丝块研磨成粉末状,选用CTAB法来提取内生真菌DNA。以提取到的基因组DNA为模板,经PCR扩增后,产物送交三联兄弟生物医药研究(北京)有限公司测序。将测序获得的ITS序列通过Blast比对,采用邻接法(Neighbor-Joining)构建系统发育树。
1.2.2 内生真菌的发酵及代谢产物提取和分离 黄芪内生真菌AR-17-S03斜面培养3 d,以改良查氏液体培养基做种子培养(接种量5%,培养温度28 ℃,振荡培养转速130 r/min,周期7 d),得种子液。大量发酵以改良大米固体培养基发酵[9],10%接种量转接至大米固体培养基,共计40瓶,培养温度28 ℃,静置黑暗培养45 d。发酵结束后,60 ℃直接将发酵培养物烘干,采用前期优化的超声波细胞破碎工艺(超声功率1500 W,超声时间5 s,间隔时间5 s,全程时间5 min),95%乙醇结合微波辅助(微波功率250 W,辐射时间6 min,液固比5∶1)萃取3次,合并提取液浓缩后得粗提物197 g。
经前期分离条件优化,该菌株发酵粗提物的初级分离采用大孔吸附柱色谱,流动相选择水-乙醇系统(体积比分别为100∶0、70∶30、50∶50、30∶70、10∶90),得到6个组分Fr.A-E,后续以L-B(醋酐-浓硫酸)[8]反应确定分离目标,确定Fr.B和C为下一级分离组分。Fr.B经硅胶柱色谱,流动相选择乙酸乙酯-石油醚系统,得sFr.B(1-7),sFr.B2再经硅胶柱色谱洗脱(乙酸乙酯-石油醚系统),得化合物1(615 mg)和化合物2(235 mg),sFr.B2-2经半制备HPLC,以乙腈-水为流动相(1∶2;流速2.5 mL·min-1),得化合物3(121 mg),sFr.B3经Sephadex LH-20凝胶柱色谱,流动相为甲醇(流速1.5 mL/min),得化合物4(239 mg)和化合物5(166 mg),sFr.B4经pTLC色谱(展开系统氯仿∶甲醇∶水=20∶2∶1),刮板回收纯化得化合物6(103 mg);Fr.C经经硅胶柱色谱洗脱(乙酸乙酯-石油醚系统),得sFr.C(1-6),sFr.C2经Sephadex LH-20凝胶柱色谱,甲醇洗脱(流速0.5 mL/min),得化合物7(93 mg),sFr.C3经多次硅胶柱色谱洗脱(乙酸乙酯-石油醚系统),HPLC检测分析,得化合物8(75 mg),sFr.C3-2经半制备HPLC,以乙腈-水为流动相(1∶3;流速3 mL·min-1),得化合物9(19 mg)。
1.2.3 甾醇类代谢产物的结构鉴定 通过物理化学性质分析,结合核磁共振测试(NMR,400 MHz,TMS为内标)和质谱测试(ESI-MS,LC/MSD离子阱XCT质谱仪测定),鉴定分离得到的甾醇类化合物的结构。
1.3 数据处理
使用核磁共振及质谱测试数据库分析甾醇类化合物结构。
2 结果与分析
2.1 内生真菌的鉴定
AR-17-S03宏观菌落观察:单一菌落,初期为白色,渐变为灰色至褐色(黑色);孢子团呈现颗粒状,且聚团;培养基从淡黄色渐变至黑褐色。显微形态观察:菌丝体表面着生有色物,单生菌丝且有隔;直立型单生孢子梗,顶端呈球形;分生孢子无色且串生,呈球形(图1)。经序列测定,ITS序列长549 bp,提交到NCBI进行序列Blast比对,Mega 6.0构建进化树(图2),该菌株与多株Aspergillussp.真菌具有同源性,聚类分析,AR-17-S03和Aspergillusniger以支持率100聚合在一起,综合形态学特征观察和进化树聚类分析,将AR-17-S03鉴定为黑曲霉Aspergillusniger。已有研究发现海藻内生真菌棘孢木霉Richodermaasperellum[10],白木香内生真菌Fimetariellarabenhorstii[11],南海红树林的内生真菌E33和K38[12],南海马尾藻内生真菌No.ZZF36[13],代谢产物都是以甾醇类为主。

图1 菌株AR-17-S03菌落形态

图2 菌株AR-17-S03系统发育分析
2.2 甾醇类代谢产物的结构鉴定
菌株AR-17-S03分离到的9个甾醇类化合物,被鉴定为麦角甾醇(化合物1),过氧化麦角甾醇(化合物2),胆固醇(化合物3),啤酒甾醇(化合物4),23-甲基麦角甾-7,22-二烯-3β,5α,9α-三醇(化合物5),5α,8α-表二氧麦角甾-6,9(11),22-三烯-3β-醇(化合物6),5α,8α-表二氧-23-甲基麦角甾-6,22-二烯-3β-醇(化合物7),麦角甾-4,6,8(14),22-四烯-3-酮(化合物8),3β,5α-二羟基麦角甾-7,22-二烯-6-酮(化合物9)(图3)。代谢产物以麦角甾醇类为主,研究结果与文献[10-13]类似,说明真菌有着相同的甾醇代谢合成途径,而在具体甾醇类别,本研究与已有的研究有很大的差异性,说明内生真菌通过与不同寄主植物的长期共生,次级代谢途径的关键酶体系出现差异性。
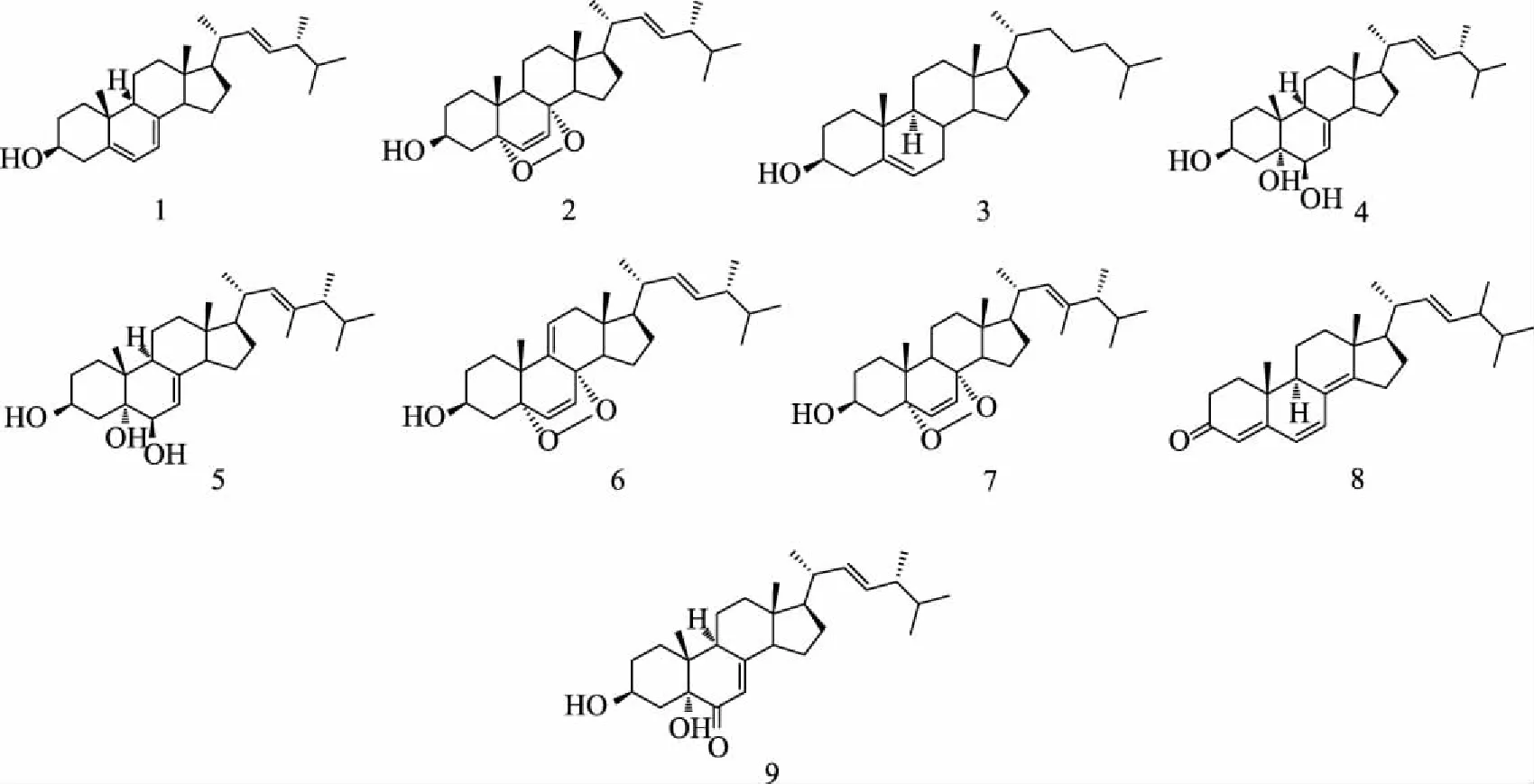
图3 黄芪内生真菌AR-17-S03的代谢产物
化合物1,白色针状结晶,mp.155~157 ℃。ESI-MS m/z 397.2[M+H]+。1H NMR(CDCl3)核磁谱图中呈现了麦角甾醇类(含有3-β-羟基)的特征:3-OH的邻位氢δ 3.66(1H,m,H-3),2个分子末端甲基氢δ 0.65(3H,s,H-18),0.97(3H,s,H-19),4个单裂分的甲基氢δ 1.06(3H,d,J=6.5 Hz,H-21),0.94(3H,d,J=7.0 Hz,H-26),0.84(3H,d,J=7.0 Hz,H-27),0.96(3H,d,J=7.0 Hz,H-28)和4个烯氢δ 5.20(1H,dd,J=15.1,6.9 Hz,H-22),5.21(1H,dd,J=15.1,7.4 Hz,H-23),5.40(1H,s,H-6),5.59(1H,s,H-7)。13C NMR及DEPT-135(CDCl3)核磁谱图中呈现了28个碳,其中6个烯碳δ139.9(C-5),119.7(C-6),116.4(C-7),141.5(C-8),135.7(C-22),131.9(C-23);1个连氧碳δ 70.6(C-3),6个甲基碳δ12.0(C-18),17.7(C-19),21.2(C-21),19.8(C-26),19.7(C-27),17.4(C-28),其他碳 δ 38.5(C-1),31.9(C-2),41.0(C-4),46.2(C-9),37.1(C-10),21.0(C-11),39.2(C-12),42.9(C-13),54.7(C-14),23.1(C-15),28.4(C-16),55.8(C-17),40.5(C-20),42.8(C-24),33.2(C-25)。与文献[14]核磁数据对比,化合物1鉴定为麦角甾醇。
化合物2,白色针状结晶,mp.180~182 ℃。ESI-MS m/z 429.4[M+H]+和451.4[M+Na]+。1H NMR(CDCl3)核磁谱图中也呈现了麦角甾醇类(含有3-β-羟基)信号:3-OH的邻位氢δ 3.97(1H,m,H-3),2个分子末端甲基氢0.81(3H,s,H-18),0.88(3H,s,H-19),4个单裂分的甲基氢δ 1.00(3H,d,J=6.8 Hz,H-21),0.84(3H,d,J=6.8 Hz,H-26),0.82(3H,d,J=7.0 Hz,H-27),0.90(3H,d,J=7.0 Hz,H-28)和4个烯氢δ 5.22(1H,dd,J=15.2,7.6 Hz,H-22),5.11(1H,dd,J=15.1,8.0 Hz,H-23),6.23(1H,d,J=8.6 Hz,H-6),6.48(1H,d,J=8.6 Hz,H-7)。13C NMR及DEPT-135(CDCl3)核磁谱图中呈现了28个碳,4个烯碳δ 135.0(C-1),130.7(C-1),135.4(C-22),132.1(C-23);2个连氧季碳δ 82.5(C-5),79.4(C-8);1个连氧次甲基碳δ 67.2(C-3),6个甲基碳δ 12.9(C-18),17.9(C-19),21.2(C-21),19.6(C-26),17.5(C-27),20.2(C-28),其他碳δ34.1(C-1),30.9(C-2),37.8(C-4),50.9(C-9),37.1(C-10),20.8(C-11),39.3(C-12),44.3(C-13),52.1(C-14),23.5(C-15),28.4(C-16),56.1(C-17),40.0(C-20),42.7(C-24),32.9(C-25)。与文献[15]核磁数据对比,化合物 2 鉴定为过氧化麦角甾醇。
化合物3,白色针状晶体,mp.147~149 ℃。ESI-MS m/z 387.2[M+H]+。1H NMR(CDCl3)核磁谱图中呈现了5个甲基氢δ 0.71(3H,s),1.04(3H,d,J=6.4 Hz),0.87(3H,d,J=7.0 Hz),0.86(3H,d,J=7.0 Hz),0.95(3H,d,J=6.4 Hz),1个双键的烯氢δ 5.38(1H,s),1个连氧碳上的氢δ 3.53(1H,m)。13C NMR及DEPT-135(CDCl3)核磁谱图中呈现了27个碳原子,2个烯碳δ 140.8(C-5),121.6(C-6),1个连氧碳δ 77.9(C-3),5个甲基碳δ22.9(C-27),22.6(C-26),19.0(C-21),18.9(C-19),12.1(C-18),其他碳δ37.4(C-1),32.0(C-2),42.2(C-4),31.9(C-7),34.0(C-8),50.2(C-9),36.9(C-10),21.3(C-11),39.9(C-12),46.0(C-13),56.7(C-14),24.4(C-15),28.3(C-16),56.2(C-17),36.0(C-20),36.4(C-22),23.2(C-23),39.9(C-24),29.3(C-25)。与文献[16]核磁数据对比,化合物3鉴定为胆固醇。
化合物4,白色针状结晶,mp.245~247 ℃。ESI-MS m/z 431.4[M+H]+。1H NMR(CDCl3)核磁谱图中也呈现了麦角甾醇类(含有3-β-羟基)信号:3位羟基邻位氢δ 4.07(1H,m,H-3),6位羟基邻位氢3.60(1H,d,J=4.8,H-6),2个分子末端甲基氢0.60(3H,s,H-18),1.09(3H,s,H-19),4个单裂分的甲基氢δ 1.04(3H,d,J=6.5 Hz,H-21),0.81(3H,d,J=7.0 Hz,H-26),0.83(3H,d,J=7.0 Hz,H-27),0.92(3H,d,J=7.0 Hz,H-28)),3个烯氢δ 5.34(1H,dd,J=4.8,2.4 Hz,H-7),5.20(1H,dd,J=15.0,8.0 Hz,H-22),5.25(1H,dd,J=15.0,7.5 Hz,H-23)。13C NMR及DEPT-135(CDCl3)核磁谱图中呈现了28个碳原子,4个烯碳δ 115.0(C-7),143.9(C-8),132.2(C-22),135.8(C-23),3个连氧碳δ 67.4(C-3),76.3(C-5),72.8(C-6),6个甲基碳δ 12.4(C-18),18.3(C-19),19.7(C-21),19.8(C-26),21.2(C-27),17.5(C-28),其他碳δ 32.7(C-1),30.5(C-2),39.6(C-4),43.6(C-9),37.3(C-10),22.2(C-11),39.5(C-12),43.8(C-13),55.1(C-14),23.1(C-15),28.7(C-16),56.2(C-17),40.7(C-20),43.1(C-24),33.3(C-25)。与文献[17]核磁数据对比,化合物4鉴定为啤酒甾醇。
化合物5,无色晶体,ESI-MS m/z 445.4[M+H]+。1H NMR(CDCl3):δ4.08(1H,m,H-3),3.61(1H,d,J=4.8 Hz,H-6),5.37(1H,dd,J=4.8,2.4 Hz,H-7),0.61(3H,s,H-18),1.09(3H,s,H-19),0.99(3H,d,J=6.6 Hz,H-21),4.91(1H,d,J=10.0 Hz,H-22),0.83(3H,d,J=7.0 Hz,H-26),0.80(3H,d,J=7.0 Hz,H-27),0.91(3H,d,J=7.0 Hz,H-28)1.49(3H,s,H-29)。13C NMR(CDCl3):32.7(C-1),30.8(C-2),67.8(C-3),39.3(C-4),76.2(C-5),72.5(C-6),115.0(C-7),143.7(C-8),43.8(C-9),37.3(C-10),22.2(C-11),39.5(C-12),43.8(C-13),54.9(C-14),22.7(C-15),28.0(C-16),56.0(C-17),12.4(C-18),18.3(C-19),39.8(C-20),21.6(C-21),131.5(C-22),135.2(C-23),43.6(C-24),33.7(C-25),19.7(C-26),19.4(C-27),17.2(C-28),13.3(C-29)。与文献[18]核磁数据对比,化合物5鉴定为23-甲基麦角甾-7,22-二烯-3β,5α,9α-三醇。
化合物6,白色粉末,ESI-MS m/z 427.3[M+H]+。该化合物核磁数据如下:1H NMR(CDCl3):4.01(1H,m,H-3),6.28(1H,d,J=8.8 Hz,H-6),6.60(1H,d,J=8.2 Hz,H-7),5.43(1H,dd,J=6.0,2.0 Hz,H-11),0.75(3H,s,H-18),1.08(3H,s,H-19),1.00(1H,d,J=6.8 Hz,H-21),5.24(1H,dd,J=15.2,7.6 Hz,H-22),5.13(1H,dd,J=15.1,8.0 Hz,H-23),0.83(3H,d,J=6.8 Hz,H-26),0.82(3H,d,J=7.0 Hz,H-27),0.91(3H,d,J=7.0 Hz,H-28)。13C NMR(CDCl3):32.9(C-1),30.7(C-2),66.8(C-3),37.0(C-4),82.7(C-5),135.3(C-6),130.7(C-7),78.9(C-8),142.6(C-9),37.8(C-10),119.8(C-11),41.1(C-12),43.6(C-13),51.1(C-14),21.3(C-15),28.0(C-16),56.5(C-17),13.1(C-18),20.9(C-19),37.2(C-20),24.3(C-21),135.9(C-22),131.2(C-23),47.7(C-24),31.8(C-25),19.8(C-26),20.1(C-27),17.2(C-28)。与文献[19]核磁数据对比,化合物6鉴定为5α,8α-表二氧麦角甾-6,9(11),22-三烯-3β-醇。
化合物7,白色无定形粉末,ESI-MS m/z 443.4[M+H]+和465.4[M+Na]+。该化合物核磁数据如下:1H NMR(CDCl3):3.97(1H,m,H-3),6.24(1H,d,J=8.6 Hz,H-6),6.50(1H,d,J=8.6 Hz,H-7),0.83(3H,s,H-18),0.89(3H,s,H-19),0.99(1H,d,J=6.8 Hz,H-21),4.86(1H,d,J=10.0 Hz,H-22),0.85(3H,d,J=6.8 Hz,H-26),0.81(3H,d,J=7.0 Hz,H-27),0.92(3H,d,J=7.0 Hz,H-28),1.48(3H,s,H-29)。13C NMR(CDCl3):33.9(C-1),30.8(C-2),66.9(C-3),37.8(C-4),82.5(C-5),135.2(C-6),130.7(C-7),79.5(C-8),50.9(C-9),37.3(C-10),20.7(C-11),39.3(C-12),44.3(C-13),52.0(C-14),23.5(C-15),28.3(C-16),55.8(C-17),12.9(C-18),17.6(C-19),40.2(C-20),21.3(C-21),135.4(C-22),132.3(C-23),42.8(C-24),32.9(C-25),19.5(C-26),17.4(C-27),19.9(C-28),12.9(C-29)。与文献[20]核磁数据对比,化合物7鉴定为5α,8α-表二氧-23-甲基麦角甾-6,22-二烯-3β-醇。
化合物8,淡黄色针状结晶,mp.118~120 ℃。ESI-MS m/z 391.1[M-H]-。比较其1H NMR、13C NMR与化合物1的核磁数据(位移、耦合常数)发现,H-3的峰消失,多了1个环内共轭酮羰基碳δ 198.9(C-3),判定化合物8是3位羟基氧化的甾酮。1H NMR(CDCl3)核磁谱图中呈现了5个烯氢δ 5.69(1H,s,H-3),6.06(1H,d,J=10.4 Hz,H-3),6.68(1H,d,J=10.4 Hz,H-7),5.18(1H,dd,J=14.8,7.8 Hz,H-22),5.33(1H,dd,J=14.8,7.8 Hz,H-23),6个甲基氢δ 0.93(3H,s,H-18),1.04(3H,s,H-19),1.09(3H,s,H-21),0.80(3H,s,H-26),0.85(3H,s,H-27),0.92(3H,s,H-28)。13C NMR及DEPT-135(CDCl3)核磁谱图中呈现了28个碳原子,8个烯碳122.5(C-4),124.6(C-5),124.6(C-6),133.3(C-7),124.0(C-8),155.5(C-14),135.3(C-22),132.3(C-23),6个甲基碳18.5(C-18),16.6(C-19),20.5(C-21),19.9(C-26),20.3(C-27),17.6(C-28),其他碳δ 34.1(C-1),33.9(C-2),43.7(C-9),35.9(C-10),19.0(C-11),35.7(C-12),44.3(C-13),24.8(C-15),27.8(C-16),55.2(C-17),39.4(C-20),42.7(C-24),32.6(C-25)。与文献[21]核磁数据对比,化合物8鉴定为麦角甾-4,6,8(14),22-四烯-3-酮。
化合物9,白色粉末,ESI-MS m/z 429.4[M+H]+。该化合物核磁数据如下:1H NMR(DMSO-d6):3.72(1H,m,H-3),5.45(1H,s,H-7),0.55(3H,s,H-18),0.82(3H,s,H-19),0.89(3H,d,J=6.5 Hz,H-21),5.19(1H,dd,J=15.4,8.2 Hz,H-22),5.29(1H,dd,J=15.4,7.6 Hz,H-23),0.81(3H,d,J=7.0 Hz,H-26),0.94(3H,d,J=7.0 Hz,H-27),0.18(3H,d,J=7.0 Hz,H-28),4.39(1H,d,J=5.0 Hz,3-OH),5.15(1H,s,5-OH)。13C NMR(DMSO-d6):31.2(C-1),30.4(C-2),65.9(C-3),38.7(C-4),75.8(C-5),198.1(C-6),119.3(C-7),159.7(C-8),42.4(C-9),39.9(C-10),21.2(C-11),36.7(C-12),43.8(C-13),54.9(C-14),22.5(C-15),28.1(C-16),55.3(C-17),12.4(C-18),16.3(C-19),40.5(C-20),20.7(C-21),131.0(C-22),135.2(C-23),43.2(C-24),32.7(C-25),19.8(C-26),19.4(C-27),17.1(C-28)。与文献[20]核磁数据对比,化合物9鉴定为3β,5α-二羟基麦角甾-7,22-二烯-6-酮。
3 结论
本研究基于这一出发点,发现了一株可以产生系列甾醇类代谢产物的黄芪内生真菌Aspergillusniger编号AR-17-S03,其产生的甾醇类代谢产物以麦角甾醇类为主,主要类别有麦角甾醇类、5α,8α-表二氧类麦角甾醇类、3-酮和6-酮类麦角甾醇类。这些甾醇类代谢产物的分离拓展了甾醇的新的来源,未来我们将进一步开展这些甾醇构效关系的研究,进一步提出功能性甾醇的结构修饰方案,为制备具有生理功能性甾醇衍生物提供资源准备。

