用自制单克隆抗体建立检测NGAL的胶体金方法
郭会灿 李君华 武晓莉 张丽媛 徐冬梅
(石家庄职业技术学院,石家庄 050000)
人中性粒细胞明胶酶相关脂质运载蛋白(Neutrophil gelatinase-associated lipocalin,NGAL),是Lipocalin 家族的成员,NGAL发现于中性粒细胞中的过氧化物酶的阴性颗粒中[1],经研究发现在人体盲肠、胃、子宫、唾液腺等多种组织器官中的表达都很稳定。研究显示,NGAL参与了炎症、免疫应答、趋化作用、信号转导的过程,并与多种肿瘤的发生发展有密切关系,NGAL在急性肾损伤早期的患者尿液中含量会迅速升高,因此作为新型肾损伤标志物受到广泛的关注[2]。国内外医院和生物医药公司对NGAL诊断研究正处在白热化阶段,虽然有部分公司已经取得一定成果,但多数停留在临床研究阶段。目前只有丹麦BioPorto公司生产的NGAL试剂盒通过了欧盟认证并批准生产销售[3]。国外进口NGAL检测试剂盒在价格上必然昂贵,一方面给患者增加了诊疗成本,同时也限制了该项检测在临床上的普及和应用。随着即时检测(POCT)[4]和电化学发光技术的飞速发展[5],这些技术以高特异、高灵敏度的抗体原料为基础,成为医学研究的一个热门方向。本文制备了高灵敏度、高特异性的NGAL单克隆抗体,在此基础上初步建立了NGAL免疫胶体金层析试纸条检测方法,为临床早期肾损伤诊断提供了快速、便捷、准确的检测方法。
1 材料与方法
1.1材料
1.1.1实验材料 弗氏佐剂(包括完全和不完全)、抗体亚型检测试剂盒购自Sigma公司;硝酸纤维素膜、PVC板、玻璃纤维膜、吸水垫等购自MILLI-PORE;HRP羊抗小鼠IgG购自北京中杉金桥;重组人NGAL(rhNGAL)为本实验室自表达;其他化学试剂为分析纯;BALB/c小鼠由本实验室饲喂;S/P20小鼠骨髓瘤细胞由本实验室传代保存。
1.1.2临床样本 临床样本为患者尿液,来自河北医科大学第二医院肾内科门诊,经酶联免疫吸附试剂盒检测后的已知结果样本。
1.2方法
1.2.1NGAL单克隆抗体的制备[6]选用5只BALB/c小鼠,采用背部多点免疫的方法,首次采用弗氏完全佐剂进行免疫,以后每2周采用弗氏不完全佐剂进行免疫。通过细胞融合技术制备杂交瘤细胞株,经有限稀释法筛选特异性抗NGAL单克隆抗体。将建株细胞混合石蜡注入小鼠腹腔,诱生腹水获得大量单一的单克隆抗体。经过硫酸铵沉淀和Protein A柱两步骤对抗体进行纯化即得到纯化的NGAL单克隆抗体,分别采用Sigma的亚型试剂盒对抗体进行亚型测定,间接ELISA法测定抗体效价,双抗夹心法进行配对测定。
1.2.2金标NGAL抗体的制备 在离心管中加入10 ml 胶体金溶液,再加入0.1 mg抗NGAL单克隆抗体,振荡混匀后调pH至8.8,在室温下搅拌1 h,用0.1%BSA溶液作为封闭液,继续搅拌1 h,将上述溶液用超低温离心机4℃下8 000 r/min离心30 min,保留下层沉淀,用1 ml pH7.5的10 mmol/L的磷酸缓冲液(含0.3%PC300、0.5%BSA%、2%蔗糖)重悬即得金标NGAL抗体溶液,4℃保存备用。
1.2.3金标NGAL抗体偶联物的质量鉴定
1.2.3.1紫外-可见分光光度计鉴定 在400~600 nm 的可见范围内,用紫外-可见分光光度计分别对金标NGAL抗体偶联物和胶体金粒子进行扫描,由于抗体表面会吸附胶体金粒子,体积变大,如果偶联成功,在最大吸收波长及峰形上胶体金粒子会有变化,也就能验证金标NGAL抗体偶联物是否偶联成功。
1.2.3.2透射电镜鉴定 通过透射电镜对金标NGAL抗体偶联物及胶体金粒子进行粒径测定,在电镜相同缩放比例下,查看两者的粒径和颗粒表面的变化情况,来判断是否偶联成功。
1.2.3.3试纸条鉴定 将羊抗鼠的二抗1∶10稀释,以10.0 μl的量分别在NC膜上划线,并标记位置,将其在干燥箱静置干燥。分别在划线处滴加金标NGAL抗体(1∶10稀释)及0.01 mol/L 磷酸缓冲液(作为阴性对照),5 min后观察试验结果。若在滴加金标NGAL抗体的划线处出现明显的红色线条,且滴加磷酸缓冲液的划线处为无色,则表明金标NGAL抗体具有活性;若划线处均不显色,则表明金标NGAL抗体失活或没有偶联成功。
1.2.4NGAL胶体金试纸条的制备 将结合垫预先处理后备用,用移液器吸取金标NGAL抗体,均匀涂布在结合垫上,干燥即得;适量的羊抗鼠IgG和配对的抗NGAL抗体用划膜仪分别喷涂在NC膜(30 cm×2.5 cm)上,作为C线质控线和T线检测线,干燥备用。NGAL胶体金试纸条由样品垫、结合垫、NC膜和吸水垫按图1所示的顺序组装而成。
1.2.5NGAL胶体金试纸条的检测方法 吸取待检样品100 μl,滴在加样孔内,待检样品基于层析原理,会由样品垫依次经过结合垫、NC膜(检测线、质控线)到达吸水区。检测时间仅为5 min,即可显示结果。
若待检样品中含有NGAL,先与吸水垫上的金标NGAL抗体偶联物结合,层析至NC膜后,与包被在检测线处的NGAL单克隆抗体结合形成NGAL单克隆抗体-NGAL抗原-金标NGAL抗体复合物,形成红色可见条带。结果判定方法:C线和T线均显色,判为阳性;C线显色,T线不显色,判为阴性;T线显色,C线不显色或C、T线均不显色,判为无效。
1.2.6NGAL胶体金试纸条的性能测定
1.2.6.1灵敏度试验 将1 mg/ml的rhNGAL贮备液稀释成下列10个浓度梯度,分别为0、2、3、4、5、6、8、10、25、50 ng/ml的标准系列溶液,分别用制备好的NGAL试纸条按1.2.5所述的检测方法对上述标准溶液进行检测,每个浓度测试3次,共测试3个批次的NGAL试纸条。
1.2.6.2重复性试验 分别配制成为阴性、5 ng/ml、50 ng/ml的NGAL标准溶液,每个浓度测试10条,共抽取3批进行测试。
1.2.6.3稳定性试验 将上述制备好的NGAL试纸条同干燥剂一起用铝箔袋塑封,在铝箔袋上标注生产日期,进行稳定性测试。分别贮存在4℃、室温、37℃三种保存条件下,进行稳定性试验。其中4℃、室温贮存的NGAL胶体金试纸条每月检测一次,37℃贮存的NGAL胶体金试纸条每天检测一次,分别对阴性样本和5、10 ng/ml阳性样本进行测试,观察稳定性测试结果。

图1 试纸条组成示意图Fig.1 Diagram of paper strip composition
1.2.6.4临床样本的检测 使用制作好的NGAL胶体金试纸条对临床样本进行检测,临床样本包括30份阳性患者样本和20份正常体检者样本,记录编号后,打乱顺序,进行检测。检测结果与临床结果进行比较,通过两者结果的一致率来判断自制的NGAL胶体金试纸条的临床应用性能。
2 结果
2.1NGAL单克隆抗体鉴定 本研究获得5株能分泌NGAL单克隆抗体的细胞株,通过双抗夹心ELISA对分泌的单克隆抗体进行两两抗体配对,最后筛选出1B4、2C6两株分泌的单克隆抗体配对成功。间接ELISA测定1B4效价为1∶1.02×106、亲和力达到2×108,亚型为IgG1;2C6效价为1∶5.12×105,亲和力达到4×108,亚型为IgM。
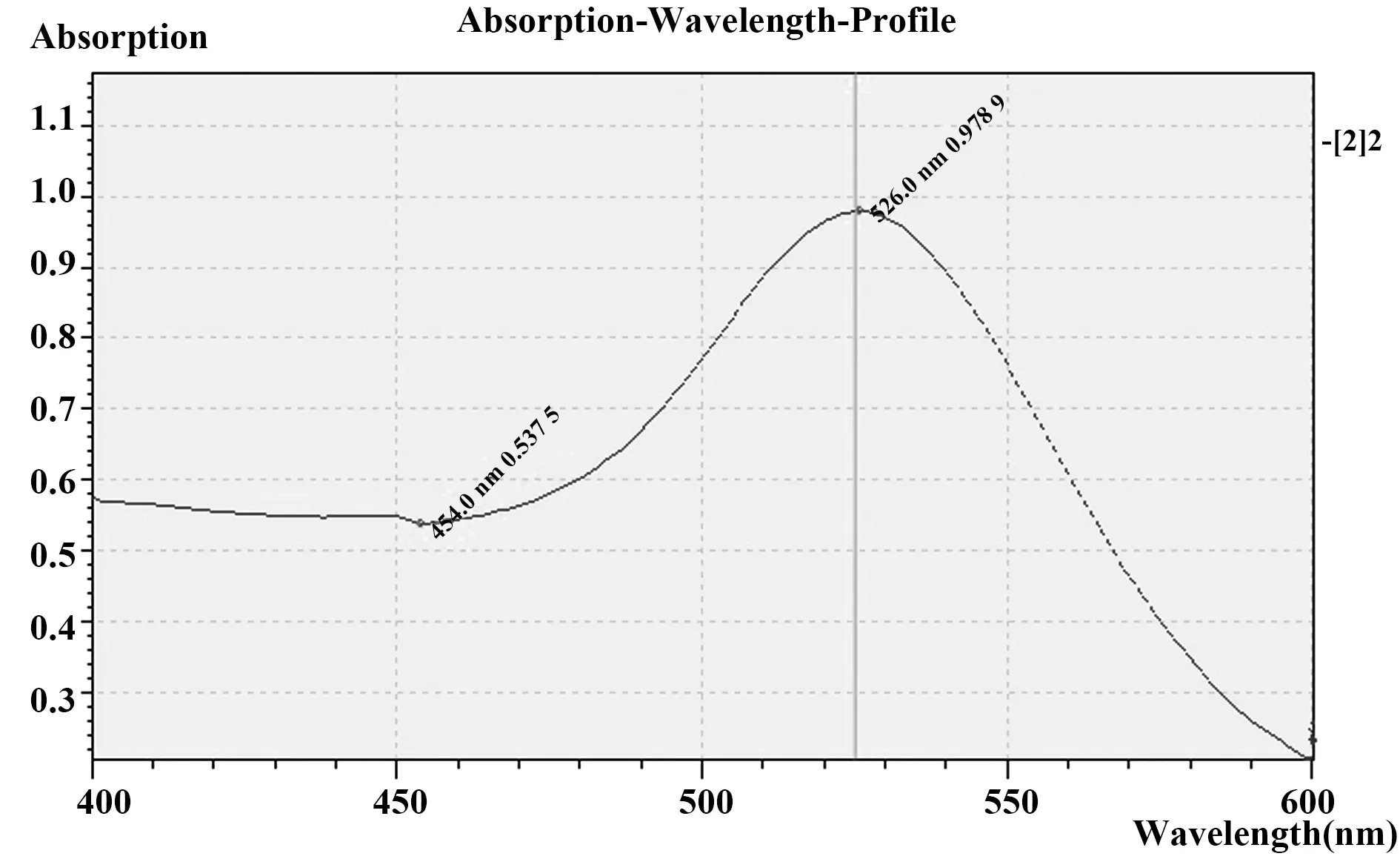
图2 胶体金溶液400~600 nm扫描图谱Fig.2 Scanning map of colloidal gold solution at 400-600 nm

图3 金标NGAL抗体2C6偶联物400~600 nm扫描图谱Fig.3 Scanning map of anti-NGAL antibody 2C6 conjugate with colloidal gold at 400-600 nm
2.2金标NGAL抗体2C6偶联物的质量鉴定
2.2.1紫外-可见分光光度仪鉴定结果 图2、图3分别为胶体金粒子和金标NGAL抗体2C6偶联物在400~600 nm波段内经紫外-可见分光光度计扫描的结果,胶体金粒子最大吸收波长为526.0 nm;金标NGAL抗体2C6偶联物最大吸收波长为536.0 nm。由此看出胶体金标记NGAL抗体后粒径增大,且最大波长出现红移,证明偶联成功。
2.2.2透射电镜法鉴定结果 经过电镜观察,图4为胶体金粒子透射电镜结果,颗粒大小均匀圆润,图5为金标NGAL抗体2C6偶联物透射电镜结果,颗粒变大且边缘出现不规则絮状物,由此表明抗NGAL单克隆抗体与胶体金偶联成功。

图4 胶体金透射电镜图Fig.4 Transmission electron microscopy of colloidal gold

图5 金标NGAL抗体2C6偶联物透射电镜图Fig.5 Transmission electron microscopy of anti-NGAL antibody 2C6 conjugate with colloidal gold
2.2.3试纸条法鉴定结果 试纸条检测结果如图6所示,在羊抗鼠二抗点样处,加入金标NGAL抗体的出现了红色条带,阴性对照则无红色条带出现,证明抗NGAL单克隆抗体与胶体金的偶联物具有活性。
2.3优化NGAL胶体金试纸条 本研究通过两两配对的双抗夹心试验,筛选出1B4、2C6两个抗体配对,通过棋盘法确定两配对抗NGAL抗体的最佳工作浓度。1B4的包被浓度为0.25、0.5、1.0 1 mg/ml,金标抗体2C6的稀释浓度为1∶5、1∶10、1∶15。如图7所示,金标NGAL抗体2C6的稀释浓度为1∶5,1B4包被浓度为0.5 mg/ml这个组合,提供了低的cut-off值、低的抗体用量、深的检测线和清晰的背景,因此筛选金标抗体1∶5和包被抗体浓度0.5 mg/ml 的稀释比例作为最佳反应组合来制备NGAL试纸条。
2.4NGAL胶体金试纸条的性能测定
2.4.1灵敏度试验 3批次NGAL试纸条重复试验的结果一致,如表1所示,样本中NGAL含量在5 ng/ml 及以上时,结果测试均为阳性。样本中NGAL含量为4 ng/ml时,T检测线较C质控线颜色变浅,没有完全消失但肉眼分辨不清楚,无法明确判定结果。样本中NGAL含量低于4 ng/ml时,检测线基本消失,肉眼很难分辨,测试结果均为阴性。经对不同批次进行反复验证,结果基本一致,由此确定本NGAL试纸条的检测限为5 ng/ml。

图6 试纸条鉴定结果Fig.6 Test strip identification resultsNote: A.Anti-NGAL antibody 2C6 conjugate with colloidal gold was added;B.Negative control.
2.4.2重复性试验 由表2可知,NGAL浓度为5 ng/ml、50 ng/ml的样本,重复10次的结果保持一致,均为阳性;阴性样本重复10次检测的结果保持一致,均为阴性;由此试验说明NGAL试纸条在批间和批内的重复性和重现性都很好。
2.4.3稳定性试验 在4℃、室温保存的试纸条,追踪一年的测试中,检测阴性样本的质控线清晰,检测线没有出现,且背景干净;检测5 ng/ml和10 ng/ml 的NGAL阳性样本时,T检测线和C质控线颜色深浅一致,并没有因为保存时间的延长出现颜色变浅的现象,并与对照试纸条比较颜色没有变弱,说明试纸条在4℃、室温下可以保存1年的有效期。NGAL试纸条在37℃条件下,前6 d,T检测线和C质控线颜色深浅一致,且与对照NGAL试纸条比较,颜色没有变弱,检测到第7天时,T检测线相对于对照NGAL试纸条的T检测线开始变浅,得出试纸条有效期1年。
2.4.4临床样本的检测 通过对自制的NGAL胶体金试纸条对50份临床样本的检测结果比对分析,检出30份阳性样本和20份阴性样本,且结果符合率100%。说明本研究制备的NGAL胶体金试纸条的准确度高、稳定性好,该试纸条在准确度、 灵敏度和稳定性上能与市售成熟的试剂盒相媲美,应用前景广阔。

图7 NGAL抗体最佳稀释浓度组合筛选Fig.7 Optimal dilution concentration combination screening of NGAL antibody
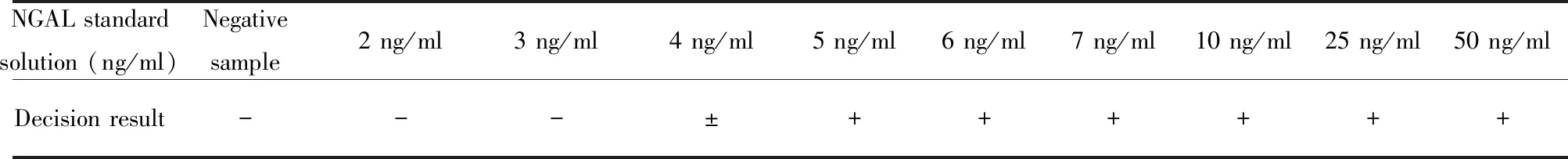
表1 试纸条灵敏度测定Tab.1 Sensitivity determination of strip

表2 试纸条重复性测定Tab.2 Repeatability determination of strip
3 讨论
经研究显示,NGAL作为Lipocalin家族的一个新成员,不但组织分布广,还参与多种病理、生理过程。Nielsen等[7]对儿童和成人的心脏手术后前瞻性研究发现,在术后2~6 h,在病人的血液和尿液中就能检测到浓度高于正常值10倍以上的NGAL,Mishra等[8]也通过研究得出急性肾损伤之后,在早期尿NGAL会急速上升,证明了NGAL是心脏手术后急性肾损伤的早期迹象。2011年Hinze等[9]利用ROC曲线对NGAL预测AKI进行了探讨,其中曲线下的面积为0.78,敏感性76%,特异性80%,得出了NGAL可以在不联合肌酐检测的情况下,独立预测亚临床的AKI。2013年最新研究发现NGAL同IL-18、MA、NAG、αl-MG及UCr相比,是预测搭桥后急性肾损伤的最佳分子,可以更早发现肾脏损伤,为临床治疗肾脏损伤提供参考价值[10]。
而本研究研制的NGAL胶体金试纸条,灵敏度高,检测限为5 ng/ml,与何莹等[11]建立的双抗夹心ELISA免疫检测方法的灵敏度4.8 ng/ml基本一致,但本研究的NGAL试纸条检测时间短,且成本低,重复性、特异性、稳定性好,保存期长达一年,能够满足临床应用要求,应用前景广阔。

