医用硫酸钙对创伤性骨折患者的临床效果及预后影响
张 琦,刘畅畅
骨移植是有效治疗创伤性缺损的手段之一,能帮助机体恢复生物力学性能、填补骨缺损等[1]。自体骨因其具备骨生成、骨诱导以及骨传导等固有特性而被公认为是骨材料的生物学金标准,但易受到年龄及供区的限制,且同种异体骨不具备良好的诱导骨生成能力,同时也增加了疾病传播的概率[2]。医用硫酸钙(CaSO4·1/2H2O)生物相容性良好,是一种应用便捷的人工骨,发生降解时产生的局部离子环境具有提升骨细胞活性的作用,并能与脱钙骨基质(demineralized bone matrix,DBM)复合,起到良好的截体支架的作用[3]。笔者医院在对创伤性骨折患者进行治疗的过程当中,使用医用硫酸钙效果良好,能有效减轻骨折带给患者的病痛,且具有降解速度快、促进骨骼愈合的显著优势,有效提升了患者的生活质量。
临床资料
1 一般资料
2016年5月—2017年5月南京市中医院骨伤科收治60例应用医用硫酸钙进行治疗的创伤性骨折患者,男性34例,女性26例;年龄20~72岁,平均51.3岁。骨折类型:桡骨远端骨折32例,胫骨平台骨折10例,肱骨近端骨折10例,胫腓骨远端骨折8例;陈旧性骨折14例,新鲜骨折46例。将患者分为应用OsteosetRDBM颗粒状医用硫酸钙组(东博生物医用硫酸钙,批号:16101502)35例(OsteosetRDBM组)和MIIGRX3注射型医用硫酸钙组(东博生物医用硫酸钙,批号:17040901)25例(MIIGRX3组)。本研究所有患者均知情同意,同时经过医院伦理委员会批准,一般资料具有可比性(P>0.05),见表1。纳入标准:(1)符合创伤性骨缺损的相关诊断标准;(2)长骨新鲜粉碎性创伤性骨折;(3)陈旧长骨骨折进行断端复位后仍存在一定程度的骨缺损。排除标准:(1)未经控制的神经血管病变、高钙血症以及糖尿病患者;(2)有精神病史或精神疾病症状者;(3)存在中枢神经障碍、长时间昏迷者。
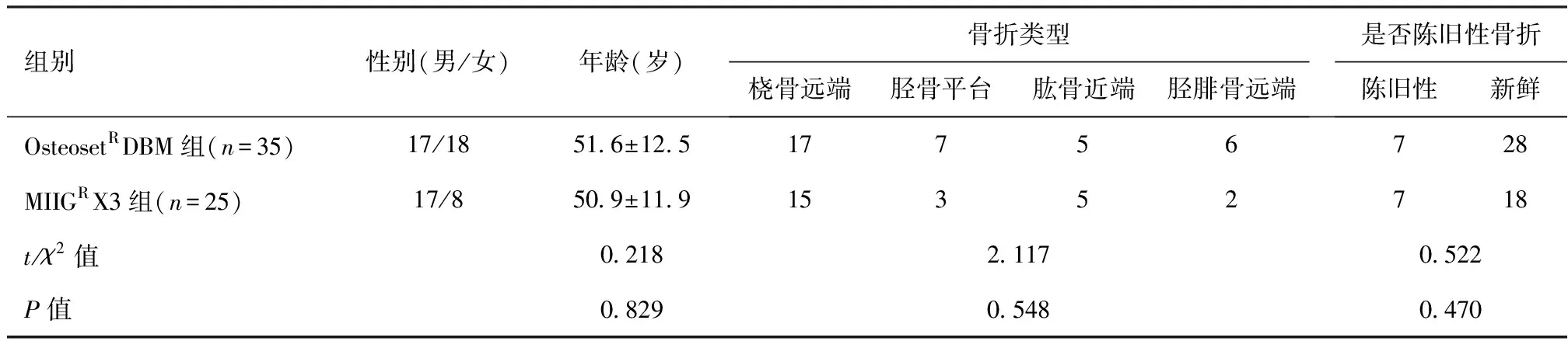
表1 两组患者一般资料比较(n)
2 治疗方法
2.1 植入材料 (1)可注射型硫酸钙。本研究采用MIIGRX3可注射型硫酸钙,由稀释剂和纯度α晶体结构的CaSO4·1/2H2O粉剂组成,在真空状态下搅拌配置直至形成糊状,5min后开始固化,10~15min后完全固化,24h内可实现完全稳定固化[4]。(2)圆柱形颗粒硫酸钙。本研究采用OsteosetRDBM颗粒状硫酸钙,主要有3mm×2.5mm或4.8mm×3mm两种规格,硫酸钙发生颗粒降解的同时,可释放出促成长因子-1(IGF-1)、转化生长因子-1(TGF-1)、骨形态发生蛋白-4(BMP-4)、骨形态发生蛋白-2(BMP-2)等促骨形成的诱导因子[5]。
2.2 植入方法 术中应确保骨折断面能形成新鲜的创面,剥离骨折局部骨膜时应遵循量少的原则[6]。骨折复位固定后,于骨折断端缺损部位置入OsteosetRDBM颗粒状硫酸钙或MIIGRX3可注射型硫酸钙,确保软组织局部覆盖,逐层将伤口严密缝合,术后24~48h常规放置引流[7]。
3 观察指标
3.1 两组治疗前后VAS评分比较 0分可判断为无痛,1~3分为轻微疼痛,尚可忍受;4~6分为患者疼痛并影响睡眠;7~10分为疼痛难忍,影响食欲和睡眠[8]。
3.2 两组医用硫酸钙灰度残留率比较 观察术后患者是否出现发热以及伤口愈合情况,于术后即刻,1、2、4、6周内借助X线对骨折愈合状况以及硫酸钙的降解情况进行判断,使用图像分析软件测量术后即刻,1、2、4、6、8周内医用硫酸钙的灰度总面积,进一步计算患者体内医用硫酸钙的残留率。医用硫酸钙灰度残留率(%)=术后N周医用硫酸钙灰度值/术后即刻医用硫酸钙灰度值×100%(N=1、2、4、6、8)[9]。
3.3 两组生活质量状况评分比较 使用36条目健康量表(SF-36)对患者的生活质量进行评估,该量表主要包括生理功能(PF)、躯体疼痛(BP)、总体健康感(GH)、心理健康(MH)、社会功能(SF)、生命活力(VT)、生理问题导致的角色受限(RP)、情感问题导致的角色受限(RE)8个维度,每个方面满分为100分,分数越低说明患者生活质量越差[10]。
4 统计学分析
结 果
1 两组患者治疗前后VAS评分比较
两组患者治疗前VAS评分差异无统计学意义[(6.8±1.4)分vs. (7.2±1.3)分,P=0.061],治疗后3、6、12个月均出现一定程度的改善,组间比较差异无统计学意义。见表2。
2 两组患者治疗后OsteosetRDBM及MIIGRX3灰度变化
两组患者术后8周未见医用硫酸钙明确显影,组间比较差异无统计学意义(P>0.05),组内比较1周与2、4、6、8周差异有统计学意义(P<0.05),见表3。
3 两组患者治疗后1个月生活质量比较
两组患者治疗前PF、RP、GH、VT、MH、RE、SF、BP评分差异无统计学意义(P>0.05),治疗后评分均上升,组间比较差异无统计学意义(P>0.05)。见表4。
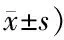
表2 两组患者治疗前后VAS评分比较(分,
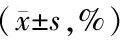
表3 OsteosetRDBM及MIIGRX3灰度变化比较
组内比较:1周与2、4、6、8周比较,P<0.05
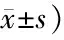
表4 两组患者生活质量比较(分,
组内比较:*P>0.05;组间比较:#P>0.05
讨 论
现阶段常用的骨移植代替物主要有磷酸钙和羟基磷灰石(活性生物陶瓷)、高分子材料、异种骨及含有骨形态发生蛋白(bone morphogentic protein,BMP)的具有骨诱导活性的植入材料等[11]。硫酸钙相对于磷酸钙来说更具有支撑强度稳定、生物相容性良好、生物降解速度快的显著特点,具有更高的临床应用价值[12]。在进行人工植骨手术时,较为常用的是颗粒填充,植入方法和传统植骨方式大致相同,但很难填充到不规则缺损区的每一个角落,只有进行严密的填充才能实现骨折断端接合的效果,促进骨传导支架的重建[13]。使用注射型硫酸钙能实现立刻凝固,可随意塑形,短时间内使受损区实现相对承重[14]。本研究对桡骨远端骨折患者采用注射硫酸钙粉剂的治疗方式取得了良好的效果,微创植入方法操作相对简便,未对骨折区产生严重干扰,促进了骨折的愈合和恢复。
本研究VAS评分数据显示,术后患者疼痛程度多出现缓解,组间比较差异无统计学意义(P>0.05),提示医用硫酸钙人工骨移植能有效促进骨愈合,减轻患者病痛。相关研究发现,无论是颗粒状还是注射型医用硫酸钙,在术后2个月,约有50%的医用硫酸钙被降解,术后6个月,90%以上都可以被降解,具有较快的降解速度,且降解速度可能与医用硫酸钙的剂型没有直接联系,这与本研究结果是一致的[14-16]。本研究数据显示,术后1周大约有69%的应用硫酸钙残留,术后2周残留度大约为54%,术后4周残留率约为26%,术后6周残留率约为7%,术后8周未见硫酸钙明确显影,组间比较差异无统计学意义(P>0.05),组内比较1周与2、4、6、8周差异有统计学意义(P<0.05),同时本研究认为,其降解速度除了受到自身的生化性特征的影响,还会受到局部软组织和材料的接触面积以及材料植入时不同程度分散的影响。软组织与材料接触面积越大、植入时松散,再加上受到血液渗出的影响,可能会加快其降解的速度,植入材料时密度越高,降解速率可能会降低,骨与材料之间的交互面可解释这一规律[17-18]。本研究使用SF-36表对患者的生活质量进行评估,经手术治疗后,两组患者PF、RP、GH、VT评分均出现了上升,OsteosetRDBM组与MIIGRX3组比较差异无统计学意义(P>0.05),提示医用硫酸钙能促进患者骨骼恢复,减轻骨折带给患者的病痛,提升患者生活质量。
医用硫酸钙应用到创伤性骨折患者的治疗中具有降解速度快的显著优势,但早期生物力学强度却得不到保障,医用硫酸钙的降解产物可能会对组织产生刺激并可能出现经伤口渗出的不良后果,在浅表部位使用时应谨慎操作[19]。本研究评价时单纯使用X线、病例较少、新生骨/金属骨痂遮挡材料等因素的影响,研究所得数据尚需进一步借助三维CT及综合影像手段进行更加系统性的评价,改进植入技术、材料调制工艺以及增加骨组织与植入材料之间的有效接触面积等都是下一阶段人工骨移植的研究重点[20]。
综上所述,医用硫酸钙应用于创伤性骨折患者的治疗中效果良好,能有效减轻骨折带给患者的病痛,且具有降解速度快、促进骨骼愈合的显著优势,有效提升了患者的生活质量,值得临床进一步推广。

