W/O型黄芩苷纳米乳的制备及质量评价
郑转弟,周 安,2,吴鸿飞
(1.安徽中医药大学药学院,安徽 合肥 230012;2.安徽中医药大学科研实验中心,安徽 合肥 230038)
黄芩苷是从唇形科植物黄芩(ScutellariabaicalensisGeorgi)的干燥根中提取分离出来的一种黄酮类化合物[1-2],具有抑制乙型肝炎病毒复制、清除乙型肝炎病毒复制模板环状DNA、抑制肝纤维化等药理作用[3-4],临床上主要用于治疗慢性乙型肝炎。研究表明,乙型肝炎病毒易藏匿于淋巴系统[5-6],而黄芩苷常规剂型难经淋巴转运,不能有效地富集于淋巴系统,导致慢性乙型肝炎的治疗受到一定的阻碍。纳米乳是一种新型淋巴靶向递药系统[7],本课题组前期成功制备出W/O型黄芩苷纳米乳,相对于黄芩苷混悬剂,所制备得到的W/O型黄芩苷纳米乳可经淋巴转运,极大提高了黄芩苷的生物利用度。为进一步评价W/O型黄芩苷纳米乳的质量体系,本研究建立了W/O型黄芩苷纳米乳的高效液相色谱分析方法,对W/O型黄芩苷纳米乳中黄芩苷进行含量测定,为该制剂质量控制提供一定的参考。
1 仪器与试药
1.1 仪器 Agilent 1260型高效液相色谱仪(包含G1311X四元梯度泵、G1329自动进样器、G1316A柱温箱、G1315C紫外检测器):美国安捷伦公司;Welch Topsil HPLC C18色谱柱(4.6 mm×250 mm,5 μm):上海月旭材料科技公司;CP225D型十万分之一电子天平:德国Sartorius公司;KQ-5200B型数控超声波清洗器:江苏省昆山市超声仪器有限公司;DF-101B型磁力搅拌器:河南省巩义市予华仪器责任公司;Malvern Zeta sizer Nano ZS-90纳米粒径电位分析仪:英国马尔文仪器有限公司;SYZ-C型石英自动亚沸高纯水蒸馏器:南京桑力电子设备厂。
1.2 试药 W/O型黄芩苷纳米乳及空白纳米乳(批号分别为20171010、20171101、20171102、20171103、20171104、20171105、20171106、20171107、20171108、20171109):自制;黄芩苷对照品(批号 110715-201318,含量≥98%):中国食品药品检定研究院;黄芩苷原料药(批号 141201,含量为85.94%):四川省玉鑫药业公司;大豆磷脂:安徽省合肥沃森生物科技公司;1,2-丙二醇、肉豆蔻酸异丙酯、磷酸、甲醇(色谱纯):国药集团化学试剂公司;苏丹红、亚甲蓝:天津市光复精细化工公司;蒸馏水:自制;其他试剂均为分析纯。
2 方法与结果
2.1 W/O型黄芩苷纳米乳的制备及载药量考察 精密称取大豆磷脂10.5 g、1,2-丙二醇10.5 g、肉豆蔻酸异丙酯9 g混合置于锥形瓶中,在45 ℃恒温下磁力搅拌至全溶,精密称定黄芩苷原料药313.5 mg溶于上述体系中,直至黄芩苷原料药全部溶解在混合溶液中,室温下往体系缓慢滴加3 g双蒸水直至体系变为透明均匀的液体,即得W/O型黄芩苷纳米乳,载药量为9.5 mg/mL。
2.2 W/O型黄芩苷纳米乳质量评价
2.2.1 外观性状 制备的W/O型黄芩苷纳米乳外观上均为橙黄色均一透明液体,流动性良好。
2.2.2 类型鉴别 采用染色法来判断纳米乳类型,取黄芩苷纳米乳(批号 20171010)5.0 mL于两只试管中,分别加入适量的水溶性染料亚甲基蓝和油溶性染料苏丹红于试管中,比较两种染料的扩散速度。结果苏丹红的扩散速度明显快于亚甲基蓝的扩散速度,表明制备的纳米乳为W/O型纳米乳。
2.2.3 粒径分布 取W/O型黄芩苷纳米乳(批号20171010)1.0 mL,用外相肉豆蔻酸异丙酯稀释至10 mL。取稀释后的纳米乳适量,用Malvern Zeta sizer Nano ZS-90纳米粒径电位分析仪测定纳米乳体系的粒径,结果见图1。本实验制备的W/O型黄芩苷纳米乳的平均粒径为(63.40±1.10)nm(n=3),PDI为(0.166±0.006)(n=3),表明制备的W/O型黄芩苷纳米乳大小均一,且分布均匀。
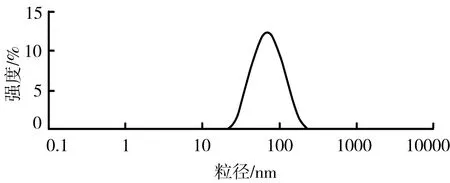
图1 W/O型黄芩苷纳米乳粒径分布图
2.3 W/O型黄芩苷纳米乳的含量测定
2.3.1 色谱条件 色谱柱:Welch Topsil HPLCC18色谱柱(4.6 mm×250 mm,5 μm);流动相:甲醇-0.1%磷酸水(55∶45);柱温为30 ℃;流速1.0 mL/min;检测波长为280 nm;进样量:10 μL。理论塔板数按黄芩苷计算,应不小于3 000。
2.3.2 对照品溶液的制备 精密称取黄芩苷对照品6.2 mg,置10 mL量瓶中,加甲醇溶解并稀释至刻度,即得620.00 μg/mL的对照品储备液,4 ℃条件下避光储存。
2.3.3 供试品溶液的制备 精密量取纳米乳1.0 mL,置10 mL量瓶中,加甲醇稀释至刻度,超声20 min破乳。精密量取1.0 mL破乳液,置10 mL容量瓶中,加甲醇稀释至刻度,混匀,即得纳米乳待测样品,避光保存。
2.3.4 方法学考察
(1)专属性考察 分别取空白溶剂(甲醇)、黄芩苷对照品(以甲醇稀释所得的溶液)、空白纳米乳(批号 20171101,按“2.3.3”项下方法制备供试品溶液)、W/O型黄芩苷纳米乳(批号 20171102,按“2.3.3”项下方法制备供试品溶液),按“2.3.1”项下方法进行检测,记录色谱图,结果见图2。黄芩苷保留时间为9.59 min,辅料与试剂不干扰药物测定,表明方法专属性良好。
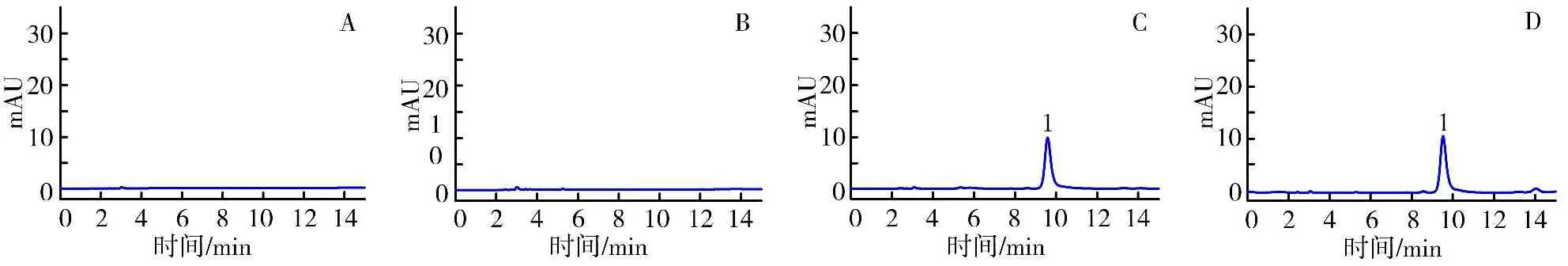
图2甲醇(A)、空白纳米乳(B)、黄芩苷对照品(C)、W/O型黄芩苷纳米乳(D)的高效液相色谱图(1.黄芩苷)
(2)线性关系 取对照品储备液0.2、0.5、1.0、2.0、3.0、4.0、5.0 mL分别置于10 mL量瓶中,用甲醇稀释至刻度,摇匀,配制成浓度为12.40、31.00、62.00、124.00、186.00、248.00、310.00 μg/mL的系列溶液。按“2.3.1”项下方法进行检测,平行测定3次,求得峰面积的平均值,以黄芩苷浓度(x)与峰面积(y)作图,绘制标准曲线,并计算得回归方程y=38.125x-32.384(r=0.999 7)。结果表明,黄芩苷在12.40~310.00 μg/mL范围内与峰面积的线性关系良好。
(3)精密度试验 取标准曲线中浓度为62.00 μg/mL对照品溶液,按“2.3.1”项的色谱条件连续进样6次,记录色谱峰面积,计算RSD为0.89%,表明仪器精密度良好。
(4)重复性试验 精密量取W/O型黄芩苷纳米乳1.0 mL(批号 20171102),共6份,按“2.3.3”项下方法制备供试品溶液,按“2.3.1”项下的色谱条件测定,记录色谱峰面积,按“2.3.4”项下“(2)”之标准曲线计算黄芩苷含量,计算RSD为1.54%,表明方法重复性良好。
(5)稳定性考察 取同一供试品溶液分别于室温放置0、2、4、6、8、12、24 h后,按照“2.3.1”项下色谱条件进样测定,记录色谱峰面积,按“2.3.4”项下“(2)”之标准曲线计算黄芩苷含量,计算RSD为1.21%,表明供试品溶液在24 h内稳定性良好。
(6)加样回收率试验 精密量取已知含量的W/O型黄芩苷纳米乳1.0 mL(批号 20171102),共9份,置于100 mL容量瓶中,分别精密加入9.5 mg/mL黄芩苷对照品溶液0.8、1.0、1.2 mL,各3份,加入一定容积的甲醇,超声20 min破乳,最后稀释至刻度,制得低、中、高质量浓度的黄芩苷供试品溶液,按“2.3.1”项下的色谱条件测定,记录色谱峰面积,按“2.3.4”项下“(2)”之标准曲线计算黄芩苷含量,结果见表1。低、中、高3个浓度的平均加样回收率分别为98.70%、99.01%、100.31%,RSD分别为0.40%、0.66%、0.87%,表明该方法准确度良好。
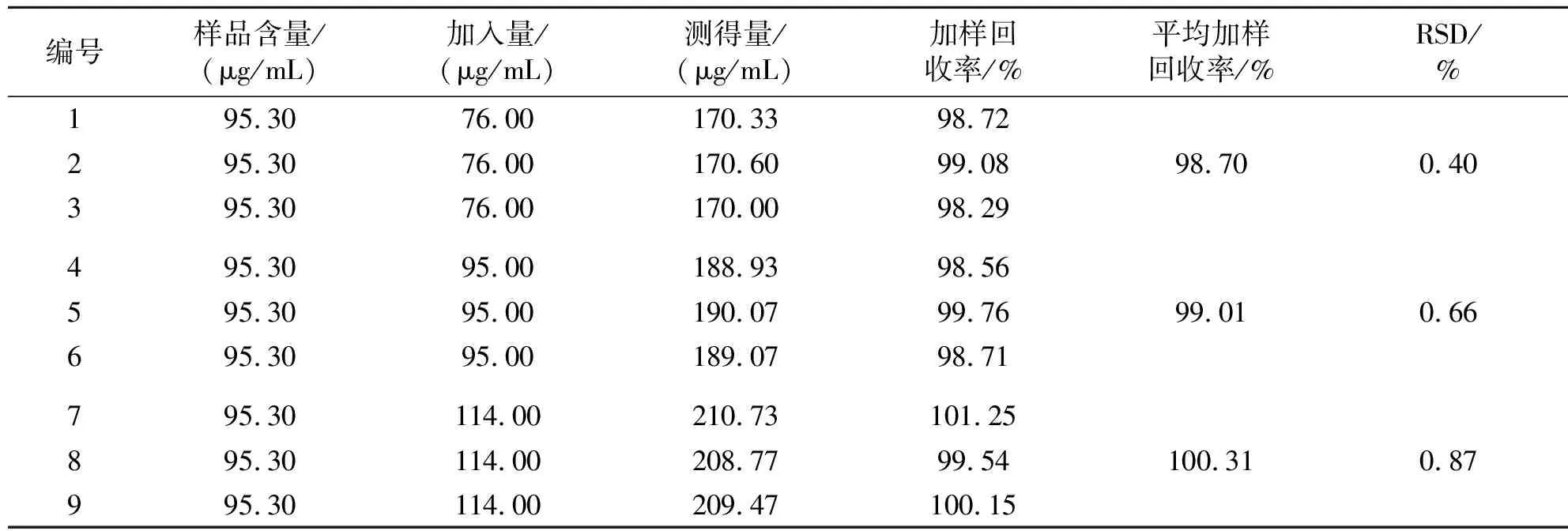
表1 加样回收率试验
2.3.5 样品含量测定 精密量取6批W/O型黄芩苷纳米乳各1.0 mL,每批3份,按“2.3.3”项下方法制备供试品溶液,以“2.3.1”项下色谱条件测定,记录色谱峰面积,按“2.3.4”项下“(2)”之标准曲线计算黄芩苷含量,结果见表2。
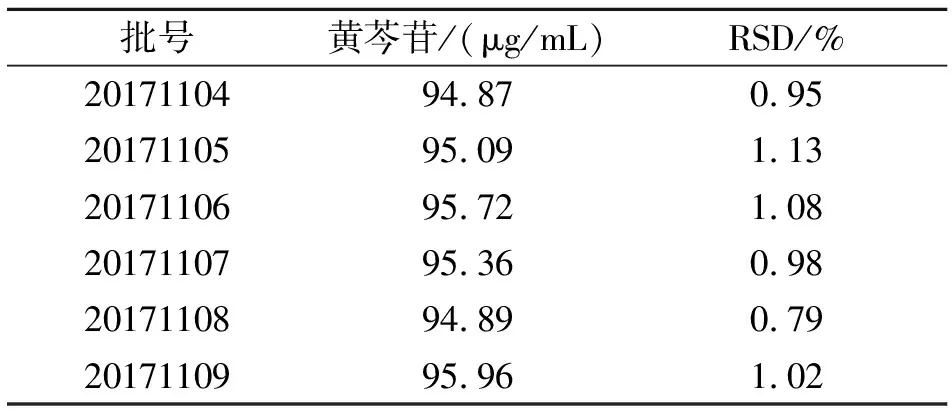
表2 黄芩苷含量测定结果(n=3)
2.4 初步稳定性考察 精密量取2.0 mL W/O型黄芩苷纳米乳封于安瓿瓶中(批号 20171103),共8份,每组4份,分别进行常温实验(25 ℃放置30 d)和低温实验(4 ℃放置30 d),分别于0、10、20、30 d时观察纳米乳的外观形状,并测定黄芩苷含量。结果见表3。在常温25 ℃、低温4 ℃条件下放置30 d,纳米乳外观澄清透明、无分层现象,且含量与0 d测定结果相比较无明显变化,表明制备的W/O型黄芩苷纳米乳在此时间内性质稳定。
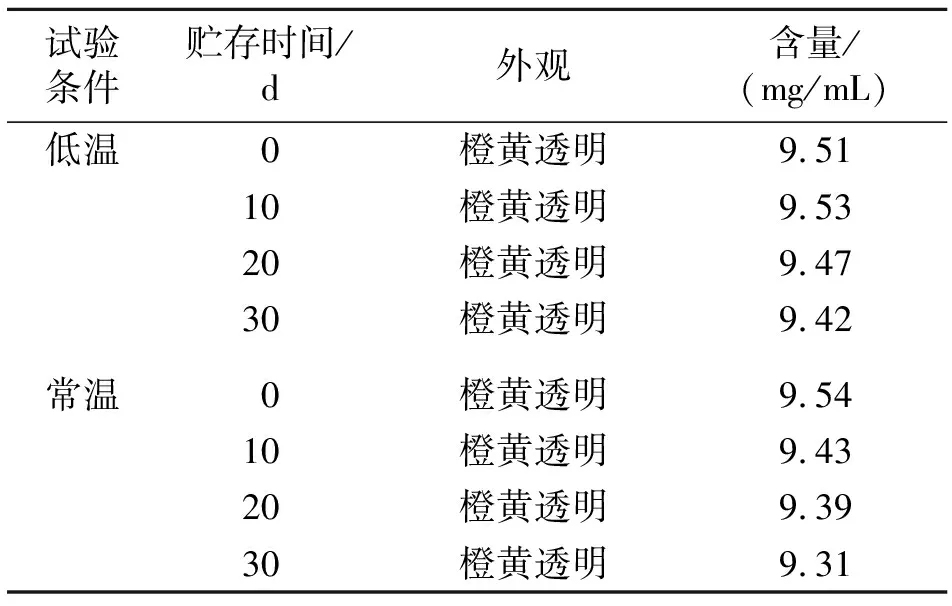
表3 稳定性试验结果
3 讨论
纳米乳是一种热力学稳定体系[8],其破乳影响药物的释放,选择适宜的破乳方法对准确检测出黄芩苷含量具有重要意义。纳米乳的破乳方法主要有化学破乳法和物理破乳法[9]。预实验中,考察了超声破乳和甲醇、乙腈的破乳效果,结果发现,超声无法破乳,乙腈破乳后出现浑浊,故选用甲醇作为破乳剂。同时,本实验考察甲醇联合超声法对所制备的W/O型黄芩苷纳米乳的破乳效果,结果发现甲醇联合超声条件下破乳效果最好(溶液澄明)。
文献报道黄芩苷含量测定时流动相的体系主要为甲醇-0.2%磷酸水[10-11],考虑到磷酸对色谱柱的损害,本实验比较了甲醇-0.2%磷酸水溶液、甲醇-0.1%磷酸水溶液的色谱行为,结果发现两者流动相条件下峰形无差异。因此,选择甲醇-0.1%磷酸水溶液为流动相条件,减小对色谱柱的损伤。
本实验对W/O型黄芩苷纳米乳中黄芩苷进行含量测定,以甲醇-0.1%磷酸水为流动相,色谱峰分离效果好,峰形尖锐,操作简便,结果准确可靠,重现性好,可用于W/O型黄芩苷纳米乳的质量控制和稳定性考察。

