Ag3PO4/Ag2S/g-C3N4复合光催化剂的制备与性能
邓军阳 汪 杰 朱思龙 聂龙辉
(湖北工业大学材料与化学工程学院,武汉 430068)
0 引 言
从1972年以来,光催化技术经过数十年的发展,已被广泛用于解决能源危机和环境污染问题[1-8]。二氧化钛是研究最广泛的光催化剂,但它存在只能利用紫外光的问题。而紫外光仅占到太阳光能量的4%~5%,可见光在太阳光能量中却高达40%以上。因此,研究制备高性能的可见光催化剂(如C3N4、改性TiO2、Ag3PO4等)是近十年来的热点课题。
Ag3PO4是一种新型可见光催化材料,它具有窄带隙,量子效率高和对有机污染物氧化能力强等特点[9-10],目前在降解有机污染物、产氧、产氢、分解水等领域已被广泛应用[11-18]。但Ag3PO4的自身结构不稳定,在光催化过程中,表面部分银离子会被还原成银单质使得自身结构遭到破坏,导致光催化性能降低。因此,研究者们通过复合、包裹、掺杂、形貌控制等方式来提高Ag3PO4光催化活性和稳定性[18-34]。如:Ag3PO4与碳材料(石墨烯、碳 60、碳纳米管等)[14-19]或贵金属(金、银、钯、铂)复合[20-26],与其它光催化材料形成异质结[27]或Z型光催化剂[13,15,28]等。Wang课题组[19]制备了碳化氮/碳纳米管/磷酸银复合Z型光催化剂,该复合催化材料表现出优异的催化性能与稳定性,在6次循环测试中对罗丹明B的降解率保持98%以上。Tian等[32]制备了碳化氮/二硫化钼/磷酸银Z型光催化剂,其产氧速率达到纯Ag3PO4的4倍,且稳定性得到提升。
研究表明,不同前驱体制备的Ag3PO4光催化剂性能不同[33-38],其中用磷酸氢二钠合成的Ag3PO4具有较高的光催化活性。适当引入g-C3N4不但可以利用间位阻效应有效减少Ag3PO4粒径,提高有机污染物吸附能力,而且还能提高光生电子与空穴的分离效率[39-42]。少量的Ag2S可提高Ag3PO4光催化剂的吸收范围和吸收效率[43]。因此,本文通过沉淀法将Ag3PO4附着在g-C3N4上,并利用溶度积的不同在Ag3PO4表面原位置换生成Ag2S,制得Ag3PO4/Ag2S/g-C3N4复合光催化剂。相比较纯Ag3PO4,该复合光催化材料表现出更好的可见光催化活性与稳定性。
1 实验部分
1.1 实验试剂
实验中所用试剂未经进一步纯化直接使用。尿素(国药集团化学试剂有限公司,分析纯),无水磷酸氢二钠(国药集团化学试剂有限公司,分析纯),乙酸银(国药集团化学试剂有限公司,分析纯),九水合硫化钠(麦克林,化学纯)。
1.2 样品的制备与表征
1.2.1 g-C3N4的制备
将尿素加到坩埚中,放入马弗炉,以5℃·min-1的升温速率升至550℃,保温2 h后降温至室温,制得g-C3N4。
1.2.2 Ag3PO4/g-C3N4复合光催化剂的制备
将0.4 g上述制备的g-C3N4加到10 mL去离子中,超声处理30 min,接着加入1.1 g乙酸银,避光搅拌1 h,标记为溶液A。另将1.2 g无水磷酸氢二钠加入到去离子水中制得0.15 mol·L-1的溶液,标记为溶液B。将溶液B逐滴加入溶液A中,避光搅拌20 min。经分离后与 80℃下干燥6 h,制得Ag3PO4/g-C3N4复合光催化剂,标记为样品AC。
1.2.3 Ag3PO4/Ag2S/g-C3N4复合光催化剂的制备
将0.4 g样品AC分散到10 mL蒸馏水中,超声处理30 min。然后逐滴加入10 mL 0.012 mmol·mL-1的九水合硫化钠溶液,加入硫化钠与Ag3PO4物质的量之比(nNa2S/nAg3PO4)为1.5%,避光剧烈搅拌6 h。经过滤分离后80℃下干燥6 h,制得Ag3PO4/Ag2S/g-C3N4复合光催化剂,其中g-C3N4与Ag3PO4的质量比为3∶7,样品标记为ASC1.5。为考察生成Ag2S量的影响,改变添加的nNa2S/nAg3PO4分别为 0.75%、5%、20%、50%和80%,其他条件不变,所得到的样品分别为ASC0.75、ASC5、ASC20、ASC50 和 ASC80。 为考察 g-C3N4添加量的影响,选择nNa2S/nAg3PO4为1.5%,改变g-C3N4的添加量,制备了g-C3N4与Ag3PO4的质量比分别为 1∶9、2∶8、3∶7、3.5∶6.5、4∶6、5∶5 的样品。
1.2.4 表征手段
样品物相分析在Empyrean型(荷兰,PANalytical)X射线粉末衍射仪进行,Cu Kα辐射(波长λ=0.154 06 nm),测试电压为45 kV,电流为40 mA,扫描范围为2θ=10°~80°。 通过 VG ESCALAB250xi测定样品 X射线光电子能谱(XPS)。以C1s位于284.6 eV处表面污染碳作为结合能的校正基准。样品的N2吸附-脱附等温线在MicromeriticsASAP2020型(美国)吸脱附装置上进行,根据N2吸附数据计算样品的BET比表面积(SBET)。样品预处理条件:180℃脱气8 h。孔径分布曲线通过吸附支的数据利用Barrett-Joyner-Halenda(BJH)方法和圆柱孔为模型计算得到。孔体积和平均孔径由在相对压力P/P0=0.97下的单点氮气吸附数据确定。样品的微观形貌是通过SU8010型(日立)扫描电子显微镜(SEM)及EOL 2100F型透射电子显微镜(TEM)进行观察,扫描电镜工作电压为1.0 kV,透射电镜工作电压为200 kV,点分辨率是0.24 nm。样品的光谱分析在Eclipse型(美国,Cary)荧光分光光度计上进行,激发光源波长为315 nm,在410 nm处测定荧光强度。紫外-可见光漫反射图谱通过Lambda 750s型紫外可见光谱仪上测定,扫描范围为 250~800 nm。样品中元素含量通过Agilent 7500a型电感耦合等离子发射光谱仪(ICPOES)测定。
1.3 可见光催化活性及稳定性评价方法
光降解催化实验中,光源为150 W氙灯,用滤玻片过滤掉波长小于420 nm的光。通入冷凝水使反应温度保持恒定。将50 mg光催化剂加入到50 mL浓度为10 mg·L-1的罗丹明B溶液中。先暗处吸附30 min达平衡后,光照进行光催化反应,每5 min取一次样品,经离心分离,取上层清液经分光光度法测定溶液浓度。回收光催化剂,再进行下一次光催化实验,实验条件相同,回收循环测试次数为5次。
1.4 自由基与空穴捕获实验
1.4.1 自由基与空穴捕获实验
为了研究光催化机理,确定光催化降解罗丹明B过程的主要中间活性物种,进行了羟基自由基(·OH)、超氧阴离子自由基(·O2-)和空穴(h+)的捕获实验,通过考察添加捕获剂前后光催化活性的变化来确定主要活性物种。异丙醇(IPA)是一种·OH捕获剂,对苯醌(BQ)是一种·O2-捕获剂,而草酸铵(AO)是一种h+捕获剂。通过在上述光催化反应过程中分别加入1μmol·L-1的IPA、BQ和AO,相同条件下测定罗丹明B浓度随时间的变化。
1.4.2 荧光光谱法测定·OH
由于·OH可与对苯二甲酸反应生成具有高荧光性的羟基对苯二甲酸,因此,可用荧光光谱法对光催化过程中产生的·OH进行进一步检测。70 mg光催化剂加入70 mL对苯二甲酸(0.5 mmol·L-1)与NaOH(2 mmol·L-1)的混合溶液中。在相同光源光照下,每隔15 min取一次样,经过离心分离取上清液。荧光光谱通过荧光光谱仪测得,激发光源为波长为315 nm的紫外光,在410 nm处测定荧光强度的变化。
2 结果与讨论
2.1 表征结果
2.1.1 XRD分析
图1为Ag3PO4和ASC1.5复合光催化剂的XRD图。 图中可见, 在位于 2θ=20.85°、29.68°、33.28°、36.56°、42.42°、47.80°、52.68°、55.02°、57.30°、61.69°和71.96°特征峰分别归属为立方相Ag3PO4(110)、(200)、 (210)、 (211)、 (220)、 (310)、 (222)、 (320)、 (321)、(400)和 (332)晶面特征峰 (PDF No.06-0505),而ASC1.5样品中在2θ=12.9°、27.6处的特征峰则归属为 g-C3N4(100)、(002)晶面特征峰(PDF No.78-1747)。ASC1.5样品中没有观测到Ag2S样品的特征峰,可能是其含量过低的缘故(理论含量0.7%(w/w))。
2.1.2 复合光催化剂的结构与形貌
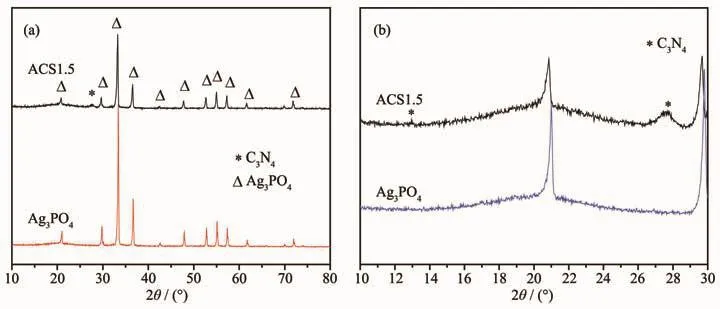
图1 样品Ag3PO4和ASC1.5的XRD图(a)及其局部放大图(b)Fig.1 XRD patterns of the Ag3PO4 and ASC1.5 samples(a)and the corresponding magnification patterns(b)

图2 (a)Ag3PO4,(b)Ag2S和(c)ASC1.5的SEM照片;(d)ASC1.5的TEM照片Fig.2 SEM images of the(a)Ag3PO4,(b)Ag2S,(c)ASC1.5 samples;(d)TEM image of the ASC1.5 sample
为进一步观察样品的结构和形貌,对样品进行了SEM和TEM表征。图2分别为样品ASC1.5、纯Ag3PO4和纯Ag2S的SEM和TEM照片。图2(a)显示Ag3PO4呈现出规则的多面体结构,粒径在300~1 000 nm间。图2(b)的Ag2S照片表明其呈现出蜂窝状多孔结构,粒子粒径在200~300 nm间,粒子间相互交联贯通。图2(c)为ASC1.5样品的SEM照片,图中显示规则的Ag3PO4经S2-离子置换后,表面变得光滑,同时生成了一些细小不规则的Ag2S粒子和g-C3N4一起包覆在Ag3PO4表面。图2(d)为ASC1.5样品的TEM图,可以看出Ag2S生成在Ag3PO4表面,粒径大约10 nm,同时g-C3N4和Ag2S一起包裹在Ag3PO4表面。细小Ag2S粒子的生成和g-C3N4的包覆一方面可增加对光的吸收,另一方面也会增加样品的比表面积,这些都有利于光催化过程中活性的提高。
2.1.3 XPS分析
通过XPS对所制备的Ag2S/g-C3N4/Ag3PO4复合光催化剂进行元素分析。由ASC1.5的全谱图可知所制备的材料中含有 Ag、O、P、S、C和 N六种元素(图3(a))。 图3(b)为Ag3d的高分辨谱图,在368.0和374.1 eV处的2个峰分别为Ag3d5/2和Ag3d3/2的特征峰[11-12,32],表明Ag元素以Ag+形式存在,来自Ag3PO4或Ag2S。图3(c)是P2p的高分辨谱图,其中132.3和133.2 eV处的特征峰为PO43-中P元素的特征峰[43]。图3(d)是O1s的高分辨谱图,其中532和533.3 eV的峰值是属于O-H键中的O特征峰,531.9 eV峰则以Ag-O-Ag形式存在的晶格氧[12,44]。图3(e)是S2p的高分辨谱图,位于161.8和163.0 eV的特征峰归属为Ag2S中S2p的特征峰[14,43],表明Ag2S通过离子交换成功的负载到了Ag3PO4表面。图3(f)为N1s高分辨图谱,其中398.9 eV处的特征峰为C-N=C键特征峰,400 eV处的特征峰为N-(C)3键的特征峰[17,40,45-46]。图3(g)为C1s的高分辨谱图,图中284.7 eV为C-C键的特征峰来自表面污染的有机物,286.1 eV为C=N键特征峰,288.3 eV为N-C=N键特征峰[17,47-48]。
2.1.4 紫外-可见光谱图
图 4 为 Ag2S、g-C3N4、Ag3PO4、AC 和 ASC1.5 的紫外-可见光谱图。图中可见,Ag3PO4在紫外和可见光区都表现出强吸收,其本征吸收边大约位于550 nm 处,由带隙计算公式 Eg=1 240/λg(其中 λg(nm)为吸收边)可得其带隙约为2.25 eV。g-C3N4本征吸收边约为430 nm,则其带隙约为2.88 eV,而Ag2S则在200~800 nm整个紫外-可见光区域中表现出强吸收,这主要是由于其带隙很小的原因。样品AC由Ag3PO4与C3N4复合而成,有2个吸收边分别位于450和 550 nm。 样品 ASC 是由 Ag3PO4、C3N4、Ag2S三者复合而成,图中显示样品ASC1.5有2个吸收边,分别位于630和470 nm,相比于Ag3PO4、C3N4和AC的吸收边,发生了明显的红移。这主要归因于表面Ag2S具有优异的敏化效果,使样品ASC1.5可以吸收更多的可见光,暗示ASC1.5催化剂可能具有更好的催化性能。
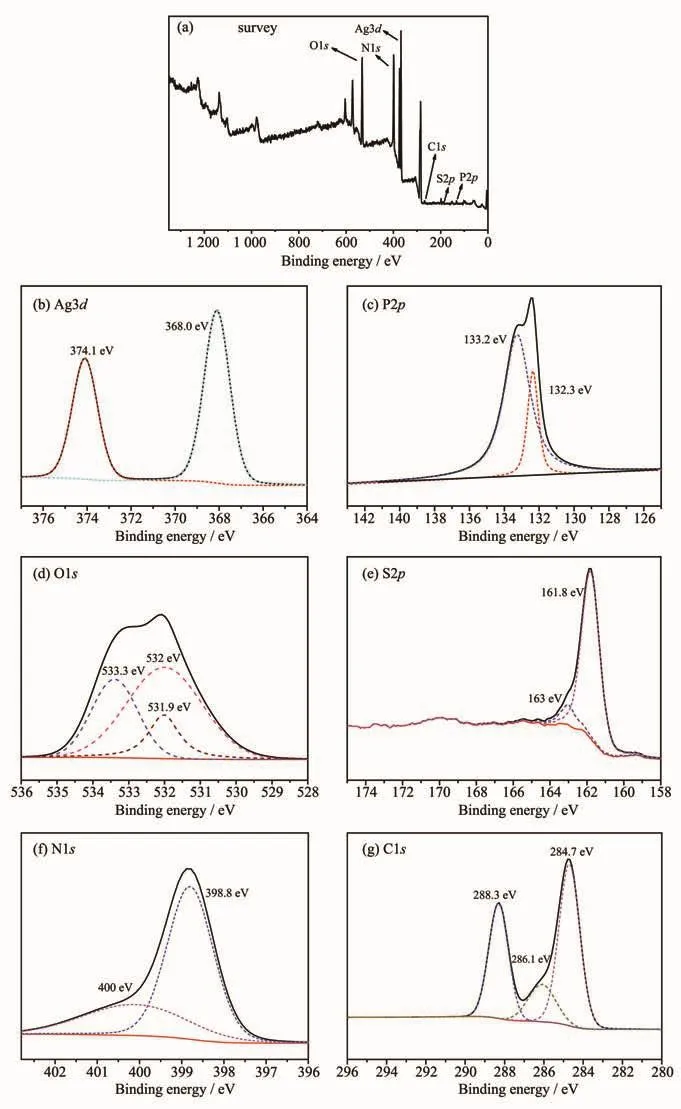
图3 ASC1.5样品的(a)XPS全谱图及(b)Ag3d,(c)P2p,(d)O1s,(e)S2p,(f)N1s和(g)C1s的高分辨XPS谱图Fig.3 (a)XPS survey spectrum and high resolution XPS spectra of(b)Ag3d,(c)P2p,(d)O1s,(e)S2p,(f)N1s and(g)C1s of the ASC1.5 sample
2.1.5 N2吸附-脱附等温线
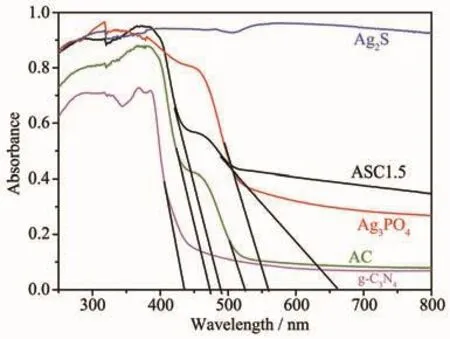
图 4 样品 Ag2S、g-C3N4、Ag3PO4、AC 和 ASC1.5的紫外-可见光吸收光谱Fig.4 UV-Vis spectra of the Ag2S,g-C3N4,Ag3PO4,AC and ASC1.5 samples
样 品 Ag3PO4、g-C3N4、Ag2S、AC 和 ASC1.5 的 N2吸附-脱附等温线及其孔分布曲线如图5所示。从N2吸附-脱附等温线(图 5a)可知,g-C3N4对 N2的吸附量最大,表明其比表面积最大,而Ag3PO4对N2的吸附最小,表明其比表面积最小。在Ag3PO4表面复合了g-C3N4及Ag2S以后,其比表面积比Ag3PO4对N2的吸附量有显著提高,表明通过表面复合能显著提高Ag3PO4的比表面积。其中ASC1.5样品的N2吸附-脱附等温线按国际纯粹与应用化学联合会(IUPAC)的分类属于Ⅳ型吸附等温线[49],表明中孔的存在。在P/P0=0.8~1.0的高压范围内可见Ⅲ型的回滞环,也说明中孔的存在。图5(b)为各样品的孔分布曲线。图中可见,Ag3PO4几乎没有孔结构,这与SEM照片中看到的规则形貌和较大的粒径有关,该形貌不易形成孔结构。而g-C3N4以及与Ag3PO4复合以后的AC和ASC1.5样品中在宽度2~100 nm的范围内有大量中孔和大孔的存在。同时,出现了2个较为明显的孔分布峰,较小的峰值约为3.5 nm,较大的峰值约在35 nm左右。表1列出了各样品的BET比表面积(SBET),孔体积(Vpore)和孔径大小(dpore)数据。从表中可见,Ag3PO4的SBET和Vpore都非常小,分别只有2 m2·g-1和 0.003 cm3·g-1。 g-C3N4的 SBET和 Vpore都比较大, 达到 115 m2·g-1和 0.364 cm3·g-1。 Ag3PO4和 g-C3N4复合后能显著增加其比表面积和孔容,SBET和Vpore分别为 26 m2·g-1和 0.156 cm3·g-1, 平均孔径也由Ag3PO4的4.3 nm增加到12 nm。进一步在Ag3PO4表面将部分PO43-置换为S2-生成细小的Ag2S后,ASC1.5比表面积增加到28 m2·g-1。高比表面积和多孔结构更有利于污染物的扩散和吸附,增加反应场所,从而有利于进一步提高其催化活性。

图5 样品ASC1.5、AC、Ag3PO4、C3N4和Ag2S的(a)N2吸附-脱附等温线及(b)孔径分布曲线Fig.5 (a)N2 adsorption and desorption isotherms and(b)corresponding pore size distribution curves of the ASC1.5,AC Ag3PO4,C3N4 and Ag2S samples

表1 所制备样品的基本属性参数Table 1 Basic parameters for the as-synthesized samples
2.2 催化活性评价

图6 (a)Ag3PO4、g-C3N4、AC和ASC1.5光催化降解罗丹明B性能图;(b)ASC1.5样品降解罗丹明B动力学线性拟合结果Fig.6 (a)Photocatalytic degradation of rhodamine B over the Ag3PO4,g-C3N4,AC and ASC1.5 samples;(b)Kinetic linear fitting result for ASC1.5
图 6(a)为样品 Ag3PO4、g-C3N4、Ag2S、AC 和 ASC1.5光催化降解罗丹明B性能图。由图可见,在光照前催化剂主要对罗丹明B存在吸附作用,其中以g-C3N4的吸附最强,而纯Ag3PO4吸附最弱,AC和ASC1.5样品对罗丹明B的吸附介于二者之间。这主要与样品的比表面积大小有关,比表面积大的样品能吸附更多吸附污染物。光照后,罗丹明B浓度降低的速率各不相同,从浓度降低速率可以看出催化活性的相对大小,浓度降低速率快,则活性高,浓度降低速率慢,则活性低。由此可见,其中Ag2S的活性最小,而ASC1.5样品催化活性最大。从SEM、TEM、UV-Vis和N2吸附-脱附等温线表征结果可知,复合g-C3N4和Ag2S后,不但增加了ASC1.5样品有利于吸附罗丹明B的比表面积及有利于污染物扩散和吸附的孔结构,而且增强了对光的响应范围,使之更易与活性物种反应,因此,ASC1.5表现出比Ag3PO4更高的催化活性。图6(b)为ASC1.5样品降解罗丹明B动力学线性拟合结果,图中显示以-ln(C/C0′)对t作图呈现良好线性关系 (C0′为吸附平衡后的浓度),相关系数R2值为0.991 9,表明ASC1.5样品降解罗丹明B的过程符合假一级动力学模型。
实验中考察了制备过程中Na2S添加量(即Ag2S的生成量)对样品催化性能的影响。不同Na2S添加量制备的样品及图6中各样品计算得到的速率常数结果如图7所示。通过元素含量分析 (ICP-OES)可知, 样品 ASC0.75、ASC5、ASC20、ASC50 和 ASC80中生成的Ag2S与Ag3PO4物质的量之比分别为2.6%、3.1%、3.6%、26.6%、90.2%和 150.0%, 说明PO43-能有效被S2-置换。图7表明,ASC1.5样品光降解罗丹明B的速率常数大于纯Ag3PO4和AC样品,也明显高于纯g-C3N4和Ag2S的速率常数。在nNa2S/nAg3PO4=0~1.5%时,随着比值的增加,速率常数依次增大,而进一步增加Na2S的投入量则速率常数逐渐减小,当比值超过5%时,复合光催化剂的活性呈现明显下降趋势。这可能是过多Na2S的生成会使得大量Ag3PO4被置换,而Ag2S的可见光催化活性不高,从而导致复合光催化剂活性逐渐下降。
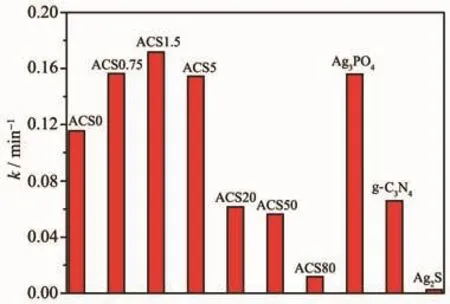
图7 Ag3PO4、g-C3N4、Ag2S及不同Na2S添加量所制备的ASC样品的反应速率常数Fig.7 Reaction rate constants of Ag3PO4,g-C3N4,Ag2S and ASC samples obtained with different amounts of Na2S
g-C3N4的添加量对所制备样品催化性能的影响如图8所示。结果表明,g-C3N4的量对复合光催化剂性能有显著的影响。随着g-C3N4质量的增加,复合光催化剂的光催化反应速率常数先增加后降低,且当二者的质量比为3∶7时,达到最佳催化性能。这是因为当二者质量比为 1∶9、2∶8、3∶7 时,随着 g-C3N4质量的增加,g-C3N4与Ag3PO4间的协同作用越明显,而当接着增加 g-C3N4与 Ag3PO4的质量(3.5∶6.5、4∶6、5∶5)时,可能由于 Ag3PO4被厚厚的 g-C3N4包裹着,不利于光的吸收,导致光催化活性的下降。
为考察催化剂活性的稳定性,对样品ASC1.5和Ag3PO4进行多次循环使用,其结果如图9所示。2种样品经5次循环使用后,催化活性出现了不同程度的下降。其中Ag3PO4从第2次开始活性明显下降,到第5次使用时对罗丹明B的降解率从初始的100%下降到40%左右。而ASC1.5样品从第3次开始催化活性才有所下降,到第5次时还能保持在80%左右的降解效率。表明ASC1.5复合光催化剂的稳定性明显高于于纯Ag3PO4。

图8 不同g-C3N4与Ag3PO4质量比所制备样品的反应速率常数Fig.8 Reaction rate constants of the ASC samples with different mass ratios of g-C3N4 and Ag3PO4

图9 ASC1.5与Ag3PO4样品循环使用5次后活性对照图Fig.9 Comparison of photocatalytic activities over the ASC1.5 and Ag3PO4 samples after 5 cycles
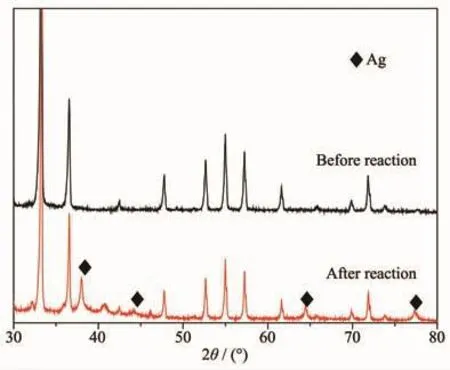
图10 ASC1.5样品光催化反应前后XRD图Fig.10 XRD patterns of ASC1.5 sample before and after photocatalytic reaction
为进一步了解ASC1.5样品在重复使用后催化剂活性下降的原因,对重复使用后的样品进行了XRD表征(图10)。多次使用后ASC1.5样品和反应前相比在 2θ=38.4°、44.5°、64.6°、77.5°处出现了单质银的特征峰,表明经多次使用后仍有部分银离子被还原成单质银,这可能是ASC1.5样品5次循环使用后活性下降的主要原因。
2.3 催化反应机理
为检测ASC1.5样品光照条件下能否产生·OH,以对苯二甲酸为探针分子,测试不同光照时间下的荧光光谱(图11)。由图可知,在410 nm处出现了明显的特征峰,且随光照时间的增加该峰强度逐渐增加,表明在ASC1.5样品上有·OH的生成。

图11 光照不同时间下的ASC1.5样品的荧光光谱图Fig.11 Fluorescence spectra of ASC1.5 samples after different illumination times
为进一步确定ASC1.5样品光催化降解罗丹明B过程中的主要活性物种,在光催化过程中分别以IPA、BQ 和 AO 为·OH、·O2-和 h+的捕获剂,探索 3种活性物种对催化性能的影响(图12)。结果显示,3种捕获剂添加后,样品光催化降解效率出现了明显的不同程度的下降,其中添加AO后催化活性下降最大,表明·OH、·O2-和 h+都是光催化过程中的主要活性物种,三者活性物种作用大小依次为:h+>·O2->·OH。
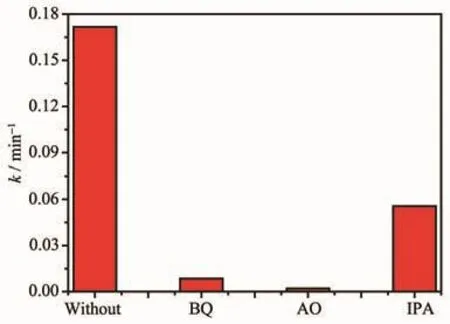
图12 捕获剂添加前后ASC1.5光催化剂的反应速率Fig.12 Reaction rates on the ASC1.5 sample with and without sacrifices
基于以上分析结果以及相关文献推测的可能的反应机理如图13所示。Ag3PO4、Ag2S和g-C3N4能带宽度分别是1.90 eV (导带值ECB=0.51 eV;价带值EVB=2.41 eV)、1.05 eV(ECB=-0.055 eV;EVB=0.995 eV)和 2.70 eV(ECB=-1.20 eV;EVB=1.50 eV)[50-53]。在可见光的照射下,Ag3PO4、Ag2S和g-C3N4同时激发产生电子-空穴对,Ag3PO4光生电子会迁移到Ag2S上与其表面的光生空穴复合,而Ag2S上产生的光生电子迁移到g-C3N4表面并与其表面产生的光生空穴复合;同时,Ag3PO4产生的光生空穴迁移到表面后可直接氧化有机污染物,也可与表面水分子反应生成·OH,而g-C3N4产生的光生电子则与O2分子反应生成·O2。·OH和·O2也都能与有机污染物发生氧化反应将其分解如二氧化碳和水等)。与此同时,Ag3PO4表面可能有部分光生电子会将Ag+还原成单质Ag,Ag单质的生成一方面降低了Ag3PO4的稳定性,另一方面也能促进Ag3PO4光生电子迁移到Ag2S表面与其光生空穴复合。综上所述,ASC复合光催化材料相对于Ag3PO4的光催化性能及稳定性都得到了明显提高。
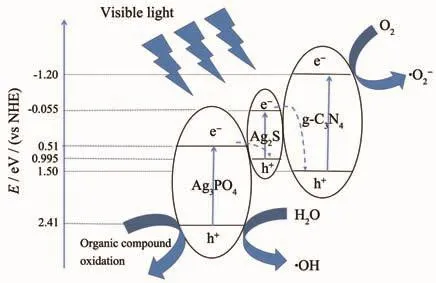
图13 光照条件下ASC1.5样品上光催化降解罗丹明B反应机理示意图Fig.13 Schematic diagram of photocatalytic degradation of rhodamine B on ASC1.5 samples under illumination
3 结 论
通过沉积-离子交换法成功制备Ag3PO4/Ag2S/g-C3N4复合光催化剂。通过复合g-C3N4以及将部分Ag3PO4取代为Ag2S,一方面可以增大样品的比表面积和多孔结构,另一方面拓宽了Ag3PO4光催化剂的响应范围,同时有利于提高光生载流子的分离效率。Na2S添加量对所制备样品催化性能的影响结果表明,随着nNa2S/nAg3PO4比值的增加,反应速率常数先增大后逐渐减小,当nNa2S/nAg3PO4为1.5%时光催化活性最好。过多的Na2S加入会使得大量Ag3PO4被置换,从而导致复合光催化剂活性逐渐下降。g-C3N4的添加量实验结果表明,随着g-C3N4质量的增加,复合光催化剂的光催化反应速率常数先增加后降低;当二者的质量比为3∶7时,达到最佳催化性能;当二者质量比为 1∶9、2∶8、3∶7 时,即在此区间内随着 g-C3N4的量的增加,g-C3N4与Ag3PO4间的协同作用越明显 ;若 进一 步 增 加 g-C3N4的量(3.5∶6.5、4∶6、5∶5),Ag3PO4将被厚厚的g-C3N4包裹着,不利于光的吸收,导致光催化活性的下降。相比较于Ag3PO4,ASC1.5复合催化剂的催化活性和稳定性提高都得到了明显提高。光催化机理研究表明,·OH、·O2-和h+都是光催化过程中的主要活性物种,三者活性物种作用大小依次为 h+>·O2->·OH。Ag3PO4/Ag2S/g-C3N4复合催化材料的制备为高活性与稳定性可见光催化材料提供了新的思路。

