核壳结构Ag@BaGdF5∶Yb3+,Ho3+多功能纳米复合材料的制备及其性能
隋晶婷 陈子禹 刘桂霞 宋 超 董相廷
(长春理工大学化学与环境工程学院,应用化学与纳米技术吉林省高校重点实验室,长春 130022)
0 引 言
近年来,镧系元素掺杂的上转换纳米晶的发光性能和潜在应用受到了研究者的广泛关注[1-7]。稀土氟化物具有较低的声子能量以及较小的能量损耗,成为常用的上转换发光材料的基质[8-15]。其中BaGdF5作为稀土氟化物中的一种,由于Gd3+特殊的4f电子构型,使其具有出色的发光和顺磁特性[16-18]。
银纳米粒子具有表面等离子共振吸收[19]、较大的原子序数[20]、较长的成像时间和光热转换性能[21-22],有潜力应用于计算机断层扫描(CT)成像和肿瘤细胞的光热治疗领域[23]。目前,对肿瘤进行光热治疗的前期、中期和后期同时成像的纳米诊疗试剂引起了人们的重视[24-28]。这种试剂能够将成像和光热治疗结合[29-31],显著提高光热治疗的效率[32-34]。将具有光热治疗效果的银纳米粒子同具有上转换发光性能的BaGdF5∶Yb3+,Ho3+纳米晶结合,合成具有磁-光-热多功能的复合纳米材料有潜力成为一种多模式成像的诊疗试剂,应用于多模式成像指导的光热治疗领域。
采用一种简单的液相法制备了核壳结构的Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料,这种纳米复合材料结合了光热治疗和双模式成像功能,有潜力成为一种新型的纳米诊疗平台。研究了纳米复合材料的磁、光、热特性,通过MTT试验确定纳米复合材料的生物相容性,进一步研究了纳米复合材料的双模式成像以及在对肿瘤细胞的光热治疗领域的应用。
1 实验部分
1.1 Ag纳米粒子的制备
将200 mg的AgNO3和1 g PVP(K30)溶解在35 mL乙二醇中,于室温下持续搅拌得到混合溶液,随后将其加热到130℃,持续反应1 h,混合物被冷却至室温。产物用大量的丙酮沉淀,然后离心分离(8 000 r·min-1,10 min),再用去离子水和乙醇分别洗涤3次,得到Ag纳米粒子,将其分散在乙醇中,备用。
1.2 Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料的制备
首先向稀土氧化物(0.01 mol的 Gd2O3、0.005 mol的Yb2O3和Ho2O3)中分别加入15 mol·L-1硝酸溶液,在加热搅拌下使其溶解,除去多余硝酸后,在室温下分别加入100 mL去离子水,配成浓度为0.1 mol·L-1的 Gd(NO3)3、0.05 mol·L-1的 Yb(NO3)3和Ho(NO3)3溶液。取50 mL制备的Ag纳米粒子溶液,在搅拌过程中加入3 mmol柠檬酸钠,随后加入已配制 的 2.34 mmol Gd(NO3)3、0.6 mmol Yb(NO3)3、0.06 mmol Ho(NO3)3溶液,在室温下持续搅拌30 min。取0.488 52 g的BaCl2·2H2O直接加入到上述溶液中,继续搅拌5 min,最后逐滴加入10 mL的NH4F(2.1 mol·L-1),室温下搅拌 1 h。在 8 000 r·min-1转速下将生成的产物离心收集。随后用去离子水和乙醇洗涤3次后,将沉淀放入60℃干燥箱中干燥6 h得到样品。
1.3 表征方法
采用Bruker D8 FOCUS型X射线衍射仪(XRD)对样品的相结构和纯度进行分析,Cu Kα辐射(λ=0.154 056 nm),测量的角度(2θ)范围为 10°~90°,扫描速度为6°·min-1,工作电压为30 kV,工作电流为20 mA。采用JSM-7610F型场发射环境扫描电子显微镜(SEM)和JEOL-2000EX型透射电子显微镜(TEM),对样品的形貌和尺寸进行分析,工作电压为15 kV。采用FEI公司生产的OXFORD ISIS-300型能量色散光谱仪对样品组成进行分析。采用SHIMADZU UV-2450型分光光度计对样品进行紫外-可见吸收光谱测试,波长范围为200~1 000 nm。采用HITACHI F-7000型荧光光谱仪对样品进行荧光分析,以MWLW 980 nm半导体激光器作为激发光源,光电倍增管(PMT)电压为700 V。采用美国生产的MPMS SQUID XL型振动样品磁强计对样品进行磁性分析,外加磁场范围为-20~20 kOe。采用980(1.2 W·cm-2)和808 nm激光器(1.0 W·cm-2)对一系列不同浓度样品的水溶液进行照射,水溶液温度的变化分别通过HTC3500C温度传感器和红外热成像相机进行记录。
1.4 细胞毒性实验
采用MTT比色法对样品的生物相容性进行评估,以HeLa细胞作为实验细胞。首先,将HeLa细胞在96孔板中于5%(V/V)CO2和37℃的环境下培养24 h;然后将细胞与不同浓度的样品溶液继续培养24 h,每个浓度做3组平行实验;最后将100μL溶解在磷酸盐缓冲溶液(PBS)中的MTT加入到每一个孔中,孔板在37℃下继续培养4 h,培养结束后,用PBS溶液进行清洗,再向每个孔中加入150μL的二甲基亚砜(DMSO)。利用酶标仪在波长为490 nm下测量吸收值。细胞活性计算公式:其中,CV为细胞存活率;ODNCs为与纳米复合材料共同培养的HeLa细胞在酶标仪检测下的吸光度;OD为未处理的对照组的HeLa细胞在酶标仪检测下的吸光度。
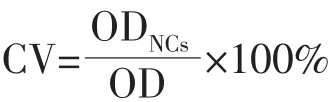
1.5 上转换荧光成像(UCL)实验
采用外接一个980 nm激光器的共聚焦荧光显微镜来观察细胞的体外上转换荧光成像。首先,HeLa细胞被种在6孔板上,在5%(V/V)CO2和37℃的环境下培养24 h;将细胞用PBS洗涤3次后,再加入所制备的样品继续培养6 h;最后用PBS洗涤将多余的样品去除。通过共聚焦显微镜记录细胞的明亮场和上转换荧光成像图片。
1.6 CT实验
采用CT成像系统 (Bruker)来测试细胞的体外CT成像。首先将制备的样品和碘比醇分散在去离子水中形成不同浓度的水溶液,将其倒入2 mL的离心管中放入CT成像系统。成像参数如下:厚度为0.9 mm,电压为82 kV,管电流为500μA。
1.7 光热治疗(PTT)实验
采用荧光素二乙酸酯(FDA)/普罗匹定(PI)共染实验评估纳米复合材料的光热治疗效果。首先,HeLa细胞被种在96孔板上,在37℃下培养24 h;然后与样品在同样的环境下继续培养12 h。用808 nm激光照射共同培养过后的细胞5 min;最后将处理后的细胞用FDA和PI共同染色30 min。通过共聚焦荧光显微镜记录细胞的生存死亡比。
2 结果与讨论
2.1 X射线衍射(XRD)分析
图1为所制备样品的XRD图。图1(a)表明所制备的Ag纳米粒子的所有衍射峰的位置和强度都与Ag的标准卡片(PDF No.04-0783)相匹配,没有其他衍射峰出现,说明所制备的Ag纳米粒子为立方相。由图 1(b)可知,所制备的 BaGdF5∶Yb3+,Ho3+纳米粒子在 26°、30°、43°、51°和 53.5°处有衍射峰出现, 分别对应立方相 BaGdF5的 (111)、(200)、(220)、(311)和(222)晶面,衍射峰的数据与立方相的BaGdF5(PDF No.24-0988)基本一致,同时观察到衍射峰向高角度位移,这是由于Yb3+、Ho3+的离子半径小于Gd3+的离子半径,Yb3+、Ho3+掺入到晶格中取代Gd3+后导致晶胞体积的缩小,从而使得纳米复合材料的衍射峰相对于BaGdF5的标准卡片向高角度发生位移。图1(c)中可以观测到BaGdF5的衍射峰和Ag的衍射峰,说明合成了 Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料。

图 1 (a)Ag纳米粒子,(b)BaGdF5∶Yb3+,Ho3+纳米粒子,(c)Ag@BaGdF5∶Yb3+,Ho3+纳 米 复 合 材 料 的 XRD图以及Ag和BaGdF5的标准卡片Fig.1 XRD patterns of the samples(a)Ag nanoparticles,(b)BaGdF5∶Yb3+,Ho3+nanoparticles and(c)Ag@BaGdF5∶Yb3+,Ho3+nanocomposites;Standard cards of Ag(PDF No.04-0783)and BaGdF5(PDF No.24-0988)
2.2 电子显微镜和能谱分析
图2 (a)为制备的Ag纳米粒子的SEM照片,从图中可以看出Ag纳米粒子为球形,表面光滑,结合图2(b)的粒径分布直方图可知Ag纳米粒子的平均直径为 77 nm。 由 Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料的SEM照片(图2(c))可知包覆后颗粒仍为球形,表面粗糙。结合纳米复合材料的粒径分布直方图(图2(d))可知,复合材料的平均直径增大,约为106 nm。为了更清晰地观察其形貌,对其进行了TEM测试。由图2(e)的TEM照片可见明显的核壳结构,壳层厚度约为14 nm,进一步说明Ag纳米粒子表面包覆上了 BaGdF5∶Yb3+,Ho3+纳米粒子。 图 2(f)的 EDS 分析表明纳米复合材料包含 F、Er、Ba、Gd、Yb、Ag、Si和 Au元素(Au元素来源于制样过程中的喷金过程)。上述结果证明成功合成了 Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料。
2.3 光学性质分析
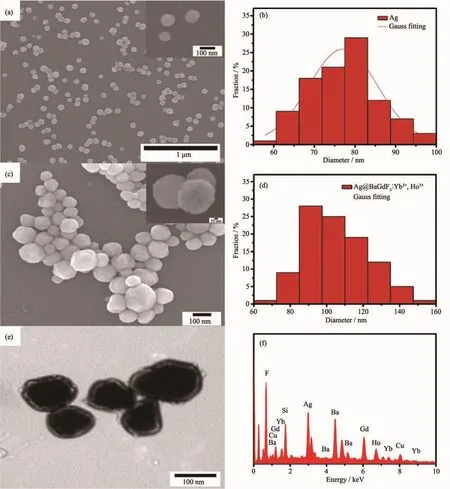
图2 Ag纳米粒子 (a,b)和Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料 (c,d)的SEM照片和粒径分布直方图;Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料的TEM照片 (e)和EDS能谱图 (f)Fig.2 SEM images and histograms of size distribution of Ag nanoparticles(a,b)and Ag@BaGdF5∶Yb3+,Ho3+nanocomposites(c,d);TEM image(e)and EDS spectrum(f)of Ag@BaGdF5∶Yb3+,Ho3+nanocomposites
图 3 是 BaGdF5∶Yb3+,Ho3+纳米粒子和 Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料的上转换发射光谱图。从图中可以看出样品中均存在2个发射谱带,分别位于540和647 nm,对应Ho3+离子的5S2/5F4-5I8和5F5-5I8跃迁。 与 BaGdF5∶Yb3+,Ho3+纳米粒子相比,复合粒子的上转换发光强度降低,并且540 nm的绿光发射下降明显。结合图3(c)的Ag纳米粒子的紫外-可见吸收光谱图分析,Ag纳米粒子在428 nm附近强的局部表面等离子体共振吸收峰与BaGdF5∶Yb3+,Ho3+纳米粒子的绿光发射部分重叠,造成了二者之间的能量传递,BaGdF5∶Yb3+,Ho3+纳米 粒子作为能量给体,Ag纳米粒子为能量受体,在980 nm激发下,BaGdF5∶Yb3+,Ho3+发射的绿光部分被 Ag 纳米粒子吸收,导致绿光发射强度明显降低。
为了分析 Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料的上转换发光过程,研究了纳米复合材料中Ho3+的特征跃迁的发射强度(IUC)随泵浦功率(P)的变化,二者关系如下:


图 3 BaGdF5∶Yb3+,Ho3+纳米粒子 (a)和 Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料 (b)的上转换发射光谱(λex=980 nm);Ag纳米粒子的紫外可见吸收光谱(c)Fig.3 Upconversion emission spectra(λex=980 nm)of BaGdF5∶Yb3+,Ho3+nanoparticles(a)and Ag@BaGdF5∶Yb3+,Ho3+nanocomposites(b);UV-Vis spectrum of Ag nanoparticles(c)
其中n代表光子数。图4为泵浦功率对Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料发光强度的双对数点图。从图中可以看出纳米复合材料在5S2/5F4-5I8(540 nm)跃迁和5F5-5I8(647 nm)跃迁处的斜率分别为1.64和1.89,均接近于 2,说明 Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料的Ho3+的红光和绿光跃迁为双光子过程。

图4 Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料的绿光和红光发射强度的功率依赖关系图Fig.4 Pump power dependence diagram of green and red emission intensity of Ag@BaGdF5∶Yb3+,Ho3+nanocomposites
图 5 是 Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料可能的上转换发光过程和能量传递示意图。Yb3+离子先吸收980 nm的光子,跃迁到2F5/2能级,处于激发态的Yb3+离子通过能量的转移(ET)传递给Ho3+离子,Ho3+离子吸收能量,产生了绿光(540 nm,5S2/5F4-5I8)和红光(647 nm,5F5-5I8)发射。由于Ag纳米粒子的等离子体共振(SPR)吸收峰同Yb3+/Ho3+的绿光发射有重叠,使两者之间发生能量传递。
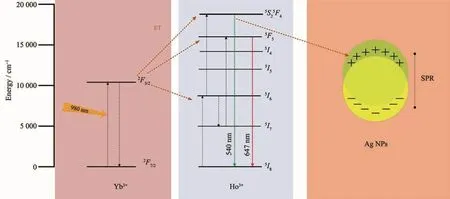
图5 Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料的上转换过程的能级图Fig.5 Energy level diagrams of upconversion process of Ag@BaGdF5∶Yb3+,Ho3+nanocomposites
2.4 磁性分析
图 6 为 BaGdF5∶Yb3+,Ho3+纳米粒子和 Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料的磁滞回线,从图中可知,在室温下的纳米粒子和复合材料均呈现顺磁性,磁化强度分别为1.28和1.16 emu·g-1。磁化强度的降低归因于引入了不具有磁性的贵金属Ag后,降低了磁性物质所占的比例。
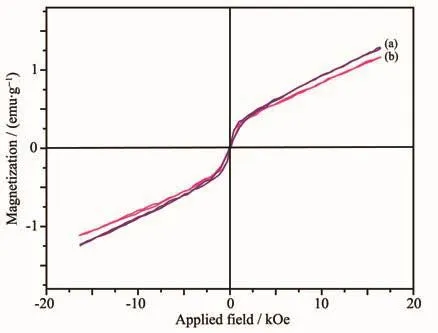
图 6 BaGdF5∶Yb3+,Ho3+纳米粒子 (a)和 Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料 (b)的磁滞回线Fig.6 Hysteresis loops of BaGdF5∶Yb3+,Ho3+nanoparticles(a)and Ag@BaGdF5∶Yb3+,Ho3+nanocomposites(b)
2.5 光热性能分析
为了证明 Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料的热效应,将其水溶液用980 nm激光进行照射,测量其温度变化。图7(a)显示了用980 nm激光照射10 min 后去离子水、BaGdF5∶Yb3+,Ho3+纳米粒子、Ag纳米粒子和 Ag@BaGdF5∶Yb3+,Ho3+纳米复合粒子溶液的温度变化。从图中可以看出去离子水和BaGdF5∶Yb3+,Ho3+纳米粒子的温度从19℃分别上升到23和24℃,同时,Ag纳米粒子的温度从19℃上升到31.8℃,而 Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料的温度则从19℃增加到了39℃,说明纳米复合材料温度上升的主要原因是Ag纳米粒子吸收光后转变为热量。 同时研究了不同浓度的 Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料的水溶液在980 nm激光照射10 min后的温度变化关系图(图7(b))。从图中可以看出随着纳米复合材料浓度的增加,悬浮液温度上升,这说明改变 Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料的浓度,其温度也会发生改变。图7(c)为在808 nm激光照射下,Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料的近红外成像照片。Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料在 808 nm NIR照射5 min后温度从22.0℃上升到59.1℃,并且随着辐射时间的增加,纳米复合材料的温度会继续上升。 这表明 Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料有望应用于肿瘤细胞的光热治疗领域。
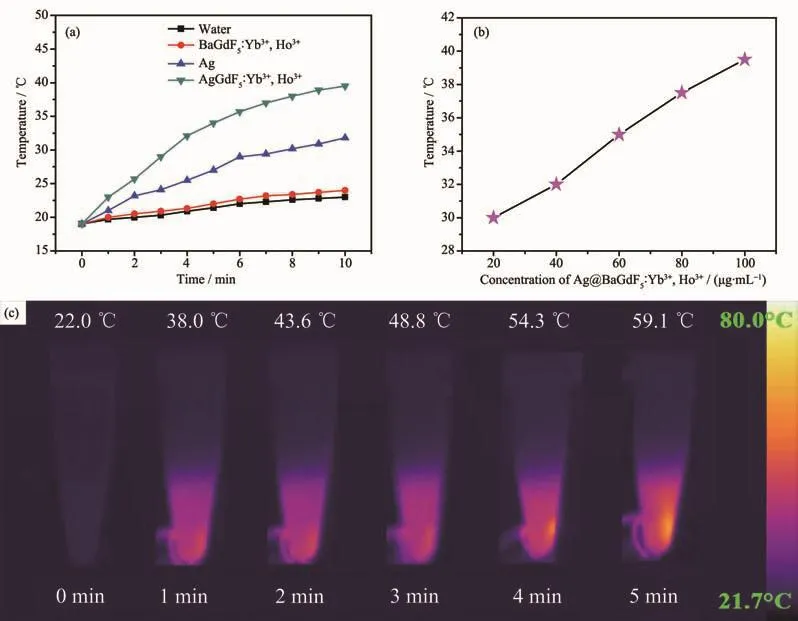
图7 在980 nm激光照射下,去离子水、BaGdF5∶Yb3+,Ho3+纳米粒子,Ag纳米粒子和Ag@BaGdF5∶Yb3+,Ho3+纳米复合粒子的温度变化曲线 (a);不同浓度的Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料的升温变化曲线 (b);808 nm激光照射下纳米复合材料的近红外成像照片(c)Fig.7 Temperature variation curves of water,BaGdF5∶Yb3+,Ho3+nanoparticles,Ag nanoparticles and Ag@BaGdF5∶Yb3+,Ho3+nanocomposites(a);Heating effect of nanocomposites with different concentrations of Ag@BaGdF5∶Yb3+,Ho3+(b)under 980 nm laser irradiation;Infrared images of nanocomposites under 808 nm irradiation(c)
2.6 MTT实验分析
细胞毒性是材料能否应用于生物领域的关键因素,选用HeLa细胞作为试验细胞进行MTT试验评估 Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料的毒性。 图 8是利用不同浓度的 Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料分别培养HeLa细胞24 h。从图中可以看出纳米复合材料的浓度达到1 mg·mL-1时,细胞成活率可以达到 79%。MTT 试验说明 Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料对细胞的毒性很小,可以应用于生物领域。

图8 HeLa细胞同不同浓度的Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料共同培养24 h的细胞活性直方图Fig.8 Cell viability histogram of HeLa cells incubated with different concentrations of Ag@BaGdF5∶Yb3+,Ho3+nanocomposites for 24 h
2.7 上转换荧光成像
选取HeLa细胞作为对象,研究了Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料的上转换荧光成像。将纳米复合材料加入到细胞中培养6 h后,采用共聚焦荧光显微镜可采集到细胞呈现明亮的绿光信号(图9(b)),并且从图9(c)中观察到细胞吸收了纳米复合材料,材料存留在细胞质中,表明所制备的纳米复合材料能够应用于癌细胞的上转换成像研究。
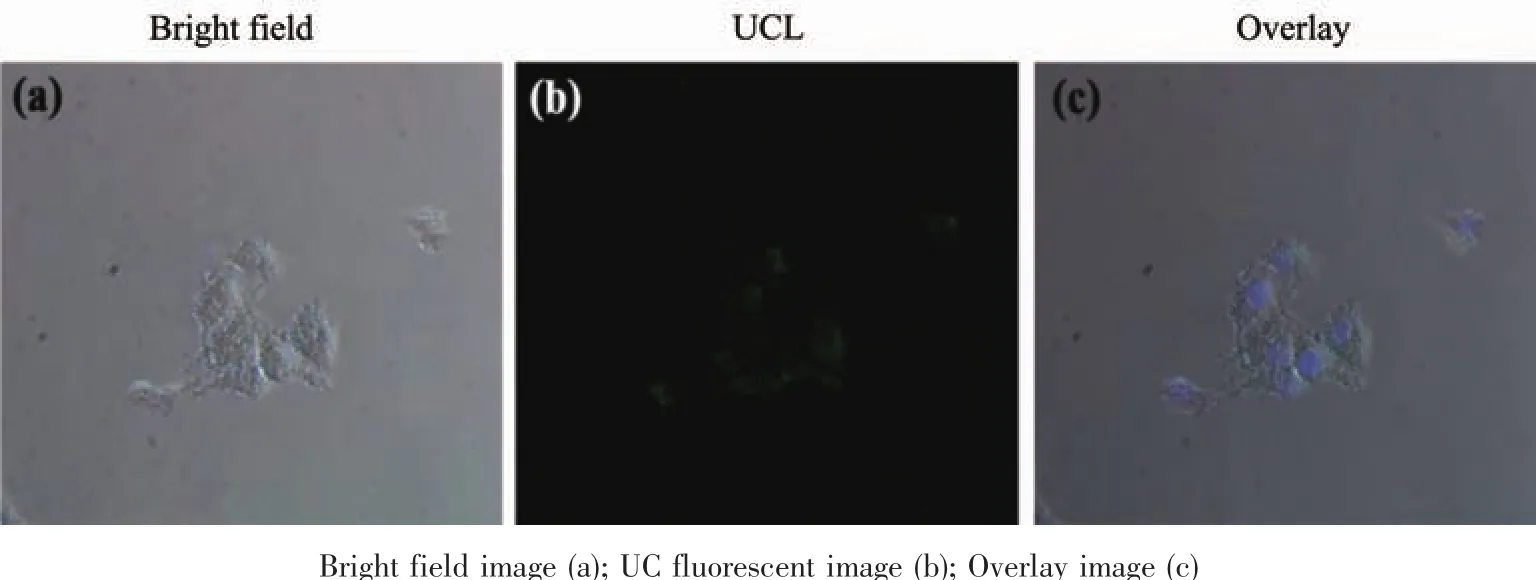
图9 同Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料共同培养的HeLa细胞在980 nm激光照射下的上转换成像照片Fig.9 UCL imaging images of HeLa cells incubated with Ag@BaGdF5∶Yb3+,Ho3+nanocomposites under 980 nm excitation
2.8 CT成像
Ag和Gd元素具有较大的原子序数,能够成为CT成像的造影剂,测试了不同浓度的商用造影剂碘比醇ガ和 Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料(NCs)的CT成像照片,如图10(a)所示。CT信号强度随着样品浓度(C)的增加而增强。图10(b)为不同浓度的Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料和碘比醇对应的hounsfield unites(HU)值,分别用 k1和 k2来表示斜率。由该图可见,k1和k2分别为10.86和5.0,说明同碘比醇相比,纳米复合材料具有较高的CT造影能力。因此,纳米复合材料能够作为CT成像的造影剂。
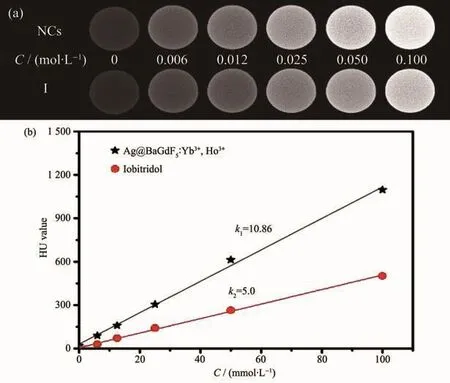
图10 不同浓度的Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料和碘比醇的CT图像 (a)和HU值的线性对比图 (b)Fig.10 CT imaging images(a)and HU values(b)of Ag@BaGdF5∶Yb3+,Ho3+nanocomposites and iobitridol with different concentrations(a)
2.9 光热治疗分析
由于Ag纳米粒子具有光热转换性质,为了证实复合材料能够作为光热治疗试剂使用,采用FDA/PI共染研究来评估其光热治疗效果。将HeLa细胞同纳米复合材料共同培养后在808 nm激光下照射5 min,通过共聚焦荧光显微镜进行表征(图11)。由图可见,在磷酸盐缓冲溶液控制组中,用808 nm激光照射,细胞没有明显的死亡现象。将纳米复合材料同HeLa细胞共同培养,没有激光照射时,HeLa细胞几乎没有死亡,这也说明纳米复合材料具有很好的生物相容性。当用808 nm激光照射后,发现大量细胞死亡。说明纳米复合材料在NIR照射下会产生热,生成的热足以杀死大部分肿瘤细胞。进一步说明了 Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料有潜力应用于光热治疗领域。
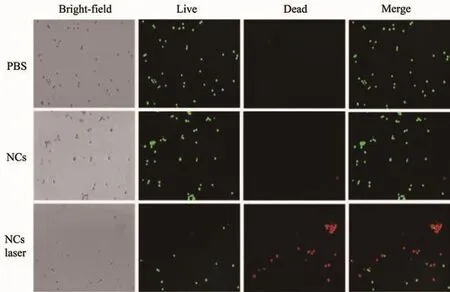
图11 Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料共同培养的FDA/PI共染的HeLa细胞在808 nm激光照射5 min后的共聚焦图像Fig.11 Confocal images of FDA/PIco-staining HeLa cells incubated with Ag@BaGdF5∶Yb3+,Ho3+nanocomposites under 808 nm laser irradiation for 5 min
3 结 论
通过简单的液相法成功合成了核壳结构的Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料。 该复合材料为球形,平均直径为106 nm。同时具有良好的生物相容性、顺磁性、上转换发光和光热转换性能,可应用于上转换荧光成像、CT成像。在NIR照射下,纳米复合材料能够生成大量的热,有效杀死癌细胞。因此Ag@BaGdF5∶Yb3+,Ho3+纳米复合材料在肿瘤细胞的双模式成像指导的光热治疗方面有潜在的应用。

