聚吡咯/二氧化锰复合材料的制备及其电化学性能研究
李倩,符婉琛,张存社,王悦,王伟
(1.长安大学 环境科学与工程学院 旱区地下水文与生态效应教育部重点实验室,陕西 西安 710054;2.陕西省石油化工研究设计院,陕西 西安 710054)
在能源储存设备中,超级电容器由于其高功率密度、快速充电/放电能力、长循环寿命、优秀的可逆性等优点使其在各个领域得到广泛应用[1-4]。目前的电极材料研究中,二氧化钌[5]、二氧化锰[6]、三氧化二钴[7]、镍氧化物[8]以及钒氧化物[9]研究较多。MnO2因其廉价、低毒、环境污染小而且理论比电容高,引起研究者的广泛关注[10-11]。单一的MnO2导电性较差、比电容低、循环稳定性差[12-14],现有的研究主要通过掺杂改性、材料复合等方法来提高MnO2的综合电化学性能。
导电聚合物具有高导电率、易制备、低廉环保以及理论比容量高等优点[15-17],也是超级电容器电极材料的研究热点。但是,聚吡咯与纳米MnO2反应复合制备PPy@MnO2纳米复合材料研究较少[18],对反应条件和参数的控制鲜有文献报道。
本文使用简便的水热合成方法,制备出海胆状MnO2纳米球[19]。在酸性条件下使用吡咯对二氧化锰纳米球进行包覆,在此反应过程中,二氧化锰充当氧化剂和模板,制备出新颖的PPy@MnO2纳米复合结构。用PPy@MnO2纳米复合材料作为工作电极,在1 mol/L的Na2SO4溶液中利用三电极体系测试了MnO2纳米球、PPy@MnO2复合材料的电化学性能,结果表明,改性后的PPy@MnO2纳米复合材料是理想的超级电容器电极材料。
1 实验部分
1.1 试剂与仪器
硫酸锰、硫酸钾、过硫酸钾、吡咯、浓硫酸、浓盐酸等均为分析纯。
Hitachi S-4800冷场发射扫描电镜;Bruker D8 Focus X射线衍射仪;科思特CS310电化学工作站;AVATAR360傅里叶红外光谱仪。
1.2 PPy@MnO2纳米材料的制备
1.2.1 MnO2纳米材料的制备 将1.812 g MnSO4·H2O、2.090 9 g K2SO4·H2O、3.243 8 g K2S2O8溶于90 mL浓度0.6 mol/L硫酸溶液中,磁力搅拌使其溶解。转移至150 mL聚四氟乙烯内衬的水热反应釜中,于不同反应温度(60,80,140 ℃)下反应12 h。过滤,用去离子水反复洗涤,过滤、干燥,得MnO2纳米材料。
1.2.2 PPy@MnO2纳米材料的制备 将MnO2纳米材料以及酸化后的乙炔黑溶于60 mL浓度0.02 mol/L HCl溶液中,标记为A溶液。根据MnO2与吡咯比例不同,量取不同体积的吡咯溶液溶于40 mL浓度0.02 mol/L HCl溶液中,标记为B溶液。将溶液B转移至溶液A中,磁力搅拌,制备PPy@MnO2纳米复合材料。过滤,用去离子水反复洗涤,过滤、干燥,得PPy@MnO2纳米复合材料。
1.3 电化学性能测试
电化学性能测试采用三电极体系进行,以所制备的材料为工作电极,Pt电极为辅助电极,Ag/AgCl电极为参比电极,1 mol/L的Na2SO4溶液为电解液,分别进行循环伏安、恒电流充放电和电化学阻抗谱测试。
2 结果与讨论
2.1 材料表征
2.1.1 物相分析 图1为在三个不同温度下制备的MnO2的XRD谱图。
由图1可知,三个样品均有9个明显的衍射峰,分别位于18.107,28.841,39.010,41.968,49.864,56.372,60.274,69.711,78.588°处,分别对应MnO2(PDF#44-0141)上的(200)、(310)、(330)、(301)、(411)、(600)、(521)、(541)、(332)晶面,表明在不同温度下合成的产物均为α-MnO2。随着温度的升高,衍射峰强度也相应增大,证明三个产物的结晶度随着温度的升高而随之增大。

图1 α-MnO2-(60,80,140)的XRD谱
2.1.2 红外光谱分析 α-MnO2、PPy@α-MnO2-60的红外谱分别见图2、图3。

图2 α-MnO2-(60,80,140)的红外谱图
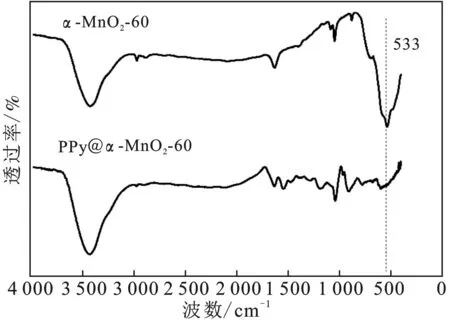
图3 α-MnO2-60和PPy@α-MnO2-60的红外谱图

2.1.3 形貌分析 图4为在不同温度下制备的MnO2的SEM图。

图4 α-MnO2-60 (a,b,c)、α-MnO2-80(d,e,f) 和α-MnO2-140 (g,h,i)的SEM图
Fig.4 The SEM images of α-MnO2-60(a,b,c),α-MnO2-80(d,e,f) and α-MnO2-140(g,h,i)
由图4 (a,d,g)可知,在不同反应温度下所得到的产物形貌均为海胆状,由图4 (c,f,i)中可以看出,这些海胆状MnO2均由MnO2纳米棒自组装而成,而且随着温度的升高,单个纳米棒的直径在增大,归因于温度升高有利于晶体的生长。
图5为PPy@α-MnO2-60的SEM图。
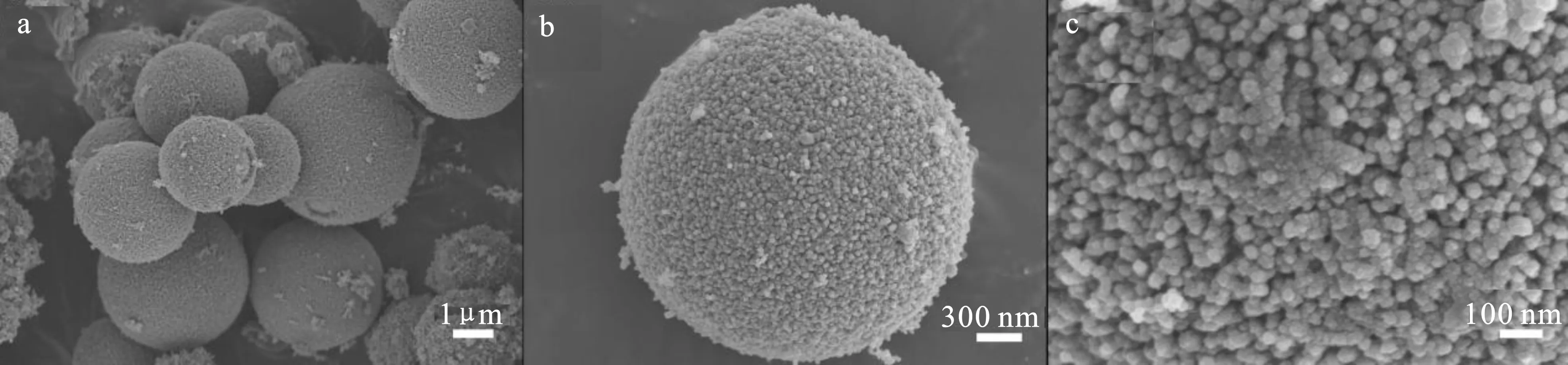
图5 PPy@α-MnO2-60 SEM图
Fig.5 The SEM image of PPy@α-MnO2-60
由图5可知,图4的MnO2纳米棒已完全消失,被纳米球所代替,结合红外谱图可以推断出,这些纳米球即为聚吡咯。在此过程中,MnO2充当氧化剂和模板的作用。
2.2 MnO2电化学性能
不同温度下制备的MnO2进行电化学性能测试,结果见图6。图6a是三个样品在电位范围为-0.2~0.6 V,扫描速率为20 mV/s的条件下得到的循环伏安曲线;图6b为三种材料在电流密度为0.5 A/g时,在三电极体系下测得的恒电流充放电曲线(GCD);图6c为α-MnO2-60电极材料的循环伏安曲线;图6d为α-MnO2-60电极材料在不同电流密度下的充放电曲线。
由图6a可知,三个样品的循环伏安曲线均无明显的氧化还原峰,这与MnO2的储能机理是一致的。三个样品的循环伏安曲线均近似矩形,表现出良好的电化学性能。60 ℃下制备的MnO2矩形的面积远大于在80 ℃和140 ℃下制备的MnO2的面积,说明60 ℃下制备的MnO2电化学性能最佳。
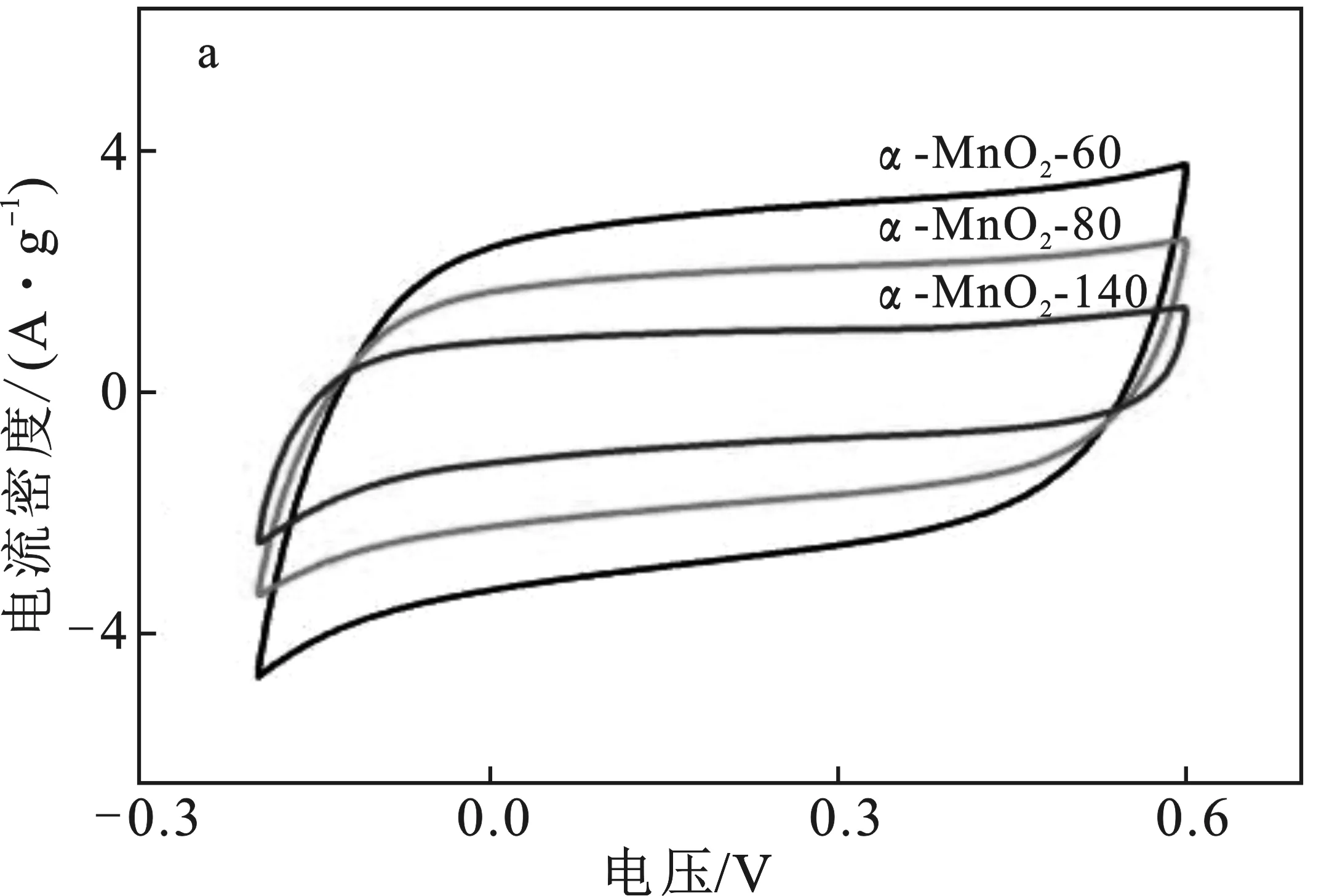


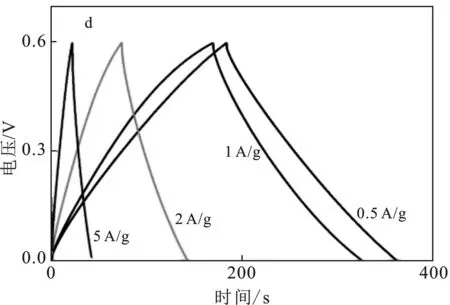
图6 α-MnO2-(60,80,140)的循环伏安曲线和充放电曲线
由图6b可知,三种MnO2电极的充放电曲线近似对称三角形,表明三种电极材料均具有优异的可逆充放电性能。60 ℃下MnO2电极材料比其它两种温度下制备的MnO2电极材料具有最长的放电时间,通过计算,60 ℃下MnO2电极材料在0.5 A/g下的比电容为135.4 F/g,其他两个电极材料的比电容分别为93.31 F/g和45.8 F/g。
由图6c可知,随着扫描速率的增加,α-MnO2-60电极材料的循环伏安曲线仍近似于矩形,说明当扫描电压在瞬间改变方向时,电流可以快速达到稳定,表明该电极材料内阻小且功率特性好,电极表面有良好的电荷传递特性,具有较好的比电容。而且随着扫描速率的增加,曲线的形状虽然有些变形,但仍近似为矩形,表明该电极材料具有良好的倍率性能,可在较快扫描速率下仍保持良好的充放电性能。
由图6d可知,随着电流密度增大,充放电时间变短,α-MnO2-60电极材料的整个充放电曲线仍近似对称三角形,与循环伏安结果相一致,证明该电极材料具有良好的可逆性。
2.3 PPy@α-MnO2-60复合材料电化学性能
2.3.1 包覆量对性能的影响 图7a为不同包覆量下PPy@α-MnO2-60循环伏安曲线,图7b为不同包覆量的PPy@α-MnO2-60在电流密度0.5 A/g的充放电曲线。

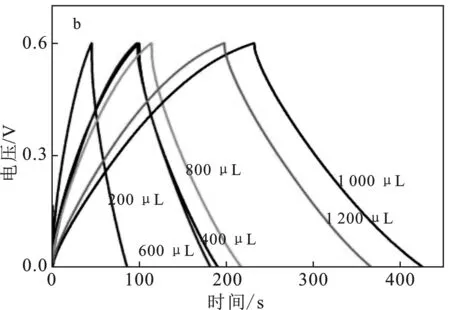
图7 不同包覆量PPy@α-MnO2-60的循环伏安曲线(a)和充放电曲线(b)
由图7a可知,不同包覆量下,PPy@α-MnO2-60循环伏安曲线均近似于矩形,表明在不同包覆量下所得到的样品均具有良好的电化学性能。当吡咯的量为1 000 μL时,所围成面积最大,所以可知当吡咯与二氧化锰质量比为10∶1时具有最大的比电容。
由图7b可知,不同包覆量的PPy@α-MnO2-60在电流密度0.5 A/g的充放电曲线均近似呈对称三角形,且当吡咯与二氧化锰质量比为10∶1时具有最长放电时间,表明PPy@α-MnO2-60复合材料在吡咯与二氧化锰质量比为10∶1时具有最大的比电容和优异的可逆性。
2.3.2 包覆时间对性能的影响 图8a为不同包覆时间下PPy@α-MnO2-60循环伏安曲线,图8b为不同包覆时间的PPy@α-MnO2-60复合材料在电流密度0.5 A/g的充放电曲线。


图8 不同包覆时间PPy@α-MnO2-60的循环伏安曲线(a)和充放电曲线(b)
由图8a可知,不同包覆时间下PPy@α-MnO2-60循环伏安曲线均近似于矩形,表明在不同包覆时间下所得到的样品均具有良好的电化学性能。包覆时间为6 h时,所围成面积最大,可知当包覆时间为6 h时具有最大的比电容。
由图8b可知,不同包覆时间的PPy@α-MnO2-60复合材料在电流密度0.5 A/g的充放电曲线均近似呈对称三角形,且当包覆时间为6 h时具有最长放电时间,表明PPy@α-MnO2-60复合材料在质量比为10∶1包覆时间为6 h时具有最大的比电容和优异的可逆性。
2.3.3 最佳PPy@α-MnO2-60复合材料电化学性能测试 图9a为最佳包覆条件下制备的PPy@α-MnO2-60复合材料在不同扫描速率下循环伏安曲线,图9b为最佳包覆条件下制备的PPy@α-MnO2-60复合材料在不同电流密度下的充放电曲线。
由图9a可知,随着扫描速率的增加,最佳包覆条件下制备的PPy@α-MnO2-60复合材料的循环伏安曲线仍近似于矩形,表明该复合电极材料具有较好的比电容。且随着扫描速率的增加,曲线的形状虽有些变形但还能保持矩形,表明该电极材料具有良好的倍率性能,可在较快扫描速率下保持良好的充放电性能。
由图9b可知,随着电流密度增大,充放电时间变短,最佳包覆条件下制备的PPy@α-MnO2-60复合材料的充放电曲线仍近似对称三角形,与循环伏安结果相一致,证明该电极材料具有良好的可逆性。经计算,该复合材料在0.5 A/g的电流密度下比电容为177.3 F/g。


图9 PPy@α-MnO2-60复合材料在不同扫描速率下循环伏安曲线(a)和不同电流密度下充放电曲线(b)
2.4 电化学阻抗测试
α-MnO2、PPy@α-MnO2-60的阻抗测试结果见图10。
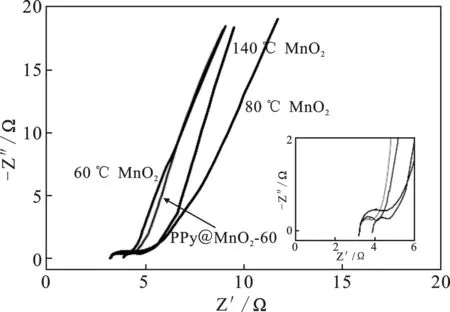
图10 α-MnO2-(60,80,140)和PPy@α-MnO2-60的阻抗图谱(插图为其高频区放大图)
由图10可知,α-MnO2-60具有最小的半径及最大的斜率,因而α-MnO2-60具有最小的电阻。这与前面通过循环伏安和充放电曲线所得结论相一致,证明60 ℃下制备的MnO2具有最佳的电化学性能。PPy@α-MnO2-60具有更小的直径及更大的斜率,表明PPy@α-MnO2-60具有更佳的电化学性能,这与之前通过循环伏安和充放电曲线所得结论相一致,证明通过包覆得到的复合材料具有更佳的电化学性能。
3 结论
(1)通过溶剂热法合成出不同温度下的海胆状MnO2,电化学性能测试表明,60 ℃下制备的MnO2具有最佳的比电容,在0.5 A/g的电流密度时比电容值为135.4 F/g。
(2)对60 ℃下制备的MnO2进行包覆改性,在包覆量为10∶1、包覆时间为6 h时,制得的复合材料具有最佳的电化学性能,在0.5 A/g的电流密度时比电容值为177.3 F/g。总体来说,包覆改性后的复合材料电化学性能较佳。

