艾滋病相关腹部淋巴瘤的CT表现及病理分析
赵强 ,王杏,孙君, 赵大伟, 李雪芹, 陈枫,史东立, 李宏军
艾滋病是由于人类免疫缺陷病毒感染引起的慢性传染病,在艾滋病患者中,淋巴瘤的发病率及疾病恶性程度高,预后较差[1]。淋巴瘤对放 、化疗较为敏感,及早诊断和治疗可提高患者的生存率,影像表现对淋巴瘤的诊断和鉴别具有重要作用。本文回顾性分析22例艾滋病相关淋巴瘤(acquired immune deficiency syndrome-related lymphoma,ARL)累及腹部病变的影像和病理表现,旨在加深对本病的了解,提高诊断水平,以期为临床诊断和治疗提供依据。
材料与方法
1.病例资料
搜集本院2012年1月-2018年1月经病理证实为淋巴瘤的艾滋病累及腹部病变患者共22例,均为男性,年龄22~53岁,平均35.6岁,CD4+T淋巴细胞计数为3~614个/μl,其中14例低于200个/μl。临床症状包括发热9例,消瘦1例,肢体乏力2例,腹部包块3例,腹股沟肿物2例,腹痛腹胀或不适5例,腹泻2例,肛周疼痛1例,皮肤、巩膜黄染1例,无明显症状1例。所有患者均诊断为AIDS,诊断标准依据2006年中华医学会感染病学会传染病分会AIDS学组制订的AIDS诊疗指南[2]。
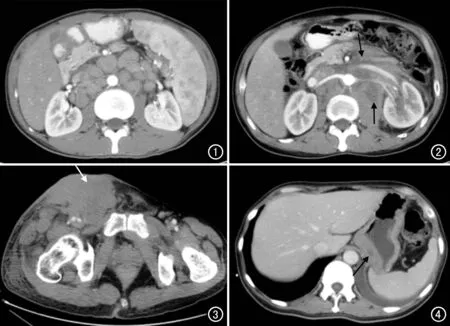
图1 艾滋病相关淋巴瘤患者,男,27岁,病变累及腹膜后。CT示腹膜后多发肿大淋巴结,病理为霍奇金淋巴瘤混合细胞型。 图2 艾滋病相关淋巴瘤患者,男,45岁,病变累及腹膜后。CT示腹膜后不规则形肿物伴坏死(箭),病理为非霍奇金淋巴瘤,弥漫大B细胞型。 图3 艾滋病相关淋巴瘤患者,男,41岁,病变累及右侧腹股沟区。CT示右侧腹股沟区多发肿大淋巴结,伴皮层软组织肿物(箭),最大径达14.8cm,病理为弥漫大B细胞淋巴瘤。 图4 艾滋病相关淋巴瘤患者,男,46岁,病变累及胃。CT示胃底部胃壁局限性增厚,增厚胃壁可见斑片状坏死(箭),中度强化,稍低于正常胃壁,病理为弥漫大B型淋巴瘤。
2.检查方法
22例患者均行腹部CT平扫及增强扫描。CT检查采用GE Light speed V CT 64层扫描仪,准直器宽度0.625 mm,管电流380 mA,管电压120 kV,层厚5 mm,层间距5 mm。扫描部位包括腹部和盆腔,增强扫描采用高压注射器经肘静脉以2.5~3.0 mL/s流率注入对比剂,分别行动脉期(25~30 s)、静脉期(65~70 s)及延迟期(180 s)扫描。
3.图像分析
所有患者的扫描图像均由两位资深腹部放射诊断医师进行分析,确定病变的密度、大小、累及范围、与周围组织的关系及强化方式等,意见不一致时经协商达成一致。选择直径大于1.5 cm的病灶,测量其平扫、动脉期、静脉期、延迟期的CT值,选取病灶显示最佳的3个不同层面,取其CT平均值作为最终CT值,CT值的测量应避开血管、囊变坏死组织及伪影等。
4.统计学分析
采用SPSS 21.0软件进行统计学分析。对腹部不同部位及不同病理分型的病变CT值比较采用单因素方差分析,采用卡方检验比较其时间-密度曲线走势的差异。以P<0.05为差异有统计学意义。
结 果
1.病理结果
22例艾滋病相关腹部淋巴瘤患者中非霍奇金淋巴瘤21例(95.5%),其中弥漫大B细胞型10例(47.1%),5例为单纯结内病变。霍奇金淋巴瘤1例,为结内及结外同时累及病变(表1)。
2.CT表现特点
本组22例中有5例为单纯结内病变,其余均可累及结外(77.3%);14例患者多部位累及(同时累及2个及2个以上部位)。
结内病变主要位于腹膜后(6例)和腹股沟(1例),腹膜后病变表现为腹膜后不规则肿物及多发肿大淋巴结(图1),不规则肿物影最大范围约12 cm×9 cm,CT平均值约40 HU,3例病变可见坏死(图2),3例肿大淋巴结可见融合,3例病变可见包绕血管(腹主动脉、下腔静脉、肾静脉),血管未见明显梗塞、栓子及中断征象(图2)。腹股沟病变表现为软组织肿物(图3),直径可达14.8 cm,密度较均匀,CT值约40 HU。

图5 艾滋病相关淋巴瘤患者,男,46岁,病变累及小肠。CT平扫示回肠管壁不对称性增厚,管壁内可见溃疡形成(箭)。 图6 艾滋病相关淋巴瘤患者,男,22岁,病变累及肝脏。肝脏病灶内可见门静脉穿行其中(箭),病理为B细胞淋巴瘤。 图7 艾滋病相关淋巴瘤患者,男,27岁,病变累及脾脏。CT示脾脏内多发结节状及类圆形低密度灶,轻度强化,明显低于脾脏实质。图8 艾滋病相关淋巴瘤患者,男,33岁,病变累及双肾、肾上腺、胰腺。CT示双肾、肾上腺及胰尾较均质肿块,强化程度明显低于肾、肾上腺及胰腺实质。病理为非霍奇金B细胞淋巴瘤,Burkitt淋巴瘤。
结外病变广泛累及胃肠道、肝、脾、胰腺、肾和肾上腺。2例胃部病变表现为胃壁局限性增厚,1例胃体及胃窦胃壁局限性较均匀增厚,1例胃底胃壁增厚伴斑片样坏死(图4),增强扫描均呈轻中度强化,强化程度低于周围正常胃壁,病灶周围脂肪间隙均较清晰。1例小肠病变表现为管壁增厚,周围脂肪间隙清晰,呈跳跃式,增强扫描呈较均匀强化,部分增厚管壁可见溃疡形成(图5)。2例结肠病变管壁较均匀增厚,周围脂肪间隙尚清晰,增强扫描呈较均匀强化。2例直肠病变管壁明显增厚,管腔狭窄,局部呈团块状软组织密度影,病变平扫CT平均值约42.5 HU,增强扫描均呈较均匀轻中度强化。
4例肝脏病变表现为肝内单发或多发类圆形稍低密度病灶,增强扫描呈轻度强化,强化程度低于周围肝实质,门静脉穿行于病灶内(图6),部分病灶分布于汇管区脉管鞘周围,沿脉管鞘延伸;均未见肝内外胆管扩张。3例脾脏病变表现:1例为脾内单发强化低密度小结节,直径约7 mm,边缘模糊。另2例表现为脾肿大,可见脾内多发结节状及类圆形低密度灶(图7),较大者直径达5 cm,增强扫描病灶均呈轻度强化,强化程度低于周围脾实质。4例累及胰腺者均表现为胰腺的等密度肿块,1例累及胰头,1例累及胰头和胰体,2例累及胰尾,均表现为较均匀轻度强化,强化程度明显低于周围正常胰腺,胰管均未见扩张(图8)。2例肾脏病变表现为双肾多发低密度结节(图8),增强扫描仍呈低密度,双肾未见积水,肾实质强化程度未见减低,1例累及输尿管,输尿管管壁增厚。2例肾上腺病变表现:1例为左肾上腺肿物伴出血坏死,直径达8 cm,增强扫描呈不均匀轻中度强化,左肾受压推移;1例表现为双侧肾上腺多发结节影,增强扫描呈轻度较均匀强化。
统计所有直径大于1.5 cm的病灶,测量其平扫、动脉期、静脉期、延迟期的CT值,得出不同部位及不同病理分型的艾滋病相关腹部淋巴瘤的时间-密度曲线图(图9、10),无论是不同部位还是不同病理分型,其时间-密度曲线的走势差异均无统计学意义(χ2=11.385,P=0.491;χ2=8.672,P=0.138。非霍奇金小B细胞淋巴瘤仅为1处病灶,故未列入统计分析)。
不同病理分型淋巴瘤(霍奇金淋巴瘤、非霍奇金弥漫大B细胞淋巴瘤、非霍奇金Burkitt瘤、非霍奇金T细胞淋巴瘤)的增强CT值差异有统计学意义(P值均<0.01,表2)。经两两比较后,霍奇金淋巴瘤增强各期(动脉期、静脉期及延迟期)的CT值均高于其他非霍奇金淋巴瘤(P值均<0.01);非霍奇金淋巴瘤中,除了弥漫大B细胞型与Burkitt瘤的动脉期CT值差异有统计学意义(P=0.025)外,其余弥漫大B细胞型、Burkitt瘤、T细胞来源三种类型的增强CT值之间差异均无统计学意义(动脉期:P=0.025,P=0.130,P=1.000;静脉期:P=0.516,P=1.000,P=1.000;延迟期P=0.309,P=0.081,P=1.000;比较顺序依次为弥漫大B细胞型与Burkitt瘤、弥漫大B细胞型与T细胞来源、Burkitt瘤与T细胞来源)。
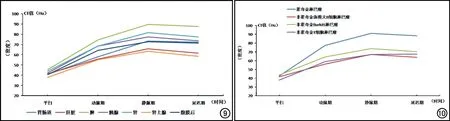
图9 艾滋病相关腹部淋巴瘤不同部位的时间-密度曲线图。 图10 艾滋病相关腹部淋巴瘤不同病理分型的时间-密度曲线图。
讨 论
1.艾滋病相关腹部淋巴瘤的临床与病理
艾滋病患者因其免疫功能下降更明显,并发淋巴瘤的概率更高。相关研究表明, ARL的发病率有增高趋势,已超过卡波西肉瘤,成为AIDS患者最常见的恶性肿瘤[3,4]。腹部各组织器官常受累及,是引发艾滋病患者多器官功能衰竭及死亡的重要原因之一。
ARL本质为免疫细胞恶变,其发生主要与患者细胞免疫功能缺陷严重程度和持续时间相关[5],本组50%以上的患者CD4+T淋巴细胞低于200个/μL,最低者为3个/μL,提示重度免疫抑制。大多数ARL伴随结外器官受累,本组病例广泛累及胃、空回肠、结肠、直肠、肝脏、脾、胰腺、肾、肾上腺等结外器官。ARL的临床表现呈多样化,发热是最常见的临床表现,累及腹部多为腹胀腹痛、腹泻、腹部包块、肛周疼痛等。
ARL源于具有临床侵袭性的单克隆B细胞系,主要病理类型为弥漫大B细胞淋巴瘤和伯基特淋巴瘤[6,7],两者中哪一种类型占多数说法不一[7,8];本组病例显示最常见的亚型为弥漫大B细胞型非霍奇金淋巴瘤。非霍奇金淋巴瘤可侵犯淋巴结、结外淋巴组织、结外非淋巴组织,或同时都有侵犯,单纯淋巴结病变仅占1/3[9],所以非霍奇金淋巴瘤中绝大多数为结外淋巴瘤。本组所有腹部相关淋巴瘤病例中非霍奇金淋巴瘤单纯结内病变为5例,比例更低(仅占23.8%),其余均累及结外病变。
2.艾滋病相关腹部淋巴瘤的CT表现
艾滋病相关腹部淋巴瘤中,结内病变是其最常见者,表现为多发肿大的淋巴结,腹腔淋巴结的解剖分布决定了结内病变的分布特征,以网膜淋巴结受累最为明显,肿大淋巴结可见融合,也可以是较大的软组织肿块影。腹膜后多发肿大的淋巴结融合后可包绕腹主动脉、下腔静脉、双肾静脉等,形成“血管包埋征”,包绕的血管可离开原来的位置而似漂浮状,形成“漂浮征”,血管多不受侵犯是其重要特点。由于肿瘤的恶性程度高,倍增时间短,肿块或肿大淋巴结因供血不足可出现中央坏死。
艾滋病相关腹部淋巴瘤结外病变的发生率较高,多部位均可受累。累及胃肠道多表现为管壁增厚,也可表现为局限性的结节状或类圆形肿物,实质脏器表现为密度较均匀且低于周围正常组织的结节状或类圆形肿物。累及胃肠道者均表现为肠壁不对称增厚,受累管壁柔软,伴或不伴溃疡形成,管腔有一定的扩张度,较少或不引起梗阻,肠管狭窄出现较晚且程度较轻为其主要特点[10];累及肝、脾、肾、肾上腺及胰腺者,增强扫描均表现为明显低于周围正常组织的结节或肿物影。发生于肝脏者可见病灶内有正常结构的门静脉穿行其中,血管于肿瘤内穿行而不受侵犯是其特征[11],病灶分布于汇管区脉管鞘周围,并沿脉管鞘延伸,具有一定的特征性。本组4例累及胰腺者胰管均未出现扩张,是其重要特征[12]。结外淋巴瘤瘤体细胞密集程度高,组织密实,密度较为均匀,坏死、囊变相对少见;瘤体细胞密集堆积于间质,肿瘤血管少而细小,多为乏血供肿瘤,肿瘤起源于脏器的间质,跨越或沿脏器解剖结构生长,因此肿瘤内常见原有解剖结构残存,周围侵犯程度相对较轻,这一点可与其他恶性肿瘤相鉴别,但需注意当淋巴瘤较小且呈孤立肿块时鉴别较为困难。
腹部不同部位或不同病理分型淋巴瘤的CT强化趋势大致相同,均表现为轻中度强化的特点。霍奇金淋巴瘤动脉期、静脉期及延迟期的增强CT值与非霍奇金淋巴瘤之间差异均存在统计学意义;非霍奇金淋巴瘤中,除了弥漫大B细胞型与Burkitt瘤的动脉期CT值差异有统计学意义外,其余三种类型的增强CT值之间差异均无统计学意义。以上表明由于病理类型不同,其CT表现存在差异,主要表现为霍奇金淋巴瘤的增强CT值均高于非霍奇金淋巴瘤。
艾滋病相关腹部淋巴瘤的CT表现具有一定的特征性,但需与淋巴结结核、淋巴结转移、Castleman病、组织坏死性淋巴结炎等相鉴别。淋巴瘤常呈均匀强化,即使少数病例增大淋巴结有坏死灶,但坏死灶周围增大淋巴结常呈均匀强化,不同于淋巴结结核的普遍呈环状强化,淋巴结结核中心为干酪样坏死物质,边缘为结核炎性肉芽肿[13]。淋巴瘤周围组织侵犯程度相对较轻,包绕血管但多不侵犯,不同于淋巴结转移瘤较大时可侵犯周围组织。淋巴瘤多为轻中度强化,而Castleman病血供较为丰富,增强扫描呈明显均匀强化[14]。组织坏死性淋巴结炎主要表现为颈部淋巴结肿大,影像表现上与淋巴瘤鉴别有时较为困难,有文献指出其肿大淋巴结呈延迟期明显强化[15]。
艾滋病相关腹部疾病中,淋巴瘤的CT表现具有一定特征性,最终确诊仍需依靠病理。AIDS相关淋巴瘤诊治专家共识指出,ARL最优治疗方案需要多学科协作,艾滋病相关腹部淋巴瘤的影像学表现具有重要价值,对疾病诊断与治疗具有重要的参考、指导及疗效监测作用[16]。随着对艾滋病相关淋巴瘤CT表现的深入研究,以期为临床提供更为准确、有价值的诊疗评估信息。

