肺肿瘤射频消融治疗的并发症分析
麦启聪 陈猛 苟庆 莫志强 时丰 陈晓明
射频消融(radiofrequency ablation,RFA)作为一 种微创治疗手段,在治疗早期不可切除非小细胞肺癌(non-small cell lung cancer,NSCLC)和转移性肺癌方面取得了显著成效,国内外已有大量文献报道[1-2]。目前RFA已成为肺癌综合治疗的手段之一,并引起了人们广泛的兴趣和重视[3]。本研究将我院近7年采用射频消融治疗肺肿瘤发生的并发症情况进行分析,并报道一例以往文献未见报道的罕见并发症肺脓肿并支气管瘘,同时总结肺肿瘤射频消融并发症的处理手段,以求将该技术更合理、安全、有效地应用于肺癌,更好地发挥该技术的临床价值。
资料与方法
一、一般资料
选取2010年4月至2017年12月我院收治的行射频消融治疗的原发性肺癌和转移性肺癌患者共150例。其中男103例,女47例;年龄32~89(58.3±7.5)岁。原发性肺癌患者纳入标准:(1)早期非小细胞肺癌不耐受手术或拒绝手术者。(2)外科手术切除后肺内复发或转移的患者。(3)经化疗、靶向治疗或放疗后肺内残留、复发或转移的病灶,不能耐受进一步的标准治疗或没有有效的标准治疗方法的患者。转移性肺癌患者纳入标准:(1)原发灶已治愈或控制良好的患者。(2)患者不耐受手术或拒绝手术者。排除标准:(1)病灶数目超过3个,或单个病灶直径>5 cm;(2)经皮穿刺肿瘤的路径有重要组织或脏器遮挡;(3)病灶与气管、主支气管、食管、主动脉及其分支、左右主肺动脉、心脏等之间的距离小于1 cm;(4)功能状态评分(PS评分)大于2分;(5)凝血功能严重异常或正在接受抗凝治疗者。150例患者中,原发性肺癌99例,转移性肺癌51例,全部患者均经术前病理或术中活检确诊。99例原发性肺癌包括非小细胞肺癌87例(鳞癌35例、腺癌48例、大细胞未分化癌4例),小细胞肺癌8例及癌肉瘤4例;51例转移性肺癌分别来自肝癌22例,来自软组织肉瘤12例,来自大肠癌9例,来自鼻咽癌6例,来自纵膈卵黄囊瘤及血管平滑肌脂肪肉瘤各1例。所有患者均为单个病灶,肿瘤直径8~47(26.0±3.6)mm。
二、消融设备
射频消融采用美国RITA公司生产的RITA1500型肿瘤射频消融治疗仪,发射频率400 kHz,功率1~250 W,电极针包括单针UniBlate和多极针StarBurat Xli 2种。操作均在CT引导下进行,采用美国GE公司的16排CT机。
三、射频消融治疗
所有患者术前均完善血常规、凝血指标及心肝肾功能检查。靶病灶行胸部CT平扫及增强扫描或行全身PET-CT扫描。术前签署知情同意书。术前半小时肌注盐酸哌替啶(杜冷丁)75~100 mg控制术中疼痛。所有患者均在CT引导下穿刺。将射频电极针通过穿刺放置在预定消融的肿瘤部位,随后根据病灶的大小设定消融功率和时间。直径≤30 mm的病灶采用单极射频针消融,>30 mm的病灶采用多极射频针消融或单针重叠消融。消融功率40~60(51.1±3.9)W,消融时间 3~12(6.3±2.7)min。行 1 次消融者133例,2次者17例;两次消融间隔1~4(2±0.5)周。
结 果
一、肺实质出血
本组发生肺实质出血35例,占23.3%(35/150)。CT扫描见肿块周围肺实质出现弥漫性高密度影,其中5例术后即有少量咯血,返回病房后给予止血治疗,1~3 d后咯血消失。
二、气胸
本组发生气胸29例,占19.3%(29/150)。其中26例患者术后CT扫描发现少量气胸,患者无明显自觉症状,血氧饱和度正常,未给予任何处理;另外3例行胸部X线片见有中等量气胸,患者轻度呼吸困难,血氧饱和度下降至90%~92%,给予吸氧后症状缓解,7~10 d后复查气胸吸收。
三、咯血
本组发生咯血12例,占8.0%(12/150)。其中包括上述5例肺实质出血患者术后即咯血,另外7例患者返回病房后开始咯血,均为少量间断咯血,给予镇静、止咳、止血等治疗,1~3 d后咯血停止。
四、胸腔积液
本组发生胸腔积液3例,占2.0%(3/150)。其中2例为少量的单纯胸腔积液,另1例在靠近穿刺点处出现一梭形包裹性积液,均未采取特别治疗,3~4周后复查积液均自行吸收。
五、肺脓肿并支气管瘘
本组发生肺脓肿并支气管瘘1例,占0.7%(1/150)。患者男性,63岁,确诊右侧肺鳞癌10年,外科手术切除术后复发,经放射治疗后肿瘤进展,行吉西他滨+卡铂化疗4周期,化疗后5个月复查PET-CT显示局部代谢增高(图1A),考虑肿瘤进展,遂行消融治疗。首次射频消融后,PET-CT复查显示肿块缩小,但仍有残留(图1B);1个月后再次行射频消融治疗(图1C),术后第5天患者咳嗽、咳浓痰、呼吸困难,并出现高热,CT显示原肿块坏死后形成空洞并与右上肺支气管相通,空洞内见有液气平面,考虑消融区域脓肿形成,故诊断为肺脓肿并支气管瘘形成(图1D)。遂于CT引导下行经皮穿刺肺脓肿置管引流,2周后症状逐步缓解,6周后复查CT见脓肿吸收,支气管瘘口愈合。
六、胸部皮下气肿
本组发生胸部皮下气肿1例,占0.7%(1/150)。射频消融术后CT扫描即发现少量皮下气体,返回病房后逐步增多。患者表现为气促、呼吸困难、上半身浮肿、胸部皮肤捻发音。给予吸氧、引流排气、包扎固定胸壁治疗,患者2周后复查,皮下气肿吸收,症状完全缓解。
讨 论
肺肿瘤射频消融的并发症较常见,部分可能造成严重后果,必须引起重视。按照文献报道的发生率可以分为常见并发症、少见并发症和严重并发症[4]。常见并发症包括气胸、胸腔积液、咯血和肺炎;少见并发症包括心包积液与心包填塞、皮下气肿、肺脓肿、膈神经损伤、支气管胸膜瘘、曲霉菌感染和针道种植转移等;严重并发症则指引起死亡。本组资料中,大多数为常见并发症,在少见并发症中发生肺脓肿并支气管瘘1例,以往文献未见报道;本组资料未出现死亡的病例。文献报道肺癌射频消融总的并发症发生率约为15.2%~55.6%,死亡率0~5.6%[4-7],各家报道的差异较大,可能与病例选择标准和样本量不同有关。下列因素可使并发症发生率明显增加:手术时间过长,尤其超过3 h;反复穿刺,尤其改变位置的多次穿刺;一次治疗多个病灶;伴有基础肺疾病或全身情况较差;操作者技术不熟练。
一、气胸
气胸是肺肿瘤射频消融最常见的并发症,其发生率约10%~61.1%[4],本组为19.3%。根据患者有无症状,可以分为有症状气胸和无症状气胸。无论是文献报道的病例,还是本组发生的病例,绝大多数气胸都没有症状,仅仅是在术中X线透视或CT扫描发现有气胸存在。而在有症状的患者中,多以轻度呼吸困难为主,给予吸氧后症状即可缓解;而吸氧无法缓解需要行胸腔闭式引流的气胸,本组患者均未行闭式引流。气胸的发生一般是脏层胸膜损伤后气体进入胸膜腔所致,穿刺本身以及消融都可以损伤脏层胸膜,因此要尽量减少穿刺次数,避免电极针留在胸壁。有学者采用呼吸针控的方法提高一次穿刺成功的几率,从而减少气胸等并发症的发生[8]。对于靠近胸膜的病灶,可以采用低功率和延长消融时间的方法减少气胸发生的风险。需要指出的是,气胸可以发生在术后若干天,称为迟发性气胸,应特别引起注意。
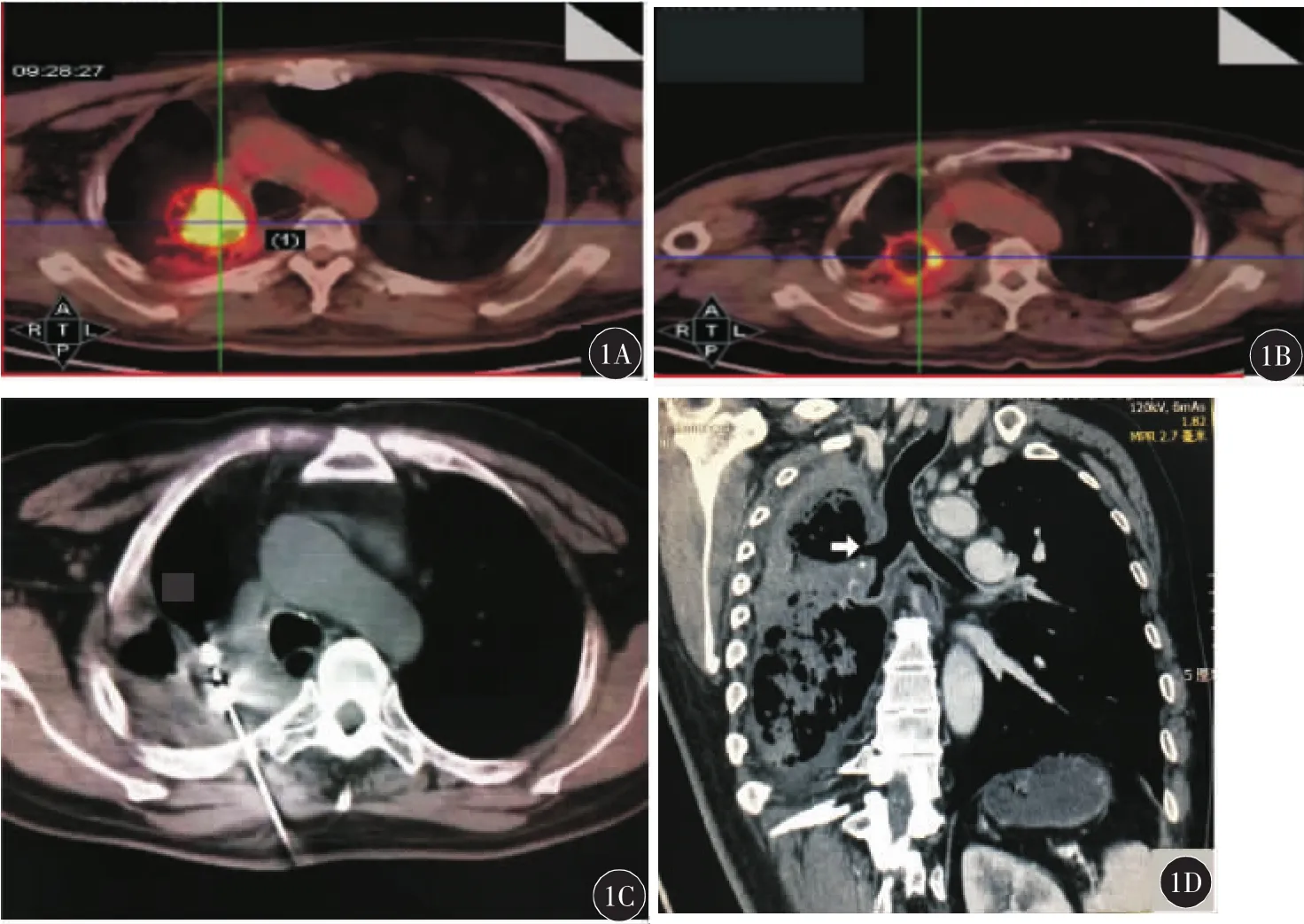
图1 典型病例(男性,63岁,右侧肺鳞癌10年,化疗后5个月肿瘤进展)行射频消融治疗前后
二、胸腔积液
文献报道胸腔积液发生率为4%~21%[4],本组为3%,属于较低水平。射频消融后并发胸腔积液的原因未见文献报道,笔者分析原因可能是一部分患者为反应性胸腔积液,是由于局部治疗后肿瘤组织坏死吸收产生的反应性积液,这类积液颜色通常为淡黄色;另一部分为损伤性胸腔积液,可能是由于穿刺时损伤了血管,导致积液为血性。无论哪种类型的积液,积液量多为少到中量,积液形式一般为单纯胸腔积液,也可以是局部包裹性积液,还可以合并液气胸。绝大多数胸腔积液可经保守治疗自行吸收,本组病例中出现胸腔积液的患者均自行吸收。
三、皮下气肿
斯晓燕等[7]报道29例中发生3例(10.3%)皮下气肿,发生率为10.3%(3/29)。本组150例中发生1例(0.6%)。患者在行肺射频消融术后行CT检查即发现少量皮下气体,回病房后逐步增多。临床表现为上半身浮肿、呼吸困难、皮肤有捻发音。发生原因可能为病灶靠近胸壁,穿刺或消融损伤壁层胸膜所致。该患者给予吸氧、引流排气、包扎固定胸壁等治疗,2周后吸收好转。
四、肺实质出血与咯血
本研究中笔者观察到肺实质出血不一定都会引起咯血,由于并非每个患者咯血发生后都行CT扫描,因此咯血是否一定合并肺实质出血暂时还不清楚。Nour-Eldin等[9]对164例患者的248个病灶进行消融后,44个病灶出现肺实质出血,其中40个导致了咯血,以消融病灶为基数计算,肺实质出血与咯血的发生率分别为 17.7%(44/248)和 16.1%(40/248);该作者提出了与肺内出血相关的一些重要危险因素:病变直径<1.5 cm(P=0.007),病变位于肺野中部和底部(P=0.026),穿刺针在肺实质内穿行的距离>2.5 cm(P=0.017),消融路径经过肺血管(P<0.001),应用多针电极(P=0.004)。笔者认为,出血与穿刺次数的关系较密切,因为在本组病例中,有75例患者于消融术前行穿刺活检,穿刺后CT扫描已发现肺实质出血。发生肺实质出血的患者大多无需治疗,而发生咯血的患者,需要根据咯血的速度和总量来判断是否需要行胸腔穿刺引流。
五、肺炎
国外有文献报道肺炎的发生率4.5%~16%[4],国内张欣等[10]报道肺炎的发生率为3.2%,本组病例无肺炎发生。消融术后发生肺炎的原因尚不清楚,可能与患者治疗前合并有肺气肿、慢性支气管炎、患者自身抵抗力低下等有关系,也可能与术中无菌操作不规范有关。消融术后严重的肺炎可以引起呼吸窘迫综合征而导致死亡,早期诊断早期治疗至关重要,如果术后出现高烧或发热时间过长的患者,尤其应引起重视。
六、心包积液与心包填塞
卢强等[11]报道了一组329例行肺肿瘤射频消融的患者中,3例出现心包填塞,发生率0.9%(3/329),其中1例死亡,该例患者的肿瘤靠近肺门,CT扫描时发现射频针已进入心包,患者死于出血引起的心包填塞。心包填塞一般继发于心包积液,可以是反应性积液,也可以是损伤性出血。如果发生缓慢,患者可以代偿;如果积液或积血过快过量,可导致患者死亡。所以如果发现患者术后有气促、胸痛、呼吸困难等症状,还应考虑是否有心包积液并行进一步检查,而一旦确诊应立即行心包穿刺,并进行抽液引流。
七、肺脓肿并支气管瘘
以往文献未见报道此并发症。本组发生1例,发生率0.7%(1/150),患者系右肺鳞癌放化疗后复发的患者,PET-CT显示右上肺局部代谢增高,标准治疗后患者症状无改善,肿块无缩小,故选用射频消融治疗。首次射频消融后患者症状明显改善,但复查PET-CT显示肿块边缘仍有残留活癌灶。再次行射频消融后第5天,患者出现咳浓痰、发烧、呼吸困难,CT显示右肺原肿块处形成一巨大空洞,其内可见液平面,空洞与右上支气管相通,考虑肺脓肿形成并支气管瘘。立即给予经皮穿刺置管引流,同时使用抗生素抗感染,患者症状逐步改善,6周后空洞愈合。
八、针道种植转移
本组中无针道种植转移并发症发生,卢强等[11]报道了6例(1.8%,6/329)发生针道种植转移,出现种植转移的发生时间在射频消融后4~6个月,发生率明显高过文献报道的0.06%(6/9 738)[12],可能与作者早期使用的射频消融治疗仪没有针道消融功能有关。目前临床上使用的设备一般都有针道消融功能,可见拔针前行针道消融还是必要的。
九、死亡
有关射频消融后出现死亡的现象,国内外文献报道的均较少。Nour-Eldin等[9]报道行射频消融治疗后因病灶部位大量出血导致死亡1例(0.4%,1/248)。卢强等[11]报道329例行射频消融治疗后2例死亡,其中1例死于消融术后大咯血;另1例死于心包出血引起的心包填塞。Simon等[13]报道75例I期非小细胞肺癌行射频消融治疗后,1例死于感染引起的急性呼吸功能衰竭。从以上作者报道的情况来看,死亡都是继发于前面讨论的一些并发症,由于处理不及时或处理效果不佳才导致死亡。因此,任何射频消融后的并发症,无论病情缓急,都应给予足够的重视。只有及时诊断并及时处理,才能减少和避免死亡的发生。

