Ag掺杂TiO2纳米颗粒的制备及光催化性能研究
汤艳娜,吴志荣
(宁波职业技术学院,浙江宁波 315800)
我国是印染大国,由此产生的印染废水量极大,加上印染废水成分复杂,常常含有难以降解的有毒有害有机污染物,已经成为工业污染的主要源头之一[1-2]。对于难降解的印染废水,目前的治理方法主要有生物法[3-4]、物理法[5-6]和化学法[7-8]。这些印染废水处理方法在研究和实际应用中都已经取得了较好的效果,但是目前仍然存在脱色困难、对不同印染废水的通用性差、可生化性低、能耗较高等问题。越来越多的研究表明,光催化能够为处理印染废水提供新的途径[9-10]。
自1972年发现TiO2具有光催化性能以来,由于优良的化学稳定性、较高的光催化活性、无毒无害等特点,被广泛应用于光催化降解各种有机污染物[11]。但是,TiO2作为光催化剂仍存在光谱响应范围窄、难以回收利用等问题,严重制约了TiO2处理实际印染废水的应用[12]。为此,研究人员进行了大量的改性尝试。其中,Ag、Au 等贵金属离子掺杂后的TiO2具有较高的催化活性,能够提高光谱响应范围,且制备方法简单,成为最常用的改性方式[13]。本实验拟通过溶胶-凝胶法制备Ag 掺杂TiO2,并以亚甲基蓝(MB)溶液为模拟印染废水,研究Ag 掺杂对TiO2光催化降解印染废水活性的影响。
1 实验
1.1 仪器
LABRAM-HR 拉曼光谱仪(Raman)(Jobin Yvon Horibra公司),D2 X射线衍射仪(XRD)(Bruker公司),Lambda 35紫外-可见分光光度计(UV-Vis)、LS 55光致发光光谱仪(PL)(Perkin Elmer 公司),JEM 2100 扫描电镜(SEM)(JEOL 公司),iS10 傅立叶红外光谱仪(FT-IR)(Nicolet公司)。
1.2 试剂
四异丙醇钛、硝酸银、冰醋酸、乙醇(均为分析纯),去离子水。
1.3 Ag掺杂TiO2纳米颗粒的制备
利用溶胶-凝胶法制备Ag掺杂的TiO2纳米颗粒:将不同量硝酸银加入到80 mL 去离子水中,并加入5 mL冰醋酸;将四异丙醇钛加入到70 mL乙醇中,并持续搅拌。将两种溶液逐滴混合并大力搅拌,形成的溶胶持续搅拌2 h,室温静置48 h得到凝胶,过滤后的沉淀物用乙醇和去离子水清洗,100 ℃干燥12 h。将干燥后的粉末研磨并在400 ℃退火4 h,再次研磨得到样品,分别标记为纯TiO2、2%Ag-TiO2、4%Ag-TiO2、6%Ag-TiO2、8%Ag-TiO2。
1.4 光催化实验
利用MB 作为模拟印染废水,研究样品在可见光照射下的光催化活性。利用500 W碘钨灯作为光催化反应的光源,光源位于反应器内部,垂直照射液面。为了保持溶液的温度恒定,反应器壁设计成双层结构,内部有连续流动的冷却水。将180 mg催化剂加入到180 mL 10 mg/L 的MB 溶液中,在无光照条件下搅拌60 min,达到吸附-解吸平衡。每隔一段时间取出5 mL 溶液,离心过滤去除光催化剂,得到降解后的MB溶液。利用UV-Vis测试MB溶液在663 nm的吸光度,利用以下公式计算降解率:
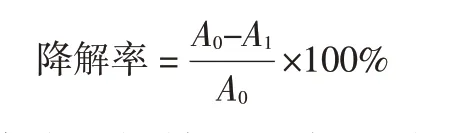
其中,A0为MB溶液的初始吸光度,At为光催化反应后MB溶液的吸光度。
2 结果与讨论
2.1 表征
2.1.1 Raman光谱
如图1所示,在143.0、193.6、394.2、515.7和637.2 cm-1处均存在衍射峰,其中515.7 cm-1处的峰为A1g峰和B1g峰重叠而成[14]。没有出现Ag 的氧化物峰,说明掺杂的Ag 进入了TiO2晶体结构。如图1插图所示,随着Ag掺杂比例的提高,位于143.0 cm-1处的峰朝着波数增加的方向轻微平移,可能是由于晶体结构存在替换、晶粒尺寸变化或晶体缺陷等[15]。另外,Ag 掺杂比例不同,峰宽也有变化,这可能是由于不同颗粒尺寸具有不同的动力常数和振动振幅[16]。

图1 TiO2和Ag掺杂TiO2的Raman光谱图
2.1.2 XRD
如图2所示,所有样品的特征峰都与TiO2的锐钛矿结构相匹配(JCPSD:21-1272)。没有发现Ag 及其氧化物的衍射峰,这与Raman光谱相符,说明Ag掺杂没有明显破坏锐钛矿的晶体结构。随着Ag 掺杂比例的提高,主要衍射峰朝着2θ减小的方向移动,并且衍射峰变宽,TiO2锐钛矿结构畸变严重。

图2 TiO2和Ag掺杂TiO2的XRD图
2.1.3 UV-Vis
如图3所示,随着Ag掺杂量的增加,样品的禁带宽度减小,这是由于Ag掺杂量增加后,光子可以在更宽的波长范围内被吸收,吸收光谱发生红移。禁带宽度减小有利于增加对太阳光的利用率,另一方面也能有效减少光生电子和空穴的复合,有利于提升光催化活性。

图3 TiO2和Ag掺杂TiO2的UV-Vis图及禁带宽度
2.1.4 FT-IR
如图4所示,3 443 cm-1处的峰为O—H 的弹性振动,1 633 cm-1处的峰为O—H 的弯曲振动,归因于水分子的吸收。羟基自由基在光催化过程中对提升光催化降解MB活性具有重要作用。在2 925~2 855 cm-1范围内的峰呈现对称和反对称振动,可能是由于表面活性剂的存在,而在450~850 cm-1范围内的峰对应Ti—O的振动。

图4 TiO2和Ag掺杂TiO2的FT-IR图
2.1.5 PL谱
PL 谱是研究半导体电子结构、迁移行为和光生电子-空穴复合概率的重要方法。如图5所示,纯TiO2和Ag 掺杂TiO2的峰位置几乎一样,但Ag 掺杂TiO2的峰强度低于纯TiO2。PL 谱的强度与电子和空穴的复合直接相关,PL强度越低,表明电子和空穴的复合概率越低,更多的光生电子和空穴可参与到光催化反应过程中。4%Ag-TiO2的PL强度最低,表明4%Ag-TiO2的光生电子-空穴复合概率最低,具有最高的光催化活性。

图5 TiO2和Ag掺杂TiO2的PL图
2.1.6 SEM
如图6所示,纯TiO2、2%Ag-TiO2和4%Ag-TiO2均为团聚的球状颗粒结构,相比纯TiO2,Ag掺杂后的催化剂颗粒尺寸有所减小。另外,利用EDX分析了样品的成分,结果表明,在Ag 掺杂TiO2样品中,Ag 离子成功与TiO2结合。

图6 TiO2和Ag掺杂TiO2的SEM图
2.2 光催化降解MB活性
4%Ag-TiO2光催化降解MB溶液的情况见图7。

图7 4%Ag-TiO2光催化降解MB溶液
如图7所示,为了确定MB溶液能否自发降解,同时证明催化剂在光催化降解MB溶液中的重要性,设置了相同条件下无催化剂的空白对照实验(图7插图),结果发现,在无催化剂条件下,MB 几乎不发生降解。当有4%Ag-TiO2催化剂存在时,在无光照条件下,MB 的浓度发生了轻微下降,这是由于染料分子吸附于催化剂表面,造成MB 浓度下降。随着光照时间的延长,吸光度显著下降,说明随着光照的进行,MB的浓度显著变小,MB发生了光催化降解。
如图8所示,随着时间的延长,MB的浓度都出现了下降,表明MB 被光催化降解,60 min 后,纯TiO2对MB 的降解程度最小,仅为30%,随着Ag 掺杂量的增加,对MB 的降解增加,当Ag 掺杂量为4%时,60 min后MB 的降解率达到96%,这是由于Ag 的加入减小了光生电子-空穴的复合概率,增强了光催化活性,这与PL谱的结果一致。继续增加Ag的掺杂量,MB的降解程度反而下降,这可能是由于过量的Ag 破坏了晶体结构,增加了材料内部的复合中心,反而造成光催化活性下降。

图8 Ag掺杂TiO2对MB溶液的光催化降解性能
可重复性是光催化剂稳定性的重要指标,为了研究Ag 掺杂TiO2的稳定性,选择光催化活性最高的4%Ag-TiO2做重复光催化降解实验。如图9所示,即使经过5 次光催化降解实验,4%Ag-TiO2的光催化活性也没有明显降低,具有良好的稳定性。

图9 4%Ag-TiO2光催化剂的降解能力随降解次数的变化
3 结论
(1)Ag 掺杂TiO2能有效光催化降解MB,其中4%Ag-TiO2展现了最佳的光催化活性,60 min 后对MB的降解率达到了96%。
(2)光催化活性的提升一方面归因于Ag 掺杂TiO2光生电子-空穴复合概率的降低,增加了载流子的利用率;另一方面是由于Ag 掺杂TiO2的吸收光谱发生红移,增加了对太阳光的利用率。

