基于TDM的血液病/恶性肿瘤患者使用伏立康唑的疗效与安全性分析
廖刚,王双英,易寒英,李婷,郑自通,姚旭,3,李荣
(1.南华大学 药学院,湖南 衡阳,421001;2.邵阳市中心医院,湖南 邵阳,422000;3.湖南省分子靶标新药研究协同创新中心,湖南 衡阳,421001 4.南华大学 附属第二医院,湖南 衡阳,421001)
随着医疗技术的发展,血液肿瘤患者的生存周期逐渐延长,但此类患者由于自身免疫功能低下,反复放、化疗及长时间使用免疫抑制剂和皮质类固醇等,极易导致侵袭性真菌感染(IFIs),增加死亡率。念珠菌及曲霉菌为侵袭性真菌感染的主要致病菌[1]。
伏立康唑为广谱三唑类抗真菌药,具有抗菌谱广、抗菌效力强的特点,对曲霉、隐球菌、念珠菌属等均具有杀菌活性,是预防和治疗血液系统疾病合并侵袭性真菌感染的一线用药[2]。但伏立康唑的药物疗效个体差异大,易发生ADR,为保证患者用药的安全性和有效性,有研究推荐1~5.5μg·mL-1为其目标谷浓度范围[3]。
文中旨在通过对我院血液病/恶性肿瘤患者使用伏立康唑治疗后的TDM数据进行回顾性分析,探索在血液病/恶性肿瘤患者中,伏立康唑血药谷浓度与临床疗效及不良反应的关系,为临床药师参与临床治疗,合理用药、促进临床安全提供参考经验。
1 资料与方法
1.1 病例选取
选取2017年1月~2017年12月参与血液肿瘤科预防性和治疗性使用伏立康唑治疗的血液病/恶性肿瘤患者,共7例,具体见表1。
表1 患者基本情况一览表
Table 1 The basic information of patients
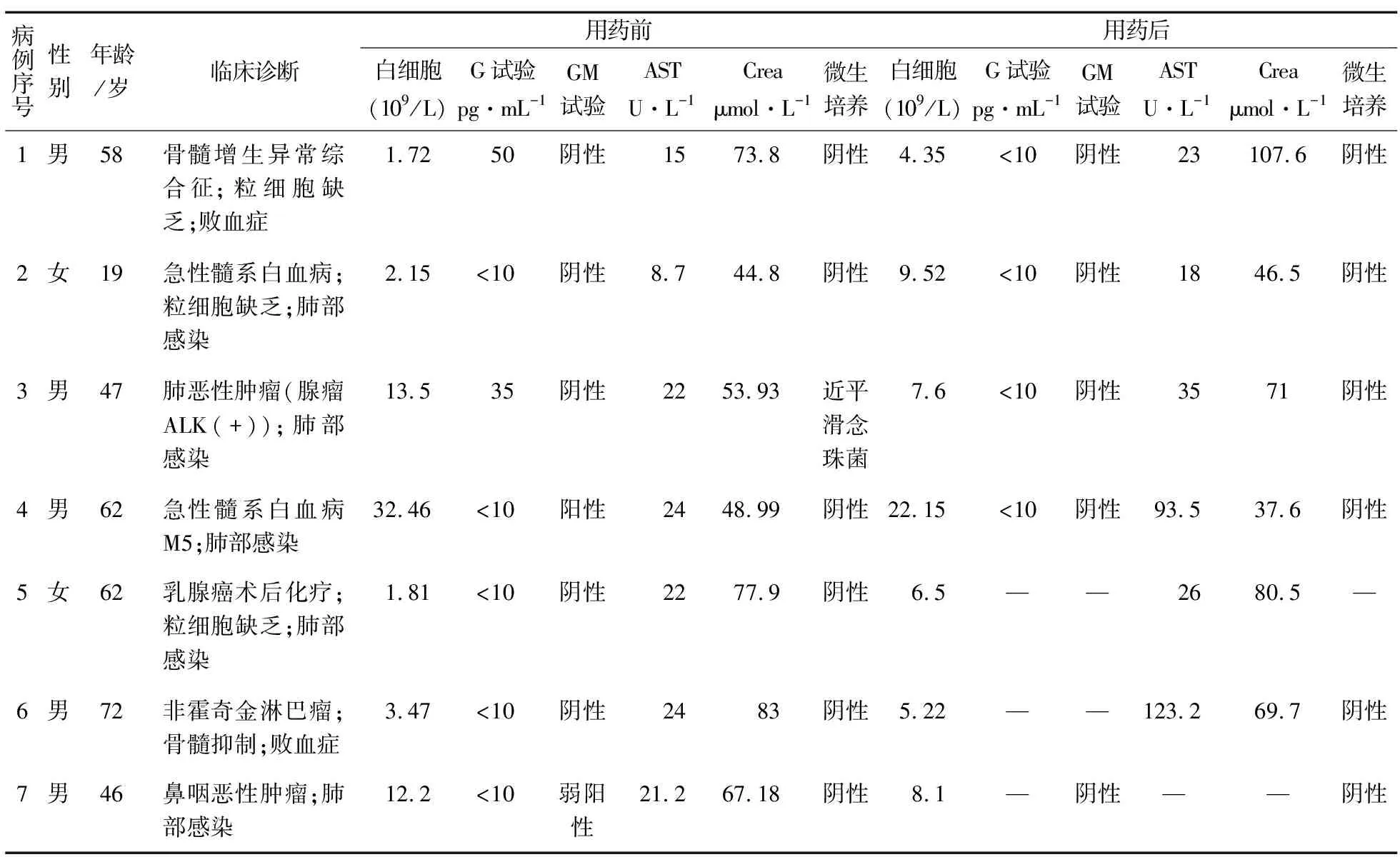
病例序号性别年龄/岁临床诊断用药前用药后白细胞(109/L)G试验pg·mL-1GM试验ASTU·L-1Creaμmol·L-1微生培养白细胞(109/L)G试验pg·mL-1GM试验ASTU·L-1Creaμmol·L-1微生培养1男58骨髓增生异常综合征;粒细胞缺乏;败血症1.7250阴性1573.8阴性4.35<10阴性23107.6阴性2女19急性髓系白血病;粒细胞缺乏;肺部感染2.15<10阴性8.744.8阴性9.52<10阴性1846.5阴性3男47肺恶性肿瘤(腺瘤ALK(+));肺部感染13.535阴性2253.93近平滑念珠菌7.6<10阴性3571阴性4男62急性髓系白血病M5;肺部感染32.46<10阳性2448.99阴性22.15<10阴性93.537.6阴性5女62乳腺癌术后化疗;粒细胞缺乏;肺部感染1.81<10阴性2277.9阴性6.5——2680.5—6男72非霍奇金淋巴瘤;骨髓抑制;败血症3.47<10阴性2483阴性5.22——123.269.7阴性7男46鼻咽恶性肿瘤;肺部感染12.2<10弱阳性21.267.18阴性8.1—阴性— —阴性
注“—”:表示未复查。
1.2 给药方案及血样采集
所有注射给药的患者均按照伏立康唑说明书推荐,第一天均给予负荷剂量6mg·kg-1,q12h;第二天起给予 4mg·kg-1,q12h维持。口服给药患者第一天给予200mg,q12h;第二天起150mg,q12h维持。7例患者均给予负荷剂量,所有患者均连续使用3d后[4],在下一次给药前抽取静脉血2~3mL置抗凝管中送检。
1.3疗效评价标准
全部入选患者的疗效根据血液病/恶性肿瘤患者侵袭性真菌感染的诊断标准与治疗原则(第五次修订)进行判定[5]。具体疗效评价指标:1)经验治疗或诊断驱动有效评判指标:①开始治疗至停药后7d 内无新发真菌感染;②开始治疗至停药后7d内患者存活;③治疗过程中未因ADR或缺乏疗效导致停药;④开始治疗后患者在中性粒细胞缺乏期间退热;⑤确诊或临床诊断IFD在治疗结束时达到完全或部分有效。2)目标治疗有效的评判指标:①有效:完全缓解和部分缓解;②无效:稳定、疾病进展与死亡。
2 结果
2.1 血药浓度测定结果与剂量调整
当测定谷浓度低于1μg·mL-1且治疗无效时,增加给药日剂量的50%;当测定谷浓度高于5.5μg·mL-1和/或发生不良反应时,减少给药日剂量的20%或停药[6],具体见表2。
2.2 疗效评价
7名患者中,6人有效,1人(病历序号3)因合并包括急性呼吸衰竭、心力衰竭等,病情复杂和危重,医治无效死亡,具体见表2。
表2 患者用药情况及转归一览表
Table 2 Status and outcome of drug use in patients
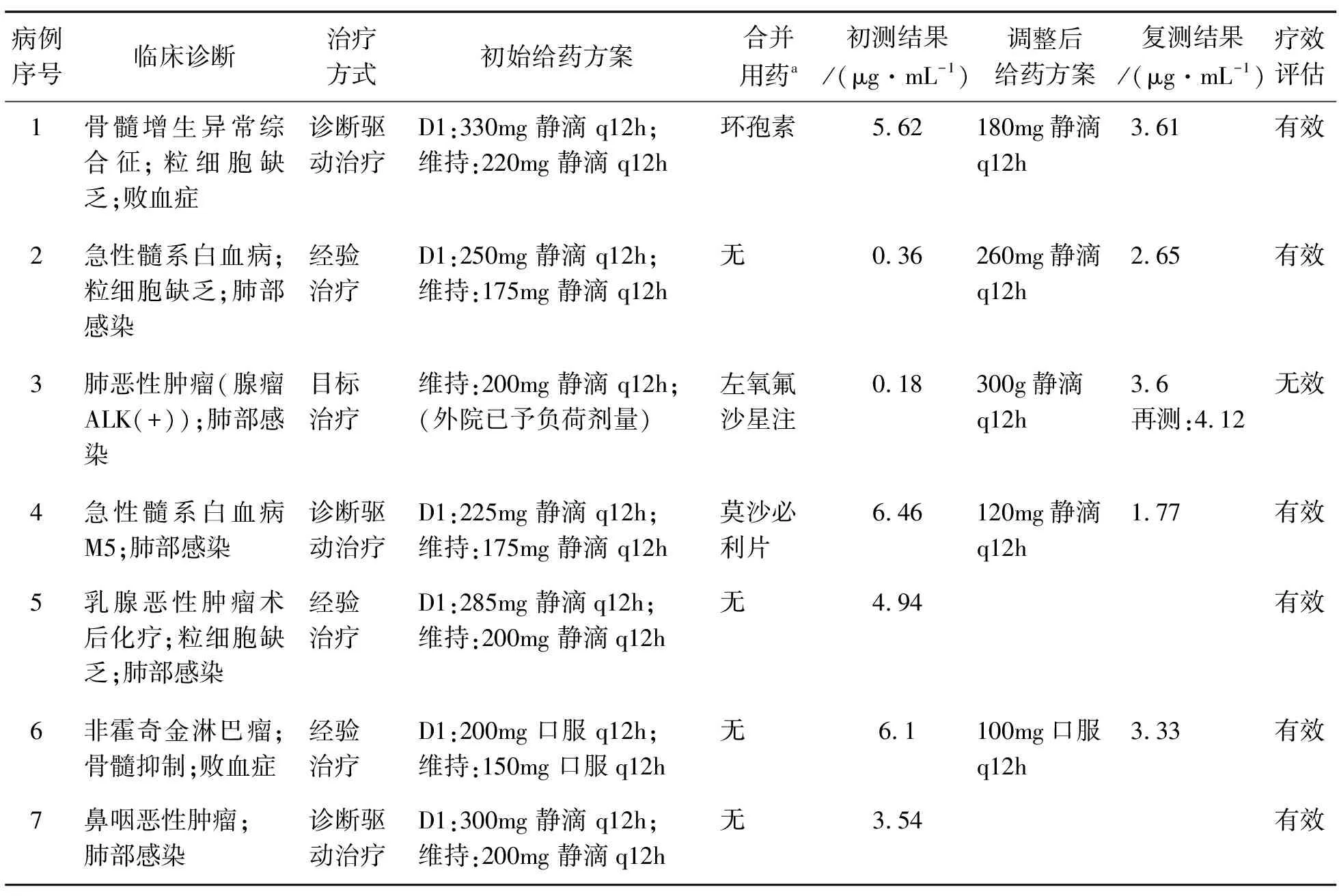
病例序号临床诊断治疗方式初始给药方案合并用药a初测结果/(μg·mL-1)调整后给药方案复测结果/(μg·mL-1)疗效评估1骨髓增生异常综合征;粒细胞缺乏;败血症诊断驱动治疗D1:330mg 静滴 q12h;维持:220mg 静滴 q12h环孢素5.62180mg静滴q12h3.61有效2急性髓系白血病;粒细胞缺乏;肺部感染经验治疗D1:250mg 静滴 q12h;维持:175mg 静滴 q12h无0.36260mg静滴q12h2.65有效3肺恶性肿瘤(腺瘤ALK(+));肺部感染目标治疗维持:200mg 静滴 q12h;(外院已予负荷剂量)左氧氟沙星注0.18300g静滴q12h3.6再测:4.12无效4急性髓系白血病M5;肺部感染诊断驱动治疗D1:225mg 静滴 q12h;维持:175mg 静滴 q12h莫沙必利片6.46120mg静滴q12h1.77有效5乳腺恶性肿瘤术后化疗;粒细胞缺乏;肺部感染经验治疗D1:285mg 静滴q12h;维持:200mg 静滴q12h无4.94有效6非霍奇金淋巴瘤;骨髓抑制;败血症经验治疗D1:200mg 口服 q12h;维持:150mg 口服q12h无6.1100mg口服q12h3.33有效7鼻咽恶性肿瘤;肺部感染诊断驱动治疗D1:300mg 静滴 q12h;维持:200mg 静滴q12h无3.54有效
注:文献显示可与伏立康唑发生相互作用的药物[7]
2.3 不良反应发生情况及转归
有2名患者在用药3天后复查肝肾功能,发现天门冬氨酸氨基转移酶升高,通过调整给药剂量,并予以还原型谷胱甘肽1200mg·d-1静滴对症处理,3天后复查转氨酶均降至正常;1名患者在开始输注伏立康唑过程中发生注射部位疼痛、面色潮红,临床药师会诊后,建议减慢输液滴速,不良反应症状逐步消失;有1名患者用药1天后发生视觉障碍,根据血药浓度,临床药师建议减少伏立康唑给药日用量的20%后症状消失;所有患者均无腹泻、恶心、呕吐、焦虑、幻觉、寒战、乏力等不良反应(表3)。
表3 不良反应累及器官及其临床表现
Table 3 Adverse reactions involving organs and their clinical manifestations

病例序号临床诊断用药前用药后AST/(U·L-1)Crea/(μmol·L-1)AST/(U·L-1)Crea/(μmol·L-1) 不良反应临床表现1骨髓增生异常综合征;粒细胞缺乏;败血症1573.823107.6视觉障碍2急性髓系白血病;粒细胞缺乏;肺部感染8.744.81846.53肺恶性肿瘤(腺瘤ALK(+));肺部感染2253.933571注射部位疼痛、面色潮红4急性髓系白血病M5;肺部感染2448.9993.537.6 转氨酶升高5乳腺恶性肿瘤术后化疗;粒细胞缺乏;肺部感染2277.92680.56非霍奇金淋巴瘤;骨髓抑制;败血症 2483123.269.7 转氨酶升高7鼻咽恶性肿瘤;肺部感染21.267.18——
注“—”:表示未复查。
3 讨论
侵袭性真菌感染是导致血液病/恶性肿瘤患者死亡的重要病因之一,白色念珠菌属和曲霉菌属是其常见的致病菌。伏立康唑是新一代广谱抗真菌药,被推荐作为预防和治疗一线用药[2,8]。
伏立康唑在体内主要通过肝脏P450酶系代谢,既是CYP450酶的底物,又是其抑制剂,易与其他具有相同代谢途径的药物发生相互作用[9],其主要代谢酶CYP2C19具有基因多态性,不同基因型患者使用相同剂量伏立康唑,其血药浓度也会有差异。另外,伏立康唑具有非线性药动学特征,患者病理生理情况、合并用药等因素均会影响其体内过程,使血药浓度具有较大的个体差异[10]。有研究证实伏立康唑的血药谷浓度与侵袭性真菌感染患者的临床疗效、不良反应密切相关,根据血药浓度监测结果调整给药剂量,控制其血清药物谷浓度在1~5.5μg·mL-1范围内,可以明显提高疗效,并减少ADR的发生,建议常规测定伏立康唑血药谷浓度[11]。
文中的7例血液病/恶性肿瘤患者中,仅2例的谷浓度初测在治疗窗范围内,2例偏低,3例偏高,经临床药师会诊,查阅文献[12]后,调整给药剂量后复测,均在治疗窗范围内,其中6例有效,总有效率达85.7%,1例患者因治疗无效死亡。该例死亡患者在上级医院确诊为近平滑念珠菌感染,初始使用伏立康唑治疗1周,临床咳嗽、胸闷等症状无好转,白细胞13.5×109/L,PCT1.65ng·mL-1,CRP 58mg·L-1,临床药师会诊建议监测伏立康唑血药谷浓度,患者的血药浓度初测值0.18μg·mL-1,调整给药剂量后复测,血药谷浓度为3.60μg·mL-1,患者咳嗽、胸闷等临床症状好转,复查白细胞8.6×109/L,PCT0.02ng·mL-1,CRP 0.77mg·L-1,痰涂片未见真菌,痰培养阴性,提示抗真菌治疗有效;5天后患者出现胸闷加重,端坐呼吸等情况,再次复测,血清药物谷浓度仍在治疗窗范围,查电解质正常,心脏彩超提示大量心包积液,最终因多器官功能衰竭救治无效死亡,综合该患者的临床情况分析,考虑患者最终死因为原发疾病恶化所致。
3例血药浓度偏高的患者均发生了ADR,其中2例表现为肝酶升高(此两例的初测血药浓度皆>6.0μg·mL-1),经调整给药剂量,并予以还原型谷胱甘肽1200mg·d-1静滴对症处理,复查转氨酶均降至正常;1例表现为视觉障碍,经减少给药剂量、减慢滴速处理后好转。还有一例患者血药浓度正常,但由于滴注速度过快导致注射部位疼痛、面色潮红,经减慢滴速处理后好转。3例初测血药浓度偏高的患者中,有1人合并使用了影响伏立康唑谷浓度的药物。本研究所涉及的患者中,最低的有效治疗浓度为1.77μg·mL-1,发生不良反应的最低浓度为5.62μg·mL-1,与文献[3,6,13]报道的伏立康唑治疗浓度范围1~5.5μg·mL-1相符。
综上所述,血液病/恶性肿瘤患者病情复杂,免疫力差,常需进行放疗和化疗,更易发生侵袭性真菌感染[14]。伏立康唑的临床疗效、不良反应与其血药谷浓度密切相关,但个体差异较大,易受患者病理生理、合并用药等多种因素影响。因此,建议临床在使用伏立康唑时常规进行TDM。临床药学是医药联系的纽带[15],在日常工作中,临床药师应与临床医生进行密切沟通,积极地参与到临床药物治疗之中,利用TDM为患者制定个体化给药方案,促进临床合理用药,保证患者用药安全。

