心脏再同步化起搏除颤器脉冲发生器电池耗竭降级治疗一例
郭兰燕 刘兵
患者,男,72岁,主因发现脉冲发生器电池耗竭1天入院。患者6年前因劳力性心慌气短半年入当地医院诊疗,无阵发性心悸、头晕、晕厥等不适。当地医院诊断为扩张型心肌病,并植入心脏再同步化起搏除颤器(CRT-D)(圣犹达V350)一级预防。术后患者规律服药,一般状况好转,且心慌气短的临床表现明显改善。2016年12月6日,常规程控检查发现起搏器电池耗竭入院治疗。既往史、个人史及入院查体无特殊异常。
访问起搏器程控界面,有四个报警,分别提示脉冲发生器达到EOL电压、电池电压<2.2 V,上次最长充电≥28 s,均提示起搏器电池耗竭;输出电路可能受损;PMT检测:4。进一步观察腔内标记图发现心房、心室感知也出现异常。2016年10月31日程控界面提示因至少一次中途取消的充电。因为V-350无自动高压阻抗测试,推断此次为电容器重整无法进行或发放高压电击治疗失败,进一步询问患者,植入期间无阵发性心悸、晕厥及起搏器放电史,且自2014年5月9日上次随访以来,CRT-D未记录到任何快速性心律失常事件。所以,高度怀疑此次报警中“输出电路可能受损出现至少一次中途取消的充电”系除颤回路故障导致电容器重整无法进行(电容器/电池维护间期为3个月/次)。为了明确除颤回路是否完好,与家属沟通后决定尝试进行高压阻抗测试,并告知病人可能会出现电击感而做好准备。但因为电池耗尽,高压阻抗测试失败,不能明确除颤回路是否故障,唯一的验证方法是连接新的CRT-D脉冲发生器进行高压阻抗测试。进一步程控,右房、右室及左室起搏导线阻抗良好。当地医院锁骨下静脉造影提示左侧锁骨下静脉完全闭塞且侧枝循环形成(图1)。为了进一步明确诊疗方案,遂转入本院。
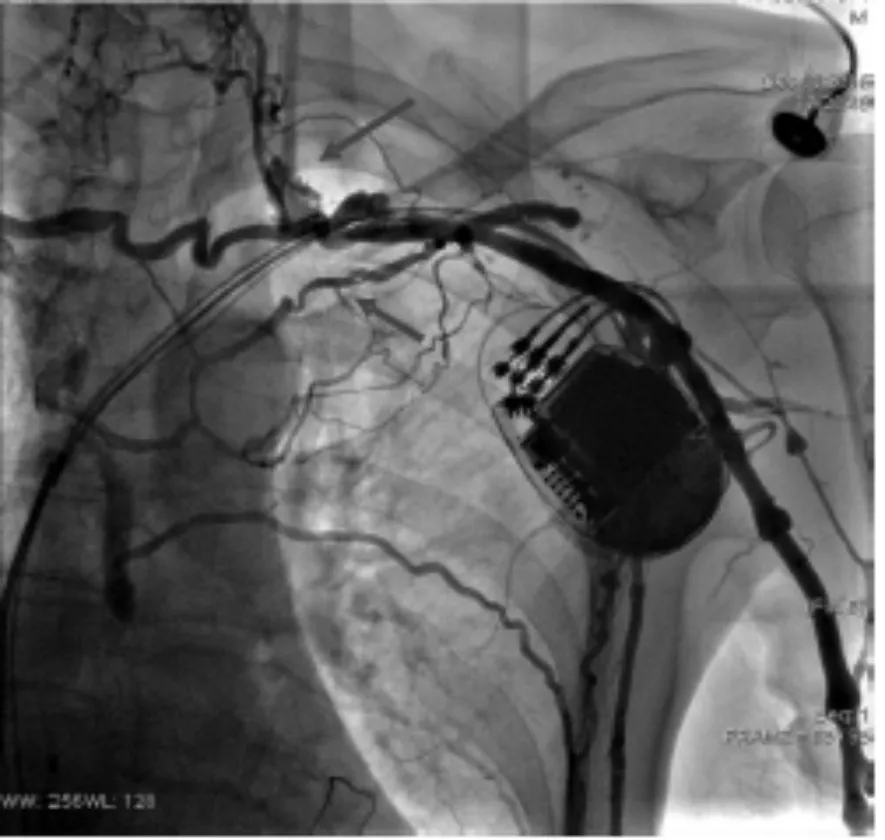
图1患者X线影像 左侧锁骨下静脉闭塞,侧枝循环形成。箭头示侧枝循环
本院术前心电图提示窦性心动过缓伴室性早搏及心室起搏节律;起搏不良。心脏彩超提示三腔起搏器安置术后,起搏器导丝位置正常,高位乳头肌水平以下左室前壁运动搏动幅度减低,双房(左房49 mm、右房44 mm)、左室(57 mm×59 mm×72 mm )大,主动脉硬化并主动脉瓣钙化,左室收缩功能减低[左室射血分数(LVEF)0.45],二、三尖瓣及主动脉瓣中量返流。血液常规及生化检查无明显异常。
与患者及家属充分沟通病情及治疗方案,权衡利弊/风险与收益比,患者及家属最终决定更换为美敦力的C2TR01 CRT-P脉冲发生器(被迫降级)。术中测试,原右室电极起搏、感知良好,继续使用,除颤电极DF1接口包埋处理(术前程控心电图显示感知异常,现怀疑与电池临近耗尽有关);心房、左室电极各项参数良好。
术后给予规范阿司匹林肠溶片100 mg,每天1次;培哚普利8 mg,每天1次;美托洛尔缓释片 95 mg,每天1次;螺内酯20 mg,每天1次;呋塞米10 mg,每天4次;辅酶Q10 20 mg,每天3次。半年后,患者常规随访提示起搏器工作正常,电极导线起搏、感知、阻抗各项参数均正常,无特殊事件发生。复查心脏彩超提示心腔缩小(左室 55 mm×50 mm×78 mm),心功能有所改善(LVEF 0.48)。
讨论CRT是心力衰竭管理中重要的非药物疗法之一。CRT超反应定义为NYHA改善≥1级且LVEF≥0.10。对于CRT-D一级预防且属于 CRT超反应的患者,初始植入期间未发生过电击治疗事件,当脉冲发生器发生电池耗竭时,是继续更换CRT-D还是降级为CRT-P,目前尚无明确的定论。
对909例CRT术后患者进行生存率分析,以LVEF≥0.50作为超反应标准,研究发现超反应的患者其生存率与正常人无明显差异[1]。有临床研究[2]发现ICD一级预防者更换时约有25%的患者没有ICD更换的指征,且更换后年接受ICD治疗的比例远远低于有ICD指征的患者(2.8% vs 10.7%)。一项大样本量的回顾性研究[3]分析了423例CRT术后的患者,270例完善术后超声且1年内无放电者纳入随后的研究统计中,结果发现CRTD术后LVEF≥0.45者 2年恰当放电的比例大概是2%。研究提出植入CRTD后LVEF改善到0.45的患者,更换时选择CRT-P可能是一个好的选择,尤其是初始植入时是一级预防且植入期间无放电的患者。
REPLACE研究[4]是一项前瞻性、多中心的临床研究,收集起搏器或ICD术后6个月内的并发症发生情况。1队列仅更换脉冲发生器,无新增电极;2队列更换且升级或新增电极。研究发现2队列较1队列整体手术并发症发生率增高,主要表现在导线脱位、导线失功能、血肿、感染等,其中CRT升级或导线重置组的并发症最高,约为18.7%。因此起搏器更换或升级时需要考虑到手术相关的风险,尤其在获益有限的情况下。Danish研究[5]是一项多中心、前瞻性、随机对照的大样本量的临床研究。研究发现非缺血性心肌病的ICD一级预防未能减少远期的全因死亡及心血管死亡风险。且年龄大于68岁的非缺血性心肌病者,ICD一级预防获益不明显,没有显著减少全因死亡率。因此,在更换起搏器时,我们应该综合评估患者的危险分层(超反应/无反应)、术者的经验、经济效益综合评价、ICD不恰当治疗经历或患者的生存期望(合并其他器官系统的终末期疾病,患者的生存欲望明显降低)等[6]。对于更换时无ICD指征的CRTD患者,更换时降级CRTP或者是继续CRTD,存在一定的学术争鸣,支持降级者主要考虑到风险与获益的平衡;支持继续CRTD者认为心功能改善后猝死风险降低,但并非降为零。因此,对于初始植入时是非缺血性心肌病的一级预防,且植入期间无ICD放电治疗的患者,更换时无ICD适应证者是选择降级还是继续CRTD治疗,尚需要进行大规模、前瞻性、随机对照的临床研究来获得最佳的临床指导。
本例患者被迫降级(“迫降”)的理由如下:患者年龄>70岁,初始植入为非缺血性心肌病的一级预防、治疗期间无ICD放电、CRT治疗后LVEF明显改善为CRT超反应者,继续优化药物治疗LVEF恢复正常后猝死的风险可能下降。其次,患者合并同侧锁骨下静脉闭塞,如果术中连接CRT-D脉冲发生器进行高压阻抗测试证实原除颤电极故障,需要拔除故障的双线圈电极,从对侧植入新的除颤电极,因此更换CRT-D的手术难度和围术期风险包括感染、血管损伤、心包压塞等等远远高于普通起搏器。再者,更换CRT-D的经济投入远远大于CRT-P。最后需要结合患者本人的意愿,此极其重要。

