4种检测方法对巧克力中亚利桑那沙门氏菌的检测结果比较
张红莉,李勇,许均华,郑文,徐文泱,欧露真,代洪梅
(1.郴州市食品药品检验检测中心,湖南郴州423000;2.郴州市疾病预防控制中心,湖南郴州423000;3.湖南省食品质量监督检验研究院,湖南长沙410111)
沙门氏菌是人畜共患病原菌之一,菌体溶解时,其细胞壁所含的脂多糖释放出来,形成内毒素[1],可引起伤寒与副伤寒(肠热症)、慢性肠炎、败血症、食物中毒等。目前已经发现近3 000 个种[2],确认的沙门氏菌血清型有2 579 种[3],每年全球因食品中沙门氏菌污染而引起的感染病例数以亿计,在世界范围内引起的食物中毒病例中常常排在首位[4-5],目前也有文献报道亚利桑那沙门氏菌感染人类致病的案例[6-8]。
由于亚利桑那沙门氏菌表型和生化反应极不稳定,因此明确其最优检测方法在食品安全检验中显得尤为重要。目前常用的检测方法有:利用生化反应的常规检验方法,如传统生化国标法[9]、VITEK 全自动微生物鉴定系统[10]等;利用VIDAS 的酶联免疫技术的法[11-12]等;利用分子生物学实时荧光聚合酶链式反应(polymerase chain reaction,PCR)等[13];利用蛋白质谱图基质辅助激光解析/电离飞行时间质谱法[14-16]等。各方法都存在一定的利弊,本实验室在2018年的中国合格评定国家认可委员会(China National Accreditation Service for Conformity Assessment,CNCA)“巧克力中沙门氏菌检验”中应用实时荧光PCR、VITEK 2、API 20E和GB 4789.4-2016《食品安全国家标准食品微生物学检验沙门氏菌检验》4 种不同的检测方法,分析比较其亚利桑那沙门氏菌检测效果。
1 材料与方法
1.1 仪器设备及试剂
实时荧光PCR7500:美国ABI 公司;VITEK 2 全自动微生物鉴定系统、API LAB 软件:法国生物梅里埃公司。
细菌DNA 提取试剂盒、沙门氏菌核酸检测试剂盒(PCR-荧光探针法):中山大学达安基因股份有限公司。VITEK 2 21341 革兰氏阴性细菌鉴定卡(GN 卡)、API 20E 试剂盒:法国生物梅里埃公司。
缓冲蛋白胨水(buffered peptone water,BPW)、四硫磺酸钠煌绿(tetrathionate broth base,TTB)增菌液、亚硒酸盐胱氨酸(seleite cystine broth,SC)增菌液、亚硫酸铋(bismuth sulfite,BS)琼脂、木糖赖氨酸脱氧胆盐(xylose lysine desoxycholate,XLD)琼脂、HE(hektoen enteric)琼脂、三糖铁(triple sugar iron,TSI)琼脂、营养琼脂(nutrient agar,NA)、邻硝基酚 β-D 半乳糖苷(2-nitrophenyl β-D-galactopyranoside,ONPG)、沙门显色平板A、沙门氏菌干制生化鉴定试剂盒:北京陆桥技术股份有限公司;沙门氏菌显色培养基B:法国科马嘉;沙门诊断血清:泰国S&A。
样品来源:中国合格评定委员会提供的含亚利桑那沙门氏菌的巧克力样本。
1.2 试验方法
1.2.1 实时荧光PCR 法
1.2.1.1 DNA 提取
把巧克力(NIFDC-PT-135)样品接种于45 ℃BPW缓冲蛋白胨水中融化后于36 ℃培养18 h,各取1 mL培养物接种10 mL TTB 于42 ℃培养24 h 和10 mL SC于36 ℃培养24 h。取1 mL 培养液于13 000 r/min 离心3 min,吸弃上清,用1 mL 已灭菌的ddH2O 悬浮,13 000 r/min 离心3 min,吸弃上清,重复上述步骤两次,加入含有200 μL 细菌裂解液瞬时离心后,将含有菌液的离心管沸水浴10 min 后,冷却2 min,13 000 r/min 离心10 min。取上清液备用。阴性质控和阳性质控品操作步骤同上,且参与提取,用于对环境进行监控。
1.2.1.2 实时荧光PCR 反应体系和参数
实时荧光PCR 反应体系为20 μL:17 μL Salm PCR反应液A(特异性引物、探针、三羟甲基氨基甲烷-盐酸缓冲液等)+3 μL Salm PCR 反应液B(热启动Taq 酶、UDG 酶等)。实时荧光PCR 反应参数为:50 ℃,2 min,95 ℃预变性15 min,94 ℃变性15 s,55 ℃退火延伸45 s,同时收集FAM 荧光,进行40 个循环,反应结束。
实时荧光PCR 结果判定:如果羧基荧光素(5-carboxyfluorescein,FAM)检测通道无扩增曲线或Ct值>38,可判样品为沙门氏菌阴性;如果FAM 检测通道Ct 值≤38,且曲线有明显的扩增,可判样品为沙门氏菌阳性。
1.2.2 VITEK 法
样品按GB4789.4-2016 经过选择性琼脂平板增菌,经TSI、赖氨酸脱羧酶初步生化确定为疑似沙门氏菌后,将菌落纯化,配制成菌悬液,充填到GN 卡内,封口后放入测试槽内,读取每小时卡片内细菌在各孔培养基内生长变化值,5 h~8 h 后出具结果。
1.2.3 API 20E 法
样品按GB4789.4-2016 经过选择性琼脂平板增菌,经TSI、赖氨酸脱羧酶初步生化确定为疑似沙门氏菌后,将菌落纯化,配制成菌悬液,接种于试剂条,于36 ℃培养18 h~24 h,观察生化反应结果。根据APILAB软件得到鉴定结果。
1.2.4 GB 4789.4-2016 法
根据GB 4789.4-2016 操作步骤进行,同时分别选择A 和B 两种显色培养基进行选择性分离后,用生化测试盒和血清做后续的鉴定步骤。
1.2.5 血清学试验
于洁净载玻片的测试区域及对照区域分别滴一滴抗血清和一滴生理盐水,用铂金丝沾取新鲜培养物单菌落一环,于载玻片上的抗血清和生理盐水中,分别将培养物和抗血清、培养物和生理盐水充分混匀,来回倾斜晃动载玻片30 s~1 min,观察凝集现象:O 抗原为颗粒状凝集;H 抗原为絮状或绒毛状凝集。
2 结果和分析
2.1 实时荧光PCR法检测结果
取1 mL 增菌液提取DNA 用于实时荧光扩增,结果如图1所示。增菌液扩增出阳性扩增曲线。
2.2 VITEK 2法鉴定结果
全自动微生物鉴定系统VITEK 2 鉴定结果见表1。
全自动微生物鉴定系统VITEK 2 分析结果为:肠沙门菌双相亚利桑那亚种Salmonella entericassp.diarizonae概率为98%,置信度极好。
2.3 API 20E法鉴定结果
肠杆菌和其它革兰氏阴性杆菌鉴定系统API 20E鉴定结果见表2。
API LAB 软件分析结果为:猪霍乱沙门菌亚利桑那亚种Salmonella choleraesuisssp.arizonae的概率为89%,被鉴定菌株与标准菌株的相似程度为0.64。
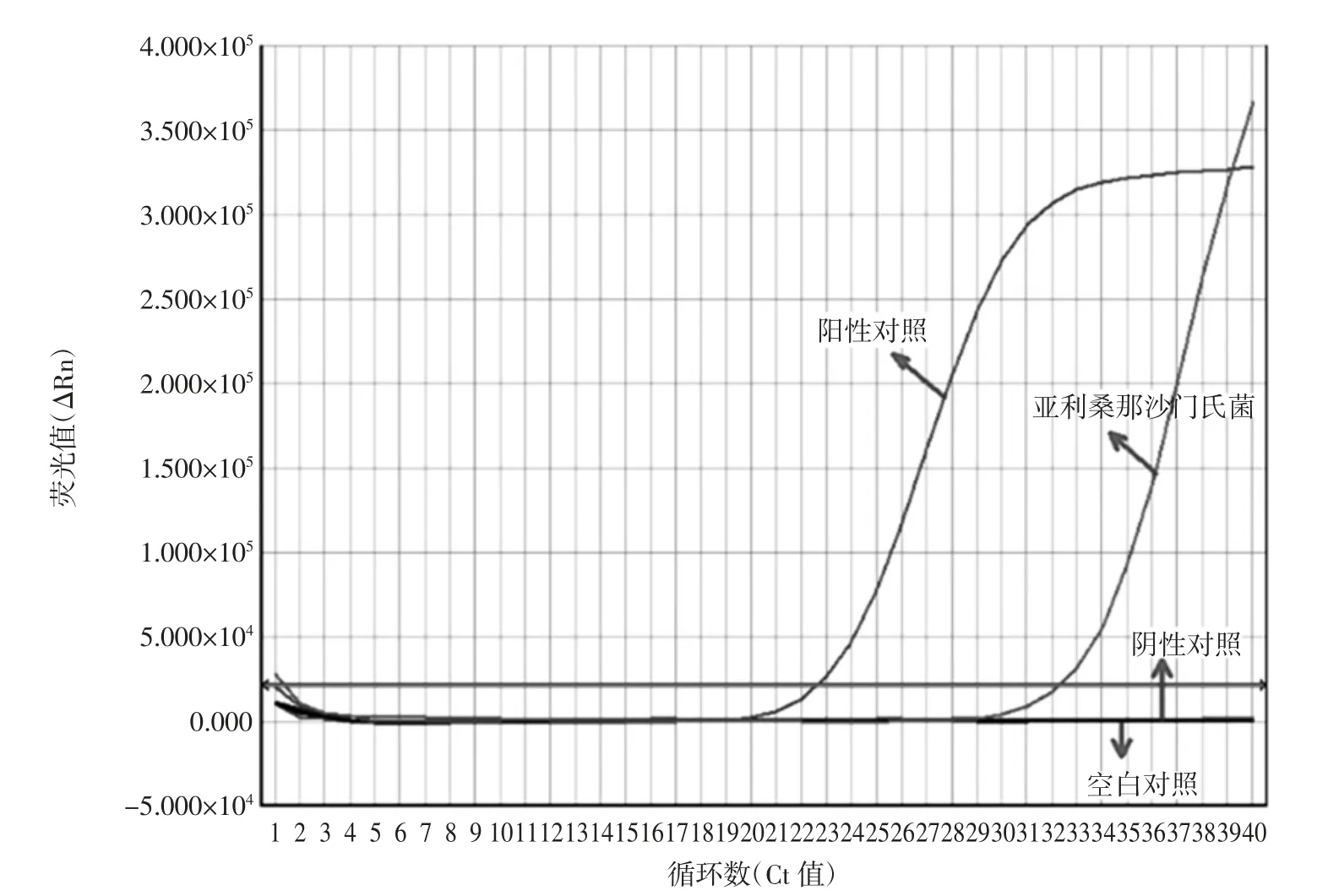
图1 亚利桑那沙门氏菌实时荧光PCR扩增图谱Fig.1 Amplification pattern of Salmonella arizonae by real-time PCR
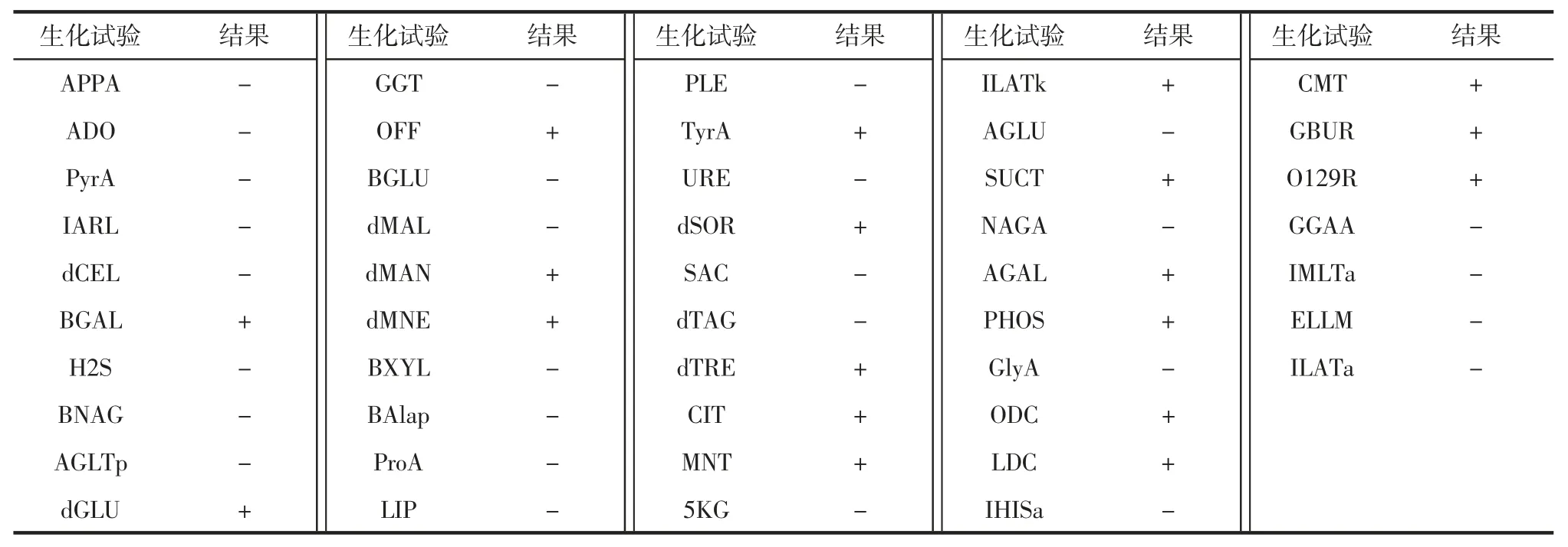
表1 样品在GN卡中的生化反应结果Table 1 The biochemical reaction results of the sample in GN card
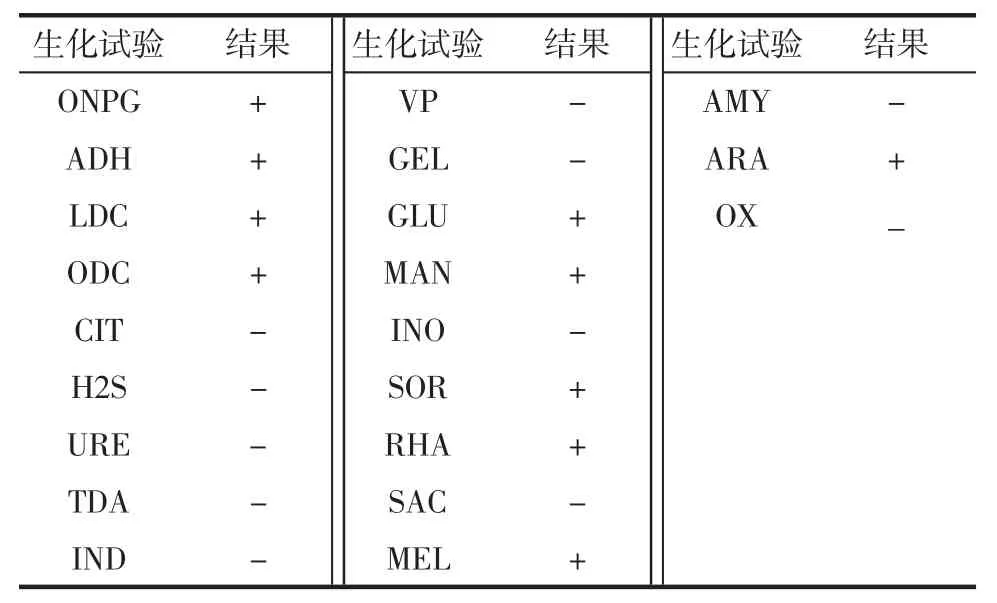
表2 样品在API 20E试条中的生化反应结果Table 2 The biochemical reaction results of the sample with API 20E system
2.4 GB4789.4-2016法鉴定结果
采用国标GB 4789.4-2016《食品安全国家标准食品微生物学检验沙门氏菌检验》对样品增菌液培养后再平板划线分离,由于沙门显色培养基的成分属于厂家保密范畴,所以同时采用了A、B 两个厂家的培养基进行生化鉴定,结果如表3所示。

表3 双相亚利桑那沙门氏菌在各种选择性培养基上的菌落特征Table 3 Colony characteristics of Salmonella arizonae in different culture mediums
双相亚利桑那在XLD、HE、沙显A 上的菌落都为非典型形态,BS、沙显B 上的菌落形态特征明显,尤其是沙显B 的金属蓝菌落,可以直接初判为乳糖阳性的沙门氏菌。此疑似阳性菌进一步做初步生化,生化反应鉴定结果见表4。
表3和表4结果符合GB 4789.4-2016 反应序号A3 的生化结果,应补做邻硝基酚β-D 半乳糖苷(2-nitrophenyl β-D-galactopyranoside,ONPG)生化鉴定,标准判读为ONPG 阴性为沙门氏菌,但实际检测结果ONPG 为阳性,标准并未给出结论。
进一步做沙门氏菌生化群的鉴别,鉴定结果如表5。

表4 生化试验鉴定结果Table 4 The results of biochemical

表5 生化试验鉴定结果Table 5 The results of biochemical
以上鉴定结果符合生化群Ⅲ的特征,需进一步血清学确认。
2.5 血清学确认
对3 种方法 (VITEK 2、API 20E 和GB 4789.4-2016)分离出的疑似沙门氏菌进行血清学凝集试验,血清分型结果为:Ⅲb,菌体O 抗原:60+++;Vi 不凝集;鞭毛H 抗原凝集,H1 相为:r+++,经诱导H2 相为:e+++,n+++,x+++,Z15+++[17]。
2.6 分析比较4种方法的优劣
从准确性、检测步骤、耗时上比较了4 种检测方法对巧克力中亚利桑那沙门氏菌的检测,见表6。

表6 4种检测方法对巧克力中亚利桑那沙门氏菌的优劣比较Table 6 Comparison of the detection results of Salmonella arizona in chocolate by four methods
在准确性上:1)PCR 法检出为沙门氏菌阳性,可鉴定到属;2)VITEK 和API 20E 法结果都可鉴定到亚种,VITEK 结果为肠沙门菌双相亚利桑那亚种Salmonella enterica ssp.diarizonae%id:98,API 20E 结果为:猪霍乱沙门菌亚利桑那亚种Salmonella choleraesuisssp.arizonae%id 为89.0,根据血清分型:最终确认为:双相亚利桑那亚种,与VITEK 法检验结果一致;3)GB4789.4-2016 法前期的生化鉴定结果不能完全确定是不是沙门氏菌,必须结合文献血清学鉴定[17]综合分析,这是由于亚利桑那沙门氏菌表型和生化反应极不稳定,因此传统国标法受限较大。而由此可见VITEK 法优于API 20E、实时荧光PCR 法、GB4789.4-2016 法。
由表6可知,操作步骤和时耗上实时荧光PCR 法优于VITEK 法优于API 20E 优于GB4789.4-2016 法。
3 结论与讨论
双相亚利桑那亚种沙门氏菌寄生于冷血动物的肠道内,可引起人和其他动物感染,国内虽有人感染双相亚利桑那亚种的报道,但由于血清价格昂贵,分型繁杂,诊断血清(A-F)群O 血清和Vi 因子均不凝集,给明确诊断带来了极大的困难。
通过上面4 种检验方法表明,实时荧光PCR 法操作步骤最简单,耗时短,效率高,但是该法只鉴定到种,可作为微生物检验的辅助快筛方式,针对双相亚利桑那亚种沙门氏菌的鉴定,VITEK 法优于API 20E和GB4789.4,该法操作简便,检验周期时短,可直接鉴定到型,且更精准。但由于双相亚利桑那亚种沙门氏菌表型和生化反应极不稳定,在沙显A 和XLD 上呈现非典型生化特征,极易与大肠埃希菌、枸橼酸杆菌混淆,所以检测过程需要结合分子生物PCR、VITEK、API 20E、GB4789.4-2016 和血清学五者进行综合诊断判别,否则漏检的几率很大。
——和田盘羊

