Ga2O3改性Cu/SiO2催化剂降低水蒸气催化重整产物中CO选择性
黄静静,蔡金孟,马奎,丁彤,田野,张静,李新刚,*天津大学化工学院,天津化学化工协同创新中心,天津市应用催化科学与工程重点实验室,天津 300354
2中国科学院,北京高能物理研究所,北京同步辐射装置,北京 100049
1 引言
能源危机和环境污染问题日益严重,建立完善的新型能源系统刻不容缓。近年来,氢气燃料电池以其环保、高效等优点而备受关注1-3。然而,氢气由于难以压缩、储存和运输等问题限制了氢气燃料电池的发展和应用。目前,液体燃料重整制氢技术成为燃料电池在线供氢的有效方式4-6。
二甲醚由于具有高能量密度、高氧含量、低沸点、便于储存和运输等优点而成为潜在的清洁燃料7-10。此外,与甲醇相比,二甲醚毒性较低11,12。因此,二甲醚水蒸气重整(DME SR)有望为燃料电池在线供氢提供一种潜在方法13-15。通常,DME SR分为两个步骤,反应方程式如下:
二甲醚水解:

首先是二甲醚在酸性催化剂上水解生成甲醇16,17,然后甲醇和水在金属催化剂上发生重整反应生成二氧化碳和氢气,这一步的金属催化剂通常选用Cu基催化剂18-21。在甲醇水蒸气重整反应中,许多文献报道 Cu是主要的活性中心,Cu2O的主要作用是促进水气变换反应从而提高二氧化碳的选择性22-24。也有研究者提出Cu2O的作用是促进甲醇水蒸气重整反应25。一般来说,在铜基催化剂中主要通过引入第三种元素产生Cu2O,例如通过引入 CeO2,Cu2+可以取代 CeO2晶格中的Ce4+,由于离子半径的尺寸兼容性,以Cu+的形式稳定存在;或者通过引入ZnO、ZrO2提供丰富的氧空位,铜原子与氧空位通过电子转移形成Cu2O26,27。文献报道采用蒸氨法制备的Cu/SiO2催化剂中同时含有CuO和硅酸铜(Cu2Si2O5(OH)2),在一定的条件下CuO还原为Cu0,Cu2SiO5(OH)2还原为Cu+28,并且目前蒸氨法制备的Cu/SiO2催化剂已广泛应用于加氢反应中29-32。考虑到由蒸氨法制备的Cu/SiO2催化剂可以同时引入Cu0和Cu+,这对于二甲醚水蒸气重整反应来说是十分有利的。
催化剂的选择性对整个重整反应过程都是至关重要的部分,尤其是对在DME SR中普遍存在的副产物CO,而少量的CO就可以毒化燃料电池的Pt电极,所以要求用于燃料电池的氢气原料中CO的浓度低于0.002%33。在DME SR中CO主要来源为逆水气变换反应34,反应方程式如下:

根据文献报道,以Ga为助剂的催化剂在重整反应中有很好的抑制CO生成的效果,例如,Tong报道Ga加入CuZnOx催化剂中有利于形成包含更多 Cu+的立方型尖晶石相,还原后在 ZnGa2O4的表面形成大量高分散的尺寸为0.5 nm左右铜簇,在低温条件下甲醇水蒸气重整反应中有效的降低了CO的选择性35;Haghofer也曾报道过在Pd2Ga合金体系中,Ga2O3的活性氧位点上可以吸附特定的甲酸盐,并且经过高温还原形成的Pd2Ga合金可以降低甲醇分解产生的CO,提高选择性36。Medina指出在 CO2加氢制甲醇反应中,Ga2O3可以提高甲醇生成反应的活性,对 CO生成反应即逆水气变换反应没有促进作用37;Zhou在ZnGaO体系中指出 Ga2O3有利于在高温下产生甲酸盐物种,从而降低CO的选择性38。基于Ga2O3在重整反应中可以抑制 CO的产生,我们研究了 Ga加入到Cu/SiO2催化剂体系中用于 DME SR产生的效果及Ga2O3对Cu0和Cu+所起的作用。
我们采用蒸氨法制备了既含有 CuO又含有Cu2SiO5(OH)2的xGa-Cu/SiO2催化剂,经过还原处理得到了具有 Cu0-Cu+的双活性铜物种的催化剂体系。经过研究发现,通过调变Ga的负载量可以调变 Cu+/(Cu0+ Cu+)的比例,其中 5Ga-Cu/SiO2催化剂在DME SR中具有最好的催化活性和选择性,活性提高的主要原因是Ga与Cu物种之间存在强相互作用,一方面可以提高铜物种的分散度,另一方面可以促进Cu+的形成。此外,Ga还可以促进水气变换反应,以降低 CO的选择性。以上几个方面的作用,使Ga改性的Cu/SiO2催化剂同时具有高的活性和CO2选择性。
2 实验部分
2.1 催化剂的制备
由蒸氨法制备Cu/SiO2前驱体,方法如下31,39:称取5.7 g硝酸铜溶于80 mL的去离子水,滴加氨水至pH为11.8,搅拌0.5 h。搅拌着缓慢滴加18 g硅溶胶并持续搅拌7 h。将以上混合溶液放在通风橱中90 °C油浴条件下蒸氨,直至pH为7。将上述膏状物洗涤抽滤,最后把滤饼放在 100 °C的烘箱中干燥12 h后研磨至粉末,获得Cu/SiO2前驱体。
将 Cu/SiO2前驱体浸渍硝酸镓获得xGa-Cu/SiO2催化剂,方法如下:取一定量的硝酸镓溶于100 mL去离子水中,加入3.0 g Cu/SiO2前驱体,搅拌0.5 h。将上述溶液在65 °C水浴条件下接到旋转蒸发仪上真空条件下蒸发,将上述获得固体研磨成粉末,过夜干燥,再放入马弗炉中以 2 °C·min-1的升温速率升温至 450 °C,保温 4 h。将以上粉末催化剂命名为xLa-Cu/SiO2(x= 0,1,5,10),其中x为Ga : Cu的质量百分比。
2.2 催化剂的表征
比表面积(BET)和孔径分布(BJH)测试是在美国康塔公司生产的QuadraSorb SI型物理吸附仪上进行的。X射线粉末衍射(XRD)是在布鲁克公司生产的D8-Focus测试的,采用的射线源为CuKα(λ=0.1542 nm)。程序升温还原(H2-TPR)测试在天津先权公司生产的TP5080上进行,用H2/N2混合气以10 °C·min-1的升温速率升温至 900 °C,气体流速为 30 mL·min-1。红外光谱测试(FT-IR)是在 Nicolet Magna IR560仪器上进行的,测试前先将溴化钾和样品按1 : 100的比例研磨均匀,取50 mg研磨后的混合物压片,采谱测试。X射线光电子能谱(XPS)是在PHI-1600 ESCA型光谱仪上测试的,测试时采用 Al靶的非单色Kα(hν= 1486.6 eV)为射线源,采集数据步长为0.25 eV。N2O滴定测试是在TP5079型号上进行,取50 mg的样品置于石英管恒温区,将10% H2/N2混合气以50 mL·min-1的流速通入催化剂床层,程序升温至350 °C,保温1.5 h。当床层温度降至60 °C时,用氮气吹扫0.5 h,设定床层温度为60 °C,将50% N2O/N2混合气以30 mL·min-1的速率滴定1 h。滴定结束后,待温度降至室温,用氮气吹扫0.5 h,切换气体为10%H2/N2混合气以50 mL·min-1的流速通入催化剂床层,程序升温至350 °C,保温1.5 h。基于滴定反应2Cu0(s)+ N2O(g)= Cu2O(s)+ N2,表面氧原子与Cu原子含量比为1 : 2,据此可以计算得到表面铜原子数,零价铜比表面积可以通过铜表面原子浓度1.46 × 1019m-2进行计算。程序升温表面反应(TPSR)的实验也是在此装置上进行,尾气送入HPR20质谱仪进行检测。取50 mg催化剂测试,将10% H2/N2混合气以50 mL·min-1的流速通入催化剂床层,程序升温至350 °C,保温1.5 h。当温度降至室温,通入速率为50 mL·min-1的氦气,吹扫0.5 h。切换气体为5% CO/He和水蒸气混合气,催化剂床层从室温升温至400 °C,尾气通过质谱检测。X射线吸收精细结构(XAFS)是在北京高能物理研究所的同步辐射实验装置(BSRF)的1W1B光束线上测试的,标样和样品采集的是Cu元素的K边信息。原始数据经过扣背景、归一化及傅立叶变换到R空间后,可得样品的径向结构函数(RSFs)谱图。
2.3 催化剂的性能测试
在MRE-962微型常压固定床反应器上进行催化剂二甲醚水蒸气重整反应性能评价实验,通过程序升温系统控制反应床和水蒸气汽化炉温度,反应前将 500 mg催化剂放入石英管中,在350 °C下10% H2/N2混合气还原1.5 h。将反应床温度设置为260 °C,水蒸气汽化炉的温度设置为140 °C,。待温度稳定后,将含有10% DME,40%N2和 50% H2O的混合气通入反应床层,其中,DME和 N2是分别由钢瓶连接管线后通入反应器,H2O则是由泵先带入145 °C的预热炉,经过汽化处理后再通入反应器中。原料气通过催化剂的空速为12000 mL·g-1·h-1。反应尾气除水后通入型号为Agilent 7890A气相色谱在线检测,最后进行数据分析。
2.4 动力学测试
动力学测试的装置和步骤如2.3节所述,不同的是称取100 mg催化剂进行测试,测试起始温度300 °C,10 °C·min-1的升温速率测到 330 °C,在此期间DME转化率均小于20%。反应速率的计算公式如下:

其中,XDME表示二甲醚的转化率;FDME表示原料气中二甲醚的摩尔流量;Wcat为催化剂的质量,MCu表示催化剂中总的铜质量。
氢气时空收率计算公式为:

其中,YH2表示氢气的收率;FDME表示原料气中二甲醚的摩尔流量;MCu为催化剂中Cu的质量。
3 结果与讨论
3.1 新鲜催化剂的性质
xGa-Cu/SiO2系列催化剂的结构性质均列于表1,由ICP-OES测试结果可知,Cu的含量均在24% (w)左右,随着Ga的负载量的增加,Cu的含量略微下降,而Ga的实际含量值略高于理论值。催化剂的氮气吸附脱附曲线和孔径分布曲线如图1a,b所示,催化剂均表现出IV型吸附脱附等温线,表明催化剂为介孔结构,其中在3 nm左右的孔为层状Cu2Si2O5(OH)2的层间孔,9 nm处的孔为蒸氨过程中SiO2颗粒沉积下来的堆积孔31。可以看出,催化剂在加入少量 Ga后,3 nm处的Cu2Si2O5(OH)2层间孔变多,9 nm处的堆积孔变少,而当Ga的含量大于5% (w,相对于Cu的质量分数)时,两种孔均变少,说明当 Ga的含量小于 5% (w,Cu的质量分数)时有利于层状Cu2Si2O5(OH)2的形成,大于5% (w,相对于Cu的质量分数)时会堵塞Cu2Si2O5(OH)2的层间孔。
图S1 (Supporting Information)给出了xGa-Cu/SiO2催化剂的TEM图片,可以看出由蒸氨法制备的xGa-Cu/SiO2催化剂中含有层状Cu2Si2O5(OH)2。图 2a为xGa-Cu/SiO2催化剂的XRD谱图,在2θ为22°左右的宽峰为无定形SiO2的特征峰40,在 31.0°、34.8°和 63.3°处的弱衍射峰为Cu2Si2O5(OH)2(JCPDS00-003-0219)的特征峰31,可以看出Cu2Si2O5(OH)2的结晶性比较差。同时,添加Ga对Cu/SiO2催化剂的主要物相没有明显影响,并且从XRD谱图中没有观察到Ga的物相,说明加入的Ga物种在Cu/SiO2催化剂中高度分散。
由于XRD谱图中的衍射峰强度较弱,难以准确区分Cu物种的存在形式,因此,我们对催化剂进行了XAFS测试。图2b,c表示的是xGa-Cu/SiO2催化剂中Cu元素K边的XAFS信息,其中CuO和 Cu2Si2O5(OH)2为标样。图 2b为xGa-Cu/SiO2催化剂的X射线吸收近边结构(XANES)谱图,其中CuO标样在8985.0 eV的吸收边为1s→4p的跃迁,而在Cu2Si2O5(OH)2标样中这个跃迁向高能偏移,吸收边位置为8987.1 eV41。而xGa-Cu/SiO2催化剂中1s→4p的跃迁吸收边能量为8986.2 eV,介于 CuO和Cu2Si2O5(OH)2标样之间,由此说明xGa-Cu/SiO2催化剂中的Cu物种的存在状态为既有 CuO又有 Cu2Si2O5(OH)2物种。图 2c给出了xGa-Cu/SiO2催化剂中Cu元素K边的RSFs谱图。由图可知,CuO标样在0.16和0.25 nm处的两个配位峰分别对应Cu―O和Cu―Cu第一配位壳层的散射信号,在 0.30 nm的配位峰为 Cu―Cu和Cu―O键之间叠加的散射信号42,43。Cu2Si2O5(OH)2标样的Cu―O和Cu―Cu第一配位壳层的配位峰分别位于0.15和0.27 nm。在xGa-Cu/SiO2催化剂中除了在0.16 nm出现了Cu―O壳层的配位峰之外,还在0.26和0.30 nm出现了两个配位峰,其中0.26 nm处的配位峰介于CuO和Cu2Si2O5(OH)2标样的中间,0.30 nm的配位峰对应于CuO标样,以上结果进一步的说明了xGa-Cu/SiO2催化剂中同时含有CuO和Cu2Si2O5(OH)2物种。
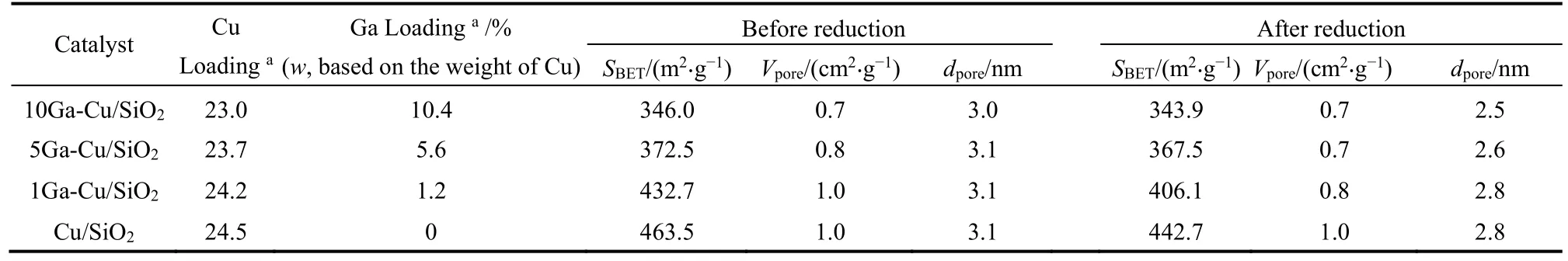
表1 催化剂的物理结构性质Table 1 Physical properties of the catalysts.

图1 新鲜催化剂的(a)氮气吸脱附曲线和(b)孔径分布图,还原后催化剂的(c)氮气吸脱附曲线和(d)孔径分布图Fig. 1 (a) N2 adsorption-desorption isotherms and (b) BJH pore size distribution of the fresh catalysts.(c) N2 adsorption-desorption isotherms and (d) BJH pore size distribution of the reduced catalysts.
为了探究Ga与Cu物种之间是否存在相互作用,我们对新鲜xGa-Cu/SiO2催化剂做了H2-TPR表征。据文献报道,高分散的CuO还原为Cu纳米颗粒的还原温度为238 °C,Cu2Si2O5(OH)2还原为Cu2O的还原温度为245 °C,Cu2O继续还原为Cu需要600 °C以上的高温44,45。如图3所示,Cu/SiO2催化剂在239 °C左右有一个较宽的还原峰,归属为Cu2Si2O5(OH)2还原为Cu2O和高分散的CuO还原为 Cu纳米颗粒的叠加。从图中可以看出,Ga改性后的xGa-Cu/SiO2催化剂的还原温度均向高温偏移,并且随着Ga的负载量的增加,还原峰的温度逐渐增高。造成这种变化的原因可能是随着Ga负载量的增大,使部分的Cu物种被Ga2O3覆盖,从而造成还原温度的升高。我们将5Ga-Cu/SiO2催化剂先用 8% H2/N2气氛下在350 °C 还原 1.5 h,将至室温后再在 450 °C 空气气氛下氧化 4 h,之后进行 H2-TPR测试(标记为5Ga-Cu/SiO2-RO),并与新鲜 5Ga-Cu/SiO2催化剂的H2-TPR对比,5Ga-Cu/SiO2-RO催化剂的主峰位置(233 °C)明显向低温方向偏移,并且大颗粒CuO的还原峰(290-350 °C)消失了。说明了Cu与Ga之间存在相互作用,并且这种相互作用使 Cu物种的分散度更高更容易被还原。由H2-TPR的耗氢峰计算了Cu物种的还原度,如表S1 (Supporting Information)结果所示,随着Ga的负载量的增加,Cu物种的还原度逐渐降低。我们推测Ga的加入促进了 Cu+物种的形成,使更多的 Cu2+物种还原为Cu+,从而使Cu物种的还原度逐渐降低。

图3 催化剂的H2-TPR谱图Fig. 3 H2-TPR profiles of the catalysts.
3.2 还原后催化剂的性质
图1c,d表示的是还原后xGa-Cu/SiO2催化剂的氮气吸脱附曲线和孔径分布曲线图。从图中可以看出还原后的吸脱附曲线和孔径分布的类型与新鲜催化剂相比没有明显变化,表明催化剂仍然为介孔结构,还原后xGa-Cu/SiO2催化剂SBET、Vpore、dpore都有所减小,可能是还原过程中Cu物种聚集堵塞部分孔道。仔细观察发现随着Ga负载量的增加,还原后xGa-Cu/SiO2催化剂的SBET、Vpore、dpore与新鲜催化剂的差值越来越小,说明Ga的加入在一定程度上可以阻碍Cu物种的迁移。
图4a,b为还原后的Cu/SiO2和5Ga-Cu/SiO2样品的 HRTEM 图。从图中可以看出,还原后的5Ga-Cu/SiO2样品相比于Cu/SiO2样品,生成有更小粒径的Cu物种,从一定程度上说明了Cu与Ga之间存在相互作用,因为相互作用限制了高温还原下Cu物种的迁移,致使5Ga-Cu/SiO2样品生成的Cu物种粒径更小。此外,我们并没有发现Ga物种的晶格条纹,说明 Ga是以高分散的状态存在,图4c-h是5Ga-Cu/SiO2催化剂的元素面分布图像,证明了Ga元素在催化剂的表面是均匀分散的,这种分布状态可以增加与 Cu物种的接触机会,促进相互作用的形成。

图4 (a,b)还原后Cu/SiO2和5Ga-Cu/SiO2催化剂的HRTEM图像;(c)新鲜5Ga-Cu/SiO2催化剂的STEM图像;(d-g)对应于图c的O、Si、Cu、Ga元素分别的面分布图像;(h)四种元素合并后的面分布图像Fig. 4 (a, b) HRTEM image of the reduced Cu/SiO2 and 5Ga-Cu/SiO2 catalysts, (c) STEM image of the fresh 5Ga-Cu/SiO2 catalyst, and (d-g) STEM-EDS element mapping of O, Si, Cu, Ga (c). (h) The overlap of element mapping of O, Si, Cu, Ga.
图5 是还原后xGa-Cu/SiO2催化剂的XRD谱图,测试前催化剂均在350 °C温度下于8% H2/N2气氛还原处理1 h。从图中看出,2θ为43.3°,50.5°和 71.2°处的衍射峰可以归属为金属 Cu (JCPDS 04-0836)物相,在 36.5°的衍射峰则归属为 Cu2O(JCPDS 05-0667)物相46,金属Cu和Cu2O分别来自 CuO和 Cu2Si2O5(OH)2的还原。图中看不到关于 Ga物种的衍射峰,说明 Ga在还原后的xGa-Cu/SiO2催化剂中还处于高度分散状态。
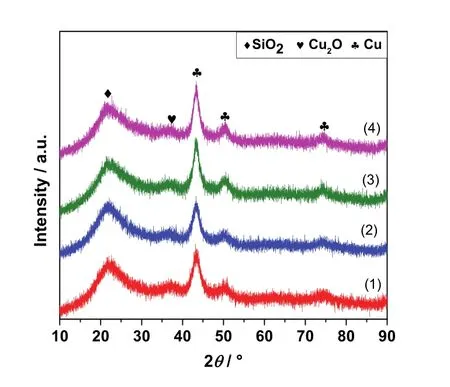
图5 还原后催化剂的XRD谱图Fig. 5 XRD patterns of the reduced catalysts.
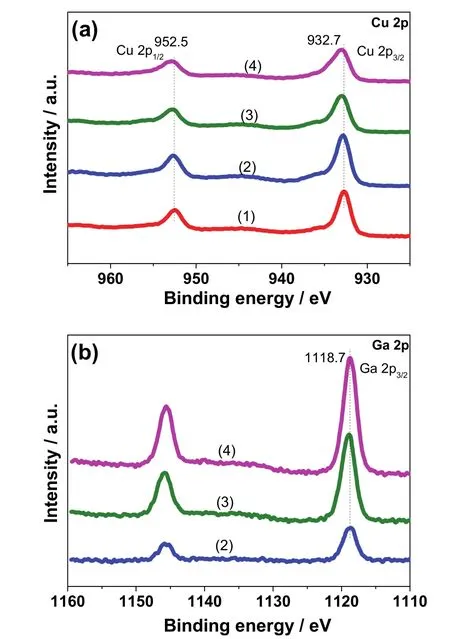
图6 还原后的催化剂的Cu 2p与Ga 2p XPS谱图Fig. 6 Cu 2p and Ga 2p XPS spectra of the reduced catalysts.
图6a为还原后xGa-Cu/SiO2催化剂的Cu 2pXPS谱图。一般结合能为932.7和952.5 eV的峰对应于Cu 2p3/2和2p1/2峰,而结合能在942-945 eV范围内的震激峰为Cu2+的特征峰45,47。图中在942-945 eV范围内没有出现震激峰,说明Cu2+已被完全还原为Cu+或Cu0(或Cu+和Cu0)物种。随着Ga负载量的增加,Cu 2p3/2峰从932.7 eV迁移到933.1 eV,向高能方向偏移。图6b为还原后xGa-Cu/SiO2催化剂的Ga 2pXPS谱图,结合能在1118.7 eV的峰为Ga 2p3/2峰48,在此处的结合能表示Ga在催化剂表面上以Ga3+形式存在。由于在XPS谱图中Cu+和Cu0结合能的位置一致,我们采用CuLMMXAES谱图来计算还原后xGa-Cu/SiO2催化剂表面的 Cu+和 Cu0物种的含量。如图 S2 (Supporting Information)所示,经过分峰处理之后,动能在915和918 eV附近的峰分别为Cu+和Cu0的特征峰47。分峰结果列于表2中,可以看出随着Ga负载量的增加,Cu+的含量逐渐上升,说明Ga与Cu物种之间的强相互作用可以调变Cu+和Cu0的比例,当Ga的负载量为5% (w,相对于Cu的质量分数)时,Cu+和Cu0大约各占50%。由CuLMMXAES结果计算的Cu物种的还原度如表S1所示,随着Ga的负载量的增加,Cu物种的还原度逐渐降低,此结果与由H2-TPR计算得出的还原度变化规律一致。
在Cu基催化剂中金属Cu的分散度对催化性能起着至关重要的作用44。在这里我们综合 N2O滴定和XPS表征计算还原后xGa-Cu/SiO2催化剂中金属 Cu的分散度(DCu),Cu0的表面积(SCu0)和Cu+的表面积(SCu+)。由表2可以看出,DCu和SCu0都随着Ga负载量的增加先增加后略有减少,当Ga的负载量为5% (w,相对于Cu的质量分数)时,DCu和SCu0值均达到最大;SCu+随着Ga负载量的增加一直增加。造成以上变化的原因主要是因为少量Ga的负载可以促进 Cu物种的分散,但是当 Ga的负载量过多时又会覆盖表面的 Cu物种,因此DCu和SCu0呈现出先增加后减少的趋势;而Ga的加入可以促进Cu+的产生,所以随着Ga负载量的增大SCu+一直变大。
3.3 催化活性和选择性
图7为xGa-Cu/SiO2催化剂用于DME SR的活性和选择性图。在测试过程中没有检测到任何的含氧化合物,CH4的选择性均小于 1%。加入Ga后催化剂的催化活性都高于Cu/SiO2催化剂,如图7a,b所示,催化剂的DME转化率和H2收率均呈现出“火山型”变化趋势,并且5Ga-Cu/SiO2催化剂表现出最好的催化活性,催化剂在380 °C的催化活性和选择性数据统计在表S2 (SupportingInformation)中,其中 5Ga-Cu/SiO2催化剂在 380 °C时DME转化率为99.8%,H2收率为98.7%。CO2和CO为主要的C1产物,其选择性图分别为图7c,d,其变化规律与活性变化规律相似,也呈现“火山型”变化趋势,同样,5Ga-Cu/SiO2催化剂表现出最好的选择性,在380 °C时其CO选择性为4.8%。
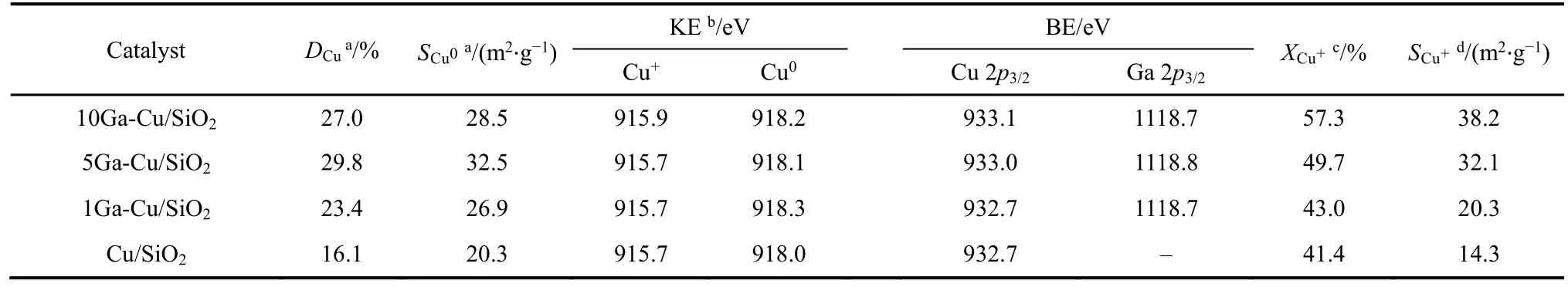
表2 还原后催化剂Cu LMM XAES分峰计算结果Table 2 Deconvolution of Cu LMM XAES of the reduced catalysts.
为了考察催化剂活性和选择性的提高是否是由于Ga的引入对反应路径的改变所引起的,我们由阿累尼乌斯方程计算了Cu/SiO2和5Ga-Cu/SiO2催化剂的表观活化能。计算之前,要根据三点假设来简化DME SR过程49,50。首先,该反应为一级反应,其次,反应器为绝热平推流反应器,第三,副反应可以忽略。根据上述三点假设,我们绘制了Cu/SiO2和5Ga-Cu/SiO2催化剂的阿累尼乌斯曲线,如图8a所示,可见催化剂的线性拟合相似度很高,表明上述三条假设适用于xGa-Cu/SiO2催化剂体系。Cu/SiO2和5Ga-Cu/SiO2催化剂的活化能分别为 109.7和 108.1 kJ·mol-1,可以认为二者的活化能相差不大,表明催化剂的活性和选择性的改变并不是因为反应机理的变化引起的。
关于Cu0和Cu+在 DME SR反应中所起的作用一直备受争议,大部分作者认为 Cu0是主要的活性位,Cu+通过促进水气变换反应提高CO2的选择性22,23;有些作者认为Cu+可以促进甲醇水蒸气重整反应25;也有文献报道,Cu0有利于CH3O物种的形成,Cu+有利于形成HCOO-和COO-物种为了进一步确定 Cu0和 Cu+对 DME SR反应的影响51-53。因此,我们研究了Cu+/(Cu0+ Cu+)对氢气时空收率的影响,如图8b所示,氢气时空收率随着Cu+/(Cu0+Cu+)的变大呈典型的“火山型”曲线变化趋势,并且大约在Cu+/(Cu0+ Cu+) = 0.5时取得最大值为 5.02 mol·g-1·h-1。说明 Cu0和 Cu+在DME SR反应中起着协同催化的作用,二者相互作用共同影响着催化活性。当Cu+/(Cu0+ Cu+)的比例大于0.5时,活性变差可能是因为某些反应中间体的改变导致。氢气时空收率结果如表S2所示,xGa-Cu/SiO2催化剂具有优异的催化性能,其中5Ga-Cu/SiO2催化剂在 380 °C下的氢气时空收率为 5.02 mol·g-1·h-1,具有比已报道的文献中更高氢气时空收率54,55。
副产物CO会引起燃料电池Pt电极中毒,在DME SR中Cu基催化剂产生的CO主要来自于高温下逆水气变换反应34,文献报道 Ga2O3在水汽变换反应中具有良好的催化性能56,57。于是,我们设计了CO和H2O的TPSR实验探究Ga对Cu/SiO2催化剂选择性的影响。图 9给出了在 Cu/SiO2和5Ga-Cu/SiO2催化剂在水气变换反应中产物 CO2和H2的MS信号,从图9a中可以看出在Cu/SiO2催化剂中165 °C之前的水气变换反应基本忽略,从165 °C之后CO2信号开始上升,直到225 °C信号趋于平稳,说明Cu/SiO2催化剂中水气变换反应的活性位有限。在5Ga-Cu/SiO2催化剂中,水气变换反应的起始温度为 90 °C,并且从 90 °C以后CO2的信号呈指数型函数上升,说明Ga的加入很好的促进了水气变换反应,提高了CO2的选择性。图9b中H2的信号规律与图9a中CO2信号规律相似,说明Ga的加入促进了水气变换反应,不仅提高了CO2的选择性也提高了H2收率。
4 结论
采用蒸氨法制备的xGa-Cu/SiO2催化剂中同时含有CuO和Cu2Si2O5(OH)2物相,经过还原后分别转化为Cu0和Cu+物种。通过对还原处理后的催化剂表征结果分析发现,Ga与Cu物种之间的相互作用不仅有利于提高Cu物种的分散度还促进了Cu+的生成。将xGa-Cu/SiO2催化剂用于DME SR反应,发现5Ga-Cu/SiO2催化剂表现出最好的催化活性和选择性,在380 °C的反应温度下其转化率为99.8%,CO选择性为4.8%。Ga可以很好的调变Cu+/(Cu0+ Cu+)比例,并且氢气时空收率结果表明催化活性与Cu+/(Cu0+ Cu+)的值密切相关,当Cu+/(Cu0+ Cu+) = 0.5时活性最优。Ga的加入在很大程度上可以促进水气变换反应,从而降低CO的选择性。

图9 还原后Cu/SiO2和5Ga-Cu/SiO2催化剂的TPSR谱图Fig. 9 TPSR profiles of the reduced Cu/SiO2 and5Ga-Cu/SiO2 catalysts.
Supporting Information:available free of chargeviathe internet at http://www.whxb.pku.edu.cn.

