三尖瓣反流对心脏再同步治疗疗效的影响
李晶晶, 陈康玉,徐 健,严 激,苏 浩,安春生,杨冬妹
慢性心力衰竭(chronic heart failure, CHF)是心血管治疗学上的难题,心脏再同步治疗(cardiac resynchronization therapy, CRT)可显著降低合并心脏不同步者的心衰住院率和病死率,得到欧洲、美国和我国急慢性心衰管理指南的I类推荐[1-3]。但无反应问题一直困扰着临床医师,研究[4]表明心衰病程、病因、QRS时限、心房颤动等多种因素影响着CRT疗效。三尖瓣反流(tricuspid regurgitation, TR)可引发右心房增大和心房颤动的出现,尤其是重度TR,严重损害心功能。对于符合CRT指征的心脏明显扩大患者,其本身即存在不同程度的TR,反流是否会对CRT疗效产生影响,且右心室导线植入后亦可能影响反流的程度,目前国内文献报道较少。本文通过前瞻性的随访研究,试图探讨TR和CRT的相互影响。
1 材料与方法
1.1病例资料连续选取2016年1~12月间安徽医科大学附属省立医院拟行CRT植入的患者,符合如下条件:在优化药物治疗的情况下,仍纽约心脏病协会(New York heart association, NYHA)心功能Ⅱ~Ⅳ级,QRS波时限≥130 ms,左室射血分数(left ventricular ejection fractio, LVEF)≤35%。植入CRT以改善患者的临床症状和预后。术前评估患者的基线情况并记录,包括性别、年龄、基础心脏疾病类型、QRS时限、心脏结构性指标、心功能分级和药物应用等情况。
1.2TR评价采用美国飞利浦公司IE33 彩色多普勒超声诊断仪,S5-1探头,患者取左侧卧位,平静呼吸,胸骨旁左室长轴与心尖四腔心切面的彩色多普勒血流图像,取三个心动周期,根据收缩末期三尖瓣最大反流束面积与右心房面积之比,将TR分为微量/无、轻度(反流束面积/心房面积<0.20)、中度(反流束面积/心房面积 0.20~0.45)和重度(反流束面积/心房面积>0.45)反流[5]。根据上述评价结果,将所有患者分为无或轻度反流组与中重度反流组。
1.3CRT植入经锁骨下静脉穿刺,采用冠状静脉引导系统,定位冠状窦开口,行冠状静脉造影,显示心脏静脉后,将左室起搏电极导线送至心脏静脉的侧支,测定左室起搏夺获的最满意参数后,再置入右房和右室电极导线,固定电极导线后连接脉冲发生器(Insync购自美国Medtronic公司,Epic+HF和Frontier购自美国St Jude公司)埋藏脉冲发生器于皮下囊袋中。
1.4临床随访患者术后进行为期6个月的随访,术后6个月评估患者NYHA分级,复查超声心动图,评价TR情况、左室舒张末期容积(left ventricular end-diastolic volume, LVEDV)、左室收缩末期容积(left ventricular end-systolic volume, LVESV)、LVEF和肺动脉压力。CRT有效定义为术后6个月LVESV缩小>15%。

2 结果
2.1TR对CRT疗效的影响共入选符合指征的患者98例,成功手术患者97例,去除资料不全的患者5例,最终入选92例患者。92例患者根据TR的程度分为无或轻度反流组(n=59)和中重度反流组(n=33)。基线资料见表1,两组在性别、年龄、心衰病程、NYHA分级、血肌酐水平、QRS时限、LVEDV、LVESV、LVEF和药物应用方面差异无统计学意义,但三尖瓣中重度反流组的肺动脉收缩压(systolic pulmonary artery pressure, SPAP)水平显著高于无或轻度反流组。根据CRT疗效标准,共有57例患者对CRT有反应,有效率为62.0%,无或轻度TR组与中重度反流组的疗效差异有统计学意义(72.9%vs42.4%,P<0.01),如图1所示。两组在逆转心脏重构方面有显著差异,无或轻度反流组优于中重度反流组,见表2。单因素分析发现,男性、缺血性心肌病、心衰病程、血肌酐水平、QRS时限、SPAP和中重度TR是影响CRT疗效的因素,但多因素结果仅纳入心衰病因、QRS时限和中重度TR,见表3。
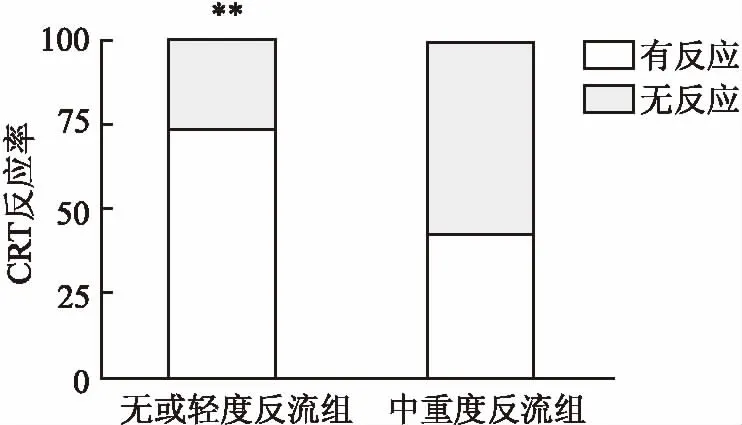
图1 不同TR组患者CRT反应率比较与中重度反流组比较:**P<0.01
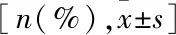
表1 CRT患者基线资料比较
ACEI/ARB:血管紧张素转化酶抑制剂/血管紧张素Ⅱ受体拮抗剂

表2 不同程度三尖瓣反流对CRT逆重构的影响
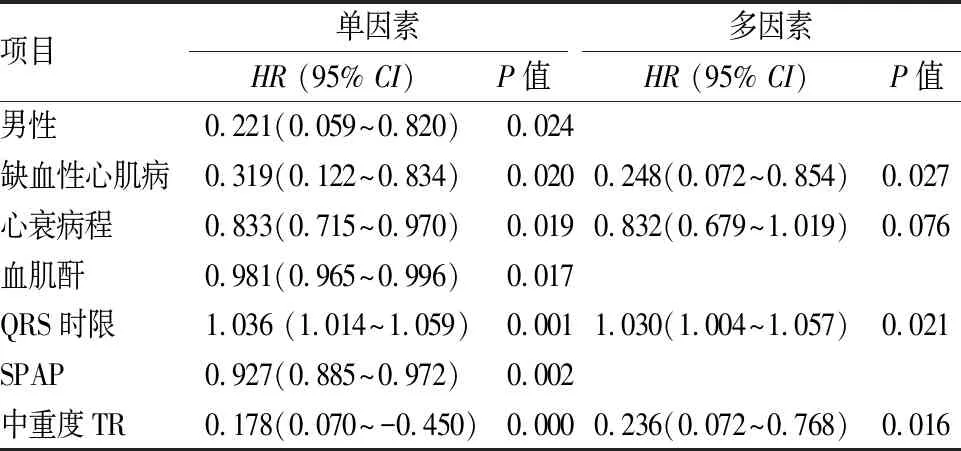
表3 影响CRT疗效单因素和多因素分析
2.2CRT起搏器植入对TR的影响CRT植入后6个月随访显示,7例患者由无或轻度TR加重至中重度反流,差异无统计学意义(35.9%vs43.5%, χ2=0.113,P=0.292)。7例患者中,3例为普通右心室导线,4例为除颤导线,差异无统计学意义。
3 讨论
TR是一种常见的临床现象,普遍存在于健康人群和器质性心脏病患者。目前为止的多项研究证实[6-8],TR在慢性心衰患者中十分常见,但是其对预后价值的大样本研究数量有限。2004年Nath et al[6]发表了一项回顾性的研究,该研究入选了5 223例患者,结果证实明显的TR可增加心衰患者的死亡率,其预测价值独立于 LVEF 和肺动脉压力。但因为缺乏患者的临床特征资料及其合并症情况,该研究结果受到一定的质疑。Neuhold et al[7]入选了576例慢性心衰患者,进行了为期 (5.8±4.2)年的前瞻性随访。结果发现,基线伴重度反流者较无明显反流者,远期1、3、5、7年存活率明显较低 ,分别为43%、27%、19%、14%与 71%、58%、49%、43% (P<0.000 1)。当纳入TR与 LVEF两者间关系分析后发现,TR与不利预后则明显相关。Sadeghpour et al[8]的研究结论与之类似,重度TR严重影响心衰患者预后。
在进展性心衰中,TR多数是功能性的,升高的左室舒张末期压会导致肺动脉压力的升高,造成右心室的扩大,进而出现TR;而TR的出现,亦会使得右心室进一步扩大,扩大的右心室使得三尖瓣环扩张,TR进一步加重,以此形成恶行循环。上述机制使得严重的TR会直接影响心衰患者的预后。对于CRT患者,本研究亦得出了类似的结论,中重度TR是CRT无反应的独立预测因子。Abu Sham'a et al[9]共入选了193例CRT患者,根据TR情况,将患者分为无或轻度反流组和中重度反流组,虽然两组的临床疗效类似,但超声有效的比例有显著差异(35%vs60%,P=0.01),多因素分析表明中重度TR是超声无反应的独立预测因子,而Grupper et al[10]的研究结果显示,尽管基线TR对CRT临床和超声疗效无明显影响,但对预后有显著影响。结果的差异与入选人群的基线特征、TR评价方式不同有一定相关,但结果均提示严重的TR影响CRT患者的预后。
导线介导的TR早已见诸文献[11]报道,其发生率在25%~29%,远高于12%~13%的普通人群。其原因除导线的机械作用外,导线植入后可能会造成右心室机械不同步和房室不同步,从而造成新发或加重TR。根据发生机制的不同,导线介导的TR可在植入后即刻或数天内出现,亦可能在术后数月或数年远期出现,且以后者更为多见。本文中导线植入后TR有加重的趋势,但未达到统计学差异,分析与患者随访时间偏短,仅为6个月有关。同时考虑到,CRT后心脏同步性的改善,可能改善TR,临床表现为CRT后TR并未显著增加[12]。此外,本研究中结果显示导线类型与TR无关,这与Al-Bawardy et al[13]的研究结果一致。
本研究结果表明,TR影响CRT疗效,三尖瓣中重度反流是CRT无反应的独立预测因素。CRT植入后6个月,TR并未显著增加,且与右心室导线是否为除颤导线无关。但因为样本量有限,随访时间偏短,上述结果有待更大规模的临床研究来进一步明确。

