金纳米棒比色检测亚铁离子
黄 帅,刘显杰,游 立
金纳米棒比色检测亚铁离子
黄 帅,刘显杰,游 立
(武汉船用电力推进装置研究所,武汉 430064)
实现亚铁离子的简单高效检测,在生化传感领域具有至关重要的作用。本文中,基于芬顿试剂(亚铁离子和过氧化氢的混合物)对金纳米棒的选择性氧化,实现了对亚铁离子的比色检测。伴随芬顿试剂的引入,金纳米棒溶胶颜色由红色逐渐演变为棕色、绿色、蓝色、紫色,乃至粉红色。基于此规律,实现了对亚铁离子的可视化检测。本文提出了一种相对Hg2+, Mg2+, Cu2+, Fe3+, Sn2+, Co2+, Cd2+, Cr3+, Zn2+, Ba2+, Ni+等离子具有良好选择性的亚铁离子检测方法。
金纳米棒 亚铁离子 芬顿试剂 比色检测
0 引言
铁元素是自然界中最丰富的过渡金属,并且广泛存在于水和土壤中。铁离子在生物体的生物代谢中扮演着重要的角色。亚铁离子的缺乏会导致诸如糖尿病、心脏病和肝、肾等器官的损害。然而亚铁离子过量会导致排泄功能障碍,甚至可能诱发癌变[1-2]。因此研发高灵敏度和高稳定性的亚铁离子检测技术具有重要意义。
金纳米棒(GNRs)因其可调节的各向异性的光学特性和较宽的光谱范围(从可见光区到近红外区)在生物化学传感领域有巨大的发展前景[3]。
GNRs因其可调节的各向异性的光学特性和较宽的光谱范围(从可见光区到近红外区)在生物化学传感领域有巨大的发展前景。GNRs紫外吸收光谱有两个表面等离子体共振(LSPR)吸收峰,分别是纵向等离子体共振吸收峰(LPAB)和横向等离子体共振吸收峰(TPAB)。其中,TPAB对周围介质环境和GNRs长径比非常敏感。基于此特性,GNRs可用于生物化学领域的检测[4,5]。
向GNRs溶胶中引入过氧化氢这种氧化试剂的时候,GNRs的端面会被氧化,且GNRs的长径比和LPAB波长随着H2O2氧化时间的延长逐渐变小。根据文献可知通过向H2O2中加入过渡金属离子产生羟基自由基能够提高其氧化能力,而Fe2+对H2O2氧化能力的提高在众多过渡金属离子中最为显著,因为Fe2+与H2O2可以形成具有强氧化性的芬顿试剂(Fenton reagent)[6,7]。
GNRs溶胶颜色随着氧化过程的进行发生规律性变化,出现了一个较宽的色域包括酒红色、棕色、绿色、蓝色、紫色、粉红色,不同氧化程度的GNRs溶胶呈现出不同的颜色[8]。Fe2+与H2O2组成芬顿试剂,比其它离子(Na+, K+, Li+, Hg2+, Mg2+, Ni+, Sn2+, Co2+, Cd2+, Cr3+, Zn2+, Ba2+, Cu2+,Fe3+)与H2O2的组合的氧化性要强很多,在相同的实验条件下,Fe2+与H2O2的组合具有更强的氧化性,使得GNRs溶胶率先到达色域中的下一个特征颜色。因此,通过观察样品颜色即可实现对Fe2+的选择性检测和比色检测。
1 实验过程
1.1 主要试剂和仪器
主要试剂:氯金酸(HAuCl·3H2O,分析纯,上海国药集团试剂公司);十六烷基三甲基溴化铵(C19H42BrN,分析纯,上海国药集团试剂公司);硼氢化钠(NaBH4,96%,上海国药集团试剂公司);抗坏血酸(C6H8O6,99.7%,上海国药集团试剂公司);盐酸(HCl,36-38%,武汉中天化工有限公司);硝酸银(AgNO3,99.8%,上海凌峰化学试剂公司);过氧化氢(H2O2,30%,上海国药集团试剂公司);氯化亚铁(FeCl2·4H2O,分析纯,上海国药集团试剂公司)。
主要仪器:恒温磁力加热搅拌器(HJ-2,中国,金坛市宏华仪器厂);数显恒温水浴锅(HH-2,中国,常州智博瑞仪器厂);离心机(TGL-16C,中国,上海宏亭科学仪器厂);分析天平(AUY220,中国,上海宏亭科学仪器厂);紫外-可见分光光度计(UV-2450,日本,岛津公司);场发射透射电子显微镜(JEM-2100F,日本,电子株式会社)。
1.2 实验步骤
1.2.1晶种法制备金纳米棒
首先,准备20 mL含5×10-4mol氯金酸和0.1 mol CTAB的混合液。之后将现配的1.5 mL NaBH4冰水溶液(0.01 mol)加入到以上溶液中并快速搅拌2分钟。溶液立刻变为棕黄色,说明成功合成了CTAB包覆的晶种。晶种在30 ℃水浴锅保存2.5小时后待用。将10 mL 0.01 M HAuCl4溶液与10 mL 0.1 mol CTAB溶液混合成金纳米棒生长液。再依次加入0.5 mL 0.01 mol AgNO3溶液,180 μL现配的抗坏血酸溶液,40 μL 1.2 mol HCl溶液和40 μL晶种溶液并快速搅拌2分钟。最后将上述配置的混合液放置于30℃水浴锅保存16小时后备用。
1.2.2过氧化氢氧化金纳米棒
取上述制备的4 mL 金纳米棒,依次加入5 μL HCL(6 mol)、240 μL H2O2(0.124 mol)并混合均匀,将混合液放置于50℃水浴中反应15分钟,然后将混合液装在紫外-可见光光谱仪的样品池中,记录其紫外-可见吸收光谱。然后将样品取出后,再加入110 μL H2O2(0.124 M),此时共加入过氧化氢的浓度为10 mmol,将样品混合均匀后置于50 ℃水浴中反应15分钟,再将样品装在紫外-可见光光谱仪的样品池中,记录其紫外-可见吸收光谱。随后加入H2O2(0.124 mol),分别控制样品中H2O2浓度为18 mmol,23 mmol,24 mmol,重复以上实验。详细记录和观察H2O2氧化的GNRs的紫外可见光吸收光谱的演变规律。另外,在H2O2氧化GNRs的实验过程中利用场发射透射电子显微镜表征相应样品的物理形貌。
1.2.3芬顿试剂氧化金纳米棒
取上述制备的4 mL金纳米棒,然后依次加入5 μL HCL(6 M)、100 μL H2O2(0.124 M)并混合均匀,将混合液放置于50℃水浴中反应8 分钟,然后将混合液装在紫外-可见光光谱仪的样品池中,记录其紫外-可见吸收光谱。然后将100 μL H2O2(0.124 mol)和50 μL FeCl2(2 mmol)混合均匀组成芬顿试剂,利用芬顿试剂取代上述实验过程的H2O2作为氧化剂,其它条件保持不变,重复上述实验。根据实验结果进行对比分析,分别以H2O2和芬顿试剂为氧化剂的GNRs的紫外-可见吸收光谱的变化,进而比较两者的氧化性。
1.2.4亚铁离子选择性和比色检测
取上述制备的4 mL金纳米棒,然后依次加入5 μL HCL(6 mol)、100 μL H2O2(0.124 mol)并混合均匀,将混合液放置于50℃水浴中反应8 分钟,然后将混合液装在紫外-可见光光谱仪的样品池中,记录其紫外-可见吸收光谱。然后将100 μL H2O2(0.124 mol)和50 μL FeCl2(2 mmol)混合均匀组成芬顿试剂,利用芬顿试剂取代上述实验过程的H2O2作为氧化剂,其它条件保持不变,重复上述实验。根据实验结果进行对比分析,分别以H2O2和芬顿试剂为氧化剂的GNRs的紫外-可见吸收光谱的变化,进而比较两者的氧化性。
2 结果与讨论
2.1 H2O2氧化GNRs
图1是GNRs被不同浓度H2O2氧化15分钟后的系列紫外-可见吸收光谱。初始状态GNRs的紫外-可见吸收光谱具有两个等离子体共振吸收峰,分别在520 nm(TPAB)和731 nm(LPAB)处(谱线a),这两个吸收峰分别来源于GNRs的横向和纵向等离子体共振。当向GNRs溶液中加入7 mmol H2O2后,GNRs的LPAB发生了明显变化,中心波长蓝移至669.7 nm,而TPAB波长却没有发生明显的变化(谱线b);当加入的H2O2浓度继续增加时,GNRs的LPAB波长进一步蓝移(谱线c和d),直至和TPAB汇合(谱线e和f)。透射电镜图显示了氧化过程中金纳米棒物理形貌的变化过程,如插图所示。在初始样品中,我们观察到了标准金纳米棒(插图,a),然后棒的长度逐渐缩短(插图,b和c),接着产生小部分的金球(插图,d),最后只观察到金纳米球(插图,e和f)。[9,10]
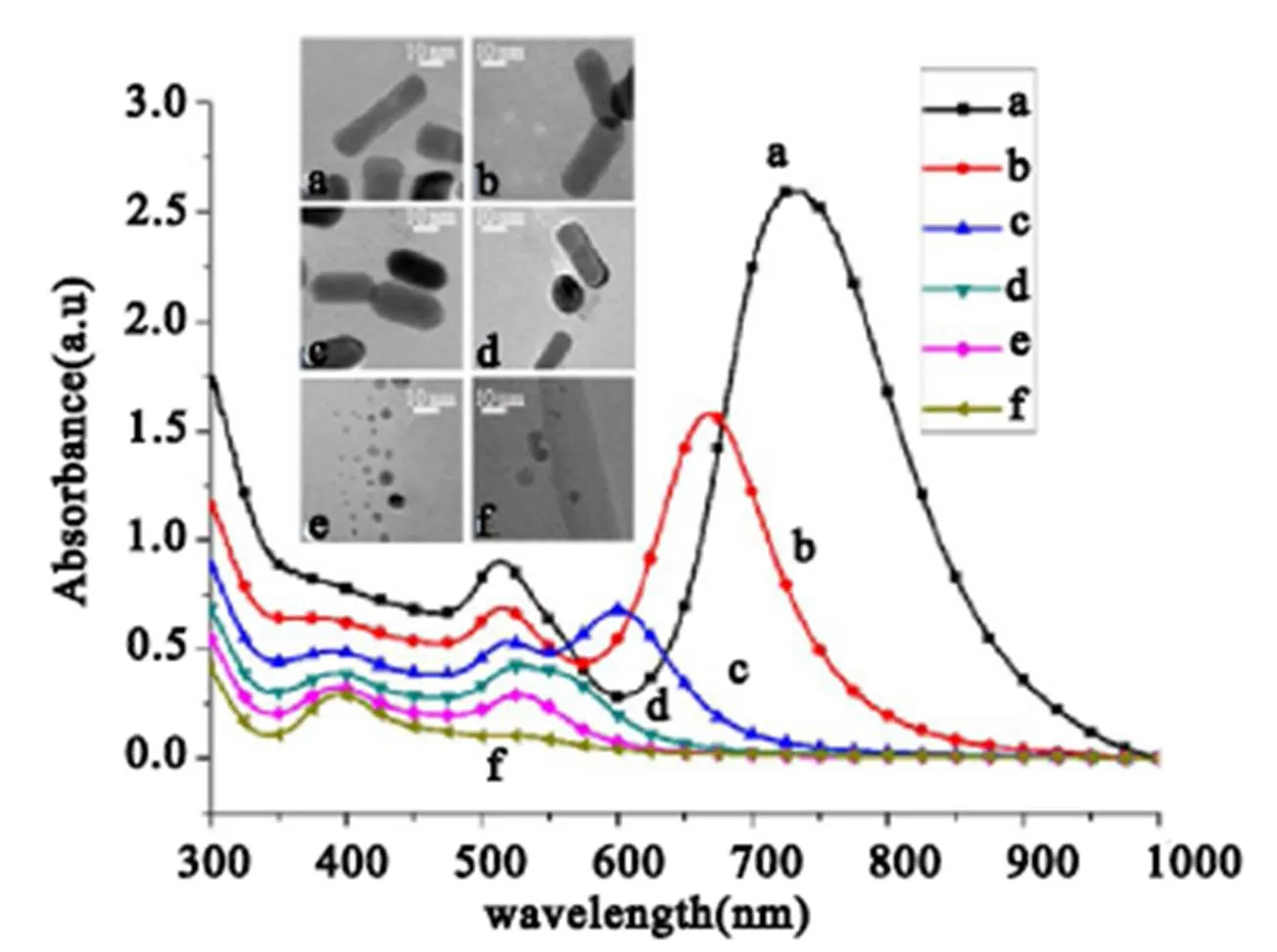
图1 GNRs被不同浓度H2O2氧化15分钟后的系列紫外-可见吸收光谱图
2.2 芬顿试剂和H2O2对GNRs氧化作用对比
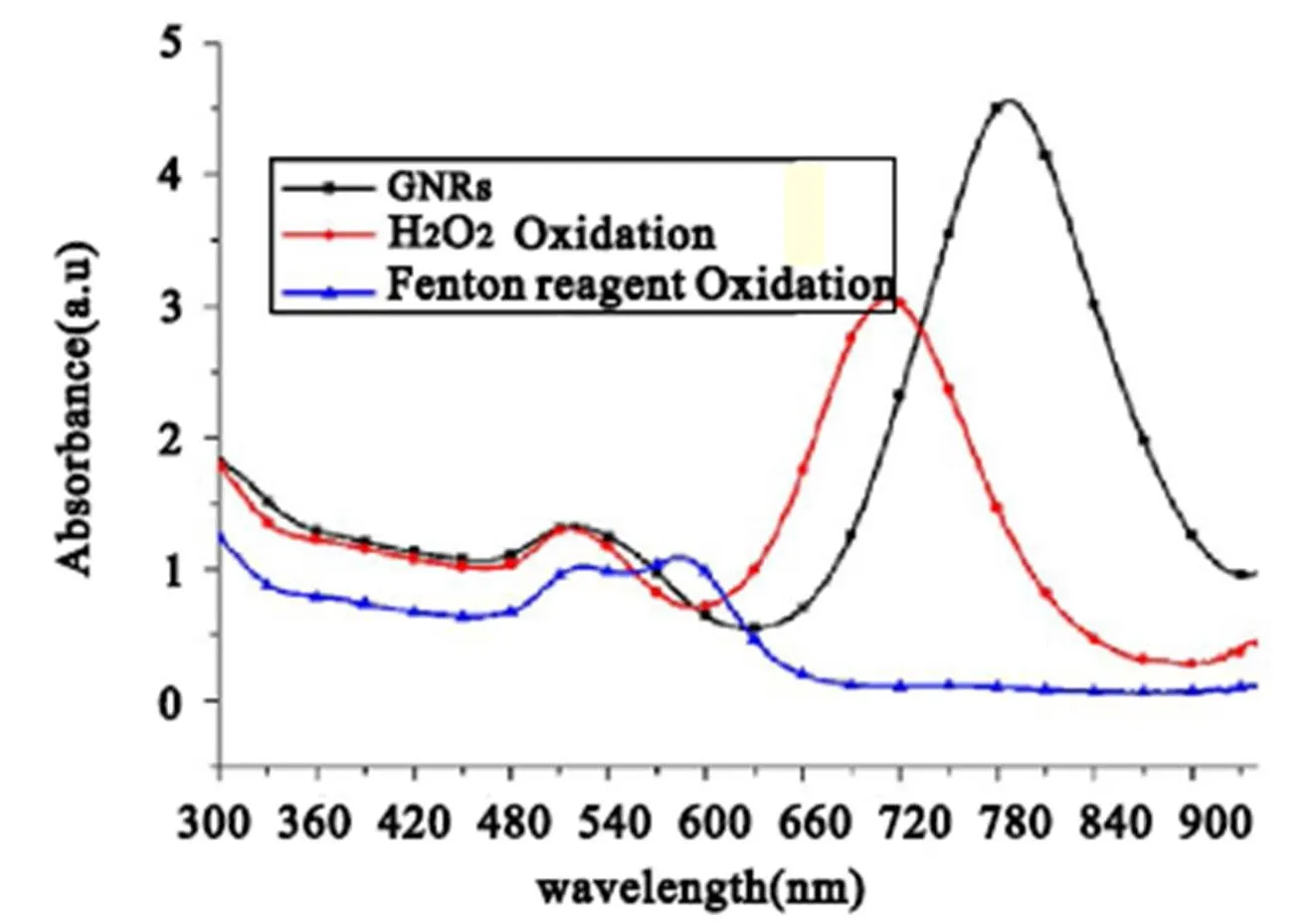
图2 紫外-可见吸收光谱
图2是GNRs被H2O2和芬顿试剂氧化前后的紫外-可见吸收光谱图。芬顿试剂由3 mmol H2O2和25 μM Fe2+组成。其它参数如H2O2浓度、水浴温度和溶液pH值分别是3 mmol,50℃和1.8。由光谱图可知,初始状态的GNRs吸收光谱中有两个等离子体共振吸收峰,分别位于520 nm和787 nm处。在GNRs经H2O2氧化8分钟后,GNRs的LPAB波长发生明显蓝移,移至712 nm。在相同的氧化时间内,经芬顿试剂氧化的GNRs的LPAB波长则蓝移至585 nm。相同的实验条件下,芬顿试剂氧化的GNRs的LPAB的蓝移量更大,这说明与H2O2相比,芬顿试剂对GNRs的氧化性更强。
2.3 金纳米棒氧化过程颜色变化

图3 GNRs氧化过程中相应溶胶的颜色变化
GNRs氧化过程中相应溶胶的颜色变化如图3所示,随着芬顿试剂的加入,GNRs溶胶颜色由酒红色(A)变为棕色(B)、绿色(C)、蓝色(D)、紫色(E)和粉红色(F),说明GNRs在氧化过程中,会随着自身尺寸的变化而呈现出不同的颜色。不同氧化能力的芬顿试剂,在相同条件下,对GNRs氧化程度不同,GNRs对应溶胶颜色不同,基于此规律可以对Fe2+进行比色法检测。
2.4 比色法检测亚铁离子
图4是GNRs被H2O2与不同金属离子组成的混合物氧化后的溶胶颜色变化图。由图4可知,H2O2与Na+, K+, Li+, Hg2+, Mg2+, Ni+, Sn2+, Co2+,Cd2+, Cr3+, Zn2+, Ba2+, Cu2+, Fe3+等离子的组合氧化GNRs后,相应的GNRs溶胶的颜色与初始GNRs溶胶颜色几乎保持一致,都是酒红色,且LPAB波长变化不大,说明这些离子对H2O2的氧化能力影响不大,既不大幅度促进H2O2的氧化能力,也不大幅度抑制H2O2的氧化能力。H2O2与Fe2+离子的组合氧化GNRs后溶胶颜色由初始的酒红色变为青色,且LPAB波长变化可达133 nm,这是因为H2O2与Fe2+离子组合形成芬顿试剂,产生了强氧化性,使GNRs被氧化的程度更深,对应的溶胶颜色相比初始状态发生变化。而其它组的GNRs溶胶颜色均保持为初始颜色酒红色。该方法对Fe2+的检测相对于其他金属离子表现出良好的选择性。而且,由于芬顿试剂氧化的GNRs的溶胶颜色变化更为显著,还可以通过肉眼判断Fe2+的存在,实现Fe2+的比色检测。

图4 溶胶颜色变化
3 结论
本文在H2O2对GNRs氧化规律的基础上,引入Fe2+与H2O2组成芬顿试剂,考察了芬顿试剂对GNRs的氧化特性,GNRs溶胶颜色随着氧化过程的进行发生规律性变化,出现了一个较宽的色域包括酒红色、棕色、绿色、蓝色、紫色、粉红色,不同氧化程度的GNRs溶胶呈现出不同的颜色。Fe2+与H2O2组成芬顿试剂,比其它离子(Na+, K+, Li+, Hg2+, Mg2+, Ni+, Sn2+, Co2+, Cd2+, Cr3+, Zn2+, Ba2+, Cu2+,Fe3+)与H2O2的组合的氧化性要强很多,在相同的实验条件下,Fe2+与H2O2的组合具有更强的氧化性,使得GNRs溶胶率先到达色域中的下一个特征颜色。因此,通过观察样品颜色即可实现对Fe2+的选择性检测和比色检测。
[1] Yuan D, Fu D. Flow-injection determination of iron based on its catalysis on the oxidation reaction of xylenol orange by potassium bromate[J]. analytical letters, 2011, 44(1-3): 271-283.
[2] Gupta A, Crumbliss A L. Treatment of iron deficiency anemia: are monomeric iron compounds suitable for parenteral administration[J]. J Lab Clin Med. 2000, 136(5): 371-378.
[3] 郑淑静, 金纳米棒的光学特性及生物检测应用研究[D]. 吉林: 东北师范大学, 2012
[4] 陈国珍, 王军, 任海晶等. 关于金纳米棒应用的研究进展[J]. 应用化工. 2014, 43(1): 159-161.
[5] Gao X, Campian J L, Qian M, et al. Mitochondrial DNA damage in iron overload[J]. Journal of Biological Chemistry. 2009, 284(8): 4767-4775.
[6] Scheers N, Andlid T, Alminger M, et al. Determinat-ion of Fe2+and Fe3+in aqueous solutions containing food chelators by differential pulse anodic stripping voltammetry[J]. electroanalysis. 2010, 22(10): 1090-1096.
[7] Díaz T G, Guiberteau A, Soto M D L, et al. Spectrophotometric and adsorptive stripping square wave voltammetric determination of iron in olive oils, as complex with 5, 5-dimethylcyclohexane-1,2,3-trione 1,2-dioxime 3-thiosemicarbazone (DCDT)[J]. J Agric Food Chem. 2003, 51(13): 3743-3747.
[8] Liu J M, Wang X X, Jiao L, et al. Ultra-sensitive non-aggregation colorimetric sensor for detection of iron based on the signal amplification effect of Fe3+ catalyzing H2O2 oxidize gold nanorods[J]. Talanta. 2013, 116(1): 199-204.
[9] Zhang Z, Chen Z, Pan D, et al. Fenton-like reaction-mediated etching of gold nanorods for visual detection of Co2+[J]. Langmuir the Acs Journal of Surfaces & Colloids. 2015, 31(1): 643.
[10] Wen X, Shuai H, Min L. Precise modulation of gold nanorods aspect ratio based on localized surface plasmon resonance[J]. Optical Materials. 2016, 60: 324-330.
Colorimetric Detection of Fe2+Based on Gold Nanorods
Huang Shuai, Liu Xianjie, You Li
(Wuhan Institute of Marine Electric Propulsion, Wuhan 430064, China)
Detection of Fe with simpleness and efficiency is of great significance in biochemical sensing field. In this paper, colorimetric detection of ferrous ion Fe is realized based on Fenton reagent (a mixture of Fe and H2O2)(). The color of GNRs sol turns from crimson to brown, green, blue, purple, and pink when Fenton reagent is introduced, based on which visual detection of Fe could be realized. A high Fe detection selectivity over other metal ions, such as Hg, Mg, Cu, Fe, Sn, Co, Cd, Cr, Zn, Ba, Ni, etc., was demonstrated.
()(Fe)
TU991
A
1003-4862(2019)03-0043-04
2018-10-30
黄帅(1991-),男,助理工程师。研究方向:微纳金属和高温银浆。E-mail: huangshuaiwhut@sina.com

