橄榄油微乳体系的 相行为及影响因素研究
,,, , ,,,*
(1.扬州市职业大学,江苏扬州 225009; 2.扬州大学化学化工学院,江苏扬州 225002)
微乳液是由油、水、表面活性剂和助表面活性剂按照适当比例混合后自发形成的各向同性、透明、热力学稳定的分散体系[1-2]。微乳液具有超低的界面张力、纳米级的分散相尺寸(10~200 nm)以及较高的增溶能力[3-5],在医药、食品、化妆品等领域被广泛用作药物、生物活性物等的优良载体[6-8]。相比于其他行业,食品微乳化技术要求较高,安全性、生物相容性等问题使得表面活性剂、油相等原料在食品级微乳液的制备中受到限制。
橄榄油富含不饱和脂肪酸、抗氧化物等营养成分和活性成分,具有降血脂、降血压、抗癌等保健功效[9-10],是医学界公认的、最有益于人体健康的食用油之一。然而,橄榄油中不饱和脂肪酸大多水溶性差,对氧气、光、热敏感,极易氧化而变质,大大影响了其功效,也因此限制了橄榄油的应用范围。龚丽等[11]利用乳化均质技术及添加复合稳定剂,制备了具有一定稳定性的橄榄油乳状液。Papadimitriou等[12]以大豆卵磷脂为表面活性剂、正丙醇为助表面活性剂对不同等级橄榄油进行微乳化,并比较了不同橄榄油微乳体系对酶催化活性的影响。Amiri-Rigi等[13]则采用大豆卵磷脂/正丙醇/橄榄油/水微乳体系从番茄渣中提取了番茄红素。
为进一步提高橄榄油微乳配方的安全性、扩大体系的微乳区间,选取天然表面活性剂大豆卵磷脂与非离子表面活性剂司盘80复配作为混合表面活性剂,乙醇为助表面活性剂,对橄榄油进行微乳化。通过拟三元相图法考察不同亲水亲油平衡值(HLB值)、表面活性剂与助表面活性剂的质量比(Km值)及水相中NaCl、甘油含量对微乳体系相行为的影响,探讨橄榄油微乳液的形成规律。并在此基础上,通过电导率、负染-透射电镜等方法,分析橄榄油微乳体系的结构,为后续研究橄榄油微乳液对物质的增溶及释放、扩大微乳液在食品、医药、化妆品等领域的应用奠定基础。
1 材料与方法
1.1 材料与仪器
大豆卵磷脂(Lecithin,纯度大于70%,如图1a) 阿拉丁试剂公司;司盘80(Span80,如图1b)、橄榄油均为化学纯 国药集团化学试剂有限公司;无水乙醇、甘油、氯化钠(NaCl)均为分析纯 国药集团化学试剂有限公司;水为去离子水。
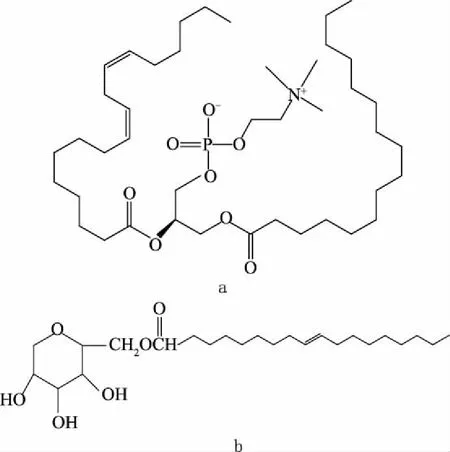
图1 大豆卵磷脂与Span80的化学结构Fig.1 Chemical structures of Lecithin and Span80注:a.大豆卵磷脂;b.Span80。
Vortex-Genie2涡漩混合仪 美国Scientific Industries公司;DDS-11A数显电导率仪 上海雷磁新泾仪器有限公司;TECNAI 12型负染-透射电镜 荷兰Philip公司;DK-S22电热恒温水浴锅 上海精宏实验设备有限公司;KQ-50B超声波清洗器 昆山市超声仪器有限公司;Barnstead Lab Tower EDI 15超纯水仪 美国Thermo Scientific公司。
1.2 实验方法
1.2.1 拟三元相图的绘制 固定大豆卵磷脂、Span80与无水乙醇的质量比,混合均匀作为表面活性剂相。将橄榄油(油相)与表面活性剂相以一定质量比(10∶0、9∶1、8∶2、7∶3、6∶4、5∶5、4∶6、3∶7、2∶8、1∶9、0∶10)在具塞管中称量,超声3 min后,采用涡旋混合仪使溶液混合均匀。在恒温水浴(25±0.1) ℃条件下,逐滴向混合液中加入水相溶液(纯水;氯化钠水溶液;甘油水溶液),当体系由澄清透明变为浑浊时,记录加入水相的质量。计算转变点下体系各相(表面活性剂相、油相及水相)所占总量的质量百分数,并由此确定转变点在相图中的位置。
1.2.2 HLB值的确定 将大豆卵磷脂和Span80按照质量比分别为1∶3、1∶1、3∶1、7∶1复配成不同HLB值(分别为5.2、6.2、7.1、7.5)的混合表面活性剂。以无水乙醇为助表面活性剂,固定混合表面活性剂与助表面活性剂的质量比为2∶1,采用1.2.1中水相滴定法制备微乳液并绘制拟三元相图,根据微乳区域面积的大小确定混合表面活性剂的最佳HLB值。
1.2.3 Km值的确定 根据1.2.2 中确定的最佳HLB值,将大豆卵磷脂和Span80进行复配,并与无水乙醇按照质量比(Km值)分别为3∶1、2∶1、1∶1、1∶2进行混合,采用1.2.1中水相滴定法制备微乳液并绘制拟三元相图,根据微乳区域面积大小确定合适的Km值。
1.2.4 盐浓度对微乳体系相行为的影响 根据1.2.2、1.2.3中结果,固定表面活性剂相中大豆卵磷脂、Span80与无水乙醇的质量比为3∶1∶2,以0.5、1.0、2.0、3.0、4.0、5.0 mol/L的氯化钠水溶液代替纯水作为水相,采用1.2.1 中水相滴定法制备微乳液并绘制拟三元相图,考察不同浓度盐溶液对橄榄油微乳体系相行为的影响。
1.2.5 甘油含量对微乳体系相行为的影响 根据1.2.2、1.2.3中结果,固定表面活性剂相中大豆卵磷脂、Span80与无水乙醇的质量比为3∶1∶2,以不同浓度甘油水溶液(w水∶w甘油=2∶1、1∶1、1∶2)代替纯水作为水相,采用1.2.1 中水相滴定法制备微乳液并绘制拟三元相图,考察甘油不同添加量对橄榄油微乳体系相行为的影响。
1.2.6 电导率的测定 将大豆卵磷脂、Span80、无水乙醇以质量比3∶1∶2混合为表面活性剂相,并与橄榄油以9∶1质量比进行混合。以甘油水溶液(w水∶w甘油=1∶1)为水相,在(25±0.1) ℃下,制备不同水相含量的大豆卵磷脂/Span80/橄榄油/乙醇/甘油/水微乳体系。采用电导率仪,在(25±0.1) ℃下,测定不同含量水相时,体系电导率的变化情况。
1.2.7 微乳液滴微观形貌分析 将1.2.6中制备的微乳液样品滴在31.0孔·cm-2具有Formvar膜的载网表面,吸附10 min后,滴加2%的磷钨酸进行染色,灯光下烤干,采用负染-透射电镜(加速电压:120 kV,放大倍数:×18500)观察微乳液的微观形态。
1.3 数据处理
每组实验重复三次,结果取其平均值。采用AutoCAD 2007软件绘制拟三元相图,并计算相图中微乳区域面积的大小(AT,以微乳单相区面积所占总面积的百分比表示)。其他则采用Origin 8.0软件进行数据分析和绘制。
2 结果与分析
2.1 大豆卵磷脂/Span80/乙醇/橄榄油/水微乳体系相行为分析
2.1.1 不同HLB值对微乳体系相行为的影响 理论上,单一表面活性剂较难满足多组分体系的微乳化要求[14]。实验发现,大豆卵磷脂或Span80作为单一表面活性剂,均无法实现橄榄油的微乳化,而将两者复配为不同HLB值的混合表面活性剂,以无水乙醇为助表面活性剂,可以不同程度地形成橄榄油微乳液。由此表明,复配表面活性剂的乳化效果优于单一表面活性剂,这与已有研究结果一致[15-16]。
固定混合表面活性剂与助表面活性剂的质量比(Km值)为2∶1,绘制拟三元相图,结果如图2所示。当大豆卵磷脂与Span80以质量比分别为1∶3、1∶1、3∶1、7∶1进行复配时,根据质量分数加和法[17]计算得到混合表面活性剂的HLB值(依次为5.2、6.2、7.1、7.5)。由图2可以看出,随着HLB值的增加,微乳区域面积呈现先增加后减小的趋势(AT=4.5%、8.8%、14.6%、10.9%)。当大豆卵磷脂与Span80的质量比为3∶1时,HLB值达到7.1,此时形成微乳区域的面积最大。Span80分子中环氧原子和羟基中氧原子通过氢键与水及H3O+结合,使得该非离子表面活性剂带有部分正电性[18]。若复配表面活性剂中Span80含量较高,易发生静电相斥作用,不利于表面活性剂分子在界面的紧密排列。当大豆卵磷脂与Span80以质量比3∶1混合时,两者亲水基团发生静电吸引作用,表面活性剂分子相互靠近的几率增加,并在油水界面达到有效吸附,降低了界面张力。若进一步增加复配表面活性剂中大豆卵磷脂的含量(大豆卵磷脂与Span80的质量比为7∶1),微乳区域面积开始减小,这可能是由于大豆卵磷脂分子体积较大,Span80在界面排列所受空间阻力较大,且大豆卵磷脂在油水界面的界面密度较低,导致其界面效力不高[19]。
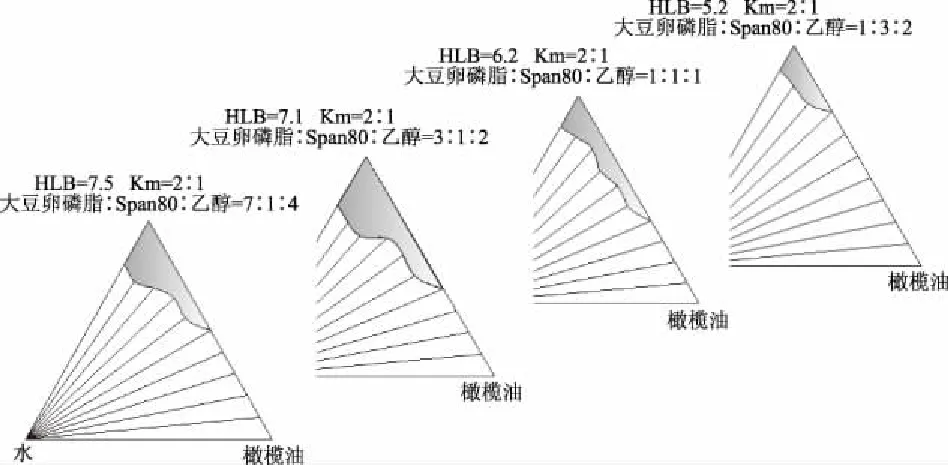
图2 不同HLB值时微乳体系拟三元相图Fig.2 Pseudo-ternary phase diagram of microemulsion with different HLB注:阴影部分表示微乳单相区,其他为多相区。
2.1.2 不同Km值对微乳体系相行为的影响 在微乳体系中加入短链醇或多元醇作为助表面活性剂,有助于改变界面膜的自发曲率,增加膜的弹性,破坏液晶相的稳定性[20]。对食用油脂橄榄油进行微乳化,体系配方的安全性是考虑的重点,因此,以乙醇为助表面活性剂、大豆卵磷脂-Span80(HLB=7.1)为混合表面活性剂,改变Km值,绘制拟三元相图,考察不同Km值对橄榄油微乳体系相行为的影响,结果如图3所示。由图3可以看出,改变表面活性剂与助表面活性剂的比例,即添加不同量的乙醇,对橄榄油微乳区域大小存在一定的影响。随着Km值的减小(依次为3∶1、2∶1、1∶1、1∶2),微乳区域面积(AT=13.1%、14.6%、5.2%、0)先略有增加后迅速减小,最终单相微乳区完全消失。其中,当Km值为2∶1(即大豆卵磷脂、Span80、无水乙醇质量比为3∶1∶2)时,所形成微乳区域的面积最大。原因可能是随着乙醇含量的增加,乙醇逐渐渗透至表面活性剂界面膜中,增加了界面膜的弯曲弹性[1,20-21],促进了微乳液的形成。乙醇含量的继续增加,使得微乳区域减小甚至消失,这与张佩华等[22]的研究结果一致。原因可能是表面活性剂相对含量减少,导致其在油水界面的密度下降,不足以维持较低的油/水界面张力[22],引起相界面稳定性下降,微乳结构破坏。
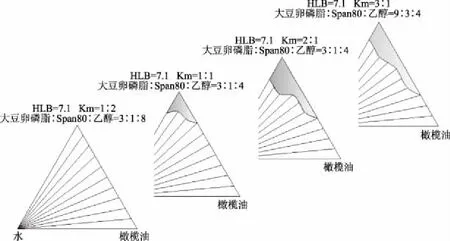
图3 不同Km值时微乳体系拟三元相图Fig.3 Pseudo-ternary phase diagram of microemulsion with different Km
2.1.3 盐浓度对微乳体系相行为的影响 固定大豆卵磷脂、Span80与无水乙醇的质量比为3∶1∶2,以不同浓度NaCl水溶液代替纯水作为水相,对橄榄油进行微乳化,绘制拟三元相图,并计算相图中单相区域面积,结果如图4、图5所示。

图4 不同浓度NaCl时微乳体系拟三元相图Fig.4 Pseudo-ternary phase diagram of microemulsion with different concentration of NaCl
由图5可见,随着NaCl浓度的增加,橄榄油微乳区域的面积先缓慢增加后迅速减小,且当NaCl溶液浓度达到3 mol/L时,微乳区域面积达到最大。大豆卵磷脂是两性离子表面活性剂,其极性头基在胶束表面所占面积易受离子强度的影响。Abbasi等[23]研究发现,随着离子强度的增加,卵磷脂亲水性头基的极性以及在油/水界面所占面积均减少,从而有利于W/O型微乳液的形成。另外,由于无机盐能够中和离子型表面活性剂极性基团的电荷,压缩双电层,使电荷密度降低[24],因此,NaCl溶液浓度的适度增加有利于降低油水界面张力,促进微乳液的形成。然而,随着NaCl浓度的继续增加(CNaCl>4 mol/L),微乳区域面积则明显减小,这可能是由于盐浓度的大量增加,使得助表面活性剂分子从界面层发生“盐析”作用,转移进入油相[23,25],导致体系形成微乳液的能力下降,微乳区域面积减小。

图5 微乳区域面积随NaCl溶液浓度的变化Fig.5 Variation of microemulsion area with different concentrations of NaCl in aqueous phase
2.1.4 甘油含量对微乳体系相行为的影响 固定大豆卵磷脂、Span80与无水乙醇的质量比为3∶1∶2,以甘油水溶液代替纯水作为水相,对橄榄油进行微乳化,绘制拟三元相图,结果如图6所示。由图6可以看出,增加水相中甘油的含量(w水∶w甘油=1∶0、2∶1、1∶1、1∶2),橄榄油微乳区域面积缓慢增加(AT=14.6%、17.3%、18.7%、21.2%)。尤其对于表面活性剂含量相对较高时,甘油含量的增加明显增大了微乳体系对水相的增溶量。甘油作为助溶剂,能够改变水溶液的物理化学性质,如密度、粘度、折射率及界面张力等[26]。Garti[27]、zhang[28]等研究得出了类似的结论,当水相中加入甘油,能一定程度增强非离子表面活性剂形成微乳液的能力。另外,有研究者[29-30]发现,甘油的加入可以提高乳液储藏的稳定性。我们认为,在橄榄油微乳体系中增加甘油含量,微乳区域能稳定存在,主要是由于乙醇在增加界面膜流动性的同时,甘油由于不具有表面活性,主要存在于水相中[26-27],加强了表面活性剂亲水基团与醇分子中羟基的结合,形成更稳定的氢键,从而有利于微乳体系的稳定。

图6 添加不同量甘油时微乳体系拟三元相图Fig.6 Variation of microemulsion area as a function of added glycerol in aqueous phase
2.2 微乳液电导率
电导率法是鉴别微乳液结构转变的一种有效方法,根据电导率数值,可以确定微乳液的连续相,进而判断微乳液的结构类型[31-32](W/O、双连续B.C.、O/W)。将大豆卵磷脂、Span80与无水乙醇按照质量比3∶1∶2混合为表面活性剂相,与橄榄油以质量比9∶1进行混合,以甘油水溶液(w水∶w甘油=1∶1)为水相,制备不同水相含量的大豆卵磷脂/Span80/橄榄油/乙醇/甘油/水体系。考察不同含量水相条件下,体系电导率的变化情况,结果如图7所示。由图7可以看出,混合液(大豆卵磷脂/Span80/乙醇)的电导率不为零,这可能是由于大豆卵磷脂的等电点为6.7,混合液的pH约为6.0,溶液呈微酸性,当水相含量为零时,两性离子质子化,溶液具有一定的导电性。当水相含量较低(Φ=0~22 wt%)时,随着水相含量的增加,微乳体系的电导率直线上升,这表明随着水相的加入,W/O型微乳液滴发生肿胀,液滴间相互吸引,并发生粘性碰撞,在油连续相中形成通道,从而连接形成电导链[33]。当水相含量进一步增加,体系电导率变化缓慢,并在Φ=25 wt%时,体系电导率达到最大值。这主要是由于微乳液滴粘性碰撞产生的水相通道扩大并连接,形成网络结构,体系处于油、水局部连续的过渡态中间结构[34],即形成B.C.型微乳液。当水相含量超过30wt%,体系电导率急剧下降,此时,体系出现浑浊(如图8),处于相分离状态。这可能是由于当含水量超过临界值,表面活性剂界面膜发生破坏,油、水两相分离,界面张力增大,水分子间的相互作用和电荷传递受到阻碍,从而使体系电导率下降[35]。
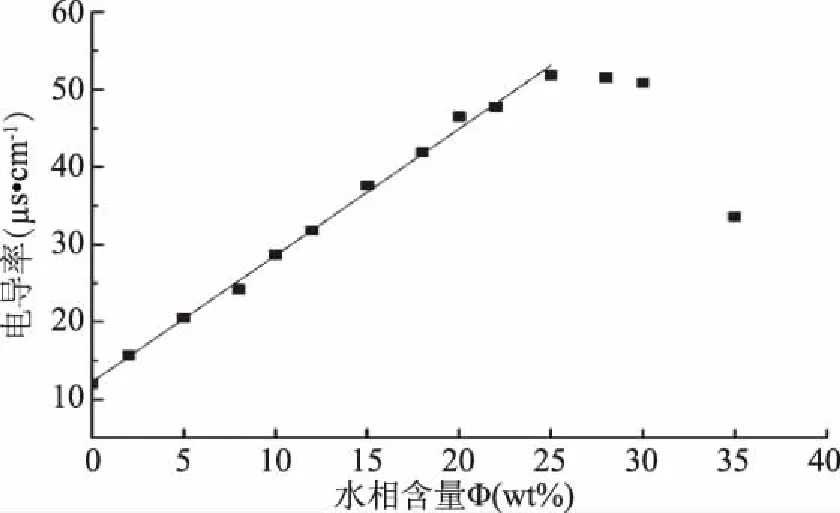
图7 体系电导率随水相含量(Φ)的变化Fig.7 Electricity of the system as a function of aqueous phase weight content(Φ)

图8 不同水相含量(Φ)时体系外观Fig.8 System appearance at different aqueous phase weight content(Φ)
2.3 微乳液滴形貌分析
图9为2.2中水相含量分别为15 wt%和25 wt%时大豆卵磷脂/Span80/橄榄油/乙醇/甘油/水微乳体系的负染-透射电镜图。由图9可以看出,当水相含量为15 wt%时,微乳液滴呈球形分布,粒径大小在10~100 nm,进一步证明体系为W/O型微乳液。当水相含量为25 wt%,体系呈相互交错的网状结构,显示出油相及水相的连续性,微乳液呈双连续型结构。

图9 不同水相含量下橄榄油微乳体系的负染-透射电镜图Fig.9 Negative-stained TEM images of olive oil microemulsions with different weight content of aqueous phase注:a.水相含量15 wt%;b.水相含量25 wt%。
3 结论
通过拟三元相图法,以大豆卵磷脂/Span80复配作为混合表面活性剂,以乙醇为助表面活性剂,构建橄榄油微乳体系。考察大豆卵磷脂/Span80不同配比形成的HLB值、表面活性剂与助表面活性剂的比值(Km值)及水相中NaCl、甘油含量对微乳体系相行为的影响。结果表明:当大豆卵磷脂/Span80质量比为3∶1,表面活性剂与助表面活性剂的比值(Km值)为2∶1时,大豆卵磷脂/Span80/乙醇/橄榄油/水体系形成的微乳区间面积最大。甘油或少量盐离子的加入,可以在一定程度上增大微乳单相区面积,但当盐浓度较高时,微乳区域面积则明显减小。
通过电导率法、负染-透射电镜探讨大豆卵磷脂/Span80/乙醇/橄榄油/甘油/水微乳体系的结构转变。当水相(w水∶w甘油=1∶1)含量低于22wt%时,体系主要呈W/O型结构;当水相含量继续增加,体系逐渐转变为双连续型结构;水相含量超过30wt%后,体系开始发生相分离。

